Изучение теоретических основ применения наноструктурированных водных эмульсий полимеров в лакокрасочной промышленности
ЛЕКЦИЯ 1.
ОБЩИЕ СВЕДЕНИЯ О НАНОТЕХНОЛОГИИ.
К наноматериалам относятся наночастицы, пленки с толщиной в нанометрической области и макроскопические объекты, содержащие нанокристаллы или нанопоры, размеры которых составляют 1–100 нм.
Наночастицы не являются истинными кристаллами, их особенность состоит в большом отношении поверхности к массе. Это можно пояснить следующим образом: шарик с поверхностью 1 см2 имеет диаметр 0,5642 см и объем 0,094 см3. Шарики с диаметром 1 нм (10–7см) имеют объем 5,236·10–22 см3, их поверхность составляет 3,1416·1014 см2. Из первого шарика можно сделать 1,7959·1020 таких шариков, у которых суммарная поверхность составит 5640000 см2, т. е. 564 м2. Такие материалы характеризуются высокой поверхностной энергией и, соответственно, большим поверхностным напряжением.
Наночастицы обладают уникальными свойствами. Важно знать, что чем меньше частица, тем большая часть составляющих ее атомов расположена на поверхности. Так, например, в частицах золота (или сульфида кадмия) размером 2 нм примерно 60 % атомов находится на поверхности. В полупроводниках такое расположение способствует электронному переходу в поверхностных частицах типа акцептор – донор или наоборот. В металлических наночастицах большое отношение поверхности к объему облегчает эффективный переход заряда и вызывает связанные с переносом заряда изменения в абсорбционном спектре.
Проявление эффектов, связанных с размером, или размерных эффектов, является одним из основных отличий нанохимии от химических превращений при обычных условиях проведения реакций. Принято различать два типа размерных эффектов: собственный, или внутренний, и внешний. Внутренний связан со специфическими изменениями в объемных и поверхностных свойствах как индивидуальных частиц, так и получаемых в результате их самоупорядочения. Внешний эффект является реакцией на внешнее поле или действие сил, независимых от внутреннего эффекта.
Эксперименты с внутренним размерным эффектом направлены на решение проблем электронных и структурных свойств. К ним относятся химическая активность, потенциал ионизации, энергия связи между атомами в частице, кристаллографическая структура. Температуру плавления и оптические свойства можно также рассматривать как функции размера частицы и ее геометрии. Было установлено, что у свободных наночастиц металлов всегда наблюдается понижение температуры плавления с уменьшением размера наночастицы.
Наночастицы состоят из 106 или меньшего количества атомов. Как уже было упомянуто, обычно наночастицами считают образования из связанных атомов или молекул размером менее 100 нм:
В химии под наночастицами подразумевают в общем виде такие образования, у которых отношение числа атомов, лежащих на поверхности, к объемным более 1. Понятно, что при таком определении наночастицами низкомолекулярных веществ считаются объекты с размерами от десятых долей до примерно 10 нм, а для высокомолекулярных – от единиц до сотен нанометров при их сфероидальной форме.
В физическом материаловедении частицы с размерами около 1 нм и менее называют кластерами, а материалы с такими морфологическими единицами – кластерными.
Кластер радиусом 1 нм содержит примерно 25 атомов, причем большинство их находится на поверхности кластера. Малые атомные агрегации-кластеры являются промежуточным звеном между изолированными атомами и молекулами, с одной стороны, и объемным твердым телом – с другой. Переход от дискретного электронного энергетического спектра, свойственного отдельным атомам и молекулам, к зонному электронному энергетическому спектру, характерному для твердых тел, происходит через кластеры. Отличительной чертой кластеров является немонотонная зависимость свойств от количества атомов в кластере. В нанокристаллических дисперсных и объемных материалах такая зависимость отсутствует, но появляется зависимость свойств от размера частиц (зерен, кристаллитов).
Кластер представляет собой группу из небольшого (счетного) и в общем случае переменного числа взаимодействующих атомов (ионов, молекул). Минимальное количество атомов в кластере равно двум. Верхней границе кластера соответствует такое количество атомов, при добавлении к которому еще одного атома свойства кластера не меняются, так как переход количественных изменений в качественные уже закончился (рис. 1). С химической точки зрения большая часть изменений заканчивается, когда число атомов не превышает 1000–2000.
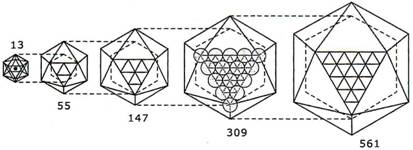
Рис. 1. Последовательный рост кластера. Цифры обозначают число атомов в кластере
Верхнюю границу размеров кластера можно рассматривать как границу между кластером и изолированной наночастицей. Переход от свойств изолированных наночастиц к свойствам объемных кристаллических веществ в течение многих десятилетий оставался «белым пятном», так как отсутствовало промежуточное звено – компактное тело с зернами нанометрического размера. Структуру и свойства объемных нанокристаллических веществ и материалов начали изучать после 1985 г.
Понятие о наноматериале нельзя смешивать с другим широко распространенным понятием о субмикрокристаллических материалах, которые по свойствам также отличаются от крупнокристаллических, крупнозернистых и монокристаллических веществ. Это отличие связано в основном с повышенной удельной поверхностью, что приводит к ускорению различных процессов с их участием, но не ведет к уменьшению энергии активации (т. е. снижению температур начала реакций). Между наноматериалами и субмикрокристаллическими материалами существует принципиальная разница.
Именно наносостояние, а не субмикрокристаллическое является промежуточным молекулярным состоянием твердого тела. На нанометровых расстояниях формируются свойства твердого тела. В этом же заключается физическая причина того, что значительное изменение свойств наблюдается в нанометровом масштабе.
Наноматериалы часто называют нанокристаллическими, но это не всегда верно. Наноматериалы, как правило, являются термодинамически неравновесными системами, и их «строительные» блоки не обязательно обладают совершенной кристаллической структурой, а, наоборот, могут иметь сильно дефектную, а иногда аморфную структуру. Более точно наноматериалы должны называться наноструктурированными материалами.
Появление во второй половине XX в. высокоразрешающих методов изучения строения вещества (ЯМР, электронная и атомно-силовая микроскопия, специальная техника для измерения очень малых поверхностных натяжений, компьютерное моделирование, фотон-корреляционная микроскопия и ряд других) позволило перейти к исследованию строения и свойств ультрадисперсных коллоидных систем, в том числе наносистем.
По геометрическому признаку наносистемы можно разделить на три группы:
- трехмерные (объемные) наночастицы, у которых все три размера находятся в наноинтервале; эти частицы имеют очень небольшой радиус кривизны. К таким системам относятся золи, микроэмульсии, зародышевые частицы, образующиеся при фазовых переходах 1-го рода (кристаллы, капли, газовые пузырьки, сферические мицеллы ПАВ в водных и неводных средах (прямые и обратные мицеллы);
- двухмерные (тонкие пленки и слои) наночастицы, у которых только один размер (толщина) находится в наноинтервале, а два других (длина и ширина) могут быть сколь угодно велики. К этим системам относятся жидкие пленки, моно - и полислои на поверхности раздела фаз (в том числе пленки Ленгмюра–Блоджетт), двухмерные пластинчатые мицеллы ПАВ;
- одномерные наночастицы, у которых поперечный размер находится в наноинтервале, а длина может быть сколь угодно велика. Это тонкие волокна, очень тонкие капилляры и поры, цилиндрические мицеллы ПАВ и имеющие с ними большое сходство нанотрубки.
В литературе принята следующая классификация наноматериалов:
- 0D – надкластерные материалы и нанодисперсии с изолированными наночастицами;
- 1D – нановолоконные и нанотубулярные, причем длина волокон или трубок составляет менее десятков микрон;
- 2D – пленки нанометрической толщины;
- 3D – поликристалл с нанометрическим размером зерен, в котором весь объем заполнен нанозернами, свободная поверхность зерен практически отсутствует. К трехмерным материалам относят порошки, волоконные, многослойные и поликристаллические материалы, в которых 0D-, 1D-, и 2D-частицы плотно прилегают друг к другу, образуя между собой поверхности раздела – интерфейсы. Получению 3D-материалов последние 20 лет уделяют особое внимание, именно их будут применять при разработке твердых сплавов, в авиастроении, водородной энергетике и других высокотехнологичных отраслях промышленности.
Кроме размера частиц, при работе с наноматериалами важна проблема, связанная с взаимодействием изолированных единичных частиц между собой, так как взаимодействие двух и более частиц может вызвать существенное изменение свойств материала или появление нежелательных характеристик, например при их изготовлении или эксплуатации. Подавить взаимодействие частиц можно с помощью второй фазы, которая удерживает дистанцию между частицами, создавая системы типа ядро – оболочка или так называемые нанокомпозиты.
Нанокомпозиты – композитный материал, содержащий по крайней мере одну фазу, имеющую особые свойства наноматериала.
Давно известный и очень важный тип нанокомпозита имеет частицы более или менее сферической формы, распределенные в матрице. Классическим примером нанокомпозита этого типа является рубиновое стекло, где наночастицы золота распределены в стеклянной матрице. Во многих случаях матрица и наночастицы проявляют взаимную растворимость, в этом случае необходимо создать диффузионный барьер вокруг каждой наночастицы (рис. 2).
При получении композитов главной проблемой является достижение хорошего распределения двух фаз. Процессы, основанные на механическом смешении, никогда не обеспечивают гомогенность распределения наночастиц. Подобным образом нельзя получить гомогенное распределение, синтезируя две фазы по отдельности и смешивая их во время образования частиц. В обоих случаях вероятность контакта двух и более частиц друг с другом очень велика. Если предположить, что наночастицы имеют одинаковый размер, вероятность столкновения частиц Рп = Сп, где п – количество частиц, С – объемная концентрация частиц.
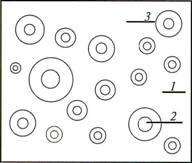
Рис. 2. Схематическое изображение 0-размерного нанокомпозита: 1 – матрица, 2 – наночастицы, 3 – диффузионный барьер
Предполагая, что концентрация С = 0,30, получаем вероятность столкновения двух частиц 0,09, а для трех частиц 0,027.
Необходимое хорошее распределение двух фаз получается только при закрытии поверхности частиц активной фазы оболочкой, которая способна поддерживать дистанцию между наночастицами. Достигается это различными методами, которые будут рассмотрены ниже. Типичным примером является покрытие наночастиц диоксида циркония аморфным оксидом алюминия. Необходимым условием является отсутствие взаимной растворимости веществ ядра и оболочки и сохранение нанометрического диапазона для частиц с оболочкой. Материал покрытия может быть как неорганическим, так и полимерным (органическим). Покрытие может быть получено нанесением нескольких слоев, причем слои могут иметь различную природу, что позволяет комбинировать свойства материалов, находящихся в одной частице. Путем выбора соответствующего полимера для самого дальнего слоя на частице можно определить ее поведение в окружающей среде и придать необходимые свойства, например гидрофобность или гидрофильность.
Покрытые оболочками наночастицы представляют собой наиболее прогрессивный тип нанокомпозитов, поскольку они позволяют, во-первых, комбинировать различные свойства в одной частице и, во-вторых, регулировать расстояние между смежными частицами в случае их сближения.
На рис. 3 приведены три основных типа нанокомпозитов, в которых наночастицы распределены в матрице другой фазы.
На рис. 4 приведен нанокомпозит с регулярной структурой. Этот тип композита создается в самоорганизующихся процессах. Успешная реализация таких процессов требует получения почти идентичных по размеру частиц.
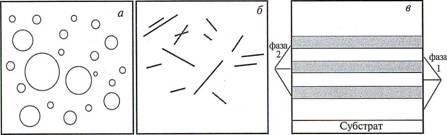
Рис 3. Три основных типа нанокомпозитов: а – композит, состоящий из 0-размерных частиц, распределенных в матрице. Идеально изолированные частицы не соприкасаются; б – одноразмерные частицы нанокомпозита, состоящие из нанотрубок или нанопалочек, распределенных в матрице; в – двухмерные нанокомпозиты, построенные из тонких пленок двух и более разных материалов

Рис. 4. Нанокомпозит с регулярной структурой
К наноматериалам относятся также так называемые наноструктурированные материалы, например фуллерены и углеродные нанотрубки.
Фуллерены относятся к молекулярным кластерам – новой структурной модификации вещества – и занимают особое место среди веществ, имеющих наноструктуру. Они представляют собой полые сферические поверхности из пяти - и шестичленных колец (рис. 5).
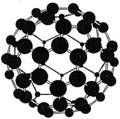
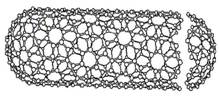
Рис. 5. Структуры молекулы фуллерена С60 и углеродной трубки
Классический фуллерен содержит 60 атомов углерода. Он представляет собой сферическую структуру, на поверхности которой шестичленные кольца связаны между собой пятичленными циклами. Путем внедрения внутрь фуллерена атомов металлов можно получать новые ценные свойства материалов, например сверхпроводимость. Однослойные и многослойные нанотрубки образуются в результате свертывания полос плоских атомных сеток графита в бесшовные цилиндры. Заполнение внутренних полостей нанотрубок проводится разными методами и открывает возможности получения совершенно новых свойств. Известны молекулярные кластеры с фуллереноподобной структурой C48N12, кластеры типа М8С12, где М – Zr, Hf, V, Cr, Mo, Fe, которые называют металлокарбогедренами или меткарами. Атомы металла и углерода в них образуют структуру, подобную клетке.
ЛЕКЦИЯ 2.
МЕТОДЫ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННЫХ ВОДНЫХ ЭМУЛЬСИЙ ПОЛИМЕРОВ.
Методы получения наночастиц отличаются от обычных технологических процессов получения дисперсных систем методическим подходом. В зарубежной литературе эти методы делятся на две группы: «top-down» – «сверху вниз», т. е. уменьшение размеров, измельчение, и «bottom-up» – «снизу вверх», т. е. создание наноструктур из более мелких исходных компонентов, точнее из атомов и молекул.
К методам получения наноструктурированных систем эмульсий (методам синтеза) относятся следующие:
- получение коллоидных растворов целевых веществ с помощью химических реакций при смешивании растворов реагентов в специальных условиях. Используются реакции обмена, гидролиза, восстановления, окисления. При проведении реакции в сильно разбавленных растворах и в присутствии избытка одного из компонентов образуется коллоидный раствор, из которого выделяют коллоидные или наночастицы;
- получение наноструктурированного материала методом послойного электрохимического осаждения из растворов;
- получение наночастиц и наноструктурированных материалов методом самосборки (спонтанная ассоциация двух и более компонентов за счет межмолекулярного взаимодействия) и самоорганизации (многокомпонентная межмолекулярная упорядоченная самоассоциация);
МЕТОД ОСАЖДЕНИЯ ИЗ РАСТВОРОВ
Метод химического осаждения из растворов основан на реакции, происходящей в водном растворе или в среде органического растворителя. На ход реакции существенно влияют температура растворов, pH среды, последовательность введения компонентов, их концентрация и другие факторы. Этот метод широко распространен и применяется для синтеза высокодисперсных порошков, а также сплошных и дискретных пленок. При получении наночастиц из образовавшегося коллоидного раствора особенно важным моментом является прерывание химической реакции в определенный момент времени, после чего систему переводят из жидкого (коллоидного) состояния в твердое, избегая коагуляционных процессов, приводящих к агломерации.
Для предотвращения агломерации частиц применяют поверхностно-активные вещества (ПАВ). Цепочки адсорбированных ПАВ препятствуют межмолекулярному контакту. Особенно важно использование ПАВ при высокой концентрации частиц. В разбавленных суспензиях агломерацию можно предотвратить, применяя электростатическое отталкивание. Контролируемое введение электролита создает двойной электрический слой, и агломерация предотвращается, когда силы электростатического отталкивания превосходят силы ван-дер-ваальсова притяжения.
Методом химического осаждения получают наночастицы металлов, для чего в кислый раствор вводят восстановитель. Осаждение из водных коллоидных растворов применяется для получения различных халькогенидов металлов, обладающих полупроводниковыми свойствами. Для получения наночастиц сульфидов металлов заданного размера в качестве сульфидизатора (донора серы) применяют диамид тиоугольной кислоты (тиомочевину) и ее производные, например тиокарбазид, тиоацетамид, а также тиосульфат и сульфид натрия. Например, наноструктурированный сульфид кадмия получают по реакции
Cd(ClO4)2 + Na2S → CdS + 2NaClO4
Рост наночастиц можно прервать путем скачкообразного увеличения pH раствора.
Для каждого конкретного случая подбирается определенная скорость формирования частиц, что влияет на свойства образующегося порошка или пленки на подложке. Для получения особо малых частиц должна быть очень быстро приготовлена затравка (центр кристаллизации), а рост частиц затравки, напротив, должен быть замедлен. При осаждении рост частиц, их кристалличность и морфология регулируются кинетикой реакции.
При исследовании осадков сульфида кадмия, диоксида титана и диоксида кремния обнаружена различная самоорганизация наночастиц. Механизм этого процесса до конца не выяснен, однако установлено, что силы взаимодействия наночастиц приводят к их самоорганизации и упорядочению в одно-, двух - и трехмерные ансамбли. В качестве таких сил рассматривают силы Ван-дер-Ваальса, капиллярного, электростатического, стерического взаимодействия и др.
Сульфат-процесс получения наночастиц диоксида титана при осаждении в жидкой фазе является конкурентным по отношению к газофазному методу (хлоридный способ синтеза диоксида титана).
МИКРОЭМУЛЬСИОННЫЙ МЕТОД
В этом конденсационном методе химическое осаждение или золь-гель-реакции проводятся в эмульсионных каплях. Использующиеся для этих целей микроэмульсии – термодинамически стабильные изотропные дисперсии двух несмешивающихся жидкостей. При смешивании таких жидкостей капли одной из них, стабилизированные межфазной пленкой ПАВ, распределяются в другой. Термодинамическая стабильность микроэмульсионных систем обусловлена низким межфазным натяжением.
В зависимости от того, какая фаза является дисперсной, а какая непрерывной, микроэмульсии могут быть прямыми (масло в воде) или обратными (вода в масле). В обоих случаях дисперсная фаза состоит из капель размером не более 100 нм. Микроэмульсии обладают большой подвижностью. Имея большую поверхность раздела фаз, они являются универсальной средой для проведения различных химических процессов, в том числе получения твердых наночастиц. В микроэмульсии компоненты дисперсной фазы постоянно сталкиваются, коалесцируют и разрушаются вновь, что приводит к непрерывному обмену их содержимым. Процесс столкновения нанокапель или мицелл определяется их диффузией в масляной среде для обратных мицелл.
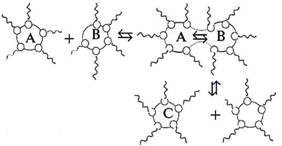
Рис. 1. Микроэмульсионный способ синтеза труднорастворимого вещества С из водных фаз А и В в обратной эмульсии
Обратные мицеллы и обратные эмульсии широко используются для синтеза нанокластеров. Внутренний объем обратной мицеллы в этом случае является нанореактором для проведения химических реакций получения нанокластеров. Синтез осуществляется следующим образом. Приготавливают две идентичные обратные микроэмульсии, водные фазы которых содержат два разных вещества, образующих при взаимодействии заданный осадок. После смешения таких эмульсий в результате обмена веществ при коалесценции мицелл образуются наночастицы нового вещества (рис. 1).
Так, например, для получения сульфида серебра Ag2S используют смеси двух типов обратных мицелл, водные фазы которых содержат сульфид натрия и ион серебра соответственно. Благодаря столкновению таких мицелл происходит коалесценция и обменная реакция с образованием сульфида серебра, причем размер частиц ограничен размером капли. Размер образующихся кластеров сульфида серебра увеличивается с ростом капель воды от 3 до 5,8 нм.
Для освобождения нанокластера от мицеллы ее разрушают тиолами, после чего осадок фильтруют и выпаривают, размер полученных нанокластеров составляет до 10 нм.
Микроэмульсионным методом, как правило, получают нанокластеры металлов, для чего на микроэмульсию, содержащую соль металла, воздействуют восстановителем. Так были получены нанокластеры Pt, Pd, Rh, Ir с размером частиц 3–5 нм. С помощью микроэмульсионного метода получены также нанокластеры CdS, CdSe, CdTe, SnO2, ТO2, Fe2O3,MoS2 HgS, InAs, GaP, GaAs, SiO2 и др.
ЛЕКЦИЯ 3.
МОДИФИКАЦИЯ НАНОЧАСТИЦ
Для обеспечения гомогенного распределения наночастиц в среде необходима их стабилизация. Например, чтобы суспензия была устойчивой, твердые частицы в ней должны постоянно находиться в броуновском движении. Для этого они должны быть защищены от агломерации. Как известно, такой защите способствует поверхностная модификация, которую традиционно осуществляют путем физической адсорбции или химической обработки таким образом, что новый материал оказывается «прикрепленным» к поверхности, что приводит к образованию непрерывной внешней оболочки. Стабилизация частиц может быть электростатической (только для водных растворов), стерической (в основном для растворов в органических растворителях, при этом адсорбирующиеся полимерные молекулы очень увеличивают диаметр частиц, поэтому предпочтительно использование короткоцепных карбоновых кислот), третий способ стабилизации – электростерическая – объединяет первые два и заключается в образовании на поверхности частицы слоя заряженных молекул, в связи с чем создается также и пространственная защита. На рис. 1 схематически изображены частицы, стабилизированные различными способами.
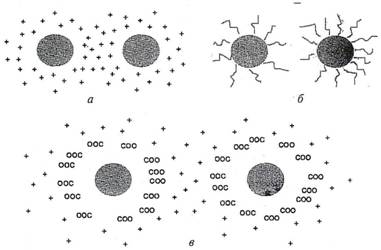
Рис. 1. Способы стабилизации частиц: а – электростатический, б – стерический, в – электростерический
Размер частиц сильно влияет на стабильность коллоидной системы. Наноразмерные частицы по сравнению с частицами микронных размеров по-иному флокулируют. Следовательно, механизм достижения их коллоидной стабильности будет иным.
Существует баланс между энергией, которая определяет стабильность коллоидной системы, и энергией, вызывающей коагуляцию. На рис. 2 приведены кривые зависимости энергии взаимодействия между частицами от расстояния между ними для частиц разного размера. Из коллоидной химии известно, что обычно барьер 15–20 кТ достаточен для коллоидной стабильности (кТ = 4,11 х 10-21 Дж).
Из данных рис. 2 видно, что вторичный минимум на кривых глубже для крупных частиц, что может привести к слабой флокуляции. Для наночастиц, наоборот, вторичный минимум мельче, и потому репептизация будет происходить легче. Кроме того, высота барьера снижается с уменьшением размера частиц. Это означает, что наночастицы более склонны к коалесценции. Известно также, что критическая концентрация электролита, вызывающая коагуляцию, быстро понижается с уменьшением размера частиц. Следовательно, для меньших частиц необходим более высокий потенциал, чтобы получить ту же энергию разделения. С другой стороны, чем больше частицы, тем они более устойчивы к коалесценции, так как «барьер» на кривой более высок. Однако первичный минимум, ассоциирующийся с коагуляцией, наоборот, меньше для наночастиц. Таким образом, стабилизация адсорбированными полимерами, ПАВ или хемосорбцией комплексообразующих агентов для них гораздо более эффективна, чем для более крупных частиц. Небольшие молекулы должны быть достаточны, чтобы предотвратить коалесценцию наночастиц. Это означает, что стерический барьер, создаваемый хемосорбированными молекулами для частиц размером менее 10 нм, достаточен для компенсации ван-дер-ваальсова взаимодействия, приводящего к коагуляции в первичном минимуме. Однако, если две частицы такого размера коалесцируют в растворе, они не будут способны разделиться вновь, так как их термальной энергии будет недостаточно, чтобы выйти из первичного минимума.
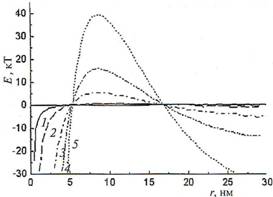
Рис. 2. Зависимость полной энергии взаимодействия частиц Е от расстояния между ними r для частиц разного размера: 1 – 2 нм, 2– 10 нм, 3 – 70 нм, 4 – 200 нм, 5 – 500 нм
Таким образом, поверхностная модификация с целью увеличения заряда поверхности и в свою очередь потенциала является мощным средством для обеспечения коллоидной стабильности наночастиц в полярных растворителях, где адсорбция органических макромолекул не очень эффективна.
ПОЛИМЕРНЫЕ ПОКРЫТИЯ
Поверхностная модификация наночастиц большей частью проводится путем адсорбции на поверхности частиц мономера с последующей его полимеризацией, гетерокоагуляционной или эмульсионной полимеризацией. Органические полимерные оболочки успешно применяют для капсулирования металлических наночастиц. В принципе они могут быть применены и к частицам оксидов металла, но при этом встречаются затруднения, например растворимость в некоторых органических растворителях или повышенная чувствительность к высокотемпературному процессу.
Оболочки из диоксида кремния. Одной из основных причин применения этого соединения является высокая стабильность коллоидов SiO2, особенно в водной среде; легкость контроля процесса осаждения, в том числе толщины оболочки; химическая инертность, возможность регулирования пористости и оптической прозрачности. Все это делает SiO2 идеальным и дешевым материалом для поверхностной обработки и изменения поверхностных свойств, в то время как основные физические свойства материала определяются нижележащим ядром. Действие ядра проявляется при сближении двух сферических частиц путем возникновения сил Ван-дер-Ваальса, преобладающих при толщине оболочки SiO2 менее нескольких нанометров. Было обнаружено, что золи диоксида кремния с размером частиц 10–100 нм обладают стабильностью при очень высокой концентрации солей в растворе (например, 0,15М NaCl) даже в изоэлектрической точке. Основная причина очень высокой стабильности золей SiO2 заключается в том, что на поверхности раздела диоксид кремния/вода при pH более 10,5 присутствует полимерный силикатный слой, в котором катионы, особенно ионы одновалентных металлов, сильно гидратированы и очень прочно связаны. Силикатный слой обусловливает как стерическую, так и электростатическую защиту частиц диоксида кремния при pH выше изоэлектрической точки и ниже 10,5.
Хотя свойства ядра, покрытого слоем диоксида кремния достаточной толщины, не проявляются, существуют задачи, для решения которых необходима их коагуляция, например для многих целей необходимы 2D и 3D кристаллы, способные диспергироваться. Это свойство может быть обеспечено при использовании диоксида кремния в качестве капсулирующей оболочки. Процесс капсулирования применялся давно для различных частиц, но только в последнее время его стали адаптировать к наночастицам.
Покрытие очень мелких частиц затруднено из-за их очень большого радиуса кривизны. Процесс капсулирования может быть осуществлен при очень незначительной тенденции материалов оболочки и ядра связываться друг с другом. Для этого поверхность наночастиц на первой стадии обрабатывается силанами, в результате чего на ней остаются силанольные группы. Затем из раствора силиката натрия медленно осаждают тонкую оболочку диоксида кремния. Для создания оболочек на металлических частицах, например на полупроводниковых частицах типа CdS, CdSe, CdTe, в качестве силанового агента можно использовать аминосилан или меркаптосилан.




