Лекция 7. Инструментальные методы определения изотопа 15N
(3 часа)
МАСС - СПЕКТРОМЕТРИЯ
А. ПРИНЦИП МЕТОДА
Масс-спектрометр, разработанный исключительно для анализа газов, состоит из пяти блоков (рис. 6.6): 1) системы ввода для введения газообразного азота; 2) источника ионов, где молекулы азота, бомбардируемые электронами, приобретают заряд и ускоряются; 3) магнитного поля, в котором заряженные молекулы разделяются по траекториям в зависимости от их удельного заряда или масс, как показано на рис. 6.6, где mi<m2<m3; 4) коллектора на конце трубки, где собираются ионы и увеличивается сила тока; 5) самописца, который регистрирует токи в виде пиков по мере сканирования диапазона масс. Высоты пиков пропорциональны потокам трех молекул — 28N2, 29N2 и 30N2 в газовой смеси. Простым измерением высоты пиков определяют степень обогащения 15N. Хотя принцип метода и прост, практическое применение масс-спектрометрии весьма сложно. Во всей системе должен поддерживаться глубокий вакуум, а электронные блоки должны быть хорошо стабилизированы. Если подобные приборы не контролируются высококвалифицированным персоналом, легко могут возникать артефакты.
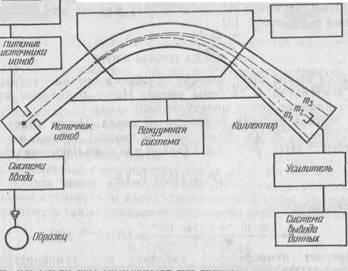 Рис. Схема масс-спектрометра для анализа газов
Рис. Схема масс-спектрометра для анализа газов
Существуют различные типы масс-спектрометров. Чаще других для анализа азота применяется масс-спектрометр с однократной фокусировкой, изображенный на рис. 6.6. Для специальных исследований могут потребоваться масс-спектрометры с двойной или циклоидальной фокусировкой. Последние известны как ква-друпольные спектрометры.
Образец газа вводят в систему ввода с пониженным давлением. Газообразный образец попадает в источник ионов. Образующиеся ионы пролетают через ускоряющие щели и превращаются в ионный пучок. В магнитном поле ион перемещается по круговой траектории с радиусом, являющимся функцией отношения его заряда к массе. Разложенный пучок ионов фокусируется на детекторе (ионной ловушке), возникающий ток усиливается и регистрируется.
В ходе ускорения в разности потенциалов V ион получает кинетическую энергию. Все ионы, имеющие одинаковый заряд, ускоряются до одного и того же энергетического уровня. В магнитном поле с направлением индукции, нормальном к направлению движения, ионный пучок отклонится по круговой траектории.
Для описания этих взаимодействий используют уравнение
![]()
где г — радиус отклонения, см; В — магнитная индукция, Гс; М — масса иона, дальтон; V — напряжение, приложенное к электроду ионного источника; п — электрический заряд иона, как правило, равный 1.
Б. МАССА ПРОБЫ АЗОТА
Масса пробы азота зависит от объема предназначенного для него контейнера и системы ввода. Ниже приведены примеры систем ламинарного и молекулярного ввода.
1. Мягкая система ламинарного ввода. Пусть объем сосуда с образцом Vb 30мл, объем системы ввода Vis 15 м, а давление Рis 40 10-6 МПа; рV = const (закон для идеального газа). Тогда


образца до рабочего давления,0,01 10 -6 МПа. Такое давление необходимо для обеспечения постоянного потока газа к источнику ионов, где поддерживается давление ~ 10 -9 МПа. Система ввода образца включает вакуумную систему, к оторой присоединяютяс газовые образцы.
КОЛЛЕКТОРНЫЕ СИСТЕМЫ
Часть масс-спектрометра, с помощью которой измеряют интенсивность потоков ионов, называется коллектором. В масс-спектро-метрии применяются одиночные и двойные коллекторы.
278 |
1. Одиночные коллекторы. На рис. 6.10 показан принцип действия одиночного коллектора, известного как ловушка Фарадея. Через заземленную разрешающую или коллекторную диафрагму, ширина которой должна обеспечивать необходимое разрешение для высоких значений т/е, пучок ионов проходит до противо-патронной диафрагмы, на которой поддерживается потенциал
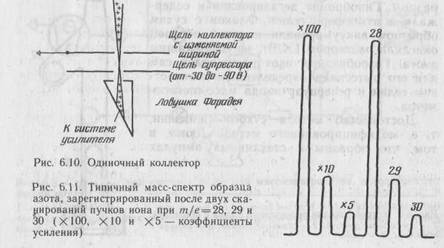
между —30 и —90 В. Функция последней заключается в предупреждении детектирования вторичных электронов, испущенных коллектором. Усиленный сигнал регистрируется как мера ионной интенсивности пучка при соответствующем значении т/е. При т/е = 28 пучок наряду с азотом может содержать СО и С2.Н4, следовательно, фон должен быть измерен перед введением образца, что позволит скорректировать нежелательные компоненты. На рис. 6.11 показана типичная запись спектра обогащенного образца.
МЕТОДЫ ПРИГОТОВЛЕНИЯ ОБРАЗЦА
... •
А. ПРЕВРАЩЕНИЕ В ГАЗООБРАЗНЫЙ АЗОТ
Для определения отношений I4N:15N необходимо все атомы азота образца превратить в единственное соединение. Как для масс-спектрометрии, так и для эмиссионной спектрометрии предпочтительно использование газообразного азота по следующим причинам:
1) из неорганических и органических соединений намного
легче получать N2, чем NO, NO2 или NH3. Азот, полученный в
виде газа, легко отделяется от остальных компонентов образца;
2) газообразный азот инертен в отношении всех материалов,
обычно использующихся в эмиссионной и масс-спектрометрии;
3) интерпретация изотопных данных проста, поскольку отсутствуют' помехи со стороны других элементов. В случае NO,
например, масс-спектроскопический пик I4N17O+ был бы идентичен
пику 15Ni6O+. Азот, связанный в виде органических и неорганических веществ, может быть переведен в газовую форму тремя
методами. Один метод основан на модификации расщепления
по Кьельдалю [38]. Расщепление образца осуществляется в
серной кислоте с добавлением пероксида водорода или другого
подходящего катализатора. Органический и неорганический азот переходят в аммиак. Аммиак извлекают путем перегонки с паром этой содержащей кислоту смеси, к которой добавлен избыток гидроксида натрия. Газообразный аммиак улавливается с помощью стандартного раствора соляной кислоты. Для определения общего содержания азота избыток кислоты оттитровывают раствором гидроксида натрия. Титрованный раствор подкисляют соляной кислотой и выпаривают до небольшого объема. Азот образца превращают в N2 с помощью метода Риттенберга [60], который включает окисление аммиака в экстракте гипобромитом натрия согласно следующей реакции:
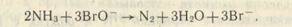
Образующийся газообразный азот можно 'использовать в эмиссионной и масс-спектрометрии.
Второй метод основан на модификации реакции Дюма [16]. Этот метод включает сухое окисление органических и (или) неорганических азотсодержащих соединений с окисью меди, медью или их смесью.
При этом могут происходить следующие реакции:
|
Вода и диоксид углерода, образовавшиеся при окислении, абсорбируются на оксиде кальция. Реакция Дюма может быть осуществлена многими путями. Модифицированная процедура Дюма позволяет превратить весь связанный азот в газ. Измерение давления позволяет определить общее содержание азота в том же образце, в котором анализируется обогащение 15N. Можно также использовать комбинацию методов Кьельдаля и Дюма. С помощью этого комбинированного метода аммиак, получающийся в результате расщепления по Кьельдалю, превращается в азот в результате окисления по Дюма.
Метод превращения азотсодержащих соединений и материалов в газообразный азот должен быть простым и требовать минимума усилий и времени. Разбавление 15N в результате перекрестного загрязнения, которое будет изменять степень обогащения образца 15N, должно быть сведено к минимуму. Использование хорошо перемешанных тонко измельченных материалов сводит ошибки предварительного отбора образца к минимуму. Потенциальная негомогенность сельскохозяйственных образцов требует, чтобы размер предварительно отобранных образцов был возможно большим. Отбор образца в большем количестве, чем это необходимо для анализа,,снижает возможность разбавления или. загрязнения в результате микроутечек или эффектов памяти и уменьшает ошибки отбора образца. Дальнейшая последовательность операций рассмотрена в работе Фидлера и Прокша [25]. Краткий обзор упомянутых методов дан ниже.
Б. МЕТОД КЬЕЛЬДАЛЯ — РИТТЕНБЕРГА
Метод был предложен Риттенбергом [60]. Метод Кьельдаля применяется для превращения азота образца в аммиак, который перегоняют в среду с соляной или серной кислотой. После концентрирования кислого дистиллята аммиак окисляется до азота щелочным раствором гипобромита натрия в вакууме. Анализ включает следующие стадии: 1) расщепление образца концентрированной серной кислотой; 2) отделение аммиака перегонкой после добавления щелочи: 3) определение аммиака обратным титрованием, колориметрией и т. п.; 4) подкисление; 5) выпаривание до небольшого объема: 6) окисление аммиака до азота.
ЭМИССИОННАЯ СПЕКТРОМЕТРИЯ
А. ПРИНЦИП МЕТОДА
В эмиссионной спектрометрии внешний источник энергии используется для перевода молекул азота в возбужденное состояние. Возбужденные молекулы возвращаются в нормальное состояние, и разница в энергиях дает электромагнитное излучение специфической энергии. Для измерения используются небольшие различия в длине волны света, испускаемого возбужденными молекулами газообразного 28N9, 29N2 и 30N2. Испущенный свет разделяется с помощью монохроматора, и измеряется его интенсивность. Высоты зарегистрированных пиков, соответствующие интенсивности испускаемого излучения, позволяют рассчитывать атомный процент обогащения I5N,. как это делается при использовании масс-спектрометрии.
На рис. 6.15 приведена блок-диаграмма эмиссионного спектрометра, состоящего из: 1) микроволнового (высокочастотного) силового генератора для возбуждения образца в безэлектродных разрядных трубках; 2) стенда возбуждения, имеющего антенну или полость, в которой фиксируется трубка с образцом для переноса энергии от генератора к газообразному азоту; 3) прерывателя для предотвращения влияния других источников света;
4) монохроматора для разделения света различных длин волн;
5) линзы для фокусировки света во входном окне монохроматора:
6) фотоумножителя и усилителя для преобразования квантов
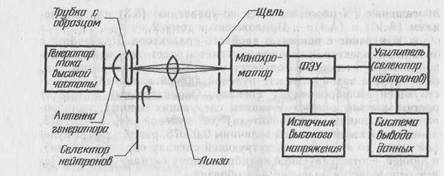
Рис. 6.15. Схема эмиссионного спектрометра для анализа I5N
света в электрические сигналы и 7) самописца или цифрового интегратора с пишущим устройством для превращения электрических сигналов в световые. Измерение высот пиков для расчета степени обогащения I5N осуществляется, как и в масс-спектро-метрии.
По сравнению с масс-спектрометрией эмиссионная спектрометрия гораздо проще. Для нее не требуется глубокий вакуум, прибор может быть смонтирован и поддерживаться в рабочем состоянии любым квалифицированным аналитиком.
Б. ТЕОРИЯ МОЛЕКУЛЯРНЫХ СПЕКТРОВ
Изотопные молекулы несколько различаются по своим энергетическим уровням, следовательно, возможно проводить изотопный анализ с помощью эмиссионной спектрометрии.
При поглощении атомами энергии один или несколько орбитальных электронов переходят в более высокое энергетическое состояние. Когда электроны возвращаются в нормальное состояние, поглощенная энергия испускается в виде электромагнитного излучения определенной длины волны. Атомные или линейные спектры формируются, если каждая линия является следствием дискретного различия энергий. Энергетические различия для идентичных переходов изотопов достигают сотен нанометров. Для рассматриваемых здесь двухатомных молекул имеется пять путей, по которым может поглощаться энергия, но для спектрометрических целей представляют интерес лишь вибрационная и вращательная энергия электронов.
Поглощение (или запасание) энергии может происходить путем: 1) перехода одного или большего числа электронов на более высокие орбиты, как и в случае атомов; 2) увеличения колебаний (осцилляции) двух атомов по межъядерным осям и
3) увеличения вращения молекулы вокруг оси, проходящей через центр тяжести, перпендикулярной межъядерной оси. Каждое изменение энергии, наблюдаемое в настоящем процессе, может быть объяснено комбинацией этих трех видов запасания энергии.
Переходы между двумя электронными состояниями, в том числе и вибрационные, дают линейный спектр, как и в случае атомов. Однако переходы между ротационными уровнями имеют значительно меньшие энергетические различия. Спектр испускания состоит из ряда полос, а поскольку вероятность переходов неодинакова, полосы имеют разную интенсивность. В случае азота наибольшую интенсивность имеет полоса 0—0 (рис. 6.16).
Различия в массе изотопных молекул проявляются главным образом в вибрационной и вращательной энергии (поскольку здесь принимают участие моменты инерции).
Изотопный сдвиг для вибрационного перехода 0—0 очень невелик или равен нулю (в случае 28N2 и 29N2 всего 0,011 нм), но становится более значительным с увеличением порядка вибрационного перехода. В то же время интенсивность полос быстро снижается, и следует найти компромисс между повышением изотопных эффектов и снижением интенсивности. Для 28N2 обычно выбирают переход 2—0 [9, 29, 32, 40, 53]. Этот переход имеет дополнительное преимущество, состоящее в отсутствии мешающих определению полос от загрязнений, за исключением полосы при 297,6 нм от оксида углерода [49].
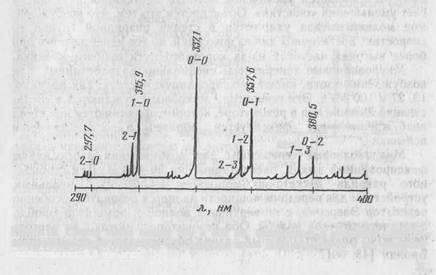 Длины волн полос трех изотопных молекул азота составляют 297,7 нм для 28N2, 298,3 для 29N2 и 298,9 нм для 30 N2. В обзоре [51 ] указываются другие полосы, использовавшиеся некоторыми исследователями. Бэрридж и Хьюитт [73] использовали переход 1—0 при длине волны 315,9 нм для определения природного атомного процента обогащения N-15 и более низких величин обогащения.
Длины волн полос трех изотопных молекул азота составляют 297,7 нм для 28N2, 298,3 для 29N2 и 298,9 нм для 30 N2. В обзоре [51 ] указываются другие полосы, использовавшиеся некоторыми исследователями. Бэрридж и Хьюитт [73] использовали переход 1—0 при длине волны 315,9 нм для определения природного атомного процента обогащения N-15 и более низких величин обогащения.



