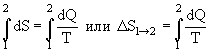ЛЕКЦИЯ №16
по учебной дисциплине «ФИЗИКА»
Занятие № 7/4. Круговой процесс
Краснодар 2011
Раздел II. Молекулярная физика и термодинамика
Тема № 7. Основы термодинамики
Лекция № 16. «Круговой процесс».
ИЗУЧАЕМЫЕ ВОПРОСЫ :
1. Круговой процесс(цикл). Работа газа за цикл. КПД цикла. Обратимые и необратимые процессы.
2. Цикл Карно. Максимальный КПД тепловой машины.
3. Привёденная энергия. Понятие энтропии. Принцип возрастания энтропии и вероятность. Второе начало термодинамики.
ЦЕЛЬ :
Изучить второе начало термодинамики
ОБЕСПЕЧЕНИЕ :
- разработка занятия № 31 ;
- цветной мел, доска.
ЛИТЕРАТУРА : [1] с. 111- 118.
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
Во вводной части указать на важность изучения второго начала термодинамики для специалиста в области авиационной техники, а также показать связь с материалом предыдущих лекций.
В основной части достигается поставленная цель.
В заключение дать краткое повторение изучаемого материала
2
Вопрос1. Круговой процесс(цикл). Работа газа за цикл. КПД цикла. Обратимые и необратимые процессы
Первое начало термодинамики Q = dU + A устанавливает точное соотношение между количеством теплоты, сообщаемой системе, изменением ее внутренней энергии и работой, выполняемой системой.
Первое начало является всеобщим законом природы и справедливо для всех без исключения процессов, в том числе и для процессов в микромире, а также для неравновесных состояний.
С точки зрения первого начала термодинамики не ясно, в каком направлении могут идти процессы изменения состояния.
Если система совершает круговой процесс (цикл), т. е. система, пройдя ряд промежуточных состояний, возвращается к исходному состоянию, то изменение внутренней энергии dU = 0 (внутренняя энергия – функция состояния). При этом
![]()
где знак означает ![]() – интегрирование по замкнутому контуру.
– интегрирование по замкнутому контуру.
Здесь количество теплоты связано с микроскопическими движениями атомов и молекул вещества. Механическая работа, как правило, обусловлена макроскопическим движением (перемещением) тела.
Опыт показывает, что энергия макроскопического движения может целиком переходить в энергию микроскопических движений молекул (тепловую энергию) самопроизвольно. Обратный процесс сам по себе, т. е. самопроизвольно, не происходит. Что управляет таким направлением процессов? Cведений об этом в первом начале не содержится.
Эту проблему решает только второе начало термодинамики и, в частности, энтропия.
Второе начало термодинамики связано с обратимыми и необратимыми процессами, с понятием термодинамического равновесия.
В механике равновесием называется такое состояние тела, при котором оно находится в покое. В термодинамике понятие равновесия иное.
3
Система находится в термодинамическом равновесии, если макроскопические параметры, определяющие ее состояние, остаются постоянными (и равными своим средним значениям). Параметры эти – давление, температура, плотность.
Термодинамическое равновесие в системе устанавливается за счет интенсивного теплового движения молекул, которое приводит к выравниванию температуры и давления во всем объеме системы.
Если система по каким–либо причинам не находится в состоянии равновесия или выведена из него, а затем предоставлена самой себе (нет внешних воздействий), то, как показывает опыт, эта система самопроизвольно совершает переход к равновесному состоянию. Но когда равновесие уже установилось, то система самопроизвольно возвратиться к первоначальному неравновесному состоянию уже не может, т. е. обратный переход от равновесного состояния к неравновесному без внешних воздействий невозможен, следовательно такой процесс необратим. Итак, всякая термодинамическая система, самопроизвольно стремится перейти к равновесному состоянию. О таком самопроизвольном направлении процесса в первом начале термодинамики не содержится никакой информации.
Обратимым процессом называется такое изменение состояния системы, которое при проведении в обратном направлении возвращает ее (систему) в исходное состояние, при этом система проходит через теже промежуточные состояния, что и в прямом процессе, но в обратной последовательности, а в окружающей среде не происходит никаких изменений.
Всякий процесс, не удовлетворяющий этим условиям, является необратимым. Любой равновесный процесс является обратимым.
Обратимыми процессами являются медленные процессы расширения и сжатия газа, заключенного в цилиндр с поршнем. Быстрые же процессы сжатия и расширения – необратимы.
Необратимыми являются диффузия, теплопроводность и внутреннее трение. Необратимыми являются расширение газа в пустоту, не уравновешенное внешними силами.
Вопрос2. 2. Цикл Карно. Максимальный КПД тепловой машины
Тепловым двигателем (машиной) называют длительно работающее устройство, позволяющее превращать тепловую энергию в механическую работу.
4
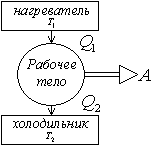
Рис. 2.34
Двигатели состоят из трех элементов:
1) рабочее тело (газ, пар и др.), заключенное в сосуд с поршнем;
2) нагреватель – резервуар, от которого рабочее тело получает определенное количество теплоты Q1 при температуре Т1;
3) холодильник – резервуар, которому рабочее тело отдает количество теплоты Q2 при температуре холодильника Т2.
Принципиальная схема теплового двигателя представлена на рис. 2.34. Чтобы тепловой двигатель работал длительное время, необходимо рабочее тело периодически возвращать в исходное состояние, т. е. должна производиться работа циклами (совершался круговой процесс). Рассмотрим реальный тепловой двигатель, работающий по прямому циклу (процесс совершается по часовой стрелке) представленному на рис. 2.35.
В качестве рабочего тела используется идеальный газ.
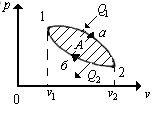
Рис. 2.35
Цикл можно разбить на 2 процесса:
1) процесс расширения (1–а–2);
2) процесс сжатия (2–б–1).
При расширении от нагревателя газ получает количество теплоты Q1. При этом за счет перемещения поршня будет выполнена положительная механическая работа А1, определяемая площадью фигуры 1 – а – 2 – V2 – V1 – 1.
5
Согласно первого начала термодинамики для этого процесса расширения имеем:
Q1 = (U2 – U1) + A1, | (2.55) |
где U2 – U1 – изменение внутренней энергии.
При сжатии от рабочего тела отдается холодильнику количество теплоты – Q2. При этом выполняется отрицательная работа А2, определяемая площадью фигуры 2 – б – 1 – V1 – V2 – 2.
Согласно первому началу термодинамики для процесса сжатия имеем:
– Q2 = (U1 – U2) – A2 | (2.56) |
Складывая почленно (2.55) и (2.56) , получим:
Q1 – Q2 = A1 – A2 = A, | (2.57) |
где А – положительная работа, выполненная газом за один цикл, равная площади, охватываемой замкнутой кривой цикла, показанного на рис. 2.35.
Работа, совершаемая за цикл, равна полученной газом извне теплоте: А = Q1 – Q2.
Работу теплового двигателя оценивают коэффициентом полезного действия – к. п.д.:
| (2.58) |
Формула (2.58) для к. п.д. справедлива для любого реального теплового двигателя. К. п.д. показывает, какая доля количества теплоты, полученного от нагревателя превращается в механическую работу. К. п.д. у реальных тепловых двигателей очень мал: порядка 10 % и менее. Поэтому одна из важнейших задач термодинамики заключается в том, чтобы найти путь повышения к. п.д.
6

Французский физик и инженер Сади Карно (1796–1832), проанализировав работу различных циклов, установил, что наиболее экономичным является цикл, состоящий из двух изотерм и двух адиабат. Этот процесс назван в честь физика – циклом Карно (рис. 2.36).
Рассмотрим прямой обратимый цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с поршнем. Двигатель, работающий по обратимому (прямому) циклу Карно, называется идеальным. Обратимость цикла Карно заключается в том, что если его работу провести в обратном направлении (против часовой стрелки), то у холодильника можно отнять теплоту Q2, израсходовать ту же самую работу А, совершаемую теперь внешними силами и вернуть нагревателю теплоту Q1 = Q2 + A , которая была взята у него при работе в прямом направлении. Таким образом, работающий двигатель по обратимому циклу Карно называется холодильной машиной.
В цикле Карно изотермическое расширение и сжатие представлены кривыми 1 – 2 и 3 – 4, а адиабатическое расширение и сжатие – кривыми 2 – 3 и 4 – 1. При этом рабочему телу (идеальному газу) в случае изотермического расширения при Т1 cообщается количество теплоты Q1. т. е. изменение энтропии S1–2 , равное приведенному количеству теплоты для этого процесса равно Q1/T1. В случае изотермического сжатия при температуре Т2 рабочее тело отдает холодильнику количество теплоты (– Q2). Изменение энтропии S3–4 , равное приведенному количеству теплоты этого процесса, равно (– Q2/T2 ). На адиабатических участках расширения 2 – 3 и сжатия 4 – 1 изменение энатропии равно нулю, т. е.
S2–3 = S1–4 =0.
При обратимом процессе, как известно, S = 0. Воспользуемся этим для нахождения к. п.д. идеальной тепловой машины.
В силу аддитивности энтропии для цикла имеем:
S = S1–2 + S2–3 + S3–4 + S4–1 = S1–2 + S3–4 = 0
![]()
Откуда:
7
![]()
Подставляя в формулу (2.58) для к. п.д. получим для идеальной тепловой машины,
| (2.59) |
Таким образом, к. п.д. идеальной машины Карно определяется только температурами нагревателя и холодильника. Идеальные машины могут иметь к. п.д. порядка 60 % , что значительно выше, чем у реальных.
Основываясь на втором начале термодинамики, Карно вывел следующие теоремы:
Первая теорема. К. п.д. идеальной тепловой машины зависит только от температуры нагревателя и холодильника и не зависит от рода рабочего тела.
Вторая теорема. Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей T1 и холодильников Т2, наибольшим к. п.д. обладают идеальные тепловые машины, т. е. работающие по циклу Карно.
В связи с работой тепловых машин второе начало термодинамики может быть сформулировано так: невозможен процесс, единственным результатом которого является самопроизвольный переход тепла от менее нагретого к более нагретому телу. Это третья формулировка второго начала термодинамики.
Вопрос3. Привёденная энергия. Понятие энтропии. Принцип возрастания энтропии и вероятность. Второе начало термодинамики
Термодинамическая вероятность W, или статистический вес, принципиально отличается от математической вероятности, которая меняется в пределах от 0 до 1.Чтобы понять смысл W, рассмотрим следующий пример.
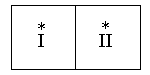
Рис.
В сосуд (рис.) будем помещать молекулы, которые пронумеруем. Сосуд мысленно разобьем на две равные части: левую (I) и правую (II). Вследствие
8
теплового движения молекул распределение их между обеими частями сосуда будет меняться. Рассмотрим состояния, отличающиеся друг от друга числом молекул в левой и правой частях сосуда. Подсчитаем число способов, которыми может быть реализовано каждое состояние.
Пример 1. Пусть число молекул N = 2. Пронумеруем их 1 и 2 . При этом возможны следующие распределения:
1. В I попали обе молекулы 1 и 2.
2. В II попали обе молекулы 1 и 2 .
3. В I попадает 1, а в II – 2.
4. В I – 2, в II – 1.
Других вариантов нет. Результаты этого мысленного опыта представлены в таблице 2.2.
Таблица 2.2
Состояние | Способы реализации состояния | Число способов реализации данного состояния W | ||
Число молекул в I | Число молекул в II | Номера молекул в I | Номера молекул в II | |
0 | 2 | – | 1,2 | 1 |
2 | 0 | 1, 2 | – | 1 |
1 | 1 | 1 | 2 | 2 |
Всего способов |
Из примера видно, что если N = 1020, то W = 21020 , т. е. будет очень велико.
Термодинамической вероятностью состояния системы, или статистическим весом, называют число различных способов, которыми может быть реализовано данное состояние. Очевидно, что при большом количестве молекул W стремится к ![]() .
.
Из таблицы видно, что из всех способов реализации более вероятными являются такие, когда в I и II частях сосуда находятся молекулы примерно поровну. Этот факт объясняют тем, что статистический вес таких состояний максимален. Но это характерно и для равновесных состояний. Статистический вес
9
состояния, когда в I или II частях молекул нет – минимален. Для молекул в сосуде в целом наблюдается стремление к состоянию с максимальным статистическим весом.
Таким образом, определяя W для системы, можно установить, находится ли система в состоянии термодинамического равновесия или нет. Использовать W в качестве меры, определяющей равновесность состояния (или полный беспорядок, хаос), неудобно, поскольку W не является аддитивной величиной.
Действительно, если данная система состоит из двух подсистем, которые могут находится в состояниях со статистическими весами W1 и W2, то состояние системы, согласно теореме об умножении вероятностей, описывается весом W = W1W2, т. е. произведением, а не суммой.
Взяв логарифм от W, получим
ln W = ln W1 + ln W2
Видно, что lnW – аддитивная величина. В качестве характеристики вероятности состояния рассматривают величину S, называемую энтропией. Больцман в 1875 г. вывел формулу, устанавливающую связь междутермодинамической вероятностью и энтропией.
| (2.50) |
Эту знаменитую формулу можно прочитать так: энтропия системы равна произведению постоянной Больцмана на логарифм термодинамической вероятности данного состояния.
Итак, энтропия системы S = S1+ S2, поскольку S1 = ln W1, S2 = ln W2.
При этом:
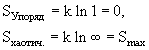
Свойства энтропии. Второе начало термодинамики
Энтропия системы характеризуется следующими свойствами:
1) является аддитивной величиной;
2) подобно внутренней энергии, она является функцией состояния системы и не зависит от протекаемого процесса;
10
3) энтропия системы, находящейся в равновесном состоянии, максимальна;
4) энтропия замкнутой системы при протекании необратимого процесса возрастает, поскольку система при этом переходит из менее вероятных состояний в более вероятные, что сопровождается ростом S;
5) при обратимых процессах система находится все время в равновесных состояниях, поэтому энтропия при этом не меняется, оставаясь максимальной.
Из свойств энтропии (в частности, из 3, 4, 5), рассмотренных детально в статистической физике, вытекает положение, известное как второе начало термодинамики:
В замкнутых (изолированных) термодинамических системах при обратимых процессах энтропия остается постоянной:
Sобр = 0, Sобр = = S2 – S1 = 0; S2 = S1;
при необратимых процессах энтропия может только возрастать Sнеобр >0; S2 > S1.
Объединяя два случая, получим неравенство Клазиуса:
| (2.51) |
Это и есть первая формулировка второго начала термодинамики.
Возрастание энтропии в замкнутых системах соответствует увеличению степени хаотичности молекулярного движения, т. е. система приближается к равновесному состоянию, в котором наблюдается полный беспорядок.
В связи с этим второе начало термодинамики можно сформулировать по–другому: термодинамические системы при любых происходящих в них самопроизвольных процессах могут совершать переходы только из менее в более вероятные состояния. Это вторая формулировка начала, отражающая его вероятностный смысл.
Второе начало в отличие от первого не является универсальным законом. Оно справедливо только для замкнутых систем, состоящих из большого числа молекул и является статистическим законом.
В незамкнутых системах энтропия может вести себя любым образом (убывать, возрастать, оставаться постоянной).
При небольшом числе молекул в системе наблюдаются флyктуации, т. е. отклонения от второго начала.
11
Энтропия и приведенное количество теплоты. Вычисление энтропии
Энтропию для определенного состояния системы не вычисляют, так как о направлении процесса можно судить лишь по величине S. Величину изменения энтропии находят с помощью приведенного количества теплоты.
Приведенным количеством теплоты называют отношение сообщаемого (отнимаемого) количества теплоты системе к температуре, при которой это происходит.
Для бесконечно малого участка процесса приведенное количество теплоты будет равно
![]()
В термодинамике показывается, что элементарное изменение энтропии равно приведенному количеству теплоты, т. е.
| (2.52) |
Взяв интеграл от левой и правой частей выражения (2.52) при равновесном переходе системы из состояния 1 в состояние 2, получим:
| (2.53) |
где подынтегральное выражение и пределы интегрирования надо выразить через величины, характеризующие исследуемый процесс.
Для адиабатических процессов dQ = 0, поэтому S = 0, S1 = S2 = const, т. е. адиабатный процесс происходит при постоянной энтропии. Поэтому его часто называют изоэнтропийным.
Как следует из свойств энтропии, в любом обратимом круговом процессе S = 0 и
| (2.54) |
т. е. суммарное приведенное количество теплоты равно нулю. Это свидетельствует о том, что подынтегральное выражение (т. е. энтропия) является функцией состояния системы.
12
Как следует из рассмотренного, единицей измерения энтропии в системе "СИ" является Дж /К.
Границы применимости второго начала термодинамики
В отличие от первого начала термодинамики, которое является всеобщим законом природы и справедливо для всех без исключения процессов, в том числе и для процессов в микромире, второе начало имеет границы применимости снизу и сверху.
Второе начало устанавливает различие между двумя формами передачи энергии – работой и теплотой. Это различие приводит к закону существования энтропии. Для систем, размеры которых сравнимы с размерами молекул (в микромире), различие между теплотой и работой исчезает. Для таких систем уже не имеют смысла ни понятие энтропии, ни деление процессов на обратимые и необратимые. Здесь большую роль играют флуктуации. Это нижняя граница применимости второго начала термодинамики.
Второе начало выведено из опыта в ограниченной части Вселенной. Распространять его на бесконечную Вселенную нельзя – это верхняя граница применимости. К явлениям в бесконечной Вселенной понятия, которыми оперирует термодинамика – температура, энтропия и пр., применять нельзя, они просто теряют смысл.
Попытка применить второе начало термодинамики, предпринятая Клаузиусом, привела к представлению о так называемой, "тепловой смерти" Вселенной. Рассматривая Вселенную как замкнутую систему и применяя к ней второе начало термодинамики, Клаузиус свел его содержание к утверждению, что энтропия Вселенной должна достигнуть своего максимума. Но это означает, что со временем все формы движения должны перейти в тепловую. Переход теплоты от горячих тел к холодным приведет к тому, что температура всех тел во Вселенной сравняется, т. е. наступит полное тепловое равновесие и все процессы во Вселенной прекратятся – наступит тепловая смерть.
Ошибочность такого вывода заключалась в том, что считать Вселенную замкнутой системой нельзя.
Третье начало термодинамики
Согласно формуле (2.53), в задачах вычисляют не саму энтропию, а разность ее значений в двух состояниях
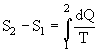
13
Нернст (1864–1941) доказал теорему, которая позволяет определить само значение энтропии в любом состоянии.
Теорема Нернста гласит, что при стремлении температуры тела к нулю Кельвина энтропия этого тела также стремится к нулю:
| (2.60) |
Это и есть третье начало термодинамики.
Так как энтропия определяется с точностью до аддитивной постоянной, то эту постоянную удобно взять равной нулю (отметим, однако, что это произвольное допущение, поскольку энтропия по своей сущности всегда определяется с точностью до аддитивной постоянной).
Из теоремы Нернста следует, что теплоемкости СP и СV при абсолютном нуле равны нулю.
Согласно теореме Нернста, энтропия любого тела при абсолютном нуле равна нулю. На этом основании энтропия тела в состоянии с температурой Т может быть представлена следующим образом:
| (2.60) |
ЗАКЛЮЧИТЕЛЬНАЯ ЧАСТЬ.
Полученные соотношения позволяют проводить количественную оценку термодинамических систем и решать конкретные задачи.
На самоподготовке:Изучить рассмотренные вопросы по конспекту и
[1]с.111-118.
СЛЕДУЮЩЕЕ ЗАНЯТИЕ ПЗ№12 «Круговой процесс». Иметь калькуляторы и повторить материал Л.№16.