Модуль 3. Занятие 4. Лабораторная работа
1. Разделение меди(II) и железа(III) методом ионообменной хроматографии с последующим титриметрическим определением меди и спектрофотометрическим определением железа.
Медь (II) и железо (III), совместно присутствующие в водном растворе, можно разделить на катионообменнике (например, на катионите КУ-2). Предварительно катионит, которым заполнена хроматографическая колонка, переводят в Н+-форму, пропуская через колонку раствор 1,0000 моль/дм3 HCI. При этом все катионы, которые могли присутствовать в сорбенте, обмениваются на ионы Н+, переходят в раствор и уносятся с ним из колонки. После этого через колонку пропускают дистиллированную воду.
Для разделения меди(II) и жeлeза (III) их переводят в комплeкcныe соединения с противоположными знаками зарядов, прибавляя в анализируемый раствор сульфосалициловую кислоту и аммиак. В этих условиях медь(II) образует положительно заряженный комплекс [Cu(NH3)4]2+, a железо(III) – отрицательно заряженный сульфосалицилатный комплекс, состав и заряд которого зависят от концентрации прибавленной сульфо-салициловой кислоты и рН среды. Обычно считается, что в условиях проведения анализа образуется трисульфосалицилатный (три аниона сульфосалициловой кислоты связаны с одним атомом железа(III)) анионный комплекс железа(III) желтого цвета с максимумом в спектре поглощения около 416 нм.
При пропускании полученного раствора через колонку с катионитом в Н+-форме катионы [Cu(NH3)4]2+ сорбируются на катионите, тогда как отрицательно заряженные сульфосалицилатные комплексы железа(III) на катионите не сорбируются и уносятся с ПФ, которую собирают в мерной колбе. После этого через колонку несколько раз пропускают смесь растворов сульфосалициловой кислоты и аммиака, собирают элюат в ту же мерную колбу, которую затем доводят до метки дистиллированной водой, и получают раствор желтого цвета, содержащий все исходное железо (III).
Медь (II) затем элюируют из колонки раствором НСI, собирая элюат в другую мерную колбу. Для этого через колонку с катионитом, содержащим медь(II), пропускают 4,0000 моль/дм3 раствор НСI, после чего колонку несколько раз промывают дистиллированной водой до отрицательной реакции на медь(II). Аммиачный комплекс меди(II) разрушается, и медь (II) элюируется уже в форме хлоридных комплексов.
Элюат и промывные воды, собранные в мерной колбе, доводят дистиллированной водой до метки и получают раствор, содержащий всю отделенную медь(II).
Содержание меди(II) в растворе определяют иодометрическим титрованием. Для этого к аликвотной части раствора, содержащего медь(II), прибавляют избыток 10,00 %-ного раствора KI и оставляют смесь на сколько минут. Протекает реакция.
2 Cu2+ + 2 I - = 2 Cu+ + I2
Образовавшийся иод оттитровывают стандартным раствором тиосульфата натрия в присутствии индикатора – крахмала до исчезновения синей окраски титруемого раствора:
I2 + 2 Na2S2О3 = 2 NaI + Na2S4O6
Определение железа(III) можно провести фотометрически, например, на фотоэлектроколориметре с использованием светофильтра с максимумом светопоглощения около 400 нм, измеряя оптическую плотность анализируемого раствора относительно раствора сравнения – дистиллированной воды.
Выполнение определений
1) Подготовка хроматографической колонки. Колонку (стеклянную бюретку с краном или затвором внизу) заполняют катионитом КУ-2 в Н-форме. Через колонку пропускают 20,0 см3 1,0000 моль/дм3 раствора НС1 со скоростью вытекания элюата 1,0-2,0 см3 в минуту. Затем через колонку пропускают с той же скоростью не менее 20,0 см3 дистиллированной воды. Необходимо следить за тем, чтобы над катионитом всегда был слой жидкости высотой 1-2см.
2) Разделение меди(II) и железа(III). К анализируемому раствору объемом несколько см3 (до 10,0-15,0 см3) в химическом стакане, содержащем медь(II) и железо(III), прибавляют из бюреток 5,0 см3 раствора 10,00 %-ной сульфосалициловой кислоты, 10,0 см3 10,00 %-ного раствора аммиака. Раствор окрашивается в темно - зеленый цвет. Полученный раствор количественно пропускают через колонку со скоростью вытекания элюата 1-2 капли в секунду. Первые ≈10,0 см3 элюата, не содержащего железа(III), собирают в градуированную пробирку и отбрасывают. Далее весь элюат собирают в мерную, колбу на 50,0 см3. Для того чтобы весь анализируемый раствор был перенесен в колонку, стакан дважды обмывают смесью, состоящей из 2,0 см3 раствора сульфосалициловой кислоты и 2,0 см3 раствора аммиака, каждый раз количественно сливая раствор в колонку. Затем колонку трижды последовательно промывают элюэнтами, состоящими из следующих смесей:
а) 5,0 см3 раствора сульфосалициловой кислоты и 5,0 см3 раствора аммиака;
б) 3,0 см3 раствора сульфосалициловой кислоты, 3,0 см3 раствора аммиака и 2,0 см3 воды;
в) 1,0 см3 раствора сульфосалициловой кислоты, 1,0 см3 раствора аммиака и 6,0 см3 воды.
При промывании колонки этими растворами поддерживают постоянную скорость вытекания элюата – 1-2 капли в секунду. Объем раствора, собранного в мерной колбе на 50,0 см3, доводят до метки дистиллированной водой и перемешивают.
Медь(II) из катионита элюируют раствором НС1 и собирают элюат в другую мерную колбу на 50,0 см3. Для этого через колонку дважды пропускают по 10,0 см3 4,0000 моль/дм3 раствора НС1 со скоростью вытекания элюата 1-2 капли в секунду. Затем через колонку пропускают дистиллированную воду порциями по 10,0 см3, собирая элюат в ту же мерную колбу, до отрицательной реакции элюата на присутствие в нем меди(II). Каплю элюата помещают на фильтровальную бумагу, пропитанную раствором K4[Fe(CN)6] . Красно-бурое окрашивание, характерное для ферроцианида меди, должно отсутствовать. В противном случае промывание продолжают.
Раствор, собранный в мерной колбе и содержащий всю элюированную медь(II), доводят до метки дистиллированной водой и перемешивают.
3) Определение меди(II). В колбу для титрования отбирают пипеткой 2 см3 раствора из мерной колбы, содержащей медь(II), прибавляют 2,0 см3 10,00 %-ного раствора иодида калия KI, накрывают колбу стеклом и оставляют в темном месте на ≈10 минут. Выделившийся йод титруют стандартным раствором тиосульфата натрия до бледно-желтой окраски титруемого раствора, после чего прибавляют 0,5 см3 свежеприготовленного раствора крахмала (титруемый раствор сразу синеет) и продолжают титровать до исчезновения синей окраски. Проводят 3-5 параллельных определений и рассчитывают мaссу меди(II) в исходном анализируемом растворе:
n(Cu2+)= n(1/2 I2)= n(Na2S2O3)
С(Cu2+) V(Cu2+)= С(Na2S2O3) V(Na2S, O3)
m(Cu2+) = С(Cu2+) M(Cu2+) Vk,
где n(Cu2+), n(1/2 I2) и n(Na2S2O3) – количество эквивалентов меди, иода тиосульфата натрия соответственно; С(Сu2+) и С(Na2S2O3) — молярная концентрация меди в мерной колбе на 50,0 см3 и стандартного раствора тиoсульфата натрия соответственно; V(Сu2+) = 2,0 см3 = 0,002 дм3; V(Na2S2O3)- объем стандартного раствора тиосульфата натрия, израсходованный на титрование;M(Сu2+) = 63,546 г/моль – молярная масса меди, Vk = 50,0 см3 = 0,05. Массу меди рассчитывают в граммах с точностью до трех значащих цифр.
4) Определение железа(III). Собранный в мерной колбе на 50,0 см3 раствор сульфосалицилатных комплексов железа(III) фотометрируют на фотоэлектроколориметре, например, на КФК-2, при светофильтре 400 нм в кювете с толщиной поглощающего слоя 1 см относительно дистиллированной воды (раствор сравнения).
Определение проводят по методу одного стандарта. Стандартный раствор сульфосалицилатных комплексов железа(III) готовят в мерной колбе на 50,0 см3. Для этого пипеткой вносят в колбу 2,0 см3 раствора соли железа(III), содержащего 0,1000 мг/см3 железа(III), прибавляют 10,0 см3 дистиллированной воды, 5,0 см3 10,00 %-ного раствора сульфосалициловой кислоты, 5,0 см3 10,00 %-ного водного аммиака, доводят объем колбы до метки дистиллированной водой и перемешивают. Измеряют последовательно оптическую плотность анализируемого и стандартного растворов в одной и той же кювете в одинаковых условиях. По полученным данным рассчитывают массу железа (III) в исходном анализируемом растворе:
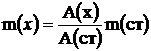
где m(ст)=0,2000 мг — масса железа (III) в стандартном растворе объемом 50,0 см3; А(х) и A(ст) — оптическая плотность измеряемого и стандартного растворов соответственно. Массу железа рассчитывают в мг с точностью до двух значащих цифр.



