Тема: Количественный анализ лекарственных веществ титриметрическими, физико-химическими методами анализа.
1.Рассчитайте объем титранта, расходуемый при количественном определении цинка оксида (М. м. 81,37) трилонометрическим методом, если точная масса вещества 0,6971 г. Цинка оксида в препарате должно быть не менее 99,0%. Титрант − 0,05 моль/л раствор трилона Б. Дайте обоснование данному методу количественного определения. Напишите уравнения реакций. Укажите условия проведения титрования. Рассчитайте молярную массу эквивалента, титр и напишите формулу расчета массовой доли препарата в процентах. Сделайте заключение.
Комплексонометрический (трилонометрический) метод. Основан на свойстве ионов цинка образовывать с трилоном Б прочные, бесцветные, растворимые в воде комплексы. Способ титрования прямой. Титрование проводят в среде аммиачного буфера (рН 9-10) в присутствии индикатора –кислотного хром черного специального.
По методике ГФ используют разведение (объем мерной колбы 100 мл, объем аликвоты, взятой на анализ-10 мл)
ZnO + 2HCl ® ZnCl2 + H2O


Когда все ионы цинка оттитрованы, под действием ЭДТА начинает разрушаться менее прочный комплекс металла с индикатором. Появление окраски свободного индикатора (сине-фиолетовой при данном значении рН 9,5 – 10,0) покажет конец титрования.

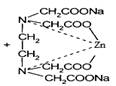
Кстех.=1/1 * 1/1 = 1
Титрованный раствор трилона Б по ГФ ХI готовится с учетом РЧ.
f экв = Кстех= 1
Э = fэкв * М. м. = 1 * М. м.= М. м. = 81,37 моль/г
Т= М * Э / 1000 = 0,05 * 81,37 / 1000 = 0,004069 г/мл
Расчет объема (V) титрант:
V= a*C *Vр= 0,6971*99 *10 = 16,9 мл
T*100 * Vмк 0,004069*100*100
Ответ: 16,9 мл 0,05 моль/л раствора трилона Б, расходуется при количественном определении цинка оксида комплексонометрическим методом.
Формула расчета массовой доли препарата в процентах:
Х % =Т * VТрБ *К *Vмк* 100
a * Vразвед
2.Напишите структурные формулы и приведите латинские и химические названия бензокаина (анестезина), прокаина гидрохлорида (новокаина), тетракаина гидрохлорида (дикаина), прокаинамида гидрохлорида (новокаинамида), тримекаина гидрохлорида, лидокаина гидрохлорида; бупивакаина гидрохлорида; натрия п-аминосалицилата, бепаска, буметанида (буфенокса), мефенаминовой кислоты и ее натриевой соли, диклофенака (ортофена, вольтарена), ибупрофена (бруфена), напроксена, кетопрофена. Сгруппируйте вещества по растворимости в воде, отношению к кислотам и щелочам.
Аминобензойные кислоты и их соли (анестезин, новокаин, дикаин, новокаинамид).
Benzocainum
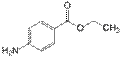
4-Аминобензойной кислоты этиловый эфир
Procainum hydrochloridum
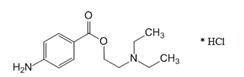
2-(Диэтиламино)этил-4-аминобензоат (в виде гидрохлорида)
Tetracainum hydrochloridum
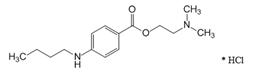
4-(Бутиламино)бензойной кислоты 2-(диметиламино)этиловый эфир ( в виде гидрохлорида)
Procainamidum hydrochloridum
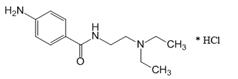
4-Амино-N-[2-(диэтиламино)этил]бензамид (в виде гидрохлорида)
Первичная ароматическая аминогруппа придает очень слабые основные свойства, т. к. электронная плотность с атома азота смещена в сторону бензольного кольца. За счет основных свойств бензокаин растворяется в разведенной кислоте хлористоводородной, но образующаяся соль не устойчива.
Третичная аминогруппа придает сильные основные свойства, которые усилены алкильными радикалами.
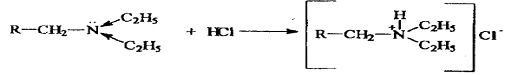
Соли гидрохлориды легко растворимы в воде, устойчивы.
Производные диэтиламиноацетанилида (лидокаин, тримекаин, бупивакаин).
Trimecainum hydrochloridum
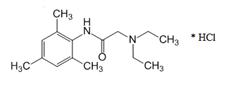
2-(Диэтиламино)-N-(2,4,6-триметилфенил)ацетамид (в виде гидрохлорида)
Lidocainum hydrochloridum
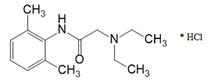
(2-Диэтиламино)-N-(2,6-диметилфенил)ацетамид ( в виде гидрохлорида)
Bupivacainum hydrochloridum
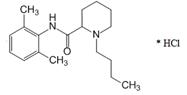
1-Бутил-N-(2,6-диметилфенил)-2-пиперидинкарбоксамид ( в виде гидрохлорида)
Как органические основания, содержащие третичный атом азота, образуют гидрохлориды (устойчивые соли, хорошо растворимые в воде).
Производные п-аминосалициловой кислоты (ПАСК, бепаск)
Acidum aminosalicylicum
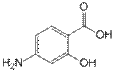
4-Амино-2-гидроксибензойная кислота
Bepascum
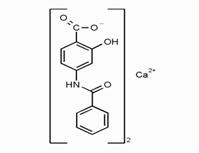
пара - бензоиламиносалицилат кальция.
Препараты обладают амфотерными свойствами (проявляют кислотные и основные свойства).
Слабые основные свойства обуславливает ароматическая аминогруппа, а сильные кислотные свойства проявляются за счет карбоксильной группы и фенольного гидроксила.
Производные амида хлорбензолсульфоновой кислоты (буфенокс)
Bumethanidum
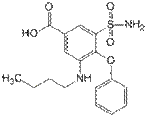
3-(Аминосульфонил)-5-(бутиламино)-4-феноксибензойная кислота
Препарат обладает кислотными свойствами за счет наличия карбоксильной и сульфаниламидной группы. Хорошо растворяется в щелочах. Образует соли с щелочами, солями тяжелых металлов.
Производные фенилуксусной и фенилпропионовой кислот, пропионовой (диклофенак, диклофенак натрия, ибупрофен, кетопрофен, напроксен)
Diclophenacum
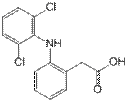
2-(2-(2,6-Дихлорфениламинo)фенил)уксусная кислота
Ibuprophenum
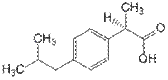
(RS)-2-(4-(2-Метилпропил)фенил)пропановая кислота
Acidum mephenamicum
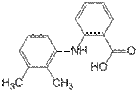
2-[(2,3-Диметилфенил)амино]бензойная кислота ( и в виде натриевой соли)
Ketoprophenum
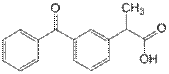
3-Бензоил-альфа-метилбензолуксусная кислота
Naproxenum
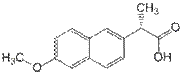
(S)-6-Метокси-альфа-метил-2-нафталинуксусная кислота (в виде натриевой соли)
За счет наличия карбоксильной группы препараты обладают сильными кислотными свойствами, образуют устойчивые соли с щелочами (например, диклофенак натрия), солями тяжелых металлов. Кислотные свойства обусловлены подвижностью протона водорода к карбоксильной группе, при этом образуется резонансный стабилизированный анион, у которого отрицательный заряд распределяется поровну между электроотрицательными атомами кислорода.
3.Количественное определение препарата «Calcii chloridum» согласно ФС 42-2567-00 проводят следующим образом: около 0,8 г препарата (точная масса), отвешенные в закрытом бюксе, растворяют в воде, переносят в мерную колбу емкостью 100 мл, доводят объем раствора водой до метки и тщательно перемешивают. К 25 мл полученного раствора прибавляют 5 мл аммиачного буферного раствора, 0,1 г индикаторной смеси или 7 капель раствора кислотного хром темно-синего и титруют при энергичном перемешивании 0,05 моль/л раствором трилона Б до синего-фиолетового окрашивания. Кальция хлорида в препарате должно быть не менее 98,0%.
Дайте обоснование данному методу количественного определения. Напишите уравнения реакций. Рассчитайте молярную массу эквивалента, титр и массовую долю препарата в процентах (навеска анализируемого порошка 0,7949 г, молярная масса кальция хлорида 219,08, объем раствора трилона Б, пошедшего на титрование, 18,1 мл). На основе полученных данных сделайте заключение о соответствии исследуемого образца требованиям ФС.
Титрант – трилон Б (динатриевая соль этилендиаминтетрауксусной кислоты).
Метод основан на свойстве ионов металлов образовывать с трилоном Б бесцветные, прочные, растворимые комплексные соединения в мольном отношении 1:1. Прямым титрованием определяют растворимые в воде или кислотах лекарственные вещества, способные легко и быстро реагировать с трилоном Б.
Кальция хлорид определяют прямым методом. Определение проводят в среде аммиачного буфера с использованием индикатора эриохрома черного Т стандартным раствором трилона Б. С учетом участия индикатора основные реакции, лежащие в основе определения записываются следующим образом:
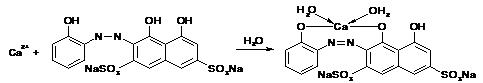
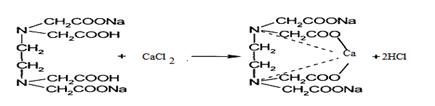
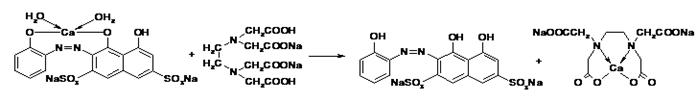
Появление окраски свободного индикатора (синей при данном значении рН 9,5 - 10,0) покажет конец титрования
Кстех = 1/1= 1
Титрованный раствор трилона Б по ГФ ХI готовится с учетом РЧ.
f экв = Кстех= 1
Э = fэкв * М. м. = 1 * М. м.= 219,08 моль/г
Т= М * Э / 1000 = 0,05 * 219,08 / 1000 = 0,01095 г/мл
Х% = Т*V*100* Vмк = 0,01095 * 18,1 * 100 * 100 = 99,7%
а*Vразвед 0,7949 * 25
Заключение: кальция хлорид соответствует требованиям ФС 42-2567-00 по количественному содержанию (не менее 98%).
4.Количественное определение кислоты салициловой по фармакопейной статье проводят следующим образом: Около 0,25 г препарата (точная масса) растворяют в 15 мл нейтрализованного по фенолфталеину этанола и титруют с тем же индикатором 0,1 моль/л раствором едкого натра до розового окрашивания. 1 мл 0,1 моль/л раствора едкого натра соответствует 0,01381 г кислоты салициловой, которой в препарате должно быть не менее 99,5%. Дайте обоснование метода, приведите уравнение реакции, фактор эквивалентности, молярную массу эквивалента, титр и расчетную формулу определения массовой доли вещества (в %) в препарате.
Кислотно-основное титрование. Способ количественного определения салициловой кислоты основан на использовании алкалиметрического метода. В качестве растворителя используют этанол (так как кислота мало растворима в воде). Этанол предварительно нейтрализуют по фенолфталеину (фенолфталеинц). Затем растворяют навеску и титруют 0,1 М раствором гидроксида натрия (не содержащим карбонатов) с тем же индикатором:
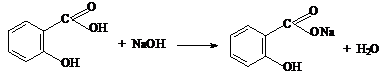
Кстех = 1/1= 1
Титрованный раствор натрия гидроксида по ГФ ХI готовится с учетом РЧ.
f экв = Кстех =1
Э = f экв * М. м. = 1 * М. м. = М. м. = 138,12 моль/г
Т= М * Э / 1000 = 0,1 * 138,12 / 1000 = 0,01381 г/мл
Формула расчета массовой доли препарата в процентах:
Х % =Т * VNaOH *К * 100
a
где, Х-содержание лекарственного вещества в препарате в % , V- объем 0,1 М раствора гидроксида натрия, пошедший на титрование, мл ; а - навеска, взятая на анализ, г.
5.Рассчитайте количественное содержание и оцените качество парацетамола по количественному содержанию, если на титрование 0,2456 г навески израсходовано 16,28 мл 0,1 моль/л раствора натрия нитрита с К=1,0123. 1 мл 0,1 моль/л раствора натрия нитрита соответствует 0,01512 г парацетамола, которого в препарате должно быть не менее 98,5%.
Парацетамол количественно определяют по образующемуся при кипячении с обратным холодильником в течение 1 часа продукту кислотного гидролиза — гидрохлориду п-аминофенола, используя нитритометрический метод:
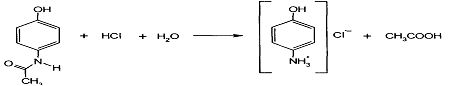
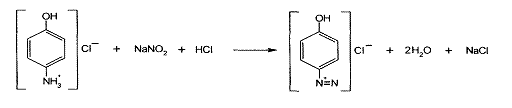
Эквивалентную точку устанавливают потенциометрически или с помощью внешнего индикатора — йодкрахмальной бумаги (ФС), которая синеет от выделившегося при добавлении избытка титранта йода:
NaNO2 + HCl ®NaCl + HNO2
KJ +HCl ® KCl + HJ
2HNO2 +2HJ ®J2+2NO↑ +2H2O
Эквивалентную точку при нитритометрическом определении парацетамола можно также установить со смешанным внутренним индикатором, содержащим 0,1% раствор тропеолина 00 и 0,15% раствор метиленового синего.
Кстех = 1/1=1
Титрованный раствор натрия нитрита по ГФ ХI готовится с учетом РЧ.
f экв = Кстех =1
Э = f экв * М. м. = 1 * М. м. = М. м. = 151,2 моль/г
Т= М * Э / 1000 = 0,1 * 151,2 / 1000 = 0,01512 г/мл
Х% = 0,01512*V*К*100 = 0,01512*16,28*1,0123*100 = 101,5%
а 0,2456
Заключение. Верхний предел не указан, следовательно подразумевается не более 100,5% (ОФС 1.1.0001.15 Правила пользования фармакопейными статьями). Парацетамол не удовлетворяет требованию ГФ по количественному содержанию.
Тема: Ароматические соединения. п -, о -, м - Аминобензойные кислоты и их производные; арилалкиламины, оксифенилалкиламины и их производные;иодированные производные ароматических аминокислот; бензолсульфаниламиды и др.
1.Приведите реакции подлинности общие для гексаметилентетрамина и формальдегида. Химизм, условия проведения и аналитические эффекты. Ответ обоснуйте.
Гексаметилентетрамин при взаимодействии с серной кислотой разлагается с выделением формальдегида.
(CH2)6N4+H2SO4+6HOH ® 6HCOHформальдегид +2(NH4)2SO4
Структура альдегидной группы (дипольный момент карбонила, частично положительный заряд на атоме углерода, поляризуемость двойной связи)обуславливает высокую реакционную способность.
Реакции окисления.
Альдегиды окисляются до кислот под влиянием сильных и слабых окислителей. Они восстанавливают в щелочной среде из растворов солей многие металлы. Поэтому для подтверждения подлинности альдегидов или веществ, выделяющих альдегиды при гидролизе, применяются реакции их окисления комплексными соединениями серебра, меди, ртути (реакция ускоряется при нагревании). При восстановлении последних образуются характерные осадки свободных металлов или их оксидов.
Реакция с аммиачным раствором нитрата серебра (реакция «серебряного зеркала»). При добавлении к раствору формальдегида аммиачного раствора AgNO3 (реактив Толленса) и нагревании на стенках пробирки образуется зеркальный налет металлического серебра.
AgNO3 + 3NH3 → [Ag(NH3)2]OH + NH4NO3
НCOH + 2[Ag(NH3)2]OH → НCOOH + 2Ag↓+ 4NH3+ H2O
Реакция с реактивом Фелинга Реактив Фелинга состоит из двух растворов: – раствор сульфата меди; – щелочной раствор сеньетовой соли KNaC4H4O6. Альдегиды восстанавливают соединения меди (II) до оксида меди (I) (кирпично-красный осадок).
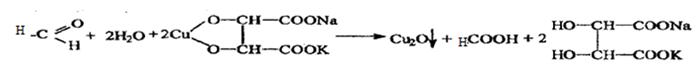
Реакция с реактивом Несслера. Выделяется темный осадок металлической ртути.
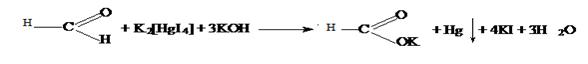
Реакции окислительной конденсации.
Реакции конденсации альдегидов с фенолами в присутствии концентрированной серной кислоты ГФ X рекомендует эту реакцию для подтверждения подлинности формальдегида, а также веществ, при гидролизе которых он выделяется (гексаметилентетрамин). В качестве реактива используется салициловая или хромотроповая кислота.
(CH2)6N4+H2SO4+6HOH ® 6HCOHформальдегид +2(NH4)2SO4

ауриновый краситель - розовое окрашивание
2.Эпинефрина (адреналина) гидротартрат и гидрохлорид. Норэпинефрина (норадреналина) гидротартрат. Методы подтверждения подлинности. Химизм, условия проведения, аналитический эффект.
Ареналина гидротартрат
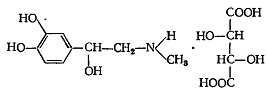
Адреналина гидрохлорид
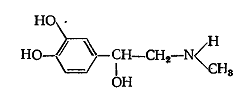 * НCl
* НCl
Норадреналина гидротартрат
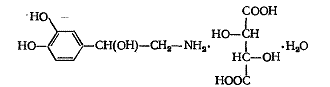
Адреналин и норадреналин, имея в структуре своих молекул ядро двухатомного фенола (пирокатехина), способны легко окисляться, обладая свойством восстановителей. Они восстанавливают серебро из аммиачного раствора нитрата серебра, а из красной закиси меди — свободную медь. Особенно легко окисляются эти препараты в щелочной среде (являются донорами водорода), что может быть использовано для получения цветной реакции с 1,2-динитробензолом (сине-фиолетовое окрашивание)

За счет наличия в структуре двух фенольных гидроксилов адреналин и норадреналин при взаимодействии с катионами Fe3+ образуют окрашенные в изумрудно-зеленый цвет феноляты. Если в пробирку добавить 1 каплю раствора аммиака, окрашивание переходит в вишнево-красное (сходное с окрашиванием продуктов окисления адреналина и норадреналина). Это испытание включено в ФС на адреналина и норадреналина гидротартраты.
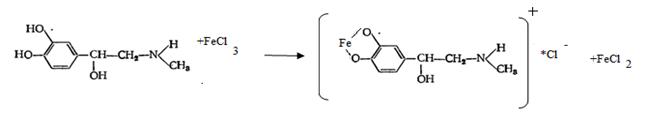
При нагревании с едкой щелочью адреналин и норадреналин претерпевают гидраминное расщепление, образуя 3,4-диоксиацетофенон и метиламин в случае адреналина, аммиак-—в случае норадреналина
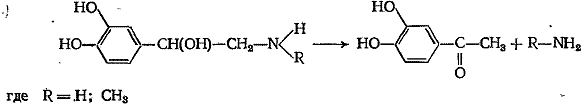
Образовавшийся амин может быть обнаружен конденсацией с 2,4-динитрохлорбензолом, в результате образуется соединение оранжево-желтого цвета, растворимое в органических растворителях:
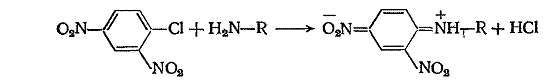
Отличать друг от друга эпинефрин и норэпинефрин можно реакцией окисления 0,1 М раствором йода в двух буферных растворах, имеющих рН соответственно 3,56 и 6,5. Эпинефрин в растворах, имеющих как рН 3,56, так и рН 6,5, образует адренохром, придающий растворам темно-красное окрашивание:
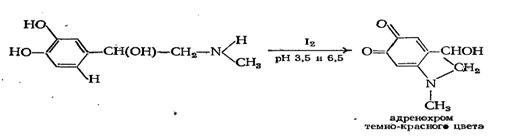
Окраска сохраняется (при рН 3,56) и после добавления 0,1 М раствора тиосульфата натрия. Норэпинефрин образует норадренохром (красно-фиолетового цвета) только в растворах, имеющих рН 6,5:
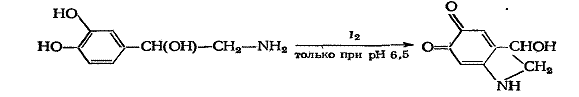
Для обнаружения тартрат-иона в солях эпинефрина и норэпинефрина используют реакцию, основанную на дегидратации и последующем окислении при нагревании с концентрированной серной кислотой в присутствии резорцина. Происходит вначале образование глиоксаля и муравьиной кислоты:
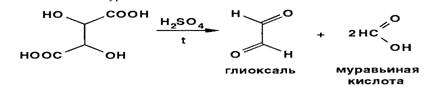
Затем муравьиная кислота вступает в реакцию конденсации с тремя молекулами резорцина. В результате образуется ауриновый краситель, имеющий хиноидную структуру:

3. Укажите внешний вид кислоты бензойной, натрия бензоата, кислоты салициловой, натрия салицилата; объясните возможности изменения внешнего вида под воздействием факторов внешней среды и увяжите с условиями хранения.
Кислота салициловая. Белые мелкие игольчатые кристаллы или легкий кристаллический порошок без запаха. Летуч с водяным паром. При осторожном нагревании возгоняется. Хранение. В хорошо укупоренной таре, предохраняющей от действия света.
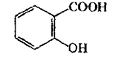
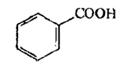
Кислота бензойная. Бесцветные игольчатые кристаллы или белый мелкокристаллический порошок. При нагревании возгоняется; перегоняется с водяным паром. Хранение. В хорошо укупоренной таре.
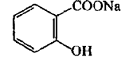
Натрия салицилат. Белый кристаллический порошок или мелкие чешуйки, без запаха, сладковато-соленого вкуса. Хранение. В хорошо укупоренной таре, предохраняющей от действия света, в сухом месте.
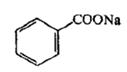
Натрия бензоат. Белый кристаллический порошок без запаха или с очень слабым запахом, сладковато-соленого вкуса. Хранение. В хорошо укупоренной таре
Хранят ароматические кислоты и их соли в сухом, защищенном от света месте, при комнатной температуре, в хорошо укупоренной таре, учитывая возможность отсыревания порошков. В связи с чем порошки комкуются. Салициловую кислоту и натрия салицилат следует также предохранять от действия света из –за возможности к окислению по фенольному гидроксилу. В связи с чем возможно потемнение порошков.
4.Объясните, какую примесь в натрия п-аминосалицилате обнаруживают с помощью реакции с раствором железа ( III ) хлорида (выпадает осадок при стоянии в течение 3-х часов).
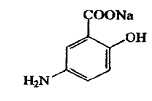
Наличие в молекуле пара-аминосалицилата фенольного гидроксила обусловливает положительную реакцию с раствором хлорида железа (III). Образуются соединения, окрашенные в кислой среде в фиолетовый цвет. После выполнения этой реакции из окрашенного раствора не должен выпадать осадок в течение трех часов. Образование осадка свидетельствует о примеси в натрия пара-аминосалицилате фармакологически неактивного м-аминосалицилата натрия:
5.В три пробирки помещены субстанции трех препаратов: салазопиридазина, сульфацил-натрия и фталазола. Объясните, как с помощью органолептических и физических методов можно различить эти препараты? Приведите уравнения химических реакций, подтверждающих их подлинность.
Фталазол
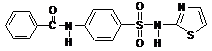
Белый или белый со слегка желтоватым оттенком кристаллический порошок, без запаха. Практически нерастворим в воде, очень мало растворим в спирте, растворим в водном растворе карбоната натрия.
Сульфацил-натрия
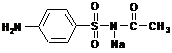
Белый кристаллический порошок, без запаха. Хорошо растворим в воде. Практически не растворим в спирте.
Салазопиридазин
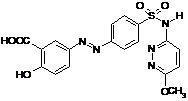
Мелкокристаллический порошок оранжевого цвета. Практически нерастворим в воде, мало растворим в спирте, растворим в растворе едкого натра
Отличие по органолептическим и физическим свойствам. Салапиридозин- порошок оранжевого цвета, в отличие от сульфацила-натрия и фталазола. Сульфацил-натрия (соль) хорошо растворим в воде, в отличие от фталазола и салазопиридазина.
Частные реакции подлинности.
Фталазол при сплавлении с резорцином и каплей серной кислоты приобретает красно-желтый цвет. После охлаждения и добавления 2 мл NaOH отбирают 1 каплю полученного раствора смеси и прибавляют к 200 мл Н2О. Появляется желтая окраска с интенсивной зелёной флуоресценцией.

Сульфацетамид натрия (альбуцид) при кислом гидролизе образует белый осадок сульфацетамида, который после высушивания должен иметь tпл. =183°С:
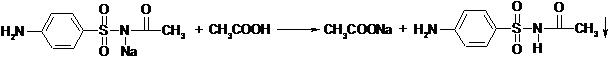
При растворении осадка сульфацетамида в этаноле и добавлении концентрированной серной кислоты образуется этилацетат, имеющий характерный запах:
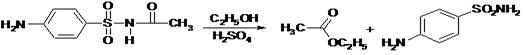
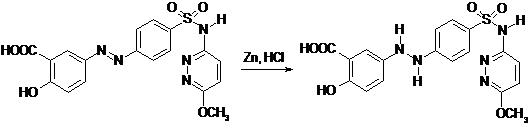
Наличие азогруппы в салазопиридазине подтверждается реакцией гидрирования. При добавлении к окрашенному раствору препарата цинковой пыли и концентрированной соляной кислоты наблюдается постепенное исчезновение окраски раствора.