Справка о результатах проведения публичных консультаций с представителями субъектов предпринимательской и иной деятельности
на проект постановления Правительства Российской Федерации «О внесении изменений в постановление Правительства Российской Федерации от 29 октября 2010 г. № 000
в связи с принятием Федерального закона «О внесении изменений
в статью 61 Федерального закона «Об обращении лекарственных средств»
Минэкономразвития России в соответствии с пунктом 28 Правил проведения федеральными органами исполнительной власти оценки регулирующего воздействия проектов нормативных правовых актов, проектов поправок к проектам федеральных законов и проектов решений Совета Евразийской экономической комиссии, утвержденных постановлением Правительства Российской Федерации от 17 декабря 2012 г. № 000 провело публичные консультации с представителями субъектов предпринимательской деятельности по проекту постановления Правительства Российской Федерации
«О внесении изменений в постановление Правительства Российской Федерации
от 29 октября 2010 г. № 000 в связи с принятием Федерального закона «О внесении изменений в статью 61 Федерального закона «Об обращении лекарственных средств» (далее – проект акта).
Обращаем внимание на следующие замечания, поступившие в ходе проведения публичных обсуждений проекта акта.
Ассоциация международных фармацевтических производителей обращает внимание.
1. Проектируемым пунктом 6(1) проекта акта предусмотрено внесение
изменений в действующую реестровую запись о государственной регистрации
предельной отпускной цены производителя на лекарственный препарат в части
изменения наименования лекарственного препарата (международного непатентованного или группировочного или химического и торгового наименования), написания лекарственной формы, написания дозировки лекарственного препарата, изменения держателя или владельца регистрационного удостоверения лекарственного препарата, изменения производителя лекарственного препарата, наименования производственных площадок, участвующих в процессе производства лекарственного препарата,
номера регистрационного удостоверения лекарственного препарата, штрихового
кода, нанесенного на вторичную (потребительскую) упаковку лекарственного
препарата, первичной упаковки лекарственного препарата, комплектности лекарственного препарата (при условии отсутствия изменения его количества во вторичной (потребительской) упаковке) на основании заявления держателя или владельца регистрационного удостоверения лекарственного препарата (уполномоченного им лица) Министерством здравоохранения Российской Федерации без согласования с Федеральной службой по тарифам с сохранением последней зарегистрированной цены на лекарственный препарат.
Представляется, что внесение данных изменений в государственный реестр зарегистрированных предельных отпускных цен производителей на лекарственные препараты, включенные в перечень жизненно необходимых и важнейших лекарственных препаратов (далее – Реестр) должно осуществляться путем дублирования с сохранением существующих данных реестровой записи.
Внесение изменений в действующую реестровую запись без сохранения существующих данных реестровой записи повлечет за собой невозможность реализации лекарственных препаратов, произведенных до внесения изменений. Все препараты, находящиеся в момент изменения реестровой записи у дистрибьюторов и в аптеках невозможно будет реализовывать далее.
Представляется, что старая реестровая запись должна быть действительна в течение всего срока годности препарата, начиная с даты одобрения изменения, чтобы была возможность реализовать лекарственный препарат, произведенный и поставленный дистрибьюторам и в аптеки до одобрения изменений.
2. При расчете цены иностранного производителя с использованием корзины референтных стран полагаем целесообразным применить в качестве базы для расчета предельной отпускной цены иностранного производителя среднее арифметическое значений меньше медианы минимальной отпускной цены производителя в государстве производителя и других государствах по формуле:
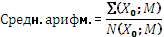
Где:
X0 – минимальная цена в перечне;
Xm – максимальная цена в перечне;
M – Медиана (X0;Xm);
N – количество значений в диапазоне не превышающем медианы;
( ; ) – диапазон значений
Использование в качестве базы для расчета предельной отпускной цены иностранного производителя цены, не превышающей минимальную отпускную цену
в государстве производителя и других государствах, не позволяет компенсировать
резкие ценовые колебания в референтных странах, которые зачастую обусловлены кризисными изменениями экономической политики под воздействием различных
внешних и внутренних факторов, и в ряде случаев препятствует раннему выводу
на российский рынок необходимых инновационных лекарственных препаратов.
Расчет с применением нижнего ценового диапазона цен стран сравнения обеспечивает выполнение государственной задачи по обеспечению стоимостной доступности лекарственных препаратов, и одновременно обеспечивает сбалансированность подхода к вопросу ценообразования импортируемых инновационных лекарственных препаратов с учетом их ценовой и фактической доступности.
Проведенный Ассоциацией международных фармацевтических производителей анализ международного опыта внешнего референтного ценообразования также указывает на наиболее частое использование странами Европейского Союза средней цены корзины референтных стран или средней от выборки минимального диапазона.
№ | Страна | Количество референтных стран, используемых для расчета цены | Методика расчета цены в «корзине» стран |
Бельгия | 24 | Среднее значение цены «корзины» стран | |
Болгария | 9 | Средняя цена из 3х минимальных цен | |
Чехия | 8 | Среднее значение цены «корзины» стран | |
Дания | Внешнее референтное ценообразование не используется | ||
Франция | 4 | На уровне значения цен в референтных странах (финально определяется в процессе переговоров) | |
Германия | Внешнее референтное ценообразование не используется | ||
Греция | 22 | Средняя цена из 3х минимальных | |
Ирландия | 9 | Среднее значение цены «корзины» стран | |
Нидерланды | 4 | Среднее значение цены «корзины» стран | |
Польша | 17 | Минимальное значение цены «корзины» стран | |
Португалия | 4 | Среднее значение цены «корзины» стран | |
Румыния | 12 | Минимальное значение цены «корзины» стран | |
Словакия | 26 | Средняя из 6 минимальных цен | |
Хорватия | 4 | Среднее значение цены «корзины» стран | |
Венгрия | 14 | Минимальное значение цены | |
Латвия | 6 | 3-ая минимальная цена, но не выше, чем в Литве и Эстонии | |
Литва | 6 | 95% от средней цены | |
Мальта | 12 (внешнее референтное ценообразование используется только для новых лекарственных препаратов) | Среднее значение цены «корзины» стран |
Кроме того, изменение методики расчета не повлечет роста стоимости
лекарственных препаратов для государственного бюджета, поскольку регистрируемая
цена является предельной величиной отпуска, а не фактической ценой
закупки, определяемой в ходе проведения государственными заказчиками торгов
в соответствии с требованиями Федерального закона от 5 апреля 2013 г. « 44-ФЗ
«О контрактной системе в сфере закупок товаров, работ, услуг для обеспечения государственных и муниципальных нужд».
3. Ассоциацией международных фармацевтических производителей предлагается исключить из списка референтных стран Турцию, Грецию и Украину.
Данное предложение объясняется тем, что в Турции при уровне ВВП на душу населения примерно на 20% ниже, чем в России, существует система всеобъемлющего 100% бесплатного лекарственного обеспечения, известная как «система возмещения». В соответствии с правилами турецкой системы возмещения, работающее население платит 20% от цены лекарственного препарата в случае, если препарат превышает по стоимости установленный государством лимит - референтную цену. Пенсионеры платят 10%, а больные с хроническими заболеваниями получают лекарства полностью бесплатно.
Цены, приводимые на сайте Министерства здравоохранения Турции и используемые в России в качестве референтных, фактически являются ценами долгосрочных государственных контрактов в системе полного лекарственного возмещения. Таким образом, используемые в качестве референтных, цены реестра Турции не отражают объективно себестоимость и не являются рыночными.
Предложение по исключению из списка референтных стран Греции и Украины обусловлено тем, что данные страны давно находятся в глубоком экономическом кризисе, по сути - на пороге дефолта. Регуляторные органы за последние три года не раз информировали страны-члены ЕС о необходимости исключения цен Греции в качестве референтных в связи с данным положением дел.
Применительно к Украине необходимо отметить, что девальвация гривны составила более 100% за последний год. В целом поставки в эти страны также не отражают себестоимость и не являются рыночными, а в ряде случаев носят сугубо социально-гуманитарный характер.
4. Ассоциацией международных фармацевтических производителей представляется целесообразным изменить расчет в отношении стоимости одной лекарственной формы по корзине референтных стран.
В отношении расчета предельной отпускной цены по корзине референтных
стран проектом методики расчета предельных отпускных цен на лекарственные препараты, включенные в перечень жизненно необходимых и важнейших
лекарственных препаратов, при их государственной регистрации и перерегистрации
(далее – методика) вводятся расчеты исходя из минимальной стоимости одной лекарственной формы в референтной стране независимо от наличия поставок данной формы в Российскую Федерацию или условий ее поставки в другие страны.
Ассоциация международных фармацевтических производителей считает такой подход нецелесообразным и экономически необоснованным.
Стоимость одной лекарственной формы в упаковке в 100 таблеток/ампул
и 10 таблеток/ампул будет разная, т. к. большая упаковка более экономичная, соответственно стоимость одной лекарственной формы будет меньше.
В связи с чем предлагается конкретизировать формулировку – «исходя из минимальной стоимости одной лекарственной формы в отношении одной и той же формы выпуска».
5. Ассоциация международных фармацевтических производителей полагает необходимым изменить подходы, предложенные в проекте методики, к перерегистрации цены иностранного производителя.
Представленный механизм перерегистрации отпускной цены лекарственного препарата иностранного производителя требует соблюдения 2-х условий:
во-первых средневзвешенная фактическая цена ввоза должна быть ниже зарегистрированной цены не более чем на прогнозируемый уровень инфляции, во-вторых не превышение размера минимальной отпускной цены в корзине стран.
Ассоциация международных фармацевтических производителей предлагает исключить второе условие как не имеющее отношения к инфляционным процессам в российской Федерации и предусмотреть унифицированный подход в части возможности ежегодной перерегистрации цен импортируемых и российских лекарственных препаратов с учетом коэффициента инфляции, равного прогнозируемому уровню инфляции.
Кроме того, данная норма носит явно дискриминирующий характер, поскольку проектом методики не предусмотрен учет экспортных поставок в другие страны российских производителей.
6. При расчете средневзвешенной фактической цены ввоза лекарственного
препарата дополнительно Ассоциация международных фармацевтических производителей предлагает исключить из общего количества поставок - поставки, осуществленные
для проведения клинических исследований в РФ, а также поставки
лекарственных препаратов с остаточным сроком годности менее 20%.
Цены данных поставок не отражают рыночную стоимость товара и нигде не подлежат учету.
7. Ассоциация международных фармацевтических производителей отмечает, что согласно проектируемым изменениям, «производитель» предлагается заменить на «держатель регистрационного удостоверения», при этом разработчиком не учитываются производственные площадки, участвующие в процессе производства, при расчете цены производителя.
Такое упущение не позволит провести корректное сравнение по референтным странам, поскольку в ряде случаев один и тот же препарат поставляется в разные страны с различных площадок и при этом себестоимость производства может существенно отличаться.
Сравнение с ценами на препарат в других странах должно проходить с равными условиями. В связи с чем, Ассоциация международных фармацевтических производителей полагает, что необходимо учитывать производственные площадки, участвующие в производстве препарата в других странах, поскольку место производства препарата напрямую влияет на расходы, которые несет производитель, и соответственно на отпускную цену производителя.
8. Проектом методики предусмотрено, что держатель или владелец регистрационного удостоверения воспроизведенного лекарственного препарата (уполномоченное им лицо) представляет для государственной регистрации предельную отпускную цену, не превышающую 80 % от зарегистрированной предельной отпускной цены на референтный лекарственный препарат в соответствии с данными государственного реестра лекарственных средств, рассчитанной исходя из минимальной стоимости одной лекарственной формы, а в случае его отсутствия - не превышающую 80 % от максимальной зарегистрированной цены на аналогичный лекарственный препарат (по МНН, лекарственной форме и дозировке), рассчитанной исходя из минимальной стоимости одной лекарственной формы.
В связи с тем, что статус референтного лекарственного препарата, очевидно, будет устанавливаться в течение длительного промежутка времени, то следовательно в первое время будет применяться только положение «80 % от максимальной зарегистрированной цены на аналогичный лекарственный препарат (по МНН, лекарственной форме и дозировке).
С целью того, чтобы воспроизведенные препараты не препятствовали выходу
на рынок оригинальных и воспроизведенных препаратов, предлагаем не распространять данный пункт на вновь включенные препараты в перечень жизненно необходимых
и важнейших лекарственных препаратов в течение 3-6 месяцев в связи с тем,
чтобы препарат, который попадет в Реестр первым, не блокировал выход на рынок оригинальным и воспроизведенным препаратам, которые еще не были включены
в Реестр.
Торгово-промышленная палата Российской Федерации полагает целесообразным следующее.
1. Положениям проекта методики из общего количества исключаются экспортные поставки, поставки, осуществленные в рамках различных видов гуманитарной помощи, а также поставки лекарственных препаратов с остаточным сроком годности
менее 5%.
Торгово-промышленная палата Российской Федерации полагает целесообразным исключить из расчета средневзвешенной цены тендерные поставки, в связи с тем, что данные поставки осуществляются по государственным заказам с минимальной прибылью, либо вообще без прибыли. Это снижает реальную средневзвешенную отпускную цену препарата и снижает мотивацию производителя осуществлять поставки препаратов в рамках госпрограмм по минимальным ценам.
2. Торгово-промышленная палата Российской Федерации полагает целесообразным увеличить размер % остаточного срока годности, т. к. после снижения срока годности до 30% препарат становится неликвидным, и его поставки осуществляются с большим дисконтом, при низкой средневзвешенной цене % максимального
дисконта производителем может быть ограничен, что ограничивает его в возможности реализовать товар, и сильно повышает риски по истечению срока годности
препарата и дополнительные затраты на его уничтожение.
3. При расчете предельной отпускной цены на лекарственные препараты, наряду
с данными, предусмотренными пунктами 2 и 4 проекта методики, учитываются
ранее зарегистрированные предельные отпускные цены на такой же лекарственный
препарат того же производителя лекарственного препарата исходя из минимальной стоимости одной лекарственной формы.
Заявленная на государственную регистрацию предельная отпускная цена не может превышать ранее зарегистрированную предельную отпускную цену на заявленный производителем лекарственный препарат исходя из минимальной стоимости одной лекарственной формы, на основании приложения № 3 к проекту методики.
4. Согласно проектируемому пункту 13(1) держатель или владелец регистрационного удостоверения воспроизведенного лекарственного препарата (уполномоченное им лицо) представляет для государственной регистрации
предельную отпускную цену, не превышающую 80 % от зарегистрированной
предельной отпускной цены на референтный лекарственный препарат в соответствии
с данными государственного реестра лекарственных средств (далее – референтный лекарственный препарат), рассчитанной исходя из минимальной стоимости
одной лекарственной формы, а в случае его отсутствия, не превышающую 80 %
от максимальной зарегистрированной цены на аналогичный лекарственный препарат
(по международному непатентованному наименованию (далее – МНН), лекарственной форме и дозировке) рассчитанной исходя из минимальной стоимости одной лекарственной формы.
Участниками публичных консультаций была обозначена необходимость установления ограничительного периода в 10 лет (в виде возможности обращения
нового препарата с повышенной предельной отпускной ценой), в связи с тем,
что после указанного срока обращения на рынок выходят воспроизведенные лекарственные препараты, и они не должны быть ограничены планкой ценового ограничения 80% навсегда, так как производитель уже вернул себе вложенные инвестиции.
5. Участники публичных консультаций полагают целесообразным исключить формулировку проектируемого проектом акта пункта 13(1) «а в случае его отсутствия, не превышающую 80 % от максимальной зарегистрированной цены на аналогичный лекарственный препарат (по МНН, лекарственной форме и дозировке)», в связи с тем,
что экономическая преференция по защите интересов первого производителя обоснована, но все последующие воспроизведенные препараты должны иметь равный статус,
вводить преференции первому дженерику в случае ухода с рынка первого
производителя не целесообразно, т. к. ограничивает экономический потенциал других производителей.
6. Согласно проектируемому проектом акта пункту 14(1) для российских производителей и производителей государств-членов Евразийского экономического союза перерегистрация осуществляется:
а) в случае увеличения цен на сырье и материалы, используемые при производстве конкретного лекарственного препарата, а также накладных расходов, которое в равной степени влияет на уровень зарегистрированных цен на лекарственные препараты, отнесенные к одному международному непатентованному наименованию;
Согласно информации участников публичных консультаций российский производитель не может оперативно изменить производителя закупаемого сырья (фармацевтической субстанции), в случае резкого подорожания, так как каждая
субстанция прописывается и утверждается в фармакопейной статье предприятия
(далее – ФСП). Срок внесения изменения в ФСП составляет более полутора лет (поставка субстанции, наработка опытных образцов, получение данных по ускоренной стабильности, процедура экспертизы и регистрации изменения).
В нормативном документе иностранного производителя ограничений по номенклатуре используемых субстанций нет, и он может оперативно менять сырье исходя из условий производства и экономической ситуации.
В связи с этим, при резком росте стоимости определенной субстанции (закупаемой за валюту), на отечественного производителя изменение в рамках одного МНН повлияет, а на иностранного производителя нет.
В связи с этим участники публичных консультаций полагают целесообразным исключить слова: «которое в равной степени влияет на уровень зарегистрированных цен на лекарственные препараты, отнесенные к одному международному непатентованному наименованию».
7. Участниками публичных консультаций была обозначена необходимость обеспечения единообразного подхода к механизму формирования предельных отпускных цен для российских производителей на основе расчетно-затратного метода вне зависимости от стадии производства лекарственного препарата на территории Российской Федерации.
Данная мера необходима для стимулирования локализации производства лекарственных препаратов в Российской Федерации. В рамках же предложенного проекта методики неравнозначные подходы к производителям на территории Российской Федерации приведут к созданию дополнительных барьеров к локализации производства и выполнению задач, поставленных программой «Стратегия развития фармацевтической промышленности Российской Федерации на период до 2020 года».
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
