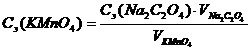Модуль 2. Занятие 7. Лабораторная работа по теме: «Перманганатометрическое титрование»
Стандартизация раствора перманганата калия по оксалату натрия
(с математической обработкой результатов анализа).
Реагенты:
Перманганат калия Сэ(KMnO4) = 0,1000 моль/дм3, fэ(KMnO4) = 1/5.
Серная кислота С(H2SO4) = 2,0000 моль/дм3.
Оксалат натрия Cэ(Na2C2O4) = 0,1000 моль/дм3, fэ(Na2C2O4)=1/2.
Этапы действий | Средства и условия выполнения | Критерии и формы самоконтроля |
1 | 2 | 3 |
1. Стандартизация рабочего раствора перманганата калия по оксалату натрия. | В колбу для титрования вместимостью 100,0 мл с помощью пипетки вносят аликвоту оксалата натрия 10,0 см3 и 20,0 см3 раствора серной кислоты. Содержимое колбы нагревают до 75-80оС. Бюретку заполняют раствором перманганата калия и устанавливают уровень жидкости в бюретке на нуле. Содержимое колбы титруют раствором перманганата калия, прибавляя раствор перманганата калия по каплям к горячему раствору. | В начале титрования каждую последующую каплю титранта прибавляют после исчезновения окраски от предыдущей капли. Затем, увеличив скорость титрования, титруют до появления бледно-розовой окраски, ослабевающей при стоянии в течение одной-двух минут. Титрование проводят не менее трех раз. Результаты параллельных определений должны совпадать. |
2. Расчет моляр-ной концентрации эквивалента, титра, титриметри-ческого фактора пересчета перман-ганата калия по оксалату натрия, поправочного коэффициента раствора перманганата калия. | Рассчитывают: а) молярную концентрацию эквивален-та рабочего раствора KMnO4
б) титр раствора KMnO4:
в) титр перманганата калия по оксалату натрия:
г) коэффициент поправки:
| Концентрация рабочего титрованного раствора KMnO4 должна быть близкой к Сэ(KMnO4) = 0,1000 моль/дм3. Коэффициент поправки приготовленного титрованного раствора перманганата калия приблизительно равен единице. |
3. Оформление протокола. | В лабораторном журнале описывают методику стандартизации рабочего раствора перманганата калия по оксалату натрия, химизм процесса, расстановку коэффициентов в реакции проводят методом полуреакций. Рассчитывают
Результаты определений проверяют у преподавателя, рассчитывают абсолютную и относительную ошибки. | Представление оформленного протокола преподавателю для проверки. |