Инженерная энзимология
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
БИОЛОГИЧЕСКИЙ ФАКУЛЬТЕТ
Кафедра биохимии
ИНЖЕНЕРНАЯ ЭНЗИМОЛОГИЯ
Практикум
МИНСК
2016
 УДК 577.15
УДК 577.15
ББК 28.902
П 69
Рекомендовано Ученым советом
биологического факультета
2016 г., протокол № 3
Составитель :
Рецензенты:
кандидат биологических наук, доцент
Инженерная энзимология. Практикум / сост. : . – Минск. : БГУ, 2016. – 11 с. |
Приводятся подробное описание методики постановки системы псевдопероксидазного окисления гемоглобином о-фенилендиамина и определения кинетических параметров процессов.
Для студентов биологического факультета БГУ специальности 1-31 01 01 «Биология (по направлениям)» учебная дисциплина предназначена для студентов направлений специальности 1-31 01 01-01 «Биология (научно-производственная деятельность)» и 1-31 01 01-03 «Биология (биотехнология)»
УДК 577.15
ББК 28.902
© БГУ, 2016
Определение кинетических параметров окисления о-фенилендиамина гемоглобином в присутствии перекиси водорода
Приготовление растворов
1) Цитратно-фосфатный буфер
Раствор А: в 250 мл дистиллированной воды растворяют: 2,8 г о-фосфорной кислоты (произвести перерасчет в объем (в мл), т. к. о-фосфорная кислота - это жидкость), 6 г лимонной кислоты и 1,77 г борной кислоты. К полученной смеси приливают 170 мл
1н NaOH (рассчитать массу навески, которую необходимо взять, чтобы приготовить
170 мл 1н раствора NaOH).
Для получения цитратно-фосфатного буфера с нужным значением рН 50 мл раствора А помещают в стакан и опускают в него электроды рН-метра. При перемешивании по каплям приливают 0,1н HCl или 0,1н NaOH пока не будет достигнуто нужное значение рН. Процедуру проделывают для каждого буфера отдельно.
Необходимо приготовить буферы со следующими значениями рН:
А) 2,0 (20мл); Б) 3,0 (20мл); В) 4,0 (20мл); Г) 5,0 (200мл); Д) 6,0 (20мл);
Е)7,0 (20мл); Ж) 8,0 (20мл).
Готовые буферы хранят в холодильнике при + 4 °С в течении недели.
2) Раствор перекиси водорода
В данной работе в качестве рабочего раствора используют 1 М раствор перекиси водорода. Молярную концентрацию стокового раствора определяют через коэффициент молярной экстинции ε 240 нм =46,3 М-1см-1. Раствор перекиси водорода готовят в день проведения эксперимента. Для этого необходимо:
1. Взять у лаборантов исходный раствор перекиси водорода.
2. Приготовить по 1 мл раствора перекиси водорода, разведенного в 10,100,1000,10000 раз. Разводить дист. водой последовательно.
3. Измерить оптическую плотность (А, в ед. опт. пл.) полученных растворов при 240 нм, контроль – дист. вода. Записать полученные значения.
4. По формуле закона Бугера-Ламберта-Бера: с=А/ε*l, (l-длина оптического пути=
1 см), произвести расчет концентрации (с, в моль/л) перекиси водорода в исходном растворе. Обязательно учесть разведение, т. е. полученную цифру необходимо умножить на разведение.
5. Исходный раствор перекиси водорода развести так, чтобы получилось 10 мл 1 М раствора перекиси водорода.
3) Раствор субстрата ( о-фенилендиамин, о-ФДА).
Готовят рабочий раствор с концентрацией субстрата 6·10 -3 М. Для этого 0,324 г
о-фенилендиамина растворяют в 25 мл диметилформамида, затем объем доводят до 50 мл дистиллированной водой. Готовый раствор субстрата хранят в холодильнике при + 4 °С в течении недели.
4) Рабочий раствор гемоглобина
В данной работе используют раствор гемоглобина концентрацией 4·10 -5 М. Необходимо рассчитать, какое количество гемоглобина (в мг) понадобиться для приготовления 5 мл раствора. В качестве растворителя использовать дист. воду. Раствор гемоглобина готовят в день проведения эксперимента. Молярная масса гемоглобина 65 000.
Экспериментальная часть
1. Зависимость начальной скорости реакции окисления о-ФДА от времени и концентрации гемоглобина
В соответствии с таблицей 1 в пробирки последовательно вносят буфер, гемоглобин, субстрат, аккуратно перемешивают при добавлении каждого компонента. Реакцию запускают внесением раствора пероксида водорода непосредственно перед измерением (поочередно в каждой пробирке).
Таблица 1
№ п/п | Рабочий раствор гемоглобина, мл | о-ФДА, мл | Н2О2, мл | Цитратно-фосфатный буфер (рН 5,0),мл |
1 серия | ||||
1* | 0,005 | 0,2 | 0,1 | 1,695 |
1 к** | 0,005 | 0,2 | - | 1,795 |
2 серия | ||||
2* | 0,01 | 0,2 | 0,1 | 1,69 |
2 к** | 0,01 | 0,2 | - | 1,79 |
3 серия | ||||
3* | 0,02 | 0,2 | 0,1 | 1,68 |
3 к** | 0,02 | 0,2 | - | 1,78 |
4 серия | ||||
4* | 0,05 | 0,2 | 0,1 | 1,65 |
4 к** | 0,05 | 0,2 | - | 1,75 |
*- опытные образцы.
** - контрольные образцы.
Проведение измерений
В качестве контроля используют контрольные образцы соответствующей серии проб. К опытным образцам приливают 0,1 мл 1 М раствора Н2О2, аккуратно перемешивают (одновременно включают секундомер и засекают время начала реакции) и переливают в кювету спектрофотометра. Измерение оптической плотности проводят при
λ = 455 нм (для гемоглобина) в течение
5 минут, записывая значения каждые 15 секунд. Все описанные операции повторяются с остальными сериями проб.
По результатам измерений строят графики зависимости ΔА455 (ΔА405) от времени для каждой концентрации гемоглобина.
Начальные скорости реакции рассчитывают по формуле:
![]()
где, l – длина оптического пути;
ε 455нм = 0,61 ·10 4 М-1 см-1 (для гемоглобина);
t (сек) – время реакции, в течении которого ΔА455 носит линейный характер.
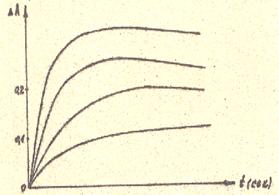
Рисунок 1 – Зависимость оптической плотности продуктов окисления о-ФДА гемоглобином в присутствии Н2О2.
Vo
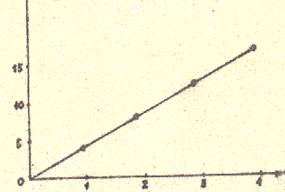 [ гемоглобин]
[ гемоглобин]
Рисунок 2 – Зависимость начальной скорости реакции окисления о-ФДА от концентрации гемоглобина
Сделать вывод о проделанной работе.
2. Зависимость начальной скорости реакции окисления о-ФДА от величин рН
В соответствии с таблицей 2 в пробирки последовательно вносят буфер, гемоглобин, субстрат, аккуратно перемешивают при добавлении каждого компонента. Реакцию запускают внесением раствора пероксида водорода непосредственно перед измерением (поочередно в каждой пробирке). Все пробы готовят, в одном повторе.
Таблица 2
№ п/п | Цитратно-фосфатный буфер (рН переменный),мл | Рабочий раствор гемоглобина, мл | О-ФДА, мл | |
рН | мл | |||
1 | Н2О | 1,75 | 0,05 | 0,2 |
2 | 2,0 | 1,65 | 0,05 | 0,2 |
3 | 3,0 | 1,65 | 0,05 | 0,2 |
4 | 4,0 | 1,65 | 0,05 | 0,2 |
5 | 5,0 | 1,65 | 0,05 | 0,2 |
6 | 6,0 | 1,65 | 0,05 | 0,2 |
7 | 7,0 | 1,65 | 0,05 | 0,2 |
8 | 8,0 | 1,65 | 0,05 | 0,2 |
Проведение измерений
В качестве контроля используют контрольный образец, приготовленный согласно таблице 2. К опытным образцам приливают 0,1 мл 1 М Н2О2 непосредственно перед измерением (поочередно в каждой пробирке), аккуратно перемешивают (одновременно включают секундомер и засекают время начала реакции) и переливают в кювету спектрофотометра. Измерение оптической плотности проводят при λ = 455 нм (для гемоглобина) в течение 3 минут, записывая значения каждых 10 секунд.
Результаты
Вычисляют значения V0 по формуле указанной в работе №1, строят графики зависимости начальной скорости окисления о-ФДА от величины рН цитратно-фосфатного буфера (рис. 3). На графиках указывают Vмакс, Km.
Vo
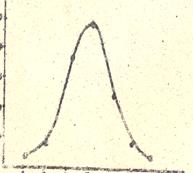 Значение рН буфера
Значение рН буфера
Рисунок 3 - Зависимость начальной скорости реакции окисления о-ФДА от величин рН цитратно-фосфатного буфера.
Сделать вывод о проделанной работе.
3. Зависимость начальной скорости реакции окисления о-ФДА от концентрации перекиси водорода
В соответствии с таблицей 3 в пробирки последовательно вносят буфер, гемоглобин, субстрат, аккуратно перемешивают при добавлении каждого компонента. Реакцию запускают внесением раствора пероксида водорода непосредственно перед измерением (поочередно в каждой пробирке). Все пробы готовят в одном повторе.
Таблица 3
№ п/п | Н2О2 | Цитратно-фосфатный буфер (рН 5,0),мл | о-ФДА, мл | Рабочий раствор гемоглобина, мл | |
Концентрация в системе,10-2 М
| 1М раствор Н2О2, (мл) | ||||
1 | - | - | 1,75 | 0,2 | 0,05 |
2 | 0,5 | 0,01 | 1,74 | 0,2 | 0,05 |
3 | 1,0 | 0,02 | 1,73 | 0,2 | 0,05 |
4 | 1,5 | 0,03 | 1,72 | 0,2 | 0,05 |
5 | 2,0 | 0,04 | 1,71 | 0,2 | 0,05 |
6 | 3,0 | 0,06 | 1,69 | 0,2 | 0,05 |
7 | 5,0 | 0,10 | 1,65 | 0,2 | 0,05 |
8 | 8,0 | 0,16 | 1,59 | 0,2 | 0,05 |
Проведение измерений
В качестве контроля используют контрольный образец (№1) приготовленный согласно таблице 3. К опытным образцам приливают указанное количество 1М Н2О2 непосредственно перед измерением (поочередно в каждой пробирке), аккуратно перемешивают (одновременно включают секундомер и засекают время начала реакции) и переливают в кювету спектрофотометра. Измерение оптической плотности проводят при
λ = 455 нм (для гемоглобина) в течение
3 минут, записывая значения каждые 10 секунд.
Результаты
Для каждой концентрации Н2О2 вычисляют значение V0 по формуле указанной в работе №1, строят графики зависимости начальной скорости окисления о-ФДА от концентрации перекиси водорода в прямых (рис. 4а) и двойных обратных координатах (рис. 4б).
На графиках указывают Vмакс, Km.
Vo
| 1/ Vo
|
Рисунок 4а - Зависимости начальной скорости окисления о-ФДА от концентрации перекиси водорода в прямых координатах | Рисунок 4б - Зависимости начальной скорости окисления о-ФДА от концентрации перекиси водорода в двойных обратных координатах |
Сделать вывод о проделанной работе.
4. Зависимость начальной скорости окисления о-ФДА от концентрации субстрата
В соответствии с таблицей 4 в пробирки последовательно вносят буфер, гемоглобин, субстрат, аккуратно перемешивают при добавлении каждого компонента. Реакцию запускают внесением раствора пероксида водорода непосредственно перед измерением (поочередно в каждой пробирке). Все пробы готовят в одном повторе.
Таблица 4
№ п/п | о-ФДА | Цитратно-фосфатный буфер (рН 5,0),мл | Рабочий раствор гемоглобина, мл | 1М Н2О2, мл | |
Концентрация в системе, 10-3 М
| Рабочий раствор (мл) | ||||
1 | - | - | 1,85 | 0,05 | 0,1 |
2 | 0,25 | 0,0085 | 1,84 | 0,05 | 0,1 |
3 | 0,5 | 0,017 | 1,83 | 0,05 | 0,1 |
4 | 1,0 | 0,034 | 1,82 | 0,05 | 0,1 |
5 | 1,5 | 0,050 | 1,80 | 0,05 | 0,1 |
6 | 2,5 | 0,083 | 1,77 | 0,05 | 0,1 |
7 | 3,5 | 0,117 | 1,73 | 0,05 | 0,1 |
8 | 6,0 | 0,2 | 1,65 | 0,05 | 0,1 |
В качестве контроля используют контрольный образец (№1) приготовленный согласно таблице 3. К опытным образцам приливают указанное количество 1 М Н2О2 непосредственно перед измерением (поочередно в каждой пробирке), аккуратно перемешивают (одновременно включают секундомер и засекают время начала реакции) и переливают в кювету спектрофотометра. Измерение оптической плотности проводят при
λ = 455 нм (для гемоглобина) в течение 3 минут, записывая значения каждые 10 секунд.
Для каждой концентрации о-ФДА вычисляют значение V0 по формуле указанной в работе №1, и строят график зависимости начальной скорости реакции от концентрации о-ФДА в прямых (см. рис. 5а) и двойных обратных координатах (см. рис. 5б). На графиках указывают Vмакс, Km.
Vo
| 1/ Vo
|
Рисунок 5а Зависимости начальной скорости окисления о-ФДА от концентрации субстрата в прямых координатах | Рисунок 5б Зависимости начальной скорости окисления о-ФДА от концентрации субстрата в двойных обратных координатах |
Сделать вывод о проделанной работе.
Учебное издание
ИНЖЕНЕРНАЯ ЭНЗИМОЛОГИЯ
Практикум
Составитель
Кузнецова Екатерина Игоревна
Редактор
Художник обложки
Технический редактор
Компьютерная верстка
Корректор
Подписано в печать. Формат 60´84/16. Бумага офсетная.
Печать офсетная. Усл. печ. л. . Уч.-изд. л. . Тираж экз. Заказ
Белорусский государственный университет.
Свидетельство о государственной регистрации издателя, изготовителя, распространителя печатных изданий № 1/270 от 03.04.2014.
Пр. Независимости, 4, 220030, Минск.
Республиканское унитарное предприятие “Издательский центр Белорусского государственного университета”.
Свидетельство о государственной регистрации издателя, изготовителя, распространителя печатных изданий № 2/63 от 19.03.2014.
Ул. Красноармейская, 6, 220030, Минск.


 [Н2О2]
[Н2О2]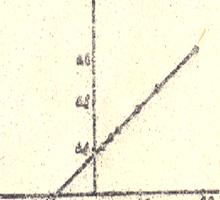 1/ [Н2О]
1/ [Н2О] [о-ФДА]
[о-ФДА] 1/ [о-ФДА]
1/ [о-ФДА]