СВОЙСТВА ЭЛЕМЕНТОВ VIII ГРУППЫ
ПЕРИОДИЧЕСКОЙ СИСТЕМЫ МЕНДЕЛЕЕВА.
СЕМЕЙСТВО ЖЕЛЕЗА
Элементы первой триады 8-й группы периодической системы образуют семейство железа. Некоторые физические свойства этих металлов приведены ниже в таблице.
Атомы этих элементов имеют во внешнем электронном слое на
s-подуровне 2 электрона (таблица), остальные валентные электроны расположены на d-подуровне предпоследнего слоя.
Сходство этих элементов выражено в свойственной им способности намагничиваться, проявлять основные степени окисления +2 и +3, а также в большой склонности к образованию комплексных соединений. Все три элемента представляют собой белые металлы с сероватым или серебристым (Fe, Co) оттенком. Железо и никель легко куются и прокатываются. Кобальт более тверд и хрупок. По значению электродных потенциалов железо значительно активнее кобальта и никеля. Эти элементы вытесняют водород из разбавленных кислот с образованием солей, проявляя при этом степень окисления +2. Концентрированная азотная кислота пассивирует эти металлы. Fe, Co, Ni устойчивы к действию концентрированной серной кислоты, а также к действию крепких щелочей.
Физико-химические свойства
Символ элемента | Поряд-ковый номер | Распре- деление электронов во внешних слоях | Атомная масса | Удельный вес, г/см3 | Темпе-ратура плавления, °С | Темпе-ратура кипения, °С | Стандартные электродные потенциалы | |
электрод | потенциал | |||||||
Fe | 26 | ..3d64s2 | 55.85 | 7.86 | 1528 | 2735 | j° Fe2+/Fe | –0,44 |
Co | 27 | ..3d74s2 | 58.94 | 8.83 | 1490 | 3100 | j° Co2+/Co | –0,27 |
Ni | 28 | ..3d84s2 | 58.71 | 8.90 | 1452 | 2840 | j° Ni2+/Ni | –0,25 |
Компактные химически чистые Fe, Co, Ni не реагируют с водой и воздухом. Однако техническое железо во влажном воздухе очень быстро корродирует с образованием ржавчины (nFe2O3∙mH2O). Продукт коррозии порист, хрупок и не предохраняет металл от дальнейшего разрушения.
В мелко раздробленном виде три металла обладают пирофорными свойствами, т. е. исключительно легко соединяются с кислородом воздуха.
Для металлов Fe, Co, Ni характерно большое сродство к кислороду и к сере. Причем сродство к кислороду в ряду слева направо падает, а к сере – возрастает. Все три металла хорошо реагируют с неметаллами: С, Р, N, Si, галогенами. Силициды, карбиды и нитриды этих металлов имеют практическое и промышленное значение.
Все три металла способны окклюдировать, т. е. включать в свою решетку водород, образуя при этом гидриды переменного состава. Особенно активно поглощает водород никель в мелко раздробленном состоянии, поэтому никель широко применяют в качестве катализатора в реакциях гидрирования. В своих устойчивых соединениях Fe, Co, Ni чаще всего проявляют степень окисления +2, +3. Для железа одинаково характерны оба этих состояния, тогда как при переходе к кобальту и особенно к никелю значение степени окисления +3 уменьшается.
Соединения с другими значениями степени окисления (+4, +5, +6 и др.) для кобальта и никеля неустойчивы и практического применения не имеют, для железа характерно образование устойчивых ферратов BaFeO4, K2 FeO4 (степень окисления +6).
Элементы этого семейства в степени окисления +2 образуют с кислородом оксиды – закиси с общей формулой ЭО. FeO – черного, СоО – серо-зеленого, NiO – зеленого цвета. Закиси не растворяются в воде и щелочах, но растворимы в кислотах. Fe(OH)2 и Co(OH)2 растворяются в концентрированных горячих щелочах с образованием комплексных соединений типа Na2Fe(OH)4, Na2Co(OH)4, проявляя при этом слабую амфотерность.
Дигидроксиды Э(ОН)2 получают взаимодействием растворов соответствующих солей с разбавленными растворами щелочей.
Образующиеся при этом осадки (Fe(OH)2 – белый, Co(OH)2 – розовый, Ni(OН)2 – светло-зеленый) сильно отличаются друг от друга по отношению к кислороду воздуха. Ni(OН)2 устойчив, Co(OH)2 медленно окисляется до бурого Co(OH)3, Fe(OH)2 очень энергично превращается в красно-бурый тригидроксид Fe(OH)3:
4 Fe(OH)2 + О2 + 2Н2О = 4 Fe(OH)3.
Дигидроксид Ni(OН)2 можно перевести в тригидроксид Ni(OН)3 только под действием окислителя (Cl2, Br2) в щелочной среде
2 Ni(OН)2 + 2NaOH + Br2 = 2 Ni(OН)3 + 2NaBr.
Хлориды, сульфаты, нитраты Fe, Co, Ni(II) хорошо растворимы в воде, их растворы вследствие гидролиза имеют слабокислую среду. Гидратированные ионы окрашены: Fe2+ – светло-зеленый, Co2+ – розово-красный, Ni2+ – ярко-зеленый.
Кислородные соединения Э+3 образуют ряд оксидов: Fe2O3 – красно-бурый, Со2О3 – темно-коричневый, Ni2O3 – серо-черный. Эти оксиды нерастворимы в воде и разбавленных щелочах, но растворимы в кислотах, концентрированных щелочах. Оксиды Со2О3 и Ni2O3 растворимы в водных растворах аммиака и аммонийных солей с образованием комплексных соединений.
Тригидроксиды Э(ОН)3 можно получить только косвенным путем. Свежеприготовленные тригидроксиды образуют гели - Э(ОН)3 и, постепенно теряя воду, переходят в кристаллическую форму ЭООН:
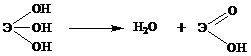
Соединения типа ЭО(ОН) получили название оксигидроксидов. Тригидроксиды Fe(OH)3, Co(OH)3, Ni(OН)3 проявляют амфотерные свойства, причем амфотерность усиливается в ряду слева направо, вследствие чего Э(ОН)3 легко растворимы в кислотах и заметно растворимы в горячих концентрированных щелочах. Тригидроксиды Co(OH)3, Ni(OН)3 легко растворяются в водных растворах аммиака и солей аммония с образованием аммиачных комплексов типа
[Co(NH3)6]3+; [Ni(NH3)6]3+.
При действии кислот на гидроксиды Co(OH)3 и Ni(OН)3 соответствующие им соли Со(Ш) и Ni(III) не могут быть получены, так как происходит восстановление до Co2+ и Ni2+. Следовательно, гидроксиды кобальта(III) и никеля(III) проявляют окислительные свойства:
4Co(OH)3 + 4H2SO4 = 4CoSO4 + 10H2O + O2
2Ni(OН)3 + 6HCl = 2NiCl2 + 6H2O + Cl2.
Тригидроксид железа, растворяясь в кислотах, образует соли железа(III):
Fe(OH)3 + 3 HCl = FeCl3 + 3 H2O.
Соли железа(III) в большинстве своем растворимы в воде и сильно подвергаются гидролизу. Наибольшее применение находит соль FeCl3∙6 H2O, соли железа(III) – слабые окислители.
Кроме указанных выше оксидов для Fe, Co, Ni, известны еще и смешанные оксиды Fe3O4, Co3O4, Ni3O4. Оксид Fe3O4 – (FeO∙Fe2O3) – наиболее устойчив и образуется при прокаливании железа на воздухе
3Fe + 2O2 = Fe3O4.
Fe3O4 – вещество черного цвета с металлическим блеском. Fe, Co, Ni – обладают склонностью к комплексообразованию, дают множество комплексных соединений. Большое значение имеют комплексные соли железа, например, K4[Fe(CN)6] – желтая кровяная соль, или феррицианид калия.
При действии соли K4[Fe(CN)6] на раствор соли Fe3+ образуется темно-синий осадок берлинской лазури
4 FeCl3 + 3 K4[Fe(CN)6] = Fe4[Fe(CN)6]3 ¯+ 12 KCl
4 Fe3+ + 3[Fe(CN)6]4– = Fe4[Fe(CN)6]3
Красная кровяная соль K3[Fe(CN)6] – является реактивом на соли железа(II), образуя с ионом Fe2+ темно-синий осадок (турнбулевая синь):
3FeSO4 + 2 K3[Fe(CN)6] = Fe3[Fe(CN)6]2 ¯+ 3 K2SO4
3 Fe2+ + 2[Fe(CN)6]3– = Fe3[Fe(CN)6]2
Кобальт и никель образуют много комплексных соединений, причем кобальт в этих соединениях почти всегда имеет степень окисления +3, а никель +2. Наиболее типичные координационные числа 6 и 4. Примерами соединений такого типа могут служить [Co(NH3)6]Cl3, Na2[NiCl4], K3[Co(NO2)6], [Ni(NH3)6](OH)2.



