Московский государственный университет имени
Факультет биоинженерии и биоинформатики
Влияние полиэтиленимина на получение антисывороток и антител к диен-платинированным ДНК и РНК.
Курсовая работа
студентки 2 курса
Тьютор
д. х.н. , заведующий лабораторией
нуклеиново-белковых взаимодействий
НИИ ФХБ им. МГУ, и аспирант
30 апреля 2010г.  //
//
Москва, 2010
ОГЛАВЛЕНИЕ
1.СПИСОК СОКРАЩЕНИЙ……………………………………………………………….....3
2. ВВЕДЕНИЕ…………………………………………………………………………………...4
3. ЛИТЕРАТУРНЫЙ ОБЗОР…………………………………………………………………6
4. МАТЕРИАЛЫ И МЕТОДЫ………………………………………………………………..9
4.1. Выделение и характеристика суммарной РНК клеток асцитной карциномы Кребс II…………………………………………………………………………………………...9
4.1.2. Выделение суммарной РНК клеток Кребс II фенольно-детергентным методом.............. 8
4.3. Иммунизация кроликов и получение антисывороток................................................ 10
4.4. Анализ специфичности антисывороток к ДНК - и РНК-(диен)платине методом «иммунозолото» 10
4.5 Выделение антител.............................................................................................................. 10
4.5.1 Сульфат-аммонийное фракционирование........................................................................ 10
5. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ..................................................................................... 12
5.1. Выделение и характеристика суммарной РНК клеток асцитной карциномы Кребс II 12
5.2. Получение и анализ специфичности антисывороток к ДНК - и РНК-(диен)платине методом «иммунозолото»......................................................................................................................... 16
1 2 3 4 5 6 7 8...................................................................................... 17
Таким образом, иммунохимическим методом было показано, что антитела узнают немеченую РНК (500 нг).......................................................................................................................................... 19
6. ВЫВОДЫ................................................................................................................................ 20
7.СПИСОК ЛИТЕРАТУРЫ..................................................................................................... 21
1.СПИСОК СОКРАЩЕНИЙ
(диен)платина - - хлордиэтилентриаминоплатина хлористая
Трис – трис(гидроксиметил)аминометан
НТХА - нетоксичный хаотропный агент
SDS – додецилсульфат натрия
ЭДТА - этилендиаминтетрауксусная кислота
ТДB - тридистиллированная вода
ВЭМК – вирус энцефаломиокардита
ПЭИ – полиэтиленимин-5000
NaФБ – натрий фосфатный буфер
2.ВВЕДЕНИЕ
В настоящее время в практической молекулярной диагностике бактериальных и вирусных инфекций используют методы, основанные на обнаружении специфических антигенов возбудителя. Наряду с иммунохимичекими методами для определения патогенов широкое применение нашли методы, основанные на гибридизации нуклеиновых кислот. Обычно ДНК или РНК, комплементарную протяженной нуклеотидной последовательности генома патогена, для получения соответствующего НК-зонда метят какой-либо меткой, для которой разработана чувствительная система ее детекции. Наиболее часто в качестве метки используется биотин, обнаружение которого опосредовано авидином или стрептавидином
В нашей лаборатории для синтеза зонда ДНК химически метили хлордиэтилентриаминоплатиной хлористой (сокращенно – (диен)платиной), а для детекции гетеродуплексов, образующихся при гибридизации НК-зонда с нуклеиновой кислотой патогена, использовали антитела к соединению ДНК-(диен)платина.
+ | + |
CH2 – CH2 – NH - CH2 – CH2 | |
| | | _ | |
NH2- - - - - - Pt- - - - - - - NH2 Cl | |
| Cl |
Рис. 1. Структурная формула хлордиэтилентриаминоплатины хлористой.
Взаимодействие ДНК-(диен)платины с ДНК происходит легко, в мягких условиях, с образованием прочных координационных связей. Антитела к ДНК-(диен)платине специфичны, они слабо взаимодействуют с немодифицированными нативными и денатурированными ДНК. Термическая обработка модифицированной ДНК не приводит к ее разрушению, т. е. комплекс достаточно стабилен. [Pt(dien)Cl]Cl практически не меняет температуру плавления ДНК. Одной из основных особенностей комплекса [Pt(dien)Cl]Cl является то, что он образует с ДНК только монофункциональные соединения. Взаимодействие [Pt(dien)Cl]Cl с ДНК происходит по N7- положению гуанина при молярном соотношении [Pt(dien)Cl]Cl и нуклеотидов ДНК 1:10. Выше этого соотношения связывание (диен)платины может происходить также по N7- положению аденина. Использованное нами аминопроизводное Pt имеет ряд особенностей, полезных для синтеза зонда и практической диагностики с использованием гибридизации нуклеиновых кислот: реакция образования аддукта при синтезе зонда идет количественно, не требуется очистки от непрореагировавших веществ, высокая скорость модификации ДНК позволяет сократить процедуру мечения гибридизационного зонда до 1,5-2 часов, модификация нуклеиновой кислоты [Pt(dien)Cl]Cl по гуанину до степени, не превышающей 10%, практически не приводит к нарушению вторичной структуры и стабильности макромолекулы, антитела к ДНК-(диен)платине обладают хорошей аффинностью, следствием чего является высокая чувствительность диагностики.
Препарат антител к ДНК-(диен)платине и РНК-(диен)платине предполагается использовать для диагностики инфекций, вызываемых представителями рода кардиовирусов (РНК-содержащих вирусов), вызывающих воспаление головного и спинного мозга грызунов - вирусом энцефаломиокардита и вирусом Менго.
Задача курсовой работы - получение антисывороток и характеристика антител к (диен)-платинированным ДНК и РНК.
3.ЛИТЕРАТУРНЫЙ ОБЗОР
Иммуногенные и антигенные свойства нуклеиновых кислот
С химической точки зрения, если проанализировать строение нуклеиновых кислот и белков, можно заметить, что по сравнению с нуклеиновыми антигенами иммуногенные свойства белков должны быть более сильными, а разнообразие иммунного ответа организма (антител) в ответ на белки более представительным, чем к нуклеиновым кислотам. Этот вывод можно сделать из анализа структуры нуклеиновых кислот и белков: на белковые молекулы приходится 20 различных по химической структуре составляющих звеньев, в то время как в нуклеиновой кислоте их всего 4. Следовательно, белки как антигены многообразнее, а антигенные свойства нуклеиновых кислот в равнении с белками – вырождены. К тому же нуклеиновые кислоты - слабые антигены. Если бы нуклеиновые кислоты были бы сильными антигенами, то антитела на чужеродную ДНК или РНК могли бы, попадая в клетки, влиять на функции похожих по составу и последовательностям нуклеотидов нуклеиновых кислот хозяина, что потенциально может приводить к автоиммунным заболеваниям.
Способы приготовления антигенов на основе нуклеиновых кислот
Для решения проблемы слабой иммуногенности нуклеиновых кислот применяются различные методы, такие как получение конъюгата белка с нуклеиновой кислотой или с нуклеиновым основанием. В качестве белка-носителя используют бычий или кроличий сывороточный альбумин, глобулины, синтетические полипептиды.
Например, были синтезированы антигены, в которых белок был соединен с пуриноилом. При определенных условиях проводили реакцию между модифицированным азотистым основанием (6-трихлорметилпурином) и аминогруппами остатков лизина белка. Образовывалось ковалентное соединение.[1]
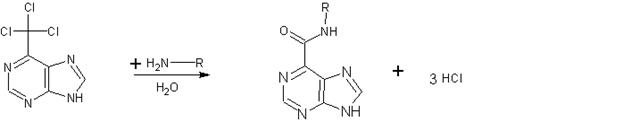
Рис.2 Реакция между (6-трихлорметилпурином) и аминогруппами остатков лизина
Антисыворотки, получаемые к конъюгированным антигенам, содержат антитела не только к нуклеиновым кислотам и основаниям, но и к белковому носителю. Поэтому необходимо проводить очистку сыворотки от антител к белку-носителю.
Другой путь – химическая модификация самой нуклеиновой кислоты. Это повышает вероятность иммунного ответа на РНК или ДНК за счет внесенных модификаций и увеличения времени жизни нуклеиновой кислоты в тканях иммунизуемого животного.
Модификации ДНК с transPt (транс-диаминдихлорплатина) и [Pt(dien)Cl]Cl, при которых образуются координационные комплексы платины и нуклеотидов, применяли в качестве метки для гибридизационных зондов. Было показано, что метод может быть использован для детекции инфекционных заболеваний в клиническом материале (Chlamydia Trachomatis и Ureaplasma Urealyticum). [2]
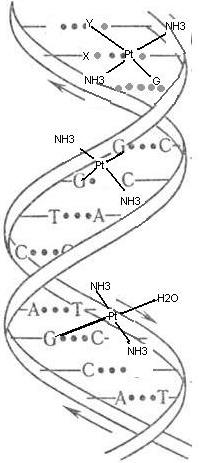
Рис.3 Взаимодействие transPt с ДНК (X и Y – нуклеотиды). [3]
Наконец, возможно образование комплекса, в котором белковый носитель объединяется с нуклеиновой кислотой или олигонуклеотидом ионными связями. Нуклеиновые кислоты как кислые полимеры способны соединяться с основными белками, например с метилированным бычим сывороточным альбумином. Ионные связи между ними достаточно прочны.[4]
Применение антител к нуклеиновым кислотам
Интерес к антителам к ДНК и РНК объясняется многими медицинскими приложениями. Известно, что при системных аутоиммунных заболеваниях отмечается повышение титра антител к нуклеиновым кислотам в сыворотках животных и человека. В настоящее время антитела к нуклеиновым кислотам используются для практической диагностики развития системных аутоиммунных заболеваний. Эти антитела можно использовать для исследования механизма аутоиммунных заболеваний. Антитела к нуклеиновым кислотам представляют интерес для изучения белок-нуклеиновых взаимодействий.
4.МАТЕРИАЛЫ И МЕТОДЫ
4.1. Выделение и характеристика суммарной РНК клеток асцитной карциномы Кребс II
4.1.1. Выделение суммарной РНК клеток асцитной карциномы Кребс II с помощью нетоксичного хаотропного агента (НХТА)
Осадок клеток асцитной карциномы Кребс II в буферном растворе с сахарозой (8% сахароза, 10 мМ трис-НCl, 1 мМ MgCl2, pH 7,5-8,0), любезно предоставленный , хранили, при температуре -70оС (сахароза в буферном растворе при пониженных температурах препятствует образованию кристаллов льда, способных разрушить клетки).
К 100 мг замороженного осадка клеток добавили 1 мл гипотонического буфера (10 мМ трис-HCl, 15 мМ NaCl, 1 мМ MgCl2, pH 7,5-8,0), суспендировали осадок и выдерживали 20 мин в ледяной бане. Затем суспензию гомогенизировали в ручном гомогенизаторе Даунса (20 тракций) и центрифугировали 10 мин при 6000 об/мин в центрифуге Eppendorf Mini Spin (в осадке – ядерная фракция). К супернатанту добавляли равный объем НТХА (4 M CCl3COONH4, 100 мМ трис-HCl, 25 мМ ЭДТА, 1,5% тритон Х-100, рН 7,5-8,0) и выдерживали 30 мин в ледяной бане, затем к смеси добавляли равный объем 100% изопропилового спирта и оставляли на ночь при 0оС. Осадок суммарной РНК выделяли центрифугированием (15 мин при 12000 об/мин), промывали 2 раза 85 % этиловым спиртом, подсушивали в вакуум-эксикаторе 5 мин и растворяли в 20-100 мкл тридистиллированной воды.
4.1.2. Выделение суммарной РНК клеток Кребс II фенольно-детергентным методом
В 2 пробирки с 200 мг замороженных в 8% сахарозе клеток Кребс II добавляли по 500 мкл гипотонического буфера 1 (10 мМ трис-HCl, 15 мМ NaCl, 1 мМ MgCl2, pH 7,5-8,0), суспендировали и выдерживали 5 мин в ледяной бане. Затем добавляли по 250 мкл гипотонического буфера 2 (10 мМ HEPES, 15 мМ (CH3COO)2Mg, 6 мМ β-меркаптоэтанол, рН 7,0), перемешивали и выдерживали 5 мин в ледяной бане. Суспензию клеток гомогенизировали в гомогенизаторе Даунса на 7 мл (6 тракций), гомогенат центрифугировали 10 мин при 7000 об/мин на холоде в центрифуге Eppendorf 5415C. К супернатанту добавляли 10% SDS до конечной концентрации 0,1% и проводили несколько депротеинизаций, добавляя равный объем депротеинизирующей смеси (насыщенный 1 М трис-HCl фенол : хлороформ = 9:1) до исчезновения интерфазы (после первой депротеинизации проводили экстракцию механически захваченной РНК из интерфазы 100-500 мкл 50 мМ трис-HCl, 10 мМ ЭДТА, 1% SDS, рН 7,5-7,8 (100 мкл буфера на 1 мм толщины интерфазы)). Для депротеинизации и экстракции суммарной РНК смесь перемешивали 3-5 мин на встряхивателе Vortex и центрифугировали на холоде при 13000 об/мин в центрифуге Eppendorf 5415C (при первой депротеинизации 10 мин, затем по 3 мин). Для высаживания РНК к водной фазе добавляли 1/10 объема 3М CH3COONa, pH 5,3 и 1,5 объема изопропилового спирта и выдерживали смесь в течение ночи при 0оС (в ледяной бане в холодной комнате). Осадки суммарной РНК выделяли центрифугированием (15 мин при 13000 об/мин на холоде в центрифуге Eppendorf 5415C), промывали 3 раза по 200 мкл 85% этиловым спиртом (центрифугировали 3 мин при 13000 об/мин в центрифуге Eppendorf Mini Spin), высушивали в вакуум-эксикаторе и растворяли в 20 мкл тридистиллированной воды.
4.1.3. Спектрофотометрическая характеристика суммарной клеточной РНК
В контрольную и измерительную кюветы вносили по 500 мкл тридистиллированной воды (ТДB) для определения базовой линии прибора. Затем в измерительную кювету помещали образец суммарной РНК, снимали спектр поглощения в ультрафиолетовой области на спектрофотометре Hitachi U-2800A и определяли значение поглощения при 230 нм (А230), 260 нм (А260) и при 280 нм (А280).
4.1.4. Электрофоретическая характеристика суммарной клеточной РНК
Образцы суммарной РНК неинфицированных, инфицированных вирусом Менго и инфицированных ВЭМК клеток Кребс II (по 3 мкг) анализировали методом нативного электрофореза в 1% агарозном геле с 0,5 мкг/мл бромистого этидия в ТВЕ-системе (89 мМ трис-HCl, 89 мМ H3BO3, 2 мМ ЭДТА, рН 8,0). Образцы РНК денатурировали 3 мин при 70оС в твердотельном термостате CycloTemp, охлаждали 5 мин в ледяной бане, добавляли по 2 мкл буфера для образцов (50% глицерин, 0,01% бромфеноловый синий, 0,01% ксиленцианол, конечный объем образцов 10 мкл), центрифугировали 3 мин при 13000 об/мин в микроцентрифуге Eppendorf MiniSpin и наносили на гель. Электрофорез проводили сначала 15 мин при 30 мА, затем 1 ч при 50 мА на приборе ПЭФ-200 (Россия). Гель смотрели на УФ-хемископе (длина волны 302 нм) и фотографировали на цифровой фотокамере.
4.2. Синтез антигенов «ДНК-(диен)платина» и «РНК-(диен)платина
Для приготовления антигенов использовали ДНК из эритроцитов цыплят (C=2,553 мг/мл) и суммарную РНК из неинфицированных клеток асцитной карциномы Кребс II. ДНК и РНК модифицировали хлордиэтилентриаминоплатиной хлористой (сокращенно – (диен)платиной, см. рис. 1) при соотношении атомов платины и нуклеотидов 1:2.
4.2.1. Модификация нуклеиновых кислот (диен)платиной
100 мкг ДНК или РНК в 10 мМ NaClO4 (конечный объем смеси 1 мл) денатурировали нагреванием: ДНК денатурировали 5 мин при 100оС (на кипящей водяной бане), РНК – 3 мин при 65 оС. После денатурации растворы быстро охлаждали до 0оС в ледяной бане. Затем добавляли 15 мкл 10 мМ (диен)платины (аккуратно на стенку пробирки, чтобы не было чрезмерной локальной модификации), перемешивали и инкубировали 1 ч при 65оС. После инкубации растворы охлаждали до 0оС в ледяной бане в течение 5 мин. Полученные антигены хранили при -20оС.
4.2.2. Приготовление антигенов
В настоящей работе в методику приготовления антигенов были внесены изменения, а именно, для усиления иммунного ответа перед иммунизацией к модифицированным (диен)платиной нуклеиновым кислотам добавляли полиэтиленимин.
Нельзя исключить, что в слабый иммунный ответ на нуклеиновые кислоты вносят отрицательный вклад клеточные нуклеазы. Чтобы защитить платинированные ДНК и РНК от действия нуклеаз в организме кроликов, мы исследовали их защиту полиэтиленимином-5000 (положительно заряженный полиэтиленимин образует комплекс с отрицательно заряженными полинуклеотидами).
…[—NH—CH2— CH2— NH—CH2— CH2—]…
Рис. 4 Структурная формула полиэтиленимина.
К растворам ДНК - и РНК-(диен)платины добавляли 1М трис-HCl, рН7,5 до 20 мМ и 0,9 мкл раствора ПЭИ-5000 (С=50 мг/мл, соотношение нуклеотидов и аминогрупп 1:3 ) и, инкубировали смесь 20 мин при комнатной температуре.
4.3. Иммунизация кроликов и получение антисывороток
4.3.1. Иммунизация кроликов
Для первых трех иммунизаций к растворам комплексов ДНК - и РНК-(диен)платины с полиэтиленимином (С~100 мкг/мл) добавляли равный объем адъюванта Фрейнда (полного для первой иммунизации и неполного для второй и третьей), для последующих иммунизаций – равный объем PBS (фосфатно-солевой буфер, по составу близок к внутренней среде организма). Адъювант Фрейнда содержит водно-масляную эмульсию (помогает антигену дольше жить в организме животного) и убитые бактерии Staphylococcus aureus, которые являются мощным стимулятором неспецифических иммунных реакций (полный адъювант Фрейнда содержит протопласты и клеточные стенки стафилококка, неполный – только протопласты). Кроликов иммунизовали подкожно в 6 точек на спине с интервалами 10-14 дней. Количество антигена при разовой иммунизации составляло 100 мкг. Всего было проведено 8 иммунизаций.
4.3.2. Отбор крови и получение антисывороток
Для получения контрольных (с «нулевым» иммунным ответом) сывороток у кроликов брали 10-15 мл преиммунной крови. Через 7-10 дней после каждой иммунизации проводили отбор крови кроликов объемом 10-15 мл из ушной вены (при необходимости смазывали ухо толуолом для усиления кровотока в вене).
Полученную кровь выдерживали на холоде в течение 1 часа, центрифугировали 10 мин при 3000-4000 об/мин в центрифуге Jouan-Paris и отбирали антисыворотку. Антисыворотки расфасовывали в пробирки по 2 мл, добавляя 4% азид натрия до конечной концентрации 0,02%, и хранили при -70оС.
4.4. Анализ специфичности антисывороток к ДНК - и РНК-(диен)платине методом «иммунозолото»
Нитратцеллюлозные мембраны Protran BA 85 (Schleicher&Schuell) 3х27 мм, вымачивали их по 5 мин в воде MilliQ и в 20*SSC, а затем удаляли избыток жидкости фильтровальной бумагой и высушивали. Готовили последовательные 10-кратные разведения меченных (диен)платиной и немеченых ДНК и РНК (от 100 до 0,1 нг/мкл) и наносили их в точку по 1 мкл на мембраны. Затем мембраны помещали лицевой стороной вверх на предметное стекло с фильтровальной бумагой, смоченной 20*SSC, и фиксировали ДНК и РНК ультрафиолетовым светом сверху (длина волны 253,7 нм, энергия 720 мДж) 6 раз по 120мДж на приборе UV Stratalink 1800 (Stratagene).
Мембраны инкубировали в блокирующем буфере (PBS с 5% BSA) 1 ч при комнатной температуре, промывали 3 раза по 5 мин буфером для промывок (PBS с 0,1% BSA). Затем мембраны инкубировали в растворах первичных антител (преиммунные и иммунные сыворотки, разбавленные в 25 раз буфером для промывок) 2 ч при комнатной температуре и в течение ночи при +6 оС, затем снова промывали 3 раза по 5 мин буфером для промывок. Далее мембраны инкубировали 1,5 ч при комнатной температуре в растворе вторичных антимкл буфера для промывок, 15 мкл желатина, 3 мкл раствора козьих антител к иммуноглобулинам кролика, конъюгированных с коллоидным золотом (GE Healthcare)) и промывали 2 раза по 5 мин буфером для промывок и 2 раза по 1 мин водой milliQ. Затем мембраны инкубировали в темноте в смеси серебряного усилителя и инициатора (1:1, GE Healthcare) до появления видимых сигналов, промывали 3 раза водой milliQ по 5 мин, высушивали на фильтровальной бумаге и сканировали на сканере Mustek 1200 CU.
4.5 Выделение антител
4.5.1 Сульфат-аммонийное фракционирование
Антисыворотки к ДНК и РНК–(диен)платине помещали в поликарбонатные центрифужные стаканы ротора JA-14, охлаждаемые на ледяной бане, и добавляли по каплям при перемешивании 0,5 объема насыщенного раствора (NH4)2SO4. Смеси оставляли на ночь при +6оС в холодной комнате. Осадки (крупные белковые агрегаты) отделяли центрифугированием при 6000 об/мин в течение 15 мин. Супернатанты осторожно переносили в чистые центрифужные стаканы, охлаждаемые во льду, добавляли по каплям при перемешивании 0,5 объема (от первоначального объема сыворотки) насыщенного холодного раствора (NH4)2SO4, снова оставляли на ночь при +6оС и центрифугировали в тех же условиях. Осадки суспендировали стеклянной палочкой в минимальном объеме насыщенного раствора (NH4)2SO4, переносили в пробирки на 50 мл, центрифугировали 15 мин при 4000 об/мин в центрифуге Jouan-Paris и отбирали супер. Осадок глобулинов к РНК-(диен)платине помещали на -20оС, осадок глобулинов к ДНК-(диен)платине растворяли в минимальном объеме 20 мМ Na-фосфатного буфера, рН 7,0.
4.5.2 Диализ раствора антител к РНК-(диен)платине
Диализную трубку кипятили сначала 5 мин в 10 мМ NaHCO3, потом 2 раза по 5 мин в 10 мМ ЭДТА, затем промывали водой MilliQ и проверяли на герметичность, зажимая с одного конца зажимом и заполняя водой MilliQ. Раствор глобулинов к ДНК-(диен)платине в 20 мМ Na-фосфатном буфере, рН 7,0 количественно переносили в диализную трубку и зажимали второй конец трубки зажимом. Диализ проводили при +6оС против 2 смен по 500 мл 20 мМ Na-фосфатного буфера, рН 7,0 (в течение 3 ч и в течение ночи) при постоянном перемешивании внешнего раствора. После диализа содержимое диализной трубки переносили в пробирку и снимали спектр поглощения раствора глобулинов.
4.5.3 Хроматография антител на протеин G сефарозе
Собрали хроматографическую систему, состоящую из колонки с протеин G сефарозой (GE Healthcare, объем 1 мл), проточного УФ-денсиметра Uvicord (ISCO, длина волны 280 нм) и перистальческого насоса Gilson. Кюветы денсиметра и все шланги промывали 1 объемом 1% SDS и 20 объемами воды milliQ и заполняли 20 мМ NaФБ, рН 7,0.
Колонку уравновешивали 10 мл 20 мМ NaФБ, рН 7,0. Наслаивали на колонку 1 мл раствора глобулинов (концентрация белка 18,32 мг/мл), собирали фракции по 1 мл в 20 пробирок, промывали колонку 100 мл 20 мМ NaФБ, рН 7,0 и 100 мл 20 мМ NaФБ, рН 7,0 с 0,5М NaCl. Антитела к ДНК-(диен)платине элюировали 100 мМ глицин-HCl, рН 2,70, собирали фракции в 30 пробирок на 0,6 мл с 40 мкл 1М трис-HCl, рН 9,05 (для быстрой нейтрализации фракций иммуноглобулинов). После элюции антител колонку промывали 3 мл 100 мМ глицин-HCl, рН 2,70, 3 мл 20 мМ NaФБ, рН 7,0 и 5 мл 20% этилового спирта. Измеряли поглощение фракций проскока (контроль - 20 мМ NaФБ, рН 7,0) и элюата (контроль – смесь 100 мМ глицин-HCl, рН 2,70: 1М трис-HCl, рН 9,05 = 23:2) при 280 нм.
Специфичность антител к ДНК-(диен)платине анализировали методом дот-блот «иммунозолото» на нитратцеллюлозных мембранах.
5. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
5.1. Выделение и характеристика суммарной РНК клеток асцитной карциномы Кребс II
Концентрацию выделенной РНК определяли спектрофотометрически. Для чистой РНК характерно соотношение А260 /А280 Оно должно быть не менее 1.8.
1) Суммарная РНК из неинфицированных клеток Кребс II (выделенная с помощью НТХА)
Ср-ра РНК = А260*37 мкг/мл = 3,256 мкг/мкл (1 оптическая единица при 260 нм = 37 мг/мл)
А230=0,019; А260= 0,088; А280= 0,044
А260 : А280 = 2
А260 : А230 = 4,63
Рис.5 Спектр поглощения суммарной РНК из неинфицированных клеток Кребс II (выделенная с помощью НТХА).
2)Суммарная РНК из неинфицированных клеток, инфицированных вирусом Менго и инфицированных ВЭМК (выделенные фенольно-детергентным методом).
Рис.6 Спектр поглощения суммарной РНК из неинфицированных клеток, инфицированных вирусом Менго и инфицированных ВЭМК (выделенные фенольно-детергентным методом).
1.Суммарная РНК из клеток Кребс II, инфицированных вирусом Менго:
Ср-ра РНК =25,604 мкг/мкл (1 оптическая единица при 260 нм = 37 мг/мл)
А230=0,083; А260= 0,173; А280= 0,112
А260 : А280 = 1,54
А260 : А230 = 2,08
2.Суммарная РНК из клеток Кребс II, инфицированных ВЭМК (вирусом энцефаломиокардита):
Ср-ра РНК =14,282 мкг/мкл (1 оптическая единица при 260 нм = 37 мг/мл)
А230=0,078; А260= 0,193; А280= 0,119
А260 : А280 = 1,62
А260 : А230 = 2,47
3.Суммарная РНК из неинфицированных клеток:
Ср-ра РНК =24,309 мкг/мкл (1 оптическая единица при 260 нм = 37 мг/мл)
А230=0,003; А260= 0,073; А280= 0,040
А260 : А280 = 1,825
А260 : А230 = 24,33
Из графиков видно, что выделенные РНК имеют максимальное поглощение при длине волны 260 нм, минимум при 230 нм и нулевое поглощение при 300 нм, что соответствует оптическим свойствам РНК.
Наличие рибосомных РНК проверяли электрофоретическим методом в агарозном геле. На Рис.7 видны полосы, соответствующие 28S, 16S, 5S рибосомным РНК.
1 2 3 |
|
← 28S
← 16S
← 5S
Рис.7 Электрофоретическая характеристика суммарной РНК клеток Кребс II, выделенной фенольно-детергентным методом:
1 – суммарная РНК неинфицированных клеток Кребс II;
2 – суммарная РНК клеток Кребс II, инфицированных вирусом Менго;
3 - суммарная РНК клеток Кребс II, инфицированных ВЭМК.
Таким образом, были получены препараты нуклеиновых кислот, по характеристикам соответствующие РНК.
5.2. Получение и анализ специфичности антисывороток к ДНК - и РНК-(диен)платине методом «иммунозолото».
ДНК преиммунная |
ДНК после 1й иммунизации |
ДНК после 2й иммунизации |
ДНК после 3й иммунизации |
ДНК после 4й иммунизации |
ДНК после 5й иммунизации |
ДНК после 6й иммунизации |
ДНК после 7й иммунизации |
ДНК после 8й иммунизации |
РНК преиммунная |
РНК после 1й иммунизации |
РНК после 2й иммунизации |
РНК после 3й иммунизации |
РНК после 4й иммунизации |
РНК после 5й иммунизации |
РНК после 6й иммунизации |
РНК после 7й иммунизации |
РНК после 8й иммунизации |
1 2 3 4 5 6 7 8 Антисыворотки к:
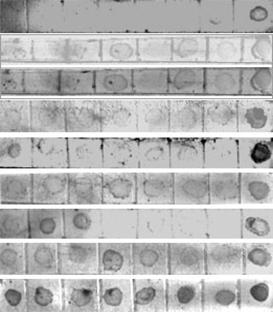

1 2 3 4 5 6 7 8
Рис.8 Характеристика антисывороток к ДНК-(диен)платине и РНК-(диен)платине методом «иммунозолото»:
1-4 - ДНК-(диен)платина (0,1, 1, 10 и 100 нг);
5-8 - немеченая ДНК (0,1, 1, 10 и 100 нг);
1-4 - РНК-(диен)платина (0,1, 1, 10 и 100 нг);
5-8 - немеченая РНК (0,1, 1, 10 и 100 нг).
Сигналы в преиммунной сыворотке, сравнимые с иммунной, говорит либо о слабом иммунном ответе на комплексные антигены (диен)Pt-ДНК-полиэтиленимин и (диен)Pt-РНК - полиэтиленимин, либо о его отсутствии.
Для дополнительной проверки слабого иммунного ответа решили выделить из соответствующих антисывороток фракцию иммуноглобулинов, для повышения концентрации антител в анализе методом дот-блот иммунозолото.
5.3Характеристика антител
Измерили поглощение белка после сульфат-аммонийного фракционирования, фракций проскока антител к РНК-(диен)платине после протеин G сефарозы и элюата антител к РНК-(диен)платине после протеин G сефарозы при 280 нм (1 о. е.=1 мг/мл)
A280= 0,229; Cбелка=18,32 мг/мл
Рис. 9. УФ-спектр раствора глобулинов к РНК-(диен)платине после сульфат-аммонийного фракционирования, проскока антител к РНК-(диен)платине после протеин G сефарозы, элюата антител к РНК-(диен)платине после протеин G сефарозы.
2) Измерили поглощение фракций проскока после протеин G сефарозы при 280 нм (1 о. е.=1 мг/мл)
Рис.10. Оптический профиль проскока антител к РНК-(диен)платине после протеин G сефарозы при 280 нм.
3) Измерили поглощение фракций элюата при 280 нм (1 о. е.=1 мг/мл)
Рис. 11. Оптический профиль элюции антител к РНК-(диен)платине с протеин G сефарозы 100 мМ глицин-HCl, рН 2,70 при 280 нм.
Мембраны с антителами после протеин G сефарозы.

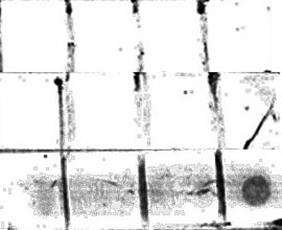
1 2 3 4
Рис.12 Характеристика антител к РНК-(диен)платине методом «иммунозолото»
(концентрация белка в препаратах антител 0,33 мг/мл):
1-2 – РНК-(диен)платина (100, 500 нг);
3-4 – немеченая РНК (100, 500 нг)
Таким образом, иммунохимическим методом было показано, что антитела узнают немеченую РНК (500 нг).
6. ВЫВОДЫ
1. Были выделены и охарактеризованы суммарные РНК фенольно-детергентным методом из клеток Кребс II неинфицированных и инфицированных вирусами Менго, ВЭМК, и с помощью НХТА из неинфицированных клеток Кребс II.
2.С помощью модификации РНК и ДНК (диен)платиной и защиты их полиэтиленимином-5000 были получены антигены, и ими была проведена иммунизация кроликов. Из антисывороток были получены препараты иммуноглобулинов.
3.На мембранах иммунохимически было установлено, что в препаратах нет антител к модифицированным РНК и ДНК. Таким образом, иммунного ответа на антиген не получили, т. к., по нашему предположению, ПЭИ нейтрализовал иммуногенные свойства антигенов. В дальнейшем предлагается не использовать ПЭИ в качестве защиты антигена.
7.СПИСОК ЛИТЕРАТУРЫ
[1] Butler V. P., Beiser S. M., Erlanger B. F., Tanenbaum S. W., Cohen S., Bendich A., Purine-specific antibodies which react with deoxyribonucleic acid (DNA), Proc. Nat. Acad. Sci. USA. 1962, V. 49, P. 1597-1602
[2] , , Детекция Chlamydia Trachomatis и Ureaplasma Urealyticum методами гибридизационного анализа с использованием ДНК-[Pt(dien)Cl]Cl-зондов и ПЦР-анализа, Биохимия 1995, Т. 60, вып. 5, стр. 783
[3] Kiseleva V. I., Kolesnik T. B., Turchinsky M. F., Wagner L. L., Kovalenko V. A., Plaksin D. J., Koukalova B., Kuhrnova V., Brabec V., Poverenny A. M., Trans-diamminedichloroplatinum (II)-modified probes for detection of picogram quantities of DNA, Analytical Biochemistry 1992, V. 260, P. 43-49
[4] Plescia O. J., Braun W., Palczuk N. C., Production antibodies to denatured deoxyribonucleic acid (DNA), Proc. Nat. Acad. Sci. USA. 1964, V. 52, P. 279-285




