ИЗУЧЕНИЕ ФАЗОВЫХ ПРЕВРАЩЕНИЙ ВОЛЬФРАМАТА ЦИРКОНИЯ, ПОЛУЧЕННОГО В УСЛОВИЯХ ГИДРОТЕРМАЛЬНОГО СИНТЕЗА
, магистрант гр. 10309
НИ Томский государственный университет, 634050, г. Томск, пр. Ленина, 36,
, аспирант, C. Н. Кульков, д. ф.-м. н., проф.,
Институт физики прочности и материаловедения СО РАН, 634021, г. Томск, пр. Академический, 2/4,
E-mail: vshadrin91@gmail.com
Введение
Вольфрамат циркония, ZrW2O8, обладает аномальным тепловым свойством –отрицательным коэффициентом теплового расширения от −273 до 770 °С, который равен α = −9,6·10-6 С-1. Традиционно вольфрамат циркония получают твердофазной реакцией между оксидами циркония и вольфрама при температурах выше 1110 °С. Несмотря на кажущуюся простоту, данный метод имеет ряд существенных недостатков, среди которых испарение оксида вольфрама при высоких температурах, что нарушает стехиометрию соединения и не позволяет получать монофазный кубический вольфрамат циркония. В связи с этим перспективными являются методы получения вольфрамата циркония при более низких температурах (до 700°С), где ZrW2O8 кинетически стабилен. В работе [1] представлены результаты синтеза вольфрамата циркония методом обратного химического осаждения. В настоящей работе предложен гидротермальный метод получения ZrW2O8 посредствам относительно низкотемпературного разложения прекурсора ZrW2O7(OH)2(H2O)2 [2].
Целью данной работы является изучение фазовых превращений при синтезе ZrW2O8 из ди(гидроксохлоро)диаквовольфрамата циркония.
Материалы и методика
В качестве исходных компонентов для получения прекурсора выступали водные растворы Na2WO4·2H2O (0,5 моль/л), ZrOCl2·8H2O (0,25 моль/л) и HCl (8 моль/л). Для приготовления растворов использовали: Na2WO4·2H2O (ч. д.а.), ZrOCl2·8H2O (х. ч.) и HCl (х. ч.). Водные растворы Na2WO4·2H2O (25 мл, 0,5 моль/л) и ZrOCl2·8H2O (25 мл, 0,25 моль/л) тщательно перемешивали, затем добавляли раствор соляной кислоты различной концентрации (8 моль/л) и снова перемешивали. Полученную суспензию помещали в стальной автоклав с тефлоновым вкладышем и выдерживали при температуре 160 °С в течение 36 часов для осуществления гидротермальной реакции. Полученный продукт многократно промывали дистиллированной водой, отфильтровывали и сушили при температуре 110 °С. Выход составил около 90% от теоретического.
Высокотемпературные рентгенограммы получены на приборе Bruker D8 с использованием CuKα-излучения. Сканирование проводилось по точкам в диапазоне углов 2θ=10-70°, шаг 0,02°, время накопления в точке 3 с. Для съёмки при высоких температурах использовалась камера Anton Paar HTK16. Данные получены на воздухе при атмосферном давлении. Образец помещался в камеру и нагревался до нужной температуры в течение 15 минут, затем проводилась запись рентгенограмм. Уточнение параметров решётки и уточнение структуры методом Ритвельда проведено с использованием программного обеспечения TOPAS v4.2 (Bruker). Термический анализ проводили на STA 449 F1 Jupiter в платиновом тигле в кислород-аргоновой смеси (20% O2). Исследование формы и размеров частиц осуществлялись на просвечивающем электронном микроскопе (ПЭМ) JEM – 2100 в ЦКП «НАНОТЕХ» ИФПМ СО РАН (ЦКП ТНЦ СО РАН). Средний размер частиц рассчитывался с помощью метода случайных секущих.
Результаты и обсуждение
Изображения с просвечивающего электронного микроскопа порошка ZrW2O7(OH, Cl)2·2H2O показаны на рисунке 1. Исходный порошок состоит из частиц двух видов: агломераты, состоящие из сросшихся нитевидных частиц, средний поперечный размер которых варьировался от 5 до 60 нм, и вытянутых единичных частиц, <dtr> = 0.2 мкм (рис. 1а). Порошок, синтезированный при 600°С, представлен в виде вытянутых частиц, которые имеют, в свою очередь, собственную структуру. Средний размер таких блоков изменялся от 20 до 50 нм. Средний продольный размер вытянутых частиц увеличивался от 0.5 до 5 мкм, средний поперечный размер - от 30 нм до 700 нм (рис. 1б). Согласно проведенному элементному анализу, соотношение атомов в синтезируемом порошке (O=59,85, W=27,09, Zr =13,06 ат.%) хорошо соответствует стехиометрии соединения кубического ZrW2O8, Zr:W=1:2. Кристаллы, синтезированные при 600 °С, наследуют форму, размер и габитус кристаллов прекурсора.
а |
б |
Рис. 1. ПЭМ изображения ZrW2O7(OH, Cl)2·2H2O при а) комнатной температуре, б) отожженный при 600 °С |
На рисунке 2 представлены результаты термического анализа синтезированного ZrW2O7(OH, Cl)2·2H2O. Видно, что нагрев порошка сопровождается потерей массы в температурном диапазоне 200–400 °С, которая составляет 9,25±0,25 %. Установление химической формулы по значению потери массы возможно в случае, если при разложении под действием температуры улетучивается часть вещества, соответствующая переменной компоненте х. Потеря массы при термораспаде протекает при следующей реакции:
ZrW2O7(OHх, Cl2-х)·2H2O → ZrW2O8 + (1+х)H2O↑+(2-x)HCl↑ (1)
Потеря массы рассчитывается по формуле 2.
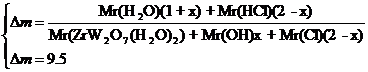 (2)
(2)
Вычисленное значение х позволило установить содержание воды, хлора и гидроксид-иона и определить истинную формулу прекурсора–ZrW2O7(OH1,5Cl0,5)·2H2O.
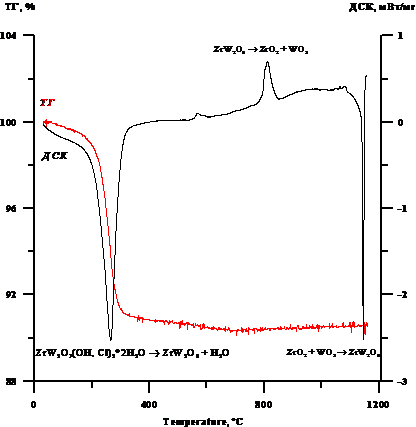
Рис. 2. Термический анализ прекурсора ZrW2O7(OH1,5Cl0,5)·2H2O
Для изучения фазовых превращений, протекающих при синтезе ZrW2O8, проведены высокотемпературные in situ рентгеновские исследования прекурсора ZrW2O7(OH1,5Cl0,5)·2H2O при различных температурах с шагом 100 °С (рис.3). Видно, что до 200 °С на рентгенограммах присутствуют только пики, соответствующие фазе ZrW2O7(OH1,5Cl0,5)·2H2O, но с повышением температуры до 500 °С все вещество переходит в рентгеноаморфное состояние. Дальнейший рост температуры до 600 °С приводит к формированию кристаллической структуры, соответствующей кубическому вольфрамату циркония. Параметр решетки получившейся кубической модификации при 600°С составил а = 9,1211 Å, что хорошо согласуется с литературными данными для кубической фазы ZrW2O8 [3]. Дальнейшее увеличение температуры приводит к появлению пиков WO3 и ZrO2 и росту их интенсивностей. Рефлексы, принадлежащие ZrW2O8, полностью исчезают при 900°С.
Мощный эндотермический пик при 200–400°С сопровождается потерей массы, и, следовательно, выходом молекул воды, хлора и гидроксильной группы и перестроением атомов из структуры прекурсора в вольфрамат циркония. Вероятно, это обуславливает переход из кристаллического состояния в рентгеноаморфное в температурном интервале от 200 до 500 °С, рисунок 3. Экзотермический пик при 554 °С сопровождается выделением тепла, что может быть связано с формированием кристаллической кубической модификации вольфрамата циркония [3, 4]. Данное предположение подтверждается наличием при 600 °С рефлексов, принадлежащих кубическому ZrW2O8. Пик при 794 °С, по нашему мнению, связан с процессом разложения вольфрама циркония на оксиды, что согласуется с литературными данными [5]. Наконец, начало эндотермического пика при 1140 °С связано с повторным синтезом вольфрамата циркония, который становится термодинамически стабильным выше указанной температуры (1140 °С), что находит подтверждение в литературе [3-5].
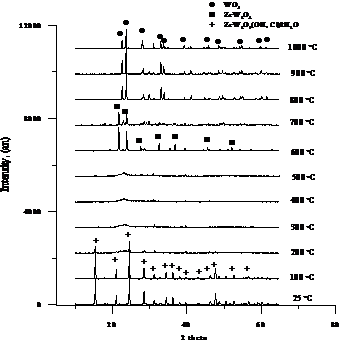
Рис. 3. Высокотемпературные рентгенограммы ZrW2O7(OH1,5Cl0,5)·2H2O при различных температурах
Выводы
Прекурсор синтеза вольфрамата циркония имеет химическую формулу ZrW2O7(OH1,5Cl0,5)·2H2O и состоит из частиц двух видов: агломераты, состоящие из сросшихся нитевидных частиц, и вытянутых частиц. Порошок вольфрамата циркония представлен вытянутыми частицами, имеющими собственную блочную структуру. Установлено, что разложение прекурсора начинается при 200 °С с образованием аморфного полупродукта, который кристаллизуется с экзоэффектом в монофазный кубический ZrW2O8 при температурах свыше 550 °С.
Список литературы:
1. Dedova E. S. Zirconia – based nanopowders synthesized by the chemical precipitation method / Dedova E. S., Klevtsova E. V., Kulkov S. N. // IOP Conf. Series: Materials Science and Engineering. – № 47. – 2013.
2. Li J., Hu L. Novel Photocatalyst ZrW2O7(OH)2(H2O)2 for Photocatalytic H2 and O2 Evolution from Water Splitting // Journal of Inorganic Materials. –2010. –vol. 25. – p. 18 – 25.
3. Single crystal growth of ZrW2O8 by hydrothermal route / Q. Xing [et al] //. Journal of Crystal Growth. –2005. –vol. 283. – p. 208 – 214.
4. Hashimoto T., Waki T., Morito Y. Synthesis a Large Amount of Pure Negative – Thermal – Expansion Materials, ZrW2O8. // Proceedings of the Institute of Natural Sciences, Nihon University. –2001. – vol. 36. –p. 121 – 126.
5. Evans J. S. O. Negative Thermal Expansion Materials // The Royal Society of Chemistry. –1999. – p. 3317 – 3326.





