Лабораторная работа №6
Окисляемость воды. Определение перманганатной окисляемости воды.
Цель: определить перманганатную окисляемость воды до и после очистки.
Оборудование и реактивы: 0,01н раствор перманганата калия, 0,01н раствор щавелевой кислоты.
Теоретическая часть
Окисляемость воды – это условная величина, характеризующая загрязнение воды различными легко окисляемыми веществами, главным образом органического происхождения, а также легко окисляющимися неорганическими примесями (H2S, Fe2+, сульфитов, нитритов и др.).
Для вычисления окисляемости, относящейся только к органическим примесям воды, вводят поправку на окисление неорганических легко окисляющихся веществ.
Различают бихроматную, перманганатную и биохимическую окисляемости.
При определении перманганатной окисляемости окислителем является перманганат калия. Однако перманганат калия не окисляет все примеси воды. Степень окисления перманганатом калия зависит от химической природы окисляемого вещества и может колебаться в широких пределах. Перманганатная окисляемость является очень хорошей характеристикой питьевых вод, а также вод рек, защищенных от попадания промышленных стоков.
Сущность метода определения перманганатной окисляемости воды заключается в использовании перманганата калия в качестве сильного окислителя для разложения органических загрязнителей в исследуемой воде. Проба воды кипятиться с заданным, заведомо избыточным объемом KMnO4, после чего его избыток оттитровывается щавелевой кислотой.
Реакция окисления примесей перманганатом калия проводится в кислой среде и протекает следующим образом
MnO4- + 8H+ +5e à Mn2+ + 4H2O
В щелочной или нейтральной среде ион Mn2+ переходит в Mn4+ образуя окись марганца – бурый осадок.
MnO4- + 2H2O +3e à MnO2 + 4OH-
Избыток перманганата калия реагирует с вводимой в раствор щавелевой кислотой
2KMnO4 + 5H2C2O4 + H2SO4 à MnSO4 + K2SO4 + 10CO2 + 8H2O
Практическая часть
50 мл исследуемой воды налили в коническую колбу на 250 мл, добавили 2 мл раствора серной кислоты, прилили 5 мл 0,01н раствора перманганата калия, и, накрыв колбу воронкой, нагрели жидкость до кипения. Прокипятили ее в течении 10 минут. Через некоторое время раствор стал более светлым. Затем, сняв колбу с плитки, внесли в нее 10 мл 0,01н раствора щавелевой кислоты до появления светло-розовой окраски. Экспериментальные данные занесли в таблицу 1.
Таблица 1 – Экспериментальные данные по определению перманганатной окисляемости воды.
№ пробы | Общий объем KMnO4, пошедший на титрование, мл | Объем KMnO4, пошедший на окисление C2H2O4, мл | Объем исследуемой воды, мл | Окисляемость воды, мг O2/л |
1 – неочищенная | 5 | 1,9; 1,9 | 50 | 9,9 |
2 – после очистки шунгитом | 2; 2,5 | 8,8 | ||
3 – после ионообменной очистки | 4; 3,5 | 4 | ||
4 – после очистки активированным углем | 3; 2,5 | 7,2 |
Расчет перманганатной окисляемости вели по формуле 1.
| (1) |
где V1 – общий объем 0,01н раствора KMnO4, добавленный в пробу.
V – объем KMnO4, пошедший на титрование H2C2O4.
N – нормальность раствора KMnO4
8 – миллиграмм-эквивалент кислорода
V2 – объем исследуемой воды
По формуле 1 определили перманганатную окисляемость в неочищенной воде (2) и в воде прошедшей очистку через шунгит (3), ионообменную очистку (4) и очистку активированным углем (5).
X = | (2) |
X = | (3) |
X = | (4) |
X = | (5) |
Вывод: выполнив лабораторную работу, изучили методы определения перманганатной окисляемости воды, провели ионообменную очистку, очистку шунгитом и активированным углем. Проанализировав полученные данные, сделали вывод, что воду с наименьшим содержанием органических и неорганических примесей мы получили при ионообменной очистке.



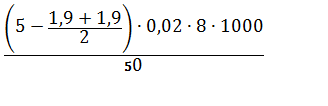 = 9,9 мг/л
= 9,9 мг/л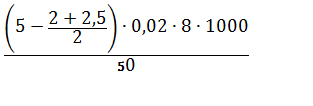 = 8,8 мг/л
= 8,8 мг/л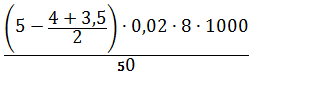 = 4 мг/л
= 4 мг/л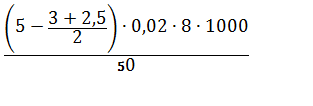 = 7,2 мг/л
= 7,2 мг/л