Областное государственное бюджетное профессиональное
образовательное учреждение «Сапожковский техникум
имени Героя Социалистического Труда »
Методическая разработка
урока по химии
Тема: Физические и химические свойства предельных одноатомных спиртов.
Применение метанола и этанола.
Подготовила
преподаватель химии
2017 г.
Тема урока: Физические и химические свойства предельных
одноатомных спиртов. Применение.
Цели урока: 1) Сформировать у обучающихся общие представления о физических и химических свойствах предельных одноатомных спиртов, показать практическое значение метанола и этанола.
2) Совершенствовать умение обучающихся сравнивать, устанавливать причинно-следственные связи «строение – свойства – применение», умение анализировать, систематизировать, обобщать, делать выводы; развивать способности к социальному взаимодействию и сотрудничеству.
3) Формировать стремление к здоровому образу жизни, нравственно-этические нормы и правила поведения, развивать коммуникабельность.
Тип урока: совершенствование знаний и умений.
Вид урока: комбинированный.
Методы обучения: словестно иллюстрированные,
проблемное обучение,
эксперимент,
работа в парах
Оснащение урока: штатив с пробирками,
фильтровальная бумага,
стеклянная палочка,
мерный цилиндр
растворы: этанола,
бутанола,
растительное масло,
фарфоровая чашка,
вода
дидактический материал (на каждом столе),
учебник «Химия – 10» автор .
Девиз урока: (на доске) «Скажи мне – и я забуду, покажи мне – и я запомню»
Ход урока.
1. Организаторская часть.
Приветствие. Настрой обучающихся на работу.
2. Актуализация опорных знаний.
Фронтальный опрос. 1) Какие вещества являются спиртами?
2) Записать общую формулу предельных одноатомных спиртов (СпН2п+1ОН)
3) По какому признаку можно классифицировать спирты? (одноатомные, двухатомные, трехатомные и т. д.)
На экране (слайд № 1 Классификация спиртов»)
4) Назовите формулы спиртов: метанола, протанола, этанола.
5) Как образуется название предельных одноатомных спиртов?
6) Запишите уравнение химической реакции получения этанола и этилена.
t, Н2SО4
![]()
![]() Обучающийся записывает на доске: СН2=СН2+Н2О С2Н5ОН
Обучающийся записывает на доске: СН2=СН2+Н2О С2Н5ОН
![]()
![]() или С2Н4+Н2О С2Н5ОН
или С2Н4+Н2О С2Н5ОН
3. Изучение нового материала
А) Демонстрация. Растворимость спиртов в воде.
В одинаковые цилиндры наливаем по 5мл спирта этанола и бутанола и приливаем столько же воды (вода подкрашена красными чернилами)
Обращаем внимание! Воду приливают к этиловому спирту, т. к. этиловый спирт не много легче воды (плотность спирта – 0,89 г/см3 , а плотность воды – 1 г/cм3
Вывод:
· Спирты обладают резким запахом;
· Этанол хорошо растворяется в воде;
· Бутанол плохо растворим в воде.
Проблема. Выясняем причину плохой растворимости спиртов в воде с увеличением молекулярной массы.
Работа с учебником: стр.81, Химия – 10.
Б) Лабораторный опыт. Спирты – органические растворители. (работа в парах)
В пробирку наливаем 1 мл спирта и добавляем 2-3 капли растительного масла. Смесь взболтали.
Вопрос? Что наблюдаем? Что можно сказать о свойствах спирта как растворителя?
Учитель: Благодаря хорошей растворимости в воде этиловый спирт проникает во все клетки организма, при этом разрушает их жировую основу, что ведет к гибели клеток всех органов. Таким образом, спирт - это яд.
В) Демонстрация опыта: «Воздействие спирта на печень»
В пробирку наливаем 5мл 70% раствора этилового спирта и опускаем в него кусочек свежей куриной печени (опыт проводим до урока)
Проблема. Что наблюдаем? Чем вызваны наблюдаемые вами изменения?
На экране слайд №2 «Схема превращения спирта в организме человека»
Учитель. Изменение цвета куриной печени вызывают промежуточные продукты окисления спирта: альдегид и уксусная кислота. Именно уксусная кислота усиливает синтез жирных кислот и приводит к жировому перерождению печени, уничтожению ее клеток, а затем к циррозу и раку.
Окисление этанола до углекислого газа и воды происходит когда его суточное потребление не превышает 20 г.
Г) Лабораторный опыт. Летучесть спиртов.
(работа в парах)
На фильтровальную бумагу нанесите стеклянной палочкой одну каплю спирта, а рядом одну каплю воды.
Вопрос. Какая капля быстрее испарится?
· Исследование химических свойств.
Беседа с группой:
1) Что такое функциональная группа?
2) Какая функциональная группа характерна для спиртов?
3) Назовите общее свойство для всех органических соединений? (горение, окисление О2)
Демонстрация опыта: Горение спирта.
В фарфоровую чашку наливаем небольшое количество этилового спирта и поджигаем. Наблюдаем горение спирта. Гасим пламя с помощью специальной пластинкой.
После демонстрации опыта обучающиеся записывают уравнение химической реакции.
(для этого используют «Информационную карту №1»)
Далее работа обучающихся в парах по карте №1.
4. Сообщение обучающихся о применение метанола и этанола.
Метанол – смертельный яд. Он проникает в организм при вдыхании воздуха, насыщенного его парами, и даже через кожу. Метанол поражает нервную и сосудистую системы, особо активно воздействует на зрительный нерв и сетчатую оболочку глаза, что может привести к слепоте, нарушает окислительные процессы и кислотно-основное равновесие в клетках и тканях. Отравление метиловым спиртом в ряде случаев заканчиваются смертью. Его используют для производства незамерзающего автомобильного стеклоомывателя, поэтому при обращении с этой жидкостью нужно соблюдать крайнюю осторожность.
Этанол используют как растворитель при производстве лаков, душистых веществ (парфюмерия), для синтеза органических веществ, в производстве синтетического каучука, как антидот при отравлении метанолом и этиленгликолем. Он применяется также для консервирования анатомических препаратов, как отличное антисептическое средство. Во время войны спирт применяли в зимнее время как горючее, так как он не замерзает.
5. Закрепление новых знаний.
Проводим в виде игры «Светофор»
Преподаватель зачитывает утверждения.
Если обучающиеся согласны с утверждением, они поднимают зеленую карточку, если нет – красную.
1. Спирты – органические соединения, содержащие гидроксильную группу (Да).
2. Метанол – многоатомный спирт (Нет).
3. Все спирты хорошо растворяются в воде (Нет).
4. Спирты реагируют с активными щелочными металлами (Да).
5. Спирты используют как добавку к моторному топливу (Да).
6. Подведение итогов урока. Оценивание знаний.
______________________________________________________
7. Домашнее задание.
А) Работа с учебниками стр. 76-83
Б) Выписать сведения о химических свойствах спиртов, которые не были рассмотрены на уроке, составить уравнения реакций.
В) Творческое задание: нарисовать плакаты о вреде алкоголизма (по 2 плаката от каждого ряда)
Учитель. В заключении хочу пожелать вам быть внимательными, с любопытством наблюдать за окружающим вас миром. Если сегодняшний урок заставил задуматься о собственном здоровье, то можно считать, что он прошел не зря.
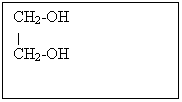
Слайд №1
 | ||
 | ||
 | ||
| ||
| ||
| ||
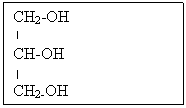 | ||
|  | |
 | ||
 |




