Муниципальный этап Всероссийской олимпиады школьников по химии
в 2012-2013 учебном году
Задания теоретического тура (50 баллов)
Уважаемые участники олимпиады! Прежде всего, внимательно ознакомьтесь с условиями всех задач и решайте их в любом порядке по мере возрастания их сложности, начиная с самой простой, на Ваш взгляд, задачи. Помните, что в каждой задаче оцениваются все разумные промежуточные результаты, ведущие к правильному ее решению. Желательно, чтобы каждый этап решения и вычислительный прием имели словесное обоснование.
1. Кроссворд (к ответам нужно приложить необходимые расчеты и пояснения)
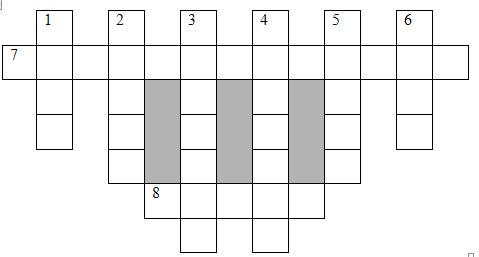
По вертикали:
1. Химический элемент – переходный металл IV периода ПС, не растворяется в разбавленном растворе серной кислоты, но растворяется в ее концентрированном растворе.
2. Одновалентный металл, при взаимодействии 13,3 г которого с водой выделяется 1,12 л (н. у.) водорода.
3. Простое газообразное вещество, которое в 24 раза легче одной из аллотропных модификаций кислорода.
4. Химический элемент, в ядре атома которого число нейтронов на 31 больше, чем протонов, а массовое число равно 165.
5. Тривиальное название карбоната одновалентного металла.
6. Простейший противоизжоговый препарат.
По вертикали:
7. Водородное соединение, 10 молекул которого имеют массу 1,345·10-21 г.
8. Металл (III), в хлориде которого массовая доля неметалла составляет 50,835 %.
2. Задачи на определение химических формул веществ:
а) В молекуле атомы элементов А и В проявляют валентность IV и II. Отношение числа электронов в атоме А к числу протонов в ядре атома В равно 3/8. Общее число протонов во всех ядрах атомов в молекуле равно 38. Определите формулу вещества.
б) Молекула газообразного вещества состоит из атомов А и В, причем на каждый атом А приходится три атома В, а относительная плотность газа по воздуху равна 1,0345. Определите формулу вещества, если атом элемента А содержит 6 электронов, а ядро атома элемента В состоит из одного протона.
в) Сосуд при одинаковых условиях поочередно заполняли сначала углекислым газом, а затем простым газообразным веществом. Массы газов составили соответственно 6,6 г и 7,2 г. Определите формулу простого вещества.
г) Относительная плотность водородного соединения трехвалентного элемента по оксиду этого элемента, в котором его валентность IV, равна 0,3696. Определите формулы газов.
д) Определите возможные формулы водородных соединений элементов, в которых массовая доля водорода составляет 12,5 %. Используя один из результатов решения этой задачи, дайте обоснование химической шутке: “Взорвали два газа одинаковой плотности - образовалось мокрое место на песке”.
3. 1,30 г цинковых опилок высыпали в раствор соли свинца. После окончания реакции масса осадка стала 2,72 г. Затем весь образовавшийся осадок погрузили в раствор с избытком соли третьего металла. Масса нового осадка составила 1,28 г. Определите состав первого осадка и третий металл, если все упомянутые в задаче металлы проявляют одинаковую валентность.
4. В 188,16 г кристаллогидрата карбоната натрия содержится 6,02∙1025 электронов. Определите формулу кристаллогидрата. Каково тривиальное название этого соединения. Назовите и приведите химические формулы других соединений с близкими тривиальными названиями.
5. Навеску разогретого металла внесли в сосуд с газообразным простым веществом, имеющим желто-зеленую окраску. После окончания реакции окраска исчезла, а твердый остаток поместили в стакан с водой, в результате чего образовался раствор голубого цвета, а на дне остался нерастворившийся осадок. Осадок отфильтровали и оказалось, что он не растворился в разбавленной, но растворился в концентрированной серной кислоте и при этом выделился газ объемом 224 мл (н. у.). К фильтрату добавили избыток раствора нитрата серебра и образовался осадок массой 1,435 г. О каком металле и газе идет речь в задаче (укажите по каким признакам Вы сделали опознание)? Рассчитайте массу металла до реакции.
6. Как соотносятся друг с другом объемы выделившегося кислорода при разложении образцов солей KMnO4, KClO3 и KNO3 одинаковой массы? Оцените эффективность этих солей как источников кислорода.
7. Экспериментальная задача. Дана смесь трех веществ – речного песка и кристаллов хлоридов натрия и бария. Как химическим путем выделить из этой смеси индивидуальные компоненты в твердом виде? Составьте и обоснуйте схему разделения, запишите уравнения реакций, проведите разделение.




