Всероссийская олимпиада школьников по химии
ШКОЛЬНЫЙ ЭТАП 2016/2017 уч. г.
Задание 1. Юный химик составил список химических явлений, которые можно наблюдать на кухне:
а) гашение соды уксусом при приготовлении теста;
б) растворение сахара в воде;
в) прокисание молока;
г) брожение сока;
д) плавание сливочного масла на горячей сковородке;
е) заваривание чая;
ж) засахаривание варенья.
Однако он включил в список и физические явления. Укажите их. (4 балла)
Задание 2. Учительница приготовила для урока химии образцы разных веществ. Но до них добрался шаловливый котенок, в результате все оказалось смешано в одной куче: кристаллы соли, медные, железные и древесные опилки. Опишите последовательность действий, с помощью которых можно разделить эту смесь и вернуть все вещества в отдельные баночки.
Какие процессы, физические или химические, использовались в предложенном вами методе разделения смеси? Какие свойства веществ, физические или химические при этом использовались? (6 баллов)
Задание 3. В природе железо образует ряд минералов. Это магнетит Fe3O4 , гематит Fe2O3, лимонит 2Fe2O3*3H2O. В каком из минералов массовая доля железа наибольшая? (6 баллов)
Задание 4. Названия некоторых химических элементов входят в состав часто употребляемых словосочетаний. Определите эти элементы и напишите их символы вместо многоточия:
а) ….солдатик; б) …. леди; в)…лихорадка; г) … долина; д) … тучи; е)… дровосек; ж)…бомба; з) … лампа; и)….голодание; к)…. муки. (10 баллов)
Задание 5. Какие химические элементы названы в честь стран? Приведите не менее четырех названий. Какой элемент впервые открыт на солнце? Укажите количество протонов и нейтронов, содержащихся в ядрах атомов, названных вами элементах. (10 баллов)
Желаем успеха!
Всероссийская олимпиада школьников по химии
ШКОЛЬНЫЙ ЭТАП 2016/2017 уч. г.
Задание 1.
Какими пятью различными способами можно получить хлорид цинка? Приведите уравнения соответствующих реакций. Классифицируйте их по типам. При протекании реакции в растворах приведите уравнения в ионном виде. (10 баллов)
Задание 2.
Рассчитайте массу оксида калия и объем (при н. у.) оксида углерода (IV), которые потребуются для получения 13,8г карбоната калия. (5 баллов)
Задание 3.
Вещество, полученное при сжигании 24,00 г кальция в кислороде, растворили в 164,25 г раствора соляной кислоты, содержащего 20% хлороводорода. Раствор выпарили и прокалили. Определите состав и массу сухого остатка. (10 баллов)
Задание 4.
Напишите уравнения реакций, соответствующие следующим превращениям (А, Б, В — соединения меди):
+ KOH t0 + H2, t0

![]()
![]()
![]()
![]() CuSO4 A Б В CuSO4 Cu(NO3)2
CuSO4 A Б В CuSO4 Cu(NO3)2
В переходах: Б→В и В→CuSO4 определите восстановитель и окислитель. (10 баллов)
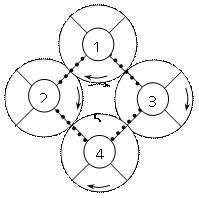 Задание 5. Решите кроссворд по свойствам простых веществ и соединений: Начиная с сектора, обозначенного стрелкой:
Задание 5. Решите кроссворд по свойствам простых веществ и соединений: Начиная с сектора, обозначенного стрелкой:
1. В виде простого вещества этот элемент - ядовитый желто-зеленый газ, в виде соединения встречается на любой кухне.
2. Металл, природное соединение которого называется "малахит".
3. Этот элемент входит в состав одной из важнейших сильных кислот, а в виде простого вещества - в состав пороха.
4. Тройная связь в молекуле этого простого вещества обуславливает его химическую инертность.
Если задание выполнено правильно, в центральных секторах вы прочитаете название пятого элемента. Используя таблицу химических элементов , охарактеризуйте строение атомного ядра и электронной оболочки этого элемента. Что Вы знаете о его применении? На чем оно основано?
(10 баллов)
Желаем успеха!
Всероссийская олимпиада школьников по химии
ШКОЛЬНЫЙ ЭТАП 2016/2017 уч. г.
Задание 1. При сжигании 1,2 г металла образуется оксид массой 2 г. Определите, какой металл был взят, если известно, что он всегда двухвалентен. (4 балла)
Задание 2. К раствору, содержащему смесь сульфита калия и хлорида натрия, сначала добавили избыток соляной кислоты, а затем – нитрата серебра. Какие ионы остались в растворе? Ответ подтвердите уравнениями реакций. (4 балла)
Задание 3. Сколько граммов вещества выпадает в осадок в результате реакции хлорида алюминия с гидроксидом натрия, если при взаимодействии гидроксида натрия той же массы с серной кислотой образуется 21,3 г сульфата натрия? (4 балла)
Задание 4. Алкен неразветвленного строения содержит двойную связь при первом атоме углерода. Образец этого алкена массой 0,84 г присоединяет максимально 1,6 г брома. Определите формулу алкена и назовите его. Приведите структурные формулы всех изомеров этого алкена и назовите каждый из них. (6 баллов)
Задание 5. Составьте структурные формулы всех изомеров состава C4H8Br2 . Дайте им названия. (6 баллов)
Желаем успеха!
Всероссийская олимпиада школьников по химии
ШКОЛЬНЫЙ ЭТАП 2016/2017 уч. г.
Задание 1. 105,8 г смеси бромида и хлорида натрия растворили в воде. Через полученный раствор пропустили избыток хлора. Затем раствор выпарили и определили массу сухого остатка, которая оказалась равной 70,2 г. Определите массовые доли солей в исходной смеси.
Количество баллов –10
Задание 2. При взаимодействии 35,55 мл раствора одноосновной органической кислоты неизвестного строения с долей 30,0% (ρ=1,04г/см3) с избытком гидрокарбоната натрия выделилось 3.36 л (н. у) углекислого газа. О какой кислоте идет речь?
Количество баллов –10
Задание 3. Газ, полученный при сжигании 5,6л (н. у.) смеси этана и пропана, плотность которой по водороду равна 19,9, пропустили через 20%-ный раствор гидроксида натрия массой 160 г. Определите массы солей, находящихся в образовавшемся растворе.
Количество баллов - 10
Задание 4. Используя метод электронного баланса, составьте уравнение реакции:
KMnO4+H2S+H2SO4→MnSO4+S+…+…
Определите окислитель и восстановитель. Количество баллов - 5
Задание 5. Определите молекулярную формулу предельного углеводорода, если известно, что при полном сгорании 8.6 г его образовалось 13.44 л CO2 (н. y.).
Количество баллов -10
Желаем успеха!



