Гомельский филиал
Государственного учреждения образования
«Университет гражданской защиты
МЧС Республики Беларусь»
УТВЕРЖДАЮ Начальник кафедры «Оперативно-тактическая деятельность и техника» ст. л-нт вн. службы, к. т.н., доцент « ____» _______________20 ___ г. |
ПЛАН
проведения лабораторного занятия по учебной дисциплине
«Материаловедение»
Тема № 2. Кристаллизация металлов и сплавов
Занятие № 2.5. Изучение диаграммы состояния «железо – цементит»
Цель:
1. Рассмотреть и изучить диаграмму состояния «железо – цементит».
2. Ознакомиться с особенностями структуры и свойствами фаз металлических сплавов.
3. Воспитать у обучаемых понимание важности кристаллизации металлов для использования понятий в производственной деятельности.
Время: 2 часа
Место: учебная аудитория
Учебная литература:
1. Лахтин, / ., . – 3-е изд. – М.: Машиностроение», 1990. – 528с.
2. Материаловедение / , , и др. –7-е изд. – М.: Изд-во МГТУим. , 2005. – 648с.
3. Материаловедение: учебник для вузов / , , и др.; под ред. . – 2изд. – М.: Машиностроение, 1986.–383с
4. Материаловедение:учебник / и др. – Минск: ИВЦ Минфина,2008.-519с
5. Технология металлов и материаловедение / , , и др. – М.: Металлургия, 1987. 800с.
Содержание задания на учебных местах
Задание: Изучение диаграмм состояния «железо – цементит»
Время: 2 часа.
Материальное обеспечение:
1. Ноутбук.
2. Мультимедийное оборудование, проектор.
3. Слайды по теме.
4. Презентация по теме.
Общая организация занятия
Организационно-методические мероприятия | Время, мин. | Действия преподавателя и методические приемы |
1. Вводная часть | 10 | Принимаю доклад дежурного по взводу. Проверяю наличие обучающихся по журналу. Проверяю усвоение обучающимися теоретического (лекционного) материала на данную тему. Довожу до обучающихся цель и порядок проведения занятия |
2. Выполнение лабораторной работы | 35 | |
1) ознакомление с темой лабораторной работы | 5 | Знакомлю обучающихся с методами исследования кристаллизации металлов и сплавов |
2) изучить диаграмму «железо – цементит» | 5 | Предлагаю обучающимся подготовить таблицу рекомендуемой формы |
3) исследование влияние количество углерода и примесей на свойства сталей. | 15 | Контролирую выполнение обучающимися экспериментальной части лабораторной работы, и оформление таблицы |
4) влияние легирующих элементов | 10 | Контролирую выполнение обучающимися обработки полученных данных и проведение необходимых записей |
3. Оформление лабораторной работы | 10 | Довожу порядок оформления лабораторной работы в тетради для лабораторных работ: - записываем тему; - формулируем цель работы; - записываем основные сведения; - описываем методику выполнения работы; - исследуемые показания заносим в подготовленную таблицу; - проводим обработку результатов исследований; - делаем вывод |
4. Подготовка и защита лабораторной работы | 30 | Самостоятельное повторение обучающимися теоретического материала по теме лабораторной работы Осуществляю прием защиты лабораторной работы. Задаю вопросы о порядке выполнения работы и о диаграмме «железо – цементит» |
5. Заключение: -проверка усвоения данного материала; -подведение итогов занятия; -ответы на вопросы; -задание на самоподготовку; -объявление темы очередного занятия и места его проведения | 5 | Подвожу итоги занятия, объявляю полученные оценки, отвечаю на вопросы, даю задание на самоподготовку и объявляю тему очередного занятия и место его проведения |
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ
лабораторной работы
Цель работы: Рассмотреть и изучить диаграмму состояния железо - цементит.
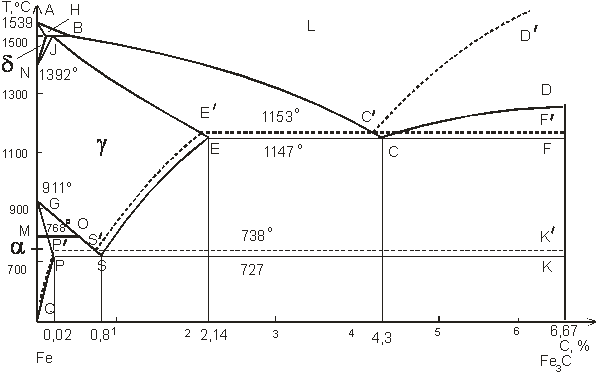
Диаграмма состояния железо - цементит
Диаграмму состояния железо - углерод чаще всего представляют в интервале концентраций от железа до цементита. При этом ось абсцисс (концентрационная) на диаграмме, как правило, даётся двойной, показывая содержание углерода и цементита.
Об открытии критических точек в стали в 1868 году и начале изучения диаграммы железо - углерод см. страницу Диаграмма железо - углерод.
Диаграмма железо-углерод, как явствует из названия, должна распространяться от железа до углерода. Железо с углеродом образует ряд химических соединений: цементит Fe3C; Fe2C; FeC и др. и, следовательно, система железо-углерод должна быть отнесена к сложной форме диаграммы с химическими соединениями.
Рассматривая диаграмму железо-углерод в участке от железа до цементита можно компонентами системы считать железо и цементит.
На рисунке приведена полная диаграмма состояния системы (стабильная система Fe-Cгр и метастабильная система Fe-FeC).
Метастабильная система железо - цементит (Fe - Fe3C)
Кривая ликвидус аустенита BC установлена данными Руэра, Хондо, Эдкока, Умино и др. Почти прямолинейный вид линии солидус γ-фазы (JE) также подтверждён в работах. Предельная растворимость углерода в γ-фазе при 1147°C составляет 2,14% (по массе), или 9,2% (ат.); при 1150°C 2,02% (по массе), или 8,7% (ат.).
Обычно из расплавов, содержащих более 0,51% (по массе) C, выделяется γ-фаза. Однако при переохлаждении расплавов, содержащих 0,5-1,5% (по массе) C, наблюдалась кристаллизация δ-фазы по метастабильному ликвидусу BB' и солидусу HH' с последующей перекристаллизацией пересыщенной углеродом δ-фазы в равновесную γ-фазу по реакции жδ+δпересыщ→жγ+γ, что указывает на существование в расплавах, содержащих 0,5-1,5% (по массе) C, смешанного ближнего порядка жδ+δ→жγ+γ.
Кривая ликвидус цементита CD экспериментально не фиксируется. Первичный цементит выделяется только при закалке расплавов, содержащих до 5,5% (по массе) C, а при нагреве белых заэвтектических чугунов цементит разлагается до плавления (Fe3C→Fe+Cгр). По расчётным данным, виртуальная температура плавления цементита оценивается равной 1200-1450°C. Возможно, цементит испытывает инконгруэнтное разложение при 1250-1300°C.
В высокоуглеродистых сплавах, содержащих более 6,7% (по массе) C после закалки из жидкого состояния в медную изложницу и ледяную воду наблюдали только Fe3C; других карбидов не обнаружено. Таким образом, метастабильная система при нормальном давлении ограничена цементитом. При повышении давления стабилизируются высшие карбиды Fe7C3, Fe2C и Cалм, однако при давлении 0,1 МПа выделение карбидов FexC (Fe2C) наблюдали лишь при низкотемпературном отпуске закалённой стали.
Температура эвтектической горизонтали ECF принята равной 1147°C, эвтектике (точке С) соответствует 4,30% (по массе), или 17,28% (ат.) C.
Превращение γ↔α (A3, кривая GS), исследованное многими авторами, также подтверждено последующими работами.
Эвтектоидная точка находится при 723°C и 0,76% (по массе), или 3,44% (ат.) C, а по другим данным, при 727,2±0,5°C и 0,765% (по массе), или 3,46% (ат.). Таким образом, температуры и концентрации для всех характерных точек метастабильной системы Fe-Fe3C подтверждены последующими работами.
Растворимость цементита в α-Fe (кривая PQ) очень мала и составляет 0,02% (по массе), или 0,095% (ат.) C. Согласно другим данным, растворимость цементита в α-Fe при 723°C равна 0,025% (по массе).
Метастабильная система Железо - Цементит проявляется только при содержании углерода до 6,67% (по массе) С (Fe3C). При высоких давлениях цементит Fe3C стабилизируется и появляется карбид Fe7C3, находящийся в равновесии с алмазом. Метастабильная система Железо - Цементит представляет фрагмент полной диаграммы Железо - Алмаз, проявляющейся полностью только при высоких давлениях, когда стабильными становятся карбиды Fe3C, Fe7C3 и алмаз. Цементит имеет узкую область гомогенности, изображаемую обычно вертикально.
1. Гуляев . - М.: Металлургия, 1977. - УДК669.0(075.8)
2. , Будберг
1. Железо– d-переходный металл серебристо-светлого цвета. Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3.
Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях - a и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Fea (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feaназывают Feδ. Высокотемпературная модификация Feaне представляет собой новой аллотропической формы.
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т. е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри. Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв = 250 МПа, предел текучести – σТ = 120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ =50 %, а относительноесужение – ψ = 80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С.
Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза.![]() Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит (Ф, a)- твердый раствор внедрения углерода в a-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 130 НВ, временное сопротивление – σв = 300 МПа) и пластичен (относительное удлинение - δ =50 %), магнитен до 768° С.
Аустенит (А, γ) – твердый раствор внедрения углерода в γ–железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ - железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение – δ =40…50 %), парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
4. Цементит – характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
5. Графит - характеристика дана выше.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо - цементит и железо - графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе - С) - графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура - содержание углерода (рис. 1). Диаграмма состояния системы железо - углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран.
Особое место среди них занимают работы . Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
Стали являются наиболее распространенными материалами. Обладают хорошими технологическими свойствами. Изделия получают в результате обработки давлением и резанием.
Достоинством является возможность, получать нужный комплекс свойств, изменяя состав и вид обработки. Стали, подразделяют на углеродистые и легированные.
2.Влияние углерода и примесей на свойства сталей
Углеродистые стали являются основными. Их свойства определяются количеством углерода и содержанием примесей, которые взаимодействуют с железом и углеродом.
3. Влияние углерода.
Влияние углерода на свойства сталей показано на рис. 10.1
4. 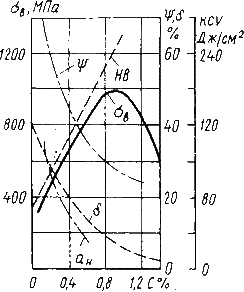
5. Рис.10.1. Влияние углерода на свойства сталей
С ростом содержания углерода в структуре стали увеличивается количество цементита, при одновременном снижении доли феррита. Изменение соотношения между составляющими приводит к уменьшению пластичности, а также к повышению прочности и твердости. Прочность повышается до содержания углерода около 1%, а затем она уменьшается, так как образуется грубая сетка цементита вторичного.
Углерод влияет на вязкие свойства. Увеличение содержания углерода повышает порог хладоломкости и снижает ударную вязкость.
Повышаются электросопротивление и коэрцитивная сила, снижаются магнитная проницаемость и плотность магнитной индукции.
Углерод оказывает влияние и на технологические свойства. Повышение содержания углерода ухудшает литейные свойства стали (используются стали с содержанием углерода до 0,4 %), обрабатываемость давлением и резанием, свариваемость. Следует учитывать, что стали с низким содержанием углерода также плохо обрабатываются резанием.
6. Влияние примесей
В сталях всегда присутствуют примеси, которые делятся на четыре группы. 1.Постоянные примеси: кремний, марганец, сера, фосфор.
Марганец и кремний вводятся в процессе выплавки стали для раскисления, они являются технологическими примесями.
Содержание марганца не превышает 0,5…0,8 %. Марганец повышает прочность, не снижая пластичности, и резко снижает красноломкость стали, вызванную влиянием серы. Он способствует уменьшению содержания сульфида железа FeS, так как образует с серой соединение сульфид марганца MnS.
Частицы сульфида марганца располагаются в виде отдельных включений, которые деформируются и оказываются вытянутыми вдоль направления прокатки.
Содержание кремния не превышает 0,35…0,4 %. Кремний, дегазируя металл, повышает плотность слитка. Кремний растворяется в феррите и повышает прочность стали, особенно повышается предел текучести, ![]() . Но наблюдается некоторое снижение пластичности, что снижает способность стали к вытяжке
. Но наблюдается некоторое снижение пластичности, что снижает способность стали к вытяжке
Содержание фосфора в стали 0,025…0,045 %. Фосфор, растворяясь в феррите, искажает кристаллическую решетку и увеличивает предел прочности ![]() и предел текучести
и предел текучести ![]() , но снижает пластичность и вязкость.
, но снижает пластичность и вязкость.
Располагаясь вблизи зерен, увеличивает температуру перехода в хрупкое состояние, вызывает хладоломкость, уменьшает работу распространения трещин, Повышение содержания фосфора на каждую 0,01 % повышает порог хладоломкости на 20…25oС.
Фосфор обладает склонностью к ликвации, поэтому в центре слитка отдельные участки имеют резко пониженную вязкость.
Для некоторых сталей возможно увеличение содержания фосфора до 0,10…0,15 %, для улучшения обрабатываемости резанием.
S – уменьшается пластичность, свариваемость и коррозионная стойкость. Р–искажает кристаллическую решетку.
Содержание серы в сталях составляет 0,025…0,06 %. Сера – вредная примесь, попадает в сталь из чугуна.
При взаимодействии с железом образует химическое соединение – сульфид железа FeS, которое, в свою очередь, образует с железом легкоплавкую эвтектику с температурой плавления 988oС. При нагреве под прокатку или ковку эвтектика плавится, нарушаются связи между зернами. При деформации в местах расположения эвтектики возникают надрывы и трещины, заготовка разрушается – явление красноломкости.
Красноломкость – повышение хрупкости при высоких температурах
Сера снижает механические свойства, особенно ударную вязкость а![]() и пластичность (
и пластичность (![]() и
и ![]() ), а так же предел выносливости. Она ухудшают свариваемость и коррозионную стойкость.
), а так же предел выносливости. Она ухудшают свариваемость и коррозионную стойкость.
Скрытые примеси- газы (азот, кислород, водород) – попадают в сталь при выплавке.
Азот и кислород находятся в стали в виде хрупких неметаллических включений: окислов (FeO, SiO2, Al2O3)нитридов (Fe 2N), в виде твердого раствора или в свободном состоянии, располагаясь в дефектах (раковинах, трещинах).
Примеси внедрения (азот N, кислород О) повышают порог хладоломкости и снижают сопротивление хрупкому разрушению. Неметаллические включения (окислы, нитриды), являясь концентраторами напряжений, могут значительно понизить предел выносливости и вязкость.
Очень вредным является растворенный в стали водород, который значительно охрупчивает сталь. Он приводит к образованию в катанных заготовках и поковках флокенов.
Флокены – тонкие трещины овальной или округлой формы, имеющие в изломе вид пятен – хлопьев серебристого цвета.
Металл с флокенами нельзя использовать в промышленности, при сварке образуются холодные трещины в наплавленном и основном металле.
Если водород находится в поверхностном слое, то он удаляется в результате нагрева при 150…180 , лучше в вакууме ![]() мм рт. ст.
мм рт. ст.
Для удаления скрытых примесей используют вакуумирование.
Специальные примеси – специально вводятся в сталь для получения заданных свойств. Примеси называются легирующими элементами, а стали - легированные сталями.
1.3 Назначение легирующих элементов.
Основным легирующим элементом является хром (0,8…1,2)%. Он повышает прокаливаемость, способствует получению высокой и равномерной твердости стали. Порог хладоломкости хромистых сталей - (0…-100)oС.
Дополнительные легирующие элементы.
Бор - 0.003%. Увеличивает прокаливаемость, а такхе повышает порог хладоломкости (+20…-60 oС.
Марганец – увеличивает прокаливаемость, однако содействует росту зерна, и повышает порог хладоломкости до (+40…-60)oС.
Титан (~0,1%) вводят для измельчения зерна в хромомарганцевой стали.
Введение молибдена (0,15…0,46%) в хромистые стали увеличивает прокаливаемость, снихает порог хладоломкости до –20…-120oС. Молибден увеличивает статическую, динамическую и усталостную прочность стали, устраняет склонность к внутреннему окислению. Кроме того, молибден снижает склонность к отпускной хрупкости сталей, содержащих никель.
Ванадий в количестве (0.1…0.3) % в хромистых сталях измельчает зерно и повышает прочность и вязкость.
Введение в хромистые стали никеля, значительно повышает прочность и прокаливаемость, понижает порог хладоломкости, но при этом повышает склонность к отпускной хрупкости (этот недостаток компенсируется введением в сталь молибдена).
Хромоникелевые стали, обладают наилучшим комплексом свойств. Однако никель является дефицитным, и применение таких сталей ограничено.
Значительное количество никеля можно заменить медью, это не приводит к снижению вязкости.
При легировании хромомарганцевых сталей кремнием получают, стали – хромансиль (20ХГС, 30ХГСА). Стали обладают хорошим сочетанием прочности и вязкости, хорошо свариваются, штампуются и обрабатываются резанием. Кремний повышает ударную вязкость и температурный запас вязкости.
Добавка свинца, кальция – улучшает обрабатываемость резанием. Применение упрочнения термической обработки улучшает комплекс механических свойств.
7. Распределение легирующих элементов в стали.
Легирующие элементы растворяются в основных фазах железоуглеродистых сплавов ( феррит, аустенит, цементит), или образуют специальные карбиды.
Растворение легирующих элементов в происходит в результате замещения атомов железа атомами этих элементов. Эти атомы создают в решетке напряжения, которые вызывают изменение ее периода.
Изменение размеров решетки вызывает изменение свойств феррита – прочность повышается, пластичность уменьшается. Хром, молибден и вольфрам упрочняют меньше, чем никель, кремний и марганец. Молибден и вольфрам, а также кремний и марганец в определенных количествах, снижают вязкость.
В сталях карбиды образуются металлами, расположенными в таблице Менделеева левее железа (хром, ванадий, титан), которые имеют менее достроенную d – электронную полосу.
В процессе карбидообразования углерод отдает свои валентные электроны на заполнение d – электронной полосы атома металла, тогда как у металла валентные электроны образуют металлическую связь, обуславливающую металлические свойства карбидов.
При соотношении атомных радиусов углерода и металла более 0,59 образуются типичные химические соединения: Fe3C, Mn3C, Cr23C6, Cr7C3, Fe3W3C – которые имеют сложную кристаллическую решетку и при нагреве растворяются в аустените.
При соотношении атомных радиусов углерода и металла менее 0,59 образуются фазы внедрения: Mo2C, WC, VC, TiC, TaC, W2C – которые имеют простую кристаллическую решетку и трудно растворяются в аустените.
Все карбиды обладают высокой твердостью и температурой плавления.
4. Случайные примеси.
Меры безопасности
Курсанты допускаются к выполнению лабораторной работы после ознакомления с правилами техники безопасности в лабораториях кафедры и разрешения преподавателя.
Курсанты обязаны знать и строго соблюдать правила пожарной и электрической безопасности. В процессе подготовки к лабораторной работе курсанты должны изучить методические указания, привести в тетради для лабораторных работ схему и таблицу для записи результатов измерения.
При выполнении лабораторных работ курсанты должен действовать в строгом соответствии с методическими указаниями и не допускать самовольных действий с приборами, пускорегулирующей аппаратурой и другими элементами установок.
Запрещается:
включать и выключать лабораторные установки без разрешения преподавателя;
вносить изменения в схемы установок, пересоединять электрические провода, производить разборку и ремонт оборудования лабораторных установок, переставлять приборы и оборудование;
прикасаться к элементам оборудования, которые могут находиться под напряжением;
прикасаться к нагретым поверхностям и движущимся частям оборудования;
облокачиваться или ставить ноги на электродвигатели, вентиляторы и другое оборудование.
При обнаружении неисправностей или повреждения лабораторного оборудования курсанты обязаны немедленно сообщить об этом преподавателю.
При нарушении правил техники безопасности курсанты отстраняются от выполнения лабораторных работ и могут быть допущены к дальнейшему их выполнению после собеседования с преподавателем по правилам выполнения работ.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Как влияет количество углерода на свойства сталей;
2. Как влияют примеси на свойства сталей;
3. Фазы диаграммы «железо – углерод»;
4. Структура диаграммы «железо – углерод»;
5. свойства диаграммы «железо – углерод»;
Оценочные показатели
1. Знание теоретических положений.
2. Практическое выполнение работ.
3. Использование оборудования.
4. Выполнение мер безопасности.
5.Качество выполнения лабораторной работы.
6. Правильность полученных результатов
7. Соблюдение воинской дисциплины.
8. Эстетичность оформления лабораторной работы.
ЗАДАНИЕ НА САМОСТОЯТЕЛЬНУЮ ПОДГОТОВКУ
Изучить следующий учебный материал:
1. Особенности эвтектических, эвтектоидных и периктектических превращений..
2.Материаловедение:учебник / и др. – Минск: ИВЦ Минфина,2008.-519с
3.Технология металлов и материаловедение / , , и др. – М.: Металлургия, 1987. 800с.
Преподаватель