В экспериментах дистиллят озонировали при различных удельных расходах О3 от 47 до 115 г/кг, полученные продукты растворяли в гексане в объемном отношении 1:5, раствор смешивали при 20°С с диметилформамидом (ДМФА) и разделяли образовавшиеся несмешивающиеся фазы. При отгонке гексана, было получено очищенное топливо (рафинат), а извлеченные из него продукты озонирования (экстракт) — посредством водной промывки диметилформамидной фазы. Изменения группового состава серосодержащих в ходе реакции прослеживали с помощью потенциометрического титриметрического анализа выделенных продуктов. Результаты такого анализа очищенных топлив показаны на рис.4.
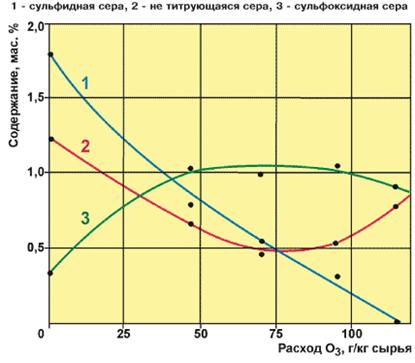
Рис.4 Влияние глубины озонирования дистиллята на функциональный состав рафинатов, полученных одноступенчатой экстракцией при соотношении гексан/ДМФА/сырье=5:2:1
Наблюдалось быстрое падение содержания сульфидов в рафинатах вплоть до исчезновения с увеличением глубины озонирования. Доля сульфоксидов при этом нарастает при повышении расхода озона до 47 г/кг (≈ 1моль/моль озонирующихся веществ), затем стабилизируется на уровне, отвечающем 1,0 мас.% сульфоксидной серы, и начинает снижаться, когда расход О3, превысит 96 г/кг (≈ 2 моль/моль). Качественно сходным образом меняется содержание сульфоксидной серы и в экстрактах, но абсолютные концентрации оказываются много выше (4,1-4,3 мас.% при расходах О3 до 100 г/кг).
Содержание нетитрующейся серы в рафинатах и экстрактах снижается, пока расход О3 не достигает ≈ 70 г/кг (1,5 моль/моль), затем начинает нарастать, что вполне объяснимо. В начале процесса тиофеновые компоненты дистиллята, связывая озон, превращаются в кислородсодержащие производные, хорошо растворимые в ДМФА и переходящие в состав экстрактов, поэтому количество этих сернистых соединений в рафинатах уменьшается. На поздних стадиях идет также окисление части сульфоксидов в нетитрующиеся сульфоны.
В итоге при одноступенчатой экстракции дистиллята, проозонированного при расходе озона 96 г/кг (≈ 2 моль/моль), из исходного топлива удаляется около 54%, при трехступенчатой — около 85%, а при четырехкратной — более 90% первоначально содержавшейся в нем серы.
Концентрация серы в извлекаемых экстрактах повышается до максимального значения 9,9 мас.%, что указывает на присутствие в них до 70 мас.% сульфоксидов и сульфонов: первых при удельных расходах О3 ниже, и вторых — выше 100 г/кг.
В статье [24] было проведено окислительное обессеривание с помощью системы пероксид водорода/озон в ионной жидкости гексафторфосфат 1-бутил-3-метилимидазолия. Озон был получен с помощью озонатора мощностью 0,5 г/ч. В качестве топлива была приготовлена модельная смесь с содержанием серы 779 ppm. Смесь 10 мл модельного топлива и 10 мл ионной жидкости перемешивали в течение 15 минут при 50°С. После этого добавляли 0,5 мл 30% раствора пероксида водорода и пропускали озон через быстро перемешивающийся раствор. Верхний органический слой периодически отбирали и анализировали на содержание серы. В работе использовались различные обессеривающие системы: экстракция ионной жидкостью, экстракция с окислением пероксидом водорода, экстракция с окислением озоном, экстракция с окислением пероксидом водорода и озоном. Экстракцией ионной жидкостью можно добиться удаления 41,9% серы; при добавлении пероксида водорода или озона оно увеличивается до 46,5% и 64,3% соответственно. Одновременным использованием пероксида водорода и озона можно добиться 98,6% удаления серы, что является очень хорошим результатом. В работе было установлено, что ионная жидкость может быть работать 5 циклов без снижения активности.
Для получения озона часто используется диэлектрический барьерный разряд. Окислением с помощью озона, полученного таким способом, и последующей экстракцией можно осуществлять глубокую десульфуризацию модельного топлива, содержащего бензотиофен и дибензотиофены [25]. В качестве экстрагента может быть применена ионная жидкость [Bmim]СH3COO. В отсутствии окисления, бензотиофен экстрагируется в чрезвычайно малых количествах из-за низкой полярности, поэтому экстракция ионной жидкостью оказывается неэффективной. Из рис.5 видно, что более 99,9% серы удаляются после 30 минут окисления, и наблюдается резкое увеличение эффективности экстракции окисленных соединений. Увеличение напряжения разряда стремительно увеличивает степень удаления серы, поскольку оно напрямую связано с количеством образовавшегося озона. Оптимальное соотношение массы топлива и ионной жидкости лежит в пределах от 2 до 9. Тиофен и бензотиофен гораздо легче окисляются, чем более объемные дибензотиофен и 4,6-диметилбензотиофен, но при использовании подходящего катализатора (TiO2/MCM-41), эти компоненты могут быть удалены на 98,6% и 95,2%, соответственно.
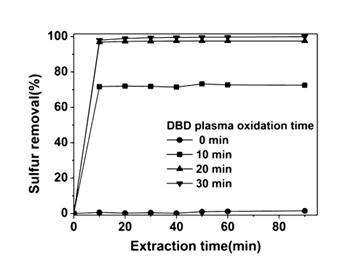
Рис.5 Зависимость степени удаления серы от времени экстракции
2.1.4. Каталитическое озонирование
Озон – один из самых сильных окислителей: его окислительно-восстановительный потенциал, равный 2,07В, уступает только фтору (2,87В). Химические свойства вытекают из структуры: озон обладает большим запасом энергии и сравнительно легко отдает атом кислорода. Реакции озона могут быть сведены к реакциям собственно озона и реакциям атома кислорода или другого активного фрагмента, образующегося в результате распада озона, с тем же реагентом. Если последние также включить в класс реакций озона, то их круг сильно расширится, поскольку легко создать условия, при которых озон быстро генерирует активные формы кислорода, и они взаимодействуют с данным веществом [26].
К реакциям озона может быть отнесено разложение озона в водном растворе. Разложение озона осуществляется по следующей 5-ти ступенчатой схеме, приведенной на рис.6.
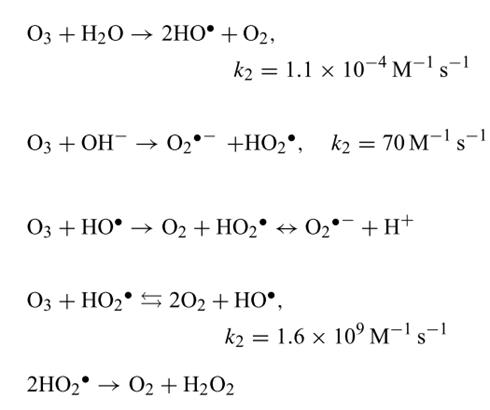
Рис.6 Схема разложения озона
Реакционная способность озона значительно увеличивается, когда удается создать благоприятные условия для образования из озона активных частиц. С целью образования активных фрагментов, таких как гидроксильные радикалы, применяются различные соединения, действие которых основано на каталитическом разложении озона в присутствии данных соединений.
Каталитическое озонирование находит широкое применение в промышленности. Благодаря высокому окислительно-восстановительному потенциалу и дезинфицирующей способности, озон используется для очистки питьевой воды от нежелательных примесей органических соединений, а также для улучшения ее качества [27].
Удаление трудноокисляемых соединений озонированием осуществляется с помощью передовых окислительных процессов. Они предназначены для получения относительно высокой концентрацию гидроксильных радикалов, обладающих высоким потенциалом окисления. Разработано несколько передовых окислительных процессов, наибольшее распространение среди которых получила очистка сточных вод системами O3/УФ и О3/Н2О2. Эти процессы имеют несколько недостатков, таких как уменьшение эффективности в присутствии частиц материалов-поглотителей радикалов и высокая стоимость пероксида водорода или ультрафиолетового излучения. Особое внимание должно быть уделено при окислении озоном трудноокисляемых соединений, для которых требуется присутствие гидроксильных радикалов. Хорошо известно, что некоторые относительно устойчивые соединения могут действовать как поглотители радикалов, в частности, влияя скорость реакции [28].
Катализаторы озонирования, основанные на генерировании активных частиц, могут быть как гомогенными, так и гетерогенными. С технологической и практической точки зрения, гетерогенные катализаторы представляют явное преимущество, поскольку могут быть гораздо проще восстановлены, как правило, путем осаждения или фильтрования, с возможность многократного повторного использования катализатора. В гетерогенных каталитических системах озонирование имеет некоторые особенности по сравнению с другими каталитическими процессами, главным из которых является необходимость мониторинга стабильности катализатора. В литературе описано использование гетерогенных катализаторов на основе оксида меди (II).
В качестве носителя использовался мезопористый оксид кремния SBA-15, как один из наиболее распространенных носителей в своем классе. В статье [29] используется оксид меди, нанесенный на носитель SBA-15 при окислении озоном щавелевой кислоты. Использование катализатора в данном случае позволяет проводить окисление со значительной эффективностью.
Использование гетерогенного катализатора CuO показало свою эффективность при озонировании гумусовых кислот [29]. Для данного процесса был изучен механизм реакции. Поверхность оксида меди связывается с молекулой озона, после чего происходит передача электронной плотности. Адсорбированный атомарный кислород реагирует с молекулой воды и образует два гидроксильных радикала, инициирующих гетерогенное каталитическое озонирование гумусовой кислоты.
Помимо гетерогенных каталитических процессов, в литературе имеются данные об использовании различных гомогенных катализаторов при озонировании органических соединений в водной среде. Несмотря на высокую окислительную способность, с некоторыми неактивированными ароматическими соединениями, озон реагирует медленно, а в некоторых случаях даже не позволяет полностью окислять их [30]. Использование различных солей металлов позволяет увеличить окислительную способность озона за счет образования свободных гидроксильных радикалов при участии ионов металлов. Однако реакции с участием радикалов не являются селективными и способствуют протеканию побочных реакций.
Использование гомогенного каталитического озонирования показало свою эффективность в очистке питьевой воды от различных органических соединений. В качестве катализаторов, как правило, используются соли различных переходных металлов, таких как Fe(II), Mn(II), Ni(II), Co(II), Cd(II), Cu(II), Ag(I), Cr(III), Zn(II).
Например, в статье [31] было использована окислительная система Mn2+/O3 для предварительного окисления цианидных соединений, образующихся в качестве побочных продуктов при процессах золотодобычи. Детальное исследование процесса показало, что процесс окисления может происходить тремя различными путями: прямым озонированием, окислением с участием гидроксильных радикалов, получаемых разложением растворившегося озона, и окислением соединениями Mn4+ и Mn7+, причем окисление соединениями марганца в высших степенях окисления является превалирующим процессом в кислых средах, а гидроксильные радикалы - основные окислители в нейтральных и щелочных растворах [32].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



