учебной дисциплины ОП.08 Химические и физико-химические метода анализа. 22.02.05. (150412) Обработка металлов давлением (базовый уровень подготовки)
Методические указания
по выполнению практических и лабораторных работ
УЧЕБНОЙ ДИСЦИПЛИНЫ
ОП.08 Химические и физико-химические методы анализа
основной профессиональной образовательной программы по специальности среднего профессионального образования
22.02.05. (150412) ОБРАБОТКА МЕТАЛЛОВ ДАВЛЕНИЕМ
(базовый уровень подготовки)
Чебаркуль
Методические указания по выполнению практических работ составлены в соответствии с Федеральным государственным стандартом (далее – ФГОС) по специальности среднего профессионального образования (далее – СПО) 22.02.05. (150412) «Обработка металлов давлением», утверждённым приказом Министерства образования и науки РФ от 01.01.2001 г. № 000.
Составитель:
, преподаватель ЕНД ГБПОУ ЧПТ
Рассмотрены и одобрены на заседании цикловой комиссии ЕНД« ___» ________________20__ г. Протокол № ____ от_______________________
Председатель ЦК : _________________/ /
Согласована с заместителем директора по УР: ________________//
Основные компетенции, реализуемые при выполнении практических и лабораторных заданий
Формирование соответствующих компетенций связано с решением за-дач по развитию у студентов специальности соответствующих знаний, умений, навыков. После выполнения практических занятий по данному курсу студент должен
В результате освоения дисциплины обучающийся должен уметь:
- проводить физико-химический анализ металлов и оценивать его результаты;
- использовать химические, физико-химические методы анализа сырья и продуктов металлургии.
В результате освоения дисциплины обучающийся должен знать:
- методы химического и физико-химического анализа свойств и структуры металлов и сплавов;
- процессы окислительно-восстановительных реакций взаимодействия металлов (сырья) металлических порошков с газами и другими веществами;
- физические процессы механических методов получения металлических порошков
Наименование практических и лабораторных работ
Наименование работы | Количество часов | Компетенции | Примечание |
Тема 1.1. Введение в аналитическую химию | |||
Практическая работа № 1 Расчет абсолютной и относительной ошибок. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Тема 1.2. Гравиметрический (весовой) анализ качества сырья и продуктов металлургии | |||
Лабораторная работа. № 1. Анализ качества сырья и продуктов металлургии с использованием аналитических весов. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Лабораторная работа № 2. Определение массовой доли влаги в хлориде бария весовым методом. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Лабораторная работа № 3. Определение серы в растворимых сульфатах. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа № 2. Решение типичных задач на гравиметрический метод. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Тема 1.3. Титриметрический (объёмный) анализ качества сырья и продуктов металлургии | |||
Лабораторная работа № 4. Приготовление и стандартизация 0,1 М раствора хлороводородной кислоты | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа № 3. Расчет концентрации растворов по различным параметрам. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа № 4. Решение типовых задач на титриметрический (объёмный) анализ качества сырья и продуктов металлургии | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Тема 2.1. Фотометрический анализ качества материалов металлургического производства | |||
Лабораторная работа № 5. Определение концентрации ионов меди в электролите латунирования дифференциально-фотометрическим методом. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа № 5. Сравнительная характеристика электрохимических методов анализа. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа № 6.Решение типовых задач на фотометрический анализ | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Тема 2.2. Хроматографический анализ качества материалов металлургического производства | |||
Практическая работа № 7. Разделение ионов железа и меди из смеси методом бумажной хроматографии. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Практическая работа №.8. Решение типовых задач по хроматографическому анализу. | 2 | ПК4.1 ПК 4.3,П 4.4 | |
Тема 3.1. Эмиссионный спектральный и рентгеноспектральный виды анализа | |||
Практическая работа №. 9. Проведение спектрального анализа сырья и продуктов металлургии с помощью спектрографа. | 2 | ПК4.1 ПК 4.3,П 4.4 |
Код | Наименование результатов освоения |
4.1 | Выбирать методы контроля, аппаратуру и приборы для контроля качества продукции. |
4.2 | Оценивать качество выпускаемой продукции. |
4.4 | Предупреждать появление, обнаруживать и устранять возможные дефекты выпускаемой продукции |
АННОТАЦИЯ
Целью практических работ является закрепление теоретического материала курса, ознакомление с методикой и практикой контрольных мероприятий, формулировка выводов, составление отчёта по работе.
По окончанию выполнения практических работ для закрепления изученного материала студент пишет итоговую работу в форме реферата по одной из изученных тем. Выбор темы - на усмотрении преподавателя.
Рекомендации по выполнению лабораторных работ
Подготовка к работе
Подготовка к выполнению лабораторной или практической работе начинается дома:
а) внимательно изучите теоретические основы лабораторной или практической работы;
б) ознакомьтесь с предстоящей работой по ее описанию и составьте план эксперимента;
в) составьте уравнения реакций, которые вы будете проводить, в случае затруднения обратитесь к учебнику;
г) перепишите в свою рабочую тетрадь - лабораторный журнал - форму лабораторного отчета, заполнив те его разделы, которые могут быть заполнены до выполнения эксперимента;
д) письменно ответьте на контрольные вопросы, помещенные после описания лабораторной работы или выданные преподавателем.
В идеале вы должны подготовиться так, чтобы выполнять эксперимент, руководствуясь только своими записями и не обращаясь в лаборатории к данному пособию.
В лаборатории
При условии добросовестного выполнения требований раздела 1 эксперимент займет у вас минимум времени. Эффективность работы еще больше возрастет, если вы будете соблюдать следующие простые правила:
а) соблюдайте чистоту и порядок на своем рабочем месте;
б) не загромождайте рабочее место посторонними предметами; не приходите в лабораторию в верхней одежде;
в) перед началом работы проверьте по списку, приведенному в описании работы, наличие на вашем рабочем месте необходимого оборудования и реактивов, убедитесь в чистоте химической посуды, при необходимости вымойте ее;
г) взяв с полки реактив и отобрав нужное количество, поставьте склянку на место, никогда не выливайте излишки реактива обратно в склянку;
д) сухие реактивы берите только специальными ложечками и кладите в чистые, сухие пробирки;
е) не проводите опыты, не указанные в лабораторной работе - это может привести к несчастному случаю;
ж) внимательно изучите правила техники безопасности при работе в химической лаборатории и неукоснительно их соблюдайте.
Правила техники безопасности
Во избежание несчастных случаев необходимо:
1) все опыты с ядовитыми, неприятно пахнущими веществами, а также упаривание кислот и кислых растворов проводить в вытяжном шкафу; при разбавлении кислот лить маленькими порциями кислоту в воду, а не наоборот;
2) опыты с легковоспламеняющимися веществами проводить вдали от огня;
3) при нагревании растворов в пробирках пользоваться держателем и всегда держать пробирку так, чтобы ее отверстие было направлено в сторону от работающих;
4) не наклонять лицо над нагреваемой жидкостью или сплавляемыми веществами;
5) нюхать любые вещества нужно с осторожностью, направляя к себе пары или газы легким движением руки;
6) со всеми веществами в лаборатории обращаться как с ядовитыми: не пробовать на вкус, не трогать руками; после работы тщательно вымыть руки;
7) при работе с солями некоторых металлов (по указанию преподавателя) производить слив реактивов в специальную тару под тягой.
Тема 1.1.
Введение в аналитическую химию
Практическое занятие № 1 Расчет абсолютной и относительной ошибок
Краткие теоретические сведения
Анализ считается выполненным более точным, чем меньше различаются результаты параллельных определений между собой.


Абсолютная ошибка – разность между полученным результатом и истинным или наиболее достоверным значением.
![]()
Относительная ошибка – отношение абсолютной ошибки к истинному значению.
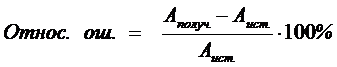
Пример 1. Определение доверительного интервала.
Условие: при определении объёма измерительного сосуда получено среднее значение ![]() из n измерений. Известно эмпирическое стандартное отклонение – S. Определить доверительный интервал с заданной доверительной вероятностью Р.
из n измерений. Известно эмпирическое стандартное отклонение – S. Определить доверительный интервал с заданной доверительной вероятностью Р.
Дано: n = 26 S = 0,0065 мл
Р = 0,95 Найти | Решение
Находим t по табл. 2.2, t = 2,060. Рассчитываем симметричную границу доверительного интервала |
Ответ: действительное значение – объём измерительного сосуда – накрывается интервалом [9,985: 9,979], т. е. 9,979 < Х0 < 9,985.
Пример 2. Определение абсолютной и относительной ошибки.
Условие: содержание кристаллизационной воды в веществе равно 14,75 г/моль найдено 14,70 г/моль. Рассчитать абсолютную и относительную ошибку определения.
Дано: g0 = 14,75г/моль gх = 14,70 г/моль Найти d | Решение: абсолютную ошибку определяем по формуле: d = qх - qо; d = 14,70 – 14,75 = - 0,05 г/моль. Относительная ошибка – это отношение абсолютной ошибки к истинному значению определяемой величины, выраженное в процентах: d 0 = |
Ответ: d = -0,05 г/моль; d 0 = -0,34 %.
Пример 3. Определение доверительного интервала по данным измерения.
Условие: результаты определения серы в керосине 0,724; 0,693; 0,755, 0,725, 0,740 % . Рассчитайте доверительные границы для истинного значения с доверительной вероятностью 95 %.
Дано:
S = 2,4 мкг/мл Рд=95 % Найти n | Решение Доверительный интервал при неизвестной дисперсии s 2х имеет вид |
По условию 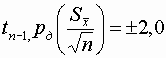 . Для обеспечения заданной точности необходимо использовать соотношение:
. Для обеспечения заданной точности необходимо использовать соотношение: 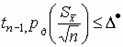 , где D · – допустимая норма погрешности. Таким образом, n – необходимое число измерений можно найти из соотношения: n
, где D · – допустимая норма погрешности. Таким образом, n – необходимое число измерений можно найти из соотношения: n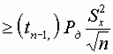 .
.
Поскольку ![]() – случайная величина, значения n находят методом последовательных приближений n = 7 и проверяют его соответствие условию: коэффициент
– случайная величина, значения n находят методом последовательных приближений n = 7 и проверяют его соответствие условию: коэффициент 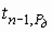 из табл. 2.1 равен t0,95 = 2,447, доверительный интервал:
из табл. 2.1 равен t0,95 = 2,447, доверительный интервал: 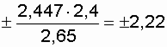 . Семь измерений не удовлетворяют условию. Предполагаем n = 9. Для n – 1 = 8 в табл. 2.1 нет значения t, поэтому применяем прием интерполяции: t0,95 = 2,262; t0,95 = 2,447, находим разницу, приходящуюся на единицу:
. Семь измерений не удовлетворяют условию. Предполагаем n = 9. Для n – 1 = 8 в табл. 2.1 нет значения t, поэтому применяем прием интерполяции: t0,95 = 2,262; t0,95 = 2,447, находим разницу, приходящуюся на единицу: ![]() , которую либо суммируем со значением t0,95, либо вычитаем из t0,95.<
, которую либо суммируем со значением t0,95, либо вычитаем из t0,95.<



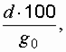 г/моль; d 0 =
г/моль; d 0 = 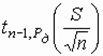 .
.