Одноатомные спирты. Многоатомные спирты»
Методическая разработка лекционного занятия
Тема. «Простые эфиры. Одноатомные спирты. Многоатомные спирты»
Учебные цели
После изучения данной темы студент должен уметь:
- доказывать с помощью химических реакций химические свойства простых эфиров, одноатомных спиртов, многоатомных спиртов;
- идентифицировать одноатомные и многоатомные спирты по физико-химическим свойствам;
- классифицировать одноатомные и многоатомные спирты по кислотно – основным свойствам;
- составлять формулы простых эфиров, одноатомных и многоатомных спиртов и давать им названия.
После изучения данной темы студент должен знать:
- строение простых эфиров, одноатомных и многоатомных спиртов с точки зрения теории ;
- реакционные способности простых эфиров, одноатомных и многоатомных спиртов;
- способы получения простых эфиров, одноатомных и многоатомных спиртов.
Воспитательные цели
Изучение данной темы способствует воспитанию:
- чувства профессиональной гордости;
- педантизма при изучении основных литературных источников;
Методические цели
использованы интерактивные методы обучения:
- лекция-диалог, сase-study (анализ конкретных ситуаций);
- лекция с применением мультимедийной презентации и видеоматериалов;
В результате освоения данной темы у студента должны формироваться следующие общие компетенции:
ОК 2. Организовывать собственную деятельность, выбирать типовые методы и способы выполнения профессиональных задач, оценивать их выполнение и качество.
ОК 3. Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность.
ОК 4. Осуществлять поиск, анализ и оценку информации, необходимой для постановки и решения профессиональных задач, профессионального и личностного развития.
Изучение данной темы способствует формированию следующих профессиональных компетенций, соответствующих основному виду профессиональной деятельности:
Реализация лекарственных средств и товаров аптечного ассортимента.
ПК 1.1. Организовывать прием, хранение лекарственных средств, лекарственного растительного сырья и товаров аптечного ассортимента в соответствии с требованиями нормативно-правовой базы.
Изготовление лекарственных форм и проведение обязательных видов внутриаптечного контроля.
ПК 2.3. Владеть обязательными видами внутриаптечного контроля лекарственных средств.
Общее время занятия – 2 часа.
Место проведения занятия: лаборатория органической химии.
Тип занятия: лекционное занятие.
Оснащение занятия: компьютер, мультимедийный проектор, мультимедийная презентация, конспект лекции.
Форма организации лекции: лекция - беседа с мультимедийной презентацией.
План проведения занятия
№/п | Название этапа | Описание этапа | Цель этапа | Время, (мин.) |
1 | Организационный этап. | Преподаватель отмечает присутствующих, проверяет наличие формы, объявляет тему, цели занятия, обосновывает актуальность изучаемой темы. | Сконцентрировать внимание на изучение данной темы и активизировать познавательную деятельность студентов. | 5 |
2 | Изложение нового материала . | Дать определение, общую формулу и классификацию спиртов и простых эфиров. Выделить гомологический ряд предельных одноатомных спиртов. Дать понятие радикально – функциональной и заместительной номенклатуре спиртов. | Создать мотив для изучения простых эфиров, одно - и многоатомных спиртов, активизировать познавательную деятельность студентов. | 15 |
Выделить особенности строения и свойств спиртов в связи с наличием межмолекулярной водородной связи. Охарактеризовать способы получения одноатомных спиртов. Дать характеристику химические свойства спиртов: кислотно – основные свойства, реакции нуклеофильного замещения, дегидратации, окисления, восстановления. | Способствовать формированию готовности получать необходимую информацию. Развивать способность принимать решение в производственной ситуации на основе критически переработанной информации. | 40 | ||
Дать сравнительную характеристику одноатомных и многоатомных спиртов. | Сформировать мотив для выработки умения сравнивать и обобщать, выделять главное. | 20 | ||
3 | Заключение | Подвести итоги, повторить основные положения лекции, ответить на вопросы студентов. | Закрепить мотив к дальнейшему самостоятельному углубленному изучению темы для будущей успешной деятельности фармацевта. | 5 |
4 | Задание на дом | Подготовить сообщения на тему « Токсичность спиртов» для закрепления и обобщения изученного материала. Подготовить ответы на контрольные вопросы к Практическому занятию. Решить задачи. | Способствовать формированию навыков организации собственной деятельности, выбора методов и способов выполнения профессиональных задач. | 3 |
5 | Резерв времени преподавателя | 2 |
Тема. Простые эфиры. Одноатомные спирты. Многоатомные спирты
План лекции
1. Классификация спиртов.
2. Гомологический ряд предельных одноатомных спиртов.
3. Радикально – функциональная и заместительная номенклатура спиртов.
4. Способы получения одноатомных спиртов.
5. Межмолякулярная водородная связь.
6. Химические свойства: кислотно – основные свойства, реакции нуклеофильного замещения, дегидратации, окисления, восстановления.
7. Сравнительная характеристика одноатомных и многоатомных спиртов. Этанол, глицерин.
Общая формула предельных одноатомных спиртов и простых эфиров: CnH2n+2O - изомеры
Спирты - производные углеводородов, в молекулах которых есть одна или несколько гидроксильных групп OH. Спирты R-OH или CnH2n+1OH;
Простыми эфирами называют органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода: R'–O–R", где R' и R" - различные или одинаковые радикалы.
???
Вопрос для размышления: Почему NH4OH имеет бытовое название «Нашатырный спирт»? Верно ли это название?
Простые эфиры
Номенклатура простых эфиров.
Простые эфиры рассматриваются как производные спиртов. Названия этих соединений строятся из названий радикалов (в порядке возрастания молекулярной массы) и слова "эфир". Например, CH3OCH3 - диметиловый эфир; C2H5OCH3 - метилэтиловый эфир.
Получение простых эфиров.
1. Симметричные простые эфиры R–O–R получают при межмолекулярной дегидратации спиртов.
![]()
При этом в одной молекуле спирта разрывается связь О-Н, а в другой - связь С-О. Реакцию можно рассматривать как нуклеофильное замещение группы HО– (в одной молекуле спирта) на группу RO– (от другой молекулы).
2. Эфиры несимметричного строения R–O–R' образуются при взаимодействии алкоголята и галогенуглеводорода (синтез Вильямсона). Например, метилэтиловый эфир можно получить из этилата натрия и хлорметана:
C2H5ONa + CH3Cl → C2H5OCH3 + NaCl
В этой реакции происходит нуклеофильное замещение галогена (Cl–) на алкоксигруппу (CH3O–)
Физические свойства. Простые эфиры имеют более низкие температуры кипения и плавления, чем изомерные им спирты. Эфиры практически не смешиваются с водой. Это объясняется тем, что простые эфиры не образуют водородных связей, т. к. в их молекулах отсутствуют полярные связи О–Н. Хорошо растворяют многие органические вещества и поэтому часто используются как растворители.
???
Вопрос для размышления: Какие лекарственные средства имеют спиртовые растворы?
Химические свойства. Простые эфиры - малоактивные соединения, они значительно менее реакционноспособны, чем спирты. Наиболее характерные реакции простых эфиров:
1. разложение под действием концентрированных иодоводородной или бромоводородной кислот
R–O–R' + HI → ROH + R'I
2. образование нестойких солей оксония (подобных солям аммония) в результате взаимодействия с сильными кислотами
R2O + HCl → [R2OH]+Cl-
К важнейшим простым эфирам относятся и гетероциклические кислородсодержащие соединения - этиленоксид (эпоксид) и диоксан.
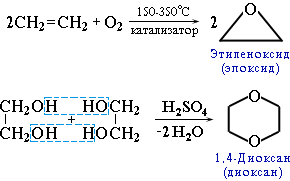
Диоксан (т. кип. 101°С) - хороший растворитель, смешивается как с водой, так и с углеводородами. За эти качества его назвали "органической водой". Достаточно токсичен. Значительно более опасны галогенсодержащие дибензопроизводные диоксана. Например, печально известный диоксин (2,3,7,8-тетрахлордибензо-п-диоксин).
???
Вопрос для размышления: В чем особенность агрегатного состояния спиртов в отличии от изученных ранее соединений? Как вы думаете, почему?
Физические свойства спиртов во многом определяются наличием между молекулами этих веществ водородных связей. С этим же связана и хорошая растворимость в воде низших спиртов.
Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей:
![]() Гидратация молекул ROH
Гидратация молекул ROH
· Низшие спирты (до С12) – жидкости, температуры кипения которых значительно выше, чем у соответствующих алканов из-за образования водородных связей за счёт полярной связи О–Н
Ассоциация молекул ROH
1. Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде
Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях.
Низшие являются сами хорошими растворителями.
!!! Смотри видеоопыт в Приложении
Растворимость фенола в воде ограничена.
2. Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т. кип. метанола +64,5оС). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.
Простейшие спирты - жидкости с характерными запахами.
С увеличением числа атомов углерода температура кипения возрастает, а растворимость в воде падает. Температура кипения у первичных спиртов больше, чем у вторичных спиртов, а у вторичных - больше, чем у третичных. Метанол крайне ядовит.
???
Вопрос для размышления: Почему введение в молекулу группы -OH повышает физиологическую активность спиртов?
Физические свойства многоатомных спиртов
Введение гидроксильной группы в молекулу углеводорода придает соединению сладкий вкус. Это свойство особенно выражено у спиртов с большим числом гидроксильных групп. Например, этиловый спирт С2Н5ОН не имеет сладкого вкуса, глицерин (трехатомный спирт) имеет сладковатый вкус, маннит (шестиатомный спирт) близок по сладости к сахарам.
Введение гидроксильной группы в молекулу углеводорода значительно повышает его физиологическую активность (в данном случае наркотические свойства вещества), но увеличение числа гидроксильных групп ведет к уменьшению активности. Например, в отличие от этилового спирта этиленгликоль, глицерин и маннит практически не имеют наркотических свойств.
В медицинской и фармацевтической практике большое значение имеют одноатомный спирт — этанол и трехатомный спирт — глицерин
Классификация.
Спирты классифицируются следующим образом :
По числу гидроксильных групп:
Одноатомные спирты: | Двухатомный спирт: | Трехатомный спирт: | |
CH3—OH | CH3CH2-OH | HO-CH2-CH2-OH (этиленгликоль) |
|
— четырёхатомные спирты (пентаэритрит);
— многоатомные спирты (пятиатомный спирт: ксилит).
В зависимости от насыщенности углеводородного заместителя:
Предельный спирт: | Непредельный спирт: | Ароматический спирт: |
CH3CH2CH2—OH (пропиловый спирт) | CH2=CH—CH2—OH (аллиловый спирт) | C6H5—CH2—OH (бензиловый спирт) |
Органические вещества, содержащие в молекуле гидроксильные группы, непосредственно связанные с атомами углерода бензольного кольца называются фенолами. Например, C6H5—OH - гидроксобензол (фенол).
В зависимости от наличия или отсутствия цикла в углеводородном заместителе:
— алициклические спирты (циклогексанол);
— алифатические или ациклические спирты (этанол).
В зависимости от того, при каком атоме углерода находится гидроксильная группа:
Первичный спирт: | Вторичный спирт: | Третичный спирт: |
CH3CH2CH2CH2—OH |
|
|
???
Вопрос для размышления: Какие типы изомерии могут быть характерны для спиртов?
Изомеры и гомологи
1. структурная изомерия
а) изомерия положения заместителя или гидроксильной группы) с С3
CH3CH2CH2OH пропанол-1 ![]() пропанол-2
пропанол-2
б) изомерия углеродного скелета с С4
CH3(CH2)3OH бутанол-1 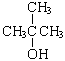 2-метил-пропанол-2
2-метил-пропанол-2
![]() 2-метил-пропанол-1
2-метил-пропанол-1
2. межклассовая изомерия с простыми эфирами
CH3(CH2)3OH бутанол-1
CH3OCH2CH2CH3 метилпропиловый эфир
CH3CH2OCH2CH3 диэтиловый эфир
3. Пространственная – оптическая (если атом углерода связан с четырьмя разными атомами или группами атомов)
 бутанол-2
бутанол-2
Оптическими называют пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное отображение ( несовместимы в пространстве, как левая и правая рука)
Систематическая номенклатура
По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол», положение которого указывается арабской цифрой.
Правила построения названий спиртов:
1. Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, с одним из которых связана функциональная группа.
2. Пронумеруйте атомы углерода в главной цепи, начиная с того конца, к которому ближе функциональная группа.
3. Назовите соединение по алгоритму для углеводородов.
4. В конце названия допишите суффикс - ол и укажите номер атома углерода, с которым связана функциональная группа.
5. Для многоатомных спиртов перед суффиксом -ол указывается число гидроксильных групп (-диол, -триол, -тетраол и т. д.).
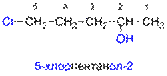
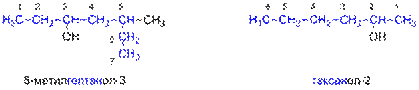
Другие номенклатуры
· Радикало-функциональная номенклатура. В рамках данной номенклатуры название образуется от названия класса соединения (спирт) с добавлением названий радикалов, присоединённых к гидроксильной группе, например: этиловый спирт C2H5OH, гексиловый спирт C6H13OH, аллиловый спирт СH2=CH-CH2OH.
· Рациональная номенклатура или Заместительная (карбинольная номенклатура) спиртов рассматривает их как производные метанола CH3OH, называемого в данном случае карбинолом: этилкарбинол – пропиловый спирт (пропанол),
· Тривиальная номенклатура. В популярной и научной литературе можно нередко встретить исторические, или тривиальные, названия спиртов, которые вследствие сложившейся традиции используются вместо систематических названий. Тривиальные названия обычно происходят от названия природного источника получения того или иного спирта. Так, например, метанол называют древесным спиртом, этанол — винным спиртом, гераниол содержится в гераниевом масле
Систематические и тривиальные названия некоторых спиртов.
Химическая формула спирта | Название по номенклатуре ИЮПАК (радикало-функциональной) | Тривиальное название (заместительная - карбинольная) |
CH3OH | Метанол (метиловый) | Древесный спирт (карбинол) |
C2H5OH | Этанол (этиловый) | Винный спирт (метилкарбинол) |
C5H11OH | Пентан-1-ол (амиловый) | Амиловый спирт (бутилкарбинол) |
C16H33OH | Гексадекан-1-ол | Цетиловый спирт |
Строение и свойства спиртов
Атом кислорода в спиртах в sp3-гибридизации.
В образовании его связей с атомами C и H участвуют две sp3-гибридные орбитали, валентный угол C–О–H близок к тетраэдрическому
I. Связи Оδ- – Нδ+ и Сδ+– Оδ- полярные ковалентные.
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
![]()
Разрыв таких связей происходит гетеролитически, т. е. преимущественно по ионному механизму.
В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
· При отщеплении протона (Н+) проявляются кислотные свойства,
· При отщеплении ОН – свойства оснований и нуклеофильного реагента.
· т. о. спирты проявляют свойства не только слабых кислот, но и слабых оснований Льюиса, т. е. они обладают амфотерными свойствами.
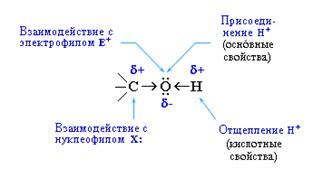
Кроме того: С разрывом связи О-Н идут реакции окисления, а по связи С-О – восстановления.
Таким образом, гидроксисоединения могут вступать в многочисленные реакции.
Следует учитывать, что
· электроноакцепторные заместители (–NO2, –CN, –F, –Cl, –Br, –I, –OR и др.) увеличивают кислотность спиртов (уменьшают pKa).
- трибромэтанол СВr3СН2ОН обладает гораздо большей активностью, чем этанол. Атом галогена как более электроотрицательный оттягивает на себя общую электронную плотность, и за счет этого связь O—H оказывается более поляризованной.
· электронодонорные заместители (например, алкильные заместители и COO−) уменьшают кислотность спиртов (увеличивают pKa).
- радикал, богатый электронными парами, легче, чем атом водорода, позволяет атому кислорода оттягивать на себя электронную пару связи R O.
Физиологическая активность и строение спиртов
???
Вопрос для размышления: Как вы считаете, влияют ли наличие галогена или кратной связи в структуре спиртов на их физиологическую активность и как?
Кроме того, на физиологическую активность спиртов оказывают влияние следующие факторы:
· длина углеродной цепи — физиологическое действие и токсичность нормальных первичных спиртов возрастают с удлинением углеродной цепи до 6 — 8 атомов, а затем уменьшаются;
· разветвление углеродной цепи — физиологическая активность спиртов усиливается с разветвлением углеродной цепи. Например, изобутиловый спирт более активен, чем нормальный бутиловый;
· положение гидроксильной группы в молекуле — вторичные спирты оказывают более сильное наркотическое действие, чем первичные спирты, а третичные, в свою очередь, более активны, чем вторичные. Например, изопропиловый спирт почти в 2 раза активнее нормального пропилового;
· наличие непредельной связи в молекуле, спирты, имеющие в молекуле непредельные связи, обладают более сильными наркотическими свойствами; при этом повышается токсичность спирта;
· введение галогенов в молекулу спирта: физиологическое действие спиртов, имеющих в молекуле галогены, усиливается. Например, проявление спиртом трифторэтанолом, СF3–СН2ОН, кислотных свойств объясняется взаимным влиянием атомов в молекуле: 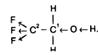
Атомы фтора, обладая отрицательным индукционным эффектом, смещают к себе электронную плотность связи F←С, в результате на втором углеродном атоме появляется частичный положительный заряд. Стремясь компенсировать свой заряд, он оттягивает электронную плотность от первого атома углерода. В свою очередь этот атом компенсирует заряд смещением электронной плотности от атома кислорода. Связь О–Н становится более полярной, атом водорода легко отщепляется в виде иона.
Химические свойства спиртов
I. Кислотно-основные свойства спиртов
1. Кислотные свойства.
Со щелочными и щелочноземельными металлами и некоторыми другими металлами, а также сильными основаниями (например: амидами или гидридами) спирты способны реагировать с образованием алкоголятов:
а) C активными металлами: 2C2H5OH + 2K → 2C2H5OK + H2↑
этилат калия (алкоголят)
CH2 OH - CH2OH + 2Na → CH2ONa - CH2 ONa +H2
ü Демонстрация видеоопыта
Из-за влияния радикала кислотные свойства спиртов убывают в ряду:
CH3OH > первичные > вторичные > третичные
б) С основаниями реагируют только многоатомные спирты
(проявляют более сильные кислотные свойства, из-за влияния нескольких О-Н групп) : C2H4(OH)2 + 2NaOH ⇄ C2H4(ONa)2 +2H2O
в) Реакция с Cu(OH)2↓ качественная реакция на многоатомные спирт
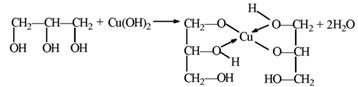 ярко-синий р-р
ярко-синий р-р
ü Демонстрация видеоопыта
2. Основные свойства. С галогеноводорными кислотами.
· Замещение –ОН на галоген или другую нуклеофильную группу, идущие по механизму SN подобно взаимодействию щелочей с кислотами:
![]()
Спирты являются слабыми основаниями, и их основность возрастает с увеличением длины или разветвлённости углеводородного радикала при гидроксильной группе.
3. Дегидратация
А. Межмолекулярная (t < 140oС, образуются простые эфиры): - замещение –ОН, по механизму SN

Б. Внутримолекулярная (t > 140oС, образуются алкены) – отщепления-элиминирования:
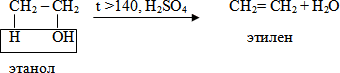
СH3–СHOH –СH2–СH3 (H2SO4 конц 170оС) → СH3– СH=СH–СH3 бутен-2+ HOH
(вторичный спирт – дегидратация идет по правилу Зайцева)
Правило Зайцева – водород отщепляется от менее гидрогенизированного атома углерода.
4. Реакция этерификации - реакция с минеральными и органическими кислотами с образованием сложных эфиров –
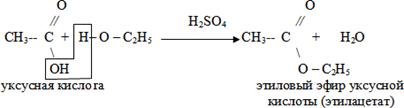
ü Демонстрация видеоопыта
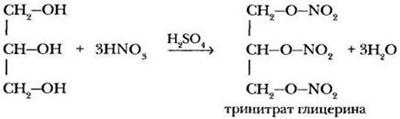
![]()
Глицерин легко нитруется, давая тринитроглицерин – сильное взрывчатое вещество (основа динамита):
5. Горение - полное окисление: С2Н5ОН + 3О2 → 2СО2 + 3Н2О
6. Неполное окисление.
Окислители KMnO4, K2Cr2O7 + H2SO4, CuO, O2+ катализатор
При неполном окислении образуются альдегиды, которые легко окисляются далее до карбоновых кислот:
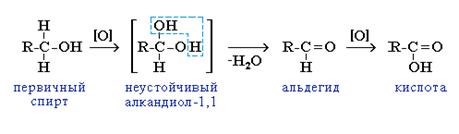
a) первичные спирты - превращаются в альдегиды - качественная р. на спирты
Этанол этаналь(уксусный альдегид)-запах яблок
ü Демонстрация видеоопыта
СН3-СН2-ОН + 2KMnO4 + 3H2SO4 → CH3-COOH + 2MnSO4 + K2SO4 +4H2O этанол уксусная кислота
Окисление хромовой смесью:
3CH3-CH2-OH + 2K2Cr2O7 + 8H2SO4 t→ 3CH3COOH + 2K2SO4 + 2Cr2(SO4)3 + 11H2O
Но метанол окисляется до углекислого газа:
CH3- OH + K2Cr2O7 + 4H2SO4 → CO2 + K2SO4 + Cr2(SO4)3 + 6H2O
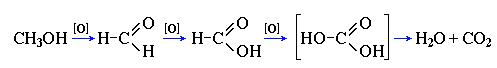
б) вторичные - в кетоны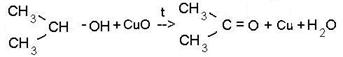
Пропанол-2 пропанон (диметилкетон, ацетон)
7. Йодоформная проба. При нагревании этилового спирта с йодом в щелочной среде ощущается запах йодоформа и постепенно образуется желтый осадок йодоформа. Эта реакция так же является качественной на определение этанола.
C2H5OH + 4I2 + 6KOH ® CHI3 ¯ + 5KI + HCOOK + 5H2O
Получение предельных одноатомных и многоатомных спиртов.
1. Щелочной Гидролиз галогеналканов:
CH3–Br + NaOH(водный) →CH3–OH +NaBr
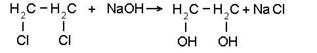
Дихлорэтан этандиол
2. Гидратация алкенов (промышленный способ):
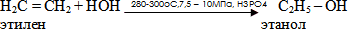
присоединение воды к несимметричным алкенам идет по правилу Марковникова с образованием вторичных и третичных спиртов.
CH3–CH=CH2 + H2O(300оС H3PO4)→CH3–CH ОН - CH3
3. Восстановление (гидрирование) карбонильных соединений.
· альдегидов - первичные спирты с кат. Pt, Pd, Co,Ni :
СН3-СОН + Н2 -(t,kat) → CH3-CH2OH этанол
· кетонов - вторичные спирты:
СН3-СО - СН3 + Н2 -(t,kat) → CH3-CH OH - СН3
пропанон пропанол-2
Специфические. Промышленные:
4. Получение метанола из синтез-газа:
![]()
5. Брожением получают этанол:
![]()
Давно известно, что фруктовые соки, например виноградный, можно использовать для получения вина – напитка с характерным вкусом и запахом. В процессе его изготовления происходит выделение газа. Кожица винограда содержит дрожжи, которые производят ферменты, катализирующие ферментацию сахара, содержащегося в соке. Установлено, что процесс брожения вызывают не сами микроорганизмы, а выделяемые ими вещества - зимазы. Для получения этилового спирта обычно используют растительное сырьё, богатое крахмалом: клубни картофеля, хлебные зёрна, зёрна риса и т. д.
6. Гликоли получают в реакции окисления алкенов 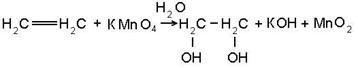
7. Глицерин - гидролизом жиров:

Применение спиртов в медицине
1. Этанол. используют в качестве наружного антисептического и раздражающего средства для приготовления компрессов и обтираний. Для приготовления различных настоек, разведений, экстрактов и прочих лекарственных форм
2. Диэтиловый эфир. В зубоврачебной практике его используют в качестве средства, осушающего полость рта. Раньше его применяли и в хирургии для местного обезболивания. Диэтиловый эфир – хороший растворитель жиров, смол, воска и других неполярных органических соединений, легко воспламеняется, поэтому при работе с ним нужно соблюдать меры предосторожности.
3. Глицерин входит в состав многих косметических средств как консервант и как средство, предотвращающее замерзание и высыхание.
4. Чистый нитроглицерин взрывается даже при слабом ударе; он служит сырьем для получения бездымных порохов и динамита ― взрывчатого вещества, которое в отличие от нитроглицерина можно безопасно бросать. Динамит был изобретен Нобелем, который основал известную всему миру Нобелевскую премию за выдающиеся научные достижения в области физики, химии, медицины и экономики. Нитроглицерин токсичен, но в малых количествах служит лекарством, так как расширяет сердечные сосуды и тем самым улучшает кровоснабжение сердечной мышцы
5. Сорбит (шестиатомный спирт) используется как заменитель сахара для больных диабетом.
Метаболизм спиртов в организме человека. Токсичность спиртов
Одноатомные предельные спирты вводят организм в наркозоподобное или гипнотическое состояние, а также оказывают токсическое действие.
Метиловый спирт — сильный яд (особенно при приеме внутрь) нервного и сердечно-сосудистого действия с выраженным кумулятивным эффектом; поражает органы зрения вплоть до полной слепоты. В больших дозах (30 г и более) вызывает смерть.
Этиловый спирт обладает токсическим эффектом. Этанол вызывает сначала возбуждение, а затем резкое угнетение центральной нервной системы (в том числе разрушает мозговую оболочку); его употребление приводит к нарушению важнейших функций организма, тяжелому поражению органов и систем. Оказывает эмбриотоксическое и тератогенное действие.
Изопропиловый спирт по своему токсическому воздействию напоминает этанол, вызывая угнетение центральной нервной системы и поражая внутренние органы. В высокой концентрации приводит к коме, конвульсиям и летальному исходу (около 3—4 г/кг).
Этиленгликоль очень токсичен при пероральном попадании в организм, поражает ЦНС и почки. Смертельная доза составляет 1,4 г/кг массы тела.
Следует помнить, что при употреблении 100гр. пива ориентировочно погибает до 3000 клеток мозга; 100 гр. вина - 5000 клеток;100 гр. водки – 7500 клеток.
Задание на дом:
Контрольные вопросы
1. Какие вещества называют спиртами?
2. Каковы общие формулы: а) предельных одноатомных спиртов; б) многоатомных спиртов;
3. Приведите примеры различных классификаций спиртов.
4. Какие виды изомерии характерны для: а) предельных одноатомных спиртов; б) многоатомных спиртов; ?
5. Каков алгоритм составления названий спиртов?
6. Какие виды химических связей есть в спиртах?
7. Каковы причины возникновения водородной связи в спиртах и каково ее влияние на физические свойства спиртов?
8. Каковы химические свойства: а) предельных одноатомных спиртов; б) многоатомных спиртов?
9. В чем сходство и отличие химических свойств одноатомных и многоатомных спиртов?
10. Каковы качественные реакции на: а) многоатомные спирты; б) одноатомные спирты?
11. Каковы способы получения спиртов?
12. Дайте определения, что такое: первичные (вторичные, третичные) спирты, водородная связь, реакция этерификации, реакция поликонденсации, диолы (триолы), простые эфиры, сложные эфиры, ароматические спирты.
Задания для самоконтроля
1. Составить структурные формулы третичных спиртов, содержащих 7 углеродных атомов, и назвать соединения.
2. Как получить этанол из этана двумя способами?
3. Какие углеводороды можно получить внутримолекулярной дегидратацией спиртов: а) 2-метилпропанола-2; б) бутанола-2; в) 2,3-диметилбутанола-2?
Составить уравнения реакций.
4. Какие одноатомные спирты нужно взять для получения углеводородов:
а) бутена-2; б) 3-метилгексена-1?Составить уравнения реакций.
5. Написать уравнения реакций, с помощью которых можно осуществить превращения:
а) этен ![]() хлорэтан
хлорэтан ![]() этанол
этанол ![]() этен
этен ![]() этандиол
этандиол ![]() 1,2-дихлорэтан
1,2-дихлорэтан ![]() этен;
этен;
б) этан ![]() хлорэтан
хлорэтан ![]() этанол
этанол ![]() этилен
этилен ![]() этан
этан ![]() хлорэтан
хлорэтан ![]() пропан
пропан ![]() 2-бромпропан
2-бромпропан ![]() пропанол-2
пропанол-2 ![]() ацетон;
ацетон;
6. Из 18,4 г этанола получили 6 г простого эфира. Найти выход продукта. Ответ. 40,5%.
7. При взаимодействии 13,8 г этанола и 28 г оксида меди(II) получили 9,24 г альдегида. Найти выход продукта. Ответ. 70%.
8. При дегидратации пропанола-2 получили пропилен, который обесцветил бромную воду массой 200 г (массовая доля брома в бромной воде равна 3,2%). Определить массу пропанола-2, взятого для реакции. Ответ. 2,4 г.
9. Какую массу бутадиена-1,3 можно получить по способу Лебедева из 230 л спирта (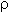 = 0,8 кг/л), если массовая доля этанола в спирте равна 95%, а выход продукта составляет 60%. Ответ. 61,56 кг.
= 0,8 кг/л), если массовая доля этанола в спирте равна 95%, а выход продукта составляет 60%. Ответ. 61,56 кг.
Рекомендуемая литература
Основные источники:
1. Органическая химия./Под ред. .- М.: «ГЭОТАР Медиа», 2014 г.
Дополнительные источники:
1. , Химия – 11, «Дрофа». 2009 г.
2. , Химия. - М.: «Академия», 2009 г.
3. , Органическая химия. СПО.- Ростов на/Д «Феникс», 2009 г.
Интернет-источники:
http://chemistry. ssu. samara. ru/index. php,
http://kazmedchem. ru/Book/web/index. html - интерактивный мультимедиа учебник по органической химии