Автор:
Проведён анализ вторичной структуры тРНК, а также внутримолекулярных контактов, поддерживающих третичную структуру молекулы.
Ключевые слова: тРНК, Yeast initiator tRNA, вторичная структура, внутримолекулярные взаимодействия.
Транспортная РНК (тРНК) узнаёт соответствующий кодон в мРНК и переносит активированный остаток определённой аминокислоты к растущей полипептидной цепи. Узнавание кодона в мРНК осуществляется с помощью трёх последовательных оснований в тРНК, называемых антикодоном. Аминокислотный остаток может присоединяться к 3’-концу молекулы тРНК. Молекула тРНК состоит примерно из 75 нуклеотидов, ковалентно связанных друг с другом в линейную цепочку. ”Клеверный лист”-это структурное представление молекулы тРНК, полученное из условия образования максимального числа уотсон-криковских пар оснований при данной нуклеотидной последовательности. Участки, в которых с помощью водородных связей образовались такие пары оснований, называются стеблями, а одноцепочечные участки – петлями.
Вторичная структура. Каждый стебель состоит из двух антипараллельных цепей, основания которых образуют друг с другом уотсон-криковские пары с помощью водородных связей. Стебли имеют форму правой двойной спирали, известной как А-форма РНК.
Третичная структура тРНК. Молекула напоминает по форме букву Г. Акцепторный и Т-стебли уложены в пространстве таким образом, что образуют одну непрерывную спираль-“перекладину” буквы Г; антикодоновый и D-стебли образуют “ножку”. Почти все основания в тРНК участвуют в вандерваальсовых и гидрофобных взаимодействиях, стабилизирующих пространственную структуру молекулы.(см. [1]).
Цель данной работы
заключается в том, чтобы на основании имеющейся пространственной структуры, изъятой из Protein Data Bank и визуализированной с помощью программы Rasmol, построить вторичную структуру тРНК (как вручную, так и с помощью программы mfold ); убедиться в том, что данная молекула действительно имеет форму клеверного листа; рассмотреть и проанализировать взаимодействия, отвечающие за пространственную (3D) форму тРНК; сравнить результаты, полученные из рассмотрения PDB структуры тРНК и полученные с помощью специальных программ (find_pair, mfold).
Результаты.
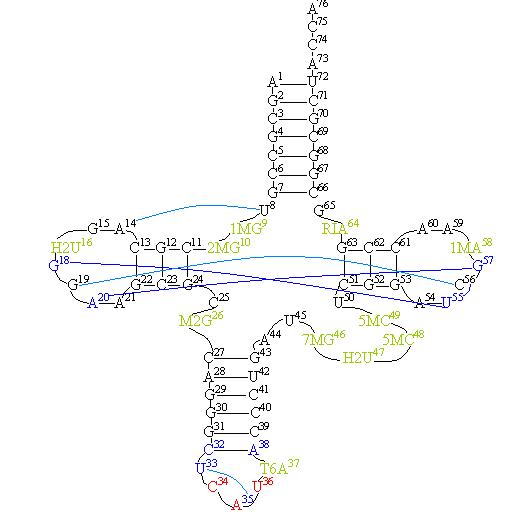
а) Схема(Fig.0) вторичной структуры, построенная вручную на основе третичной структуры тРНК (программа Rasmol, PDB ID – 1yfg). Указаны все пары комплементарных оснований.
Fig.0.

На схеме:
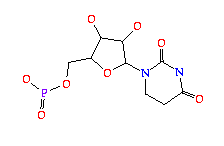
- в зелёный прямоугольник обведены нестандартные основания (Fig.1);
- в фиолетовый прямоугольник заключены основания, входящие в состав антикодона.
Fig.1
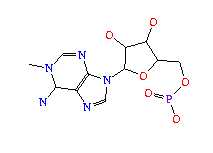
2MG (2N-METHYLGUANOSINE-5'-MONOPHOSPHATE); formula: C11H16N5O8P
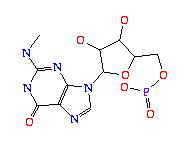
1MG (1N-METHYLGUANOSINE-5'-MONOPHOSPHATE); formula: C11H16N5O8P
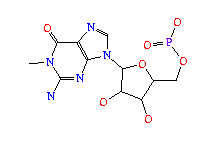
H2U (5,6-DIHYDROURIDINE-5'-MONOPHOSPHATE); formula: C9H15N2O9P
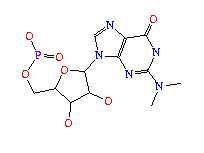
M2G (N2-DIMETHYLGUANOSINE-5'-MONOPHOSPHATE); formula: C12H18N5O8P
T6A (N-[N-(9-B-D-RIBOFURANOSYLPURIN-6-YL)CARBAMOYL]THREONINE-5'-MONOPHOSPHATE; N-(NEBULARIN-6-YLCARBAMOYL)-L-THREONINE-5'-MONOPHOSPHATE); formula: C15H21N6O11P.
Class: STANDARD ALPHA AMINO ACIDS.
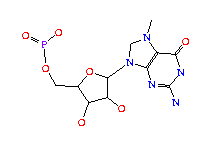
7MG (7N-METHYL-8-HYDROGUANOSINE-5'-MONOPHOSPHATE); formula: C11H18N5O8P
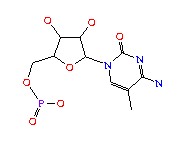
5MC (5-METHYLCYTIDINE-5'-MONOPHOSPHATE); formula: C10H16N3O8P
RIA (2'-O-[(5'-PHOSPHO)RIBOSYL]ADENOSINE-5'-MONOPHOSPHATE); formula: C15H23N5O14P2.
Class: NUCLEOTIDES
1MA (6-HYDRO-1-METHYLADENOSINE-5'-MONOPHOSPHATE); formula: C11H18N5O7P.
Схема вторичной структуры, построенная на основе данных (Table1, Table2), полученных с помощью программы find_pair:
4 длинные связи голубого цвета, отмеченные на основании Table1 и Table2, отвечают за Г-образную структуру тРНК. Это не-уотсон-криковские взаимодействия.
Table1.
RMSD of the bases (----- for WC bp, + for isolated bp, x for helix change)
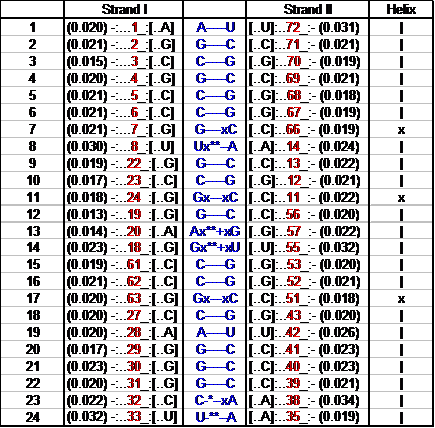
This structure contains 5[4] non-Watson-Crick base-pairs (данная структура содержит 5[4] не-уотсон-криковских пар оснований).
Table2.
Detailed H-bond information: atom-name pair and length [ON]
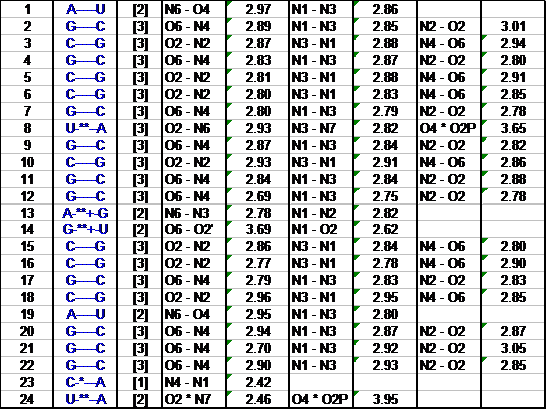
This structure contains more than one helical regions (эта структура содержит более, чем 1 спиральный участок).
This nucleic acid structure is *unusual* (структура этой нуклеиновой кислоты “необычная”)
В этих таблицах почему-то не отображены нестандартные основания и, соответственно, те связи, которые они образуют с другими частями молекулы.
Например:
1)
Взаимодействующие атомы | Длина водородной связи |
A54.N1 ---- 1MA58.N6 | 2.78Å |
A54.N6 ---- 1MA58.N7 | 2.76Å |
=>Образуются 2 водородные связи:
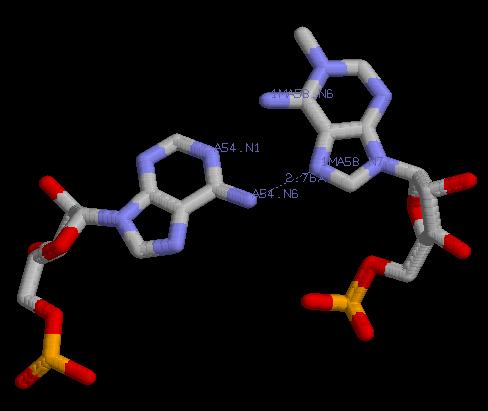
2)
Взаимодействующие атомы | Длина водородной связи |
U50.O4 ---- RIA64.N6 | 2.90 Å |
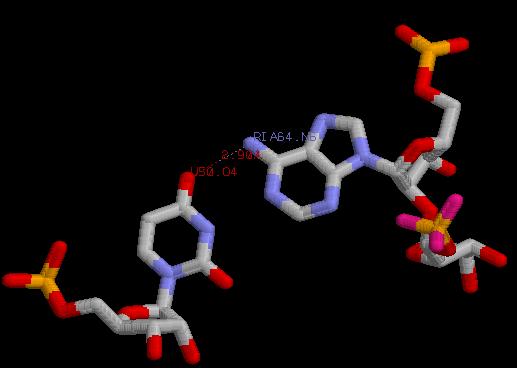
3)
Взаимодействующие атомы | Длина водородной связи |
5MC49.O2 ---- G65.N2 | 2.87Å |
5MC49.N4 ---- G65.O6 | 2.80 Å |
5MC49.N3 ---- G65.N1 | 2.84 Å |
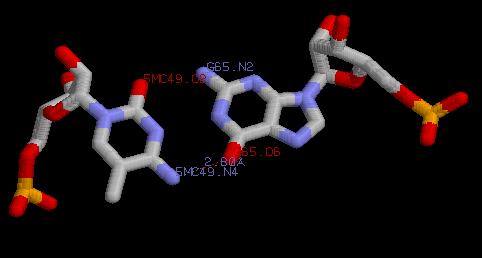
4)
Взаимодействующие атомы | Длина водородной связи |
2MG10.N2 ---- C25.O2 | 2.88 Å |
2MG10.N1 ---- C25.N3 | 2.84 Å |
2MG10.O6 ---- C25.N4 | 2.83 Å |
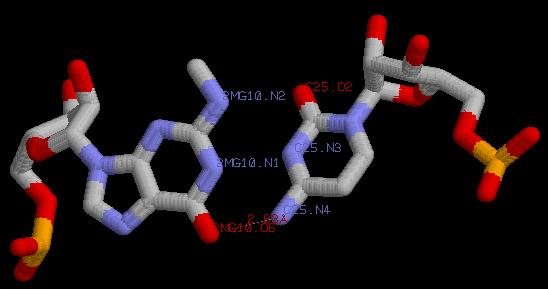
5)
Взаимодействующие атомы | Длина водородной связи |
A44.N1 ---- M2G26.N1 | 2.96 Å |
A44.N6 ---- M2G26.O6 | 2.81 Å |
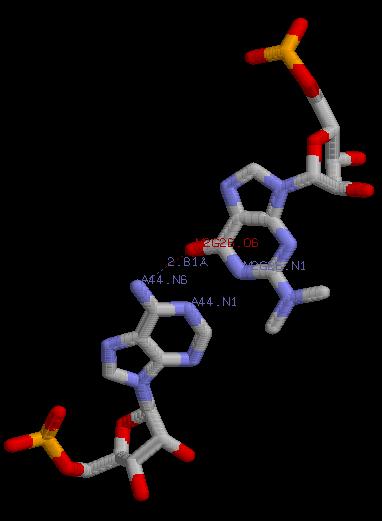
б) Таблица контактов нуклеотидов, которые отвечают за стабильность L-образной пространственной структуры тРНК (не сводящиеся к комплементарности водородные связи; неспиральный стэкинг) на основании анализа 3D-структуры.
Мне кажется, что за стабильность L-образной пространственной структуры отвечают следующие основания: u55, c56, g57, g18, g19, 1ma58, a60, a20, a59, a21, g15, a14, 5mc48, 7mg46, 1mg9, c13, 2mg10, u45, c25.
Не сводящиеся к комплементарности водородные связи:
Взаимодействующие атомы | Длина водородной связи |
C56.N4 ---- G19.O6 | 2.68 Å |
C56.N3 ---- G19.N1 | 2.74 Å |
C56.O2 ---- G19.N2 | 2.78 Å |
U55.O2 ---- G18.N1 | 2.62 Å |
U55.N3 ---- 1MA58.O2P | 2.55 Å |
G57.N2 ---- A20.N1 | 2.82 Å |
G57.N3 ---- A20.N6 | 2.77 Å |
1MA58.O2* ---- A60.N7 | 2.65 Å |
A20.O2* ---- A59.N6 | 3.05 Å |
C25.N4 ---- 2MG10.O6 | 2.83 Å |
C25.N3 ---- 2MG10.N1 | 2.84 Å |
C25.O2 ---- 2MG10.N2 | 2.88 Å |
1MG9.O2P ---- C13.N4 | 2.63 Å |
A14.N6 ---- U8.O2 | 2.92 Å |
A14.N7 ---- U8.O4 | 3.51 Å (очень слабая связь) |
5MC48.O2 ---- G15.N1 | 2.77 Å |
5MC48.N3 ---- G15.N2 | 2.88 Å |
Неспиральный стэкинг:
a)1MA58
G18
G57
Группа из 3-х оснований, участвующих в стэкинг взаимодействии.
б)A59
A60
Группа из 2-х оснований, участвующих в стэкинг взаимодействии.
в)5MC48
A21
7MG46
1MG9
U45
Группа из 5 оснований, участвующих в стэкинг взаимодействии.
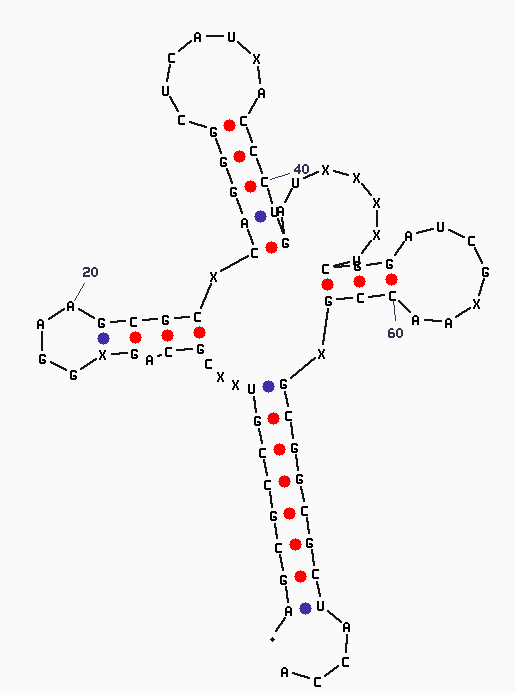
в) Предсказанная программой Зукера схема (Fig.2) вторичной структуры РНК.
Была выбрана структура, наиболее соответствующая реальности из предлагаемых программой вариантов.
Fig.2.
Обсуждение.
Несколько фраз о том, какими взаимодействиями поддерживается L-образная форма тРНК (с некоторыми деталями).
Почти все основания в тРНК участвуют в вандерваальсовых и гидрофобных взаимодействиях, стабилизирующих пространственную структуры молекулы. В стеблях, являющихся двойными спиралями, образуются уотсон-криковскиеводородные связи. Многие основания, расположенные вне стеблей, образуют водородные связи с другими основаниями, но эти связи отличаются от уотсон-криковских. Помимо этого2’-гидроксильные группы полинуклуетидной цепи также образуют водородные связи – с основанимями и с атомами водорода основной цепи.(см. [1]).
Несколько фраз о том, насколько предсказание вторичной структуры данной тРНК совпадает с данными, полученными по 3D.
В общем, структура, полученная с помощью программы Зукера довольно похожа на правду, но всё же есть некоторые смещения и несостыковки. В этом Вы можете убедиться, сравнив рисунок Fig.0. с картинкой из Fig.2.!
О роли структуры тРНК в ее функционировании.
Все тРНК имеют одинаковый 3’-конец, построенный из 2-х остатков цитозина и одного – аденозина (CCA-конец). Именно 3’-концевой аденозин связывается с аминокислотным остатком при образовании аминоацил-тРНК.
Участки тРНК:
1. Антикодон (остатки 34-36). Определяет на рибосоме включение аминокислоты в растущую цепь белка, участвует в отборе этой аминокислоты на стадии реакции аминоацилирования тРНК. Данные последних лет показывают, что в узнавании может участвовать один или более нуклеотидов антикодона.
2. Нуклеотид 73, предшествующий ССА-концу. Присутствие в этом положении того или другого пуринового нуклеотида (A или G) коррелирует с типом аминокислот, присоединяемых к тРНК. Если в этом положении находится А, то тРНК акцептирует гидрофобные аминокислоты, а если G – то полярные.
3. Первые три пары нуклеотидов акцепторного стебля (1-72, 2-71, 3-70). В разных случаях в узнавании синтетазой может вовлекаться от одной до трёх пар нуклеотидов акцепторного стебля.
Более подробно про тРНК см. [2].
Сопроводительные материалы.
В файлах 1yfg_scr. spt и hand. spt. содержится 2 скриптa для Rasmol, позволяющих визуализировать основные элементы структуры тРНК из PDB записи 1yfg.
Материалы и методы.
3D структура tRNA извлечена и записи 1yfg Protein Data Bank.
Комплементарность пар определена программой find-pair пакета 3DNA.
Результаты обработаны с помощью Word, Excel, Rasmol, ChemSketch и Paint.
Литература.
[1]. Э. Рис, М. Стенберг “Введение в молекулярную биологию. От клеток к атомам.” Издательство “Мир”, 2002.
[2]. 1. , 1998. Строение транспортных РНК и их функция на первом (предрибосомальном) этапе биосинтеза белков. Соросовский образовательный журнал, №11, 71-77 (http://www. pereplet. ru/nauka/Soros/pdf/9811_071.pdf)