ЗАДАНИЯ К ЭКЗАМЕНУ
по дисциплине «ОБЩАЯ И НЕОРГАНИЧЕСКАЯ ХИМИЯ»
1. При хроническом гастрите язвенной болезни желудка иногда назначают в качестве противовоспалительного средства внутрь 0.05 % раствор AgNO3 по 15 мл. Какая масса ионов серебра содержится в дозе объемом 15 мл (р = 1г/мл).
2. При отравлениях белым фосфором, принятым внутрь, назначают 0.5г сульфата меди в 100 г теплой воды. Какую массу (г) медного купороса необходимо взять, чтобы массовая для сульфата меди была равна 0.5%?
3. При взаимодействии 0,91 г некоторого металла с раствором соляной кислоты выделилось 0,314 л водорода. Чему равна атомная масса металла?
4. Найдите молярную концентрацию 30%-ной серной кислоты (плотность раствора 1,22 г/мл).
5. В больнице для промывания слизистых оболочек пациенту назначили 0.5%-ный раствор перманганата калия, а в наличии оказался только 6%-ный раствор этого вещества. Сколько воды и 6%-ного раствора (р = 1.01 г/мл) потребуется для приготовления 1 л 0.5%-ного раствора перманганата калия?
6. В медицинской практике для промывания ран применяют 0.5%-ный раствор перманганата калия (р = 1 г/мл). Какой объем раствора можно приготовить из 10 г перманганата калия?
7. В лаборатории имеется раствор с массовой долей гидроксида натрия 30%, плотность которого 1,33 г/мл. Какой объем этого раствора надо взять для приготовления раствора объемом 250 мл с массовой долей гидроксида натрия 14: и плотностью 1,15 г/мл?
8. Как приготовить 300 г 15%ного раствора смешиванием 5%-ного и 30%-ного?
9. Металл массой 4,1 г вытесняет из кислоты 1,4 л водорода (н. у.). Вычислите молярную массу эквивалента этого металла.
10. Рассчитайте рН 0,1 М раствора Н2S (КД = 1,1·10 –7).
11. Константа неустойчивости иона [Ag(CN)2]– составляет 10–21. Вычислите концентрацию ионов серебра в 0,1 н растворе K[Ag(CN)2], содержащем 0,01 моль KCN в 1 л раствора.
12. В начальный момент протекания реакции 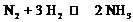 концентрации были равны (моль/л) СN2 = 1,5 ; CH2 = 2,5 ; CNH3 = 0. Каковы концентрации N2 и Н2 при концентрации NH3 0,5 моль/л?
концентрации были равны (моль/л) СN2 = 1,5 ; CH2 = 2,5 ; CNH3 = 0. Каковы концентрации N2 и Н2 при концентрации NH3 0,5 моль/л?
13. Константа равновесия КР реакции 2SO2+O2→2SO3 при 950К равна 1,062·10–2. Рассчитайте КС для этой реакции
14. ПР (PbI2) при 160С равно 8,7·10–9. Вычислите концентрацию ионов Pb2+ и I– в насыщенном растворе PbI2.
15. Реакция выражается уравнением ![]() . Через некоторое время после начала реакции концентрации участвующих в ней веществ стали (моль/л): СHCl = 0,8 ; CO2 = 0,4 ; CCl2 = 0,3. Какими были концентрации HCl и О2 в начале реакции?
. Через некоторое время после начала реакции концентрации участвующих в ней веществ стали (моль/л): СHCl = 0,8 ; CO2 = 0,4 ; CCl2 = 0,3. Какими были концентрации HCl и О2 в начале реакции?
16. При соединении 2,1 г железа с серой выделилось 3,8 кДж теплоты. Рассчитать теплоту образования сульфида железа.
17. Осмотическое давление крови равно в норме 740 – 780 кПа при 370C. Вычислите осмолярность крови.
18. Осмолярность апельсинового сока равна 0,6 осмоль/л. Вычислите его осмотическое давление при 50С.
19. Рассчитайте концентрацию ионов ОН - в растворе, рН которого равен 3,28.
20. Человек в течение дня потребил: белка 100 гр., углеводов 300 гр., жиров 40 гр.. Рассчитайте количество энергии, полученной человеком в течении дня (в килокалориях и килоджоулях).
21. Вычислите соотношение концентрации CH3COONa и CH3COOH в буферном растворе с pH, равным 6,1 (рКСН3СООН = 4,76).
22. В каком направлении пойдет реакция, если реагирующие вещества взяты в стандартных условиях SiO2(k) +2NaOH(p) = Na2SiO3(k) + H2O(ж)
(DGof (SiO2(к)) = - 803,75 кДж/моль; DGof (NaOHp) = -419,5 кДж/моль; DGof (Na2SiO3(к)) = - 1427,8 кДж/моль; DGof (H2Oж) = -237,5 кДж/моль)
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Составьте электронно-ионные схемы и закончите уравнения реакций:
Mg + HNO3 à Mg(NO3)2 + NH4NO3 + H2O
Cl2 + I2+ H2O à HCl + HIO3
S + KOH à K2SO3 + K2S +H2O
CrCl3 +Br2 + KOH à K2CrO4 +KBr +KCl + H2O
KI + K2CrO4 + H2SO4 à I2 + Cr2(SO4)3 + K2SO4 + H2O
HBr + H2SO4 à SO2 + Br2 + H2O
HNO3 + As2S3 + H2O à H3AsO4 + H2SO4 + NO
KNO3 + KI + H2SO4 à NO + I2 + K2SO4 + H2O
FeSO4 + KMnO4 + H2SO4 à Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
KCrO2 + Br2 + KOH à K2CrO4 + KBr + H2O
P + HNO3 + H2O à H3PO4 + NO
MnO2 + HCl à MnCl2 + Cl2 + H2O
KNO2 + KI + H2SO4 à NO + I2 + K2SO4 + H2O
HCl + K2Cr2O7 à CrCl3 +Cl2 + KCl + H2O
NaNO2 + KMnO4 + H2SO4 à MnSO4 + NaNO3 + K2SO4 + H2O
Na2SO3 + K2Cr2O7 + H2SO4 à Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O
NaBr + MnO2 + H2SO4 à Br2 + MnSO4 + Na2SO4 + H2O
H2O2 + KMnO4 + H2SO4 à O2 + MnSO4 + K2SO4 + H2O
MnSO4 + PbO2 + HNO3 à Pb(NO3)2 + PbSO4 + Pb(MnO4)2 + H2O
MnSO4 + KClO + KOH à MnO2 + KCl + K2SO4 + H2O
Al + HNO3 à Al(NO3)3 + NH4NO3 + H2O
KMnO4 + HBr + H2SO4 à MnSO4 + Br2 + K2SO4 + H2O
SO2 + HClO4 + H2O à H2SO4 + HCl
Al + K2Cr2O7 + H2SO4 à Al2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O




