Министерство образования Республики Карелия
Государственное автономное профессиональное образовательное учреждение Республики Карелия
«Сортавальский колледж»
Методические указания по выполнению лабораторных и практических работ по дисциплине «Химия»
специальности 19.02.10 Технология продукции общественного питания
(базовая подготовка среднего профессионального образования)
Сортавала 2016
Одобрена цикловой методической комиссией на заседании «__»____________________2016г. Протокол № ______ Председатель цикловой комиссии: ___________________ Автор: _____________ Преподаватель первой квалификационной категории | Составлена в соответствии с примерной программой дисциплины Химия 2008 года Заместитель директора по учебной работе ______________________ |
Рецензент:___________________
«Химии никоим образом научиться
Невозможно, не видав самой
практики и не принимаясь
за химические операции
Введение
В данных методических указаниях описаны методики выполнения лабораторных работ по общей и органической химии, дано краткое теоретическое введение к каждой теме, которое при самостоятельной подготовке поможет студентам выполнить эти работы. Методические указания выполнены в соответствии с рабочей программой.
Пособие поможет студентам совершенствовать практические умения и закрепить теоретические знания по дисциплине «Химия».
Пособие состоит из двух частей: первая посвящена лабораторным работам по общей и неорганической химии; вторая – по органической химии.
Описаны методики выполнения лабораторных работ, приведены контрольные вопросы, фиксирующие внимание студентов на наиболее важные этапы изучаемого материала.
В процессе выполнения лабораторных работ студенты должны наблюдать за ходом эксперимента, отмечать все его особенности (изменение цвета, тепловые эффекты, выпадение осадка, образование газообразных веществ). Результаты наблюдений записывают в тетради для лабораторных работ, поддерживаясь определенной последовательности:
- дата выполнения, название лабораторной работы;
- цель работы;
- краткие теоретические сведения, касающиеся данной работы;
- зарисовка схемы установки (выполняется карандашом);
- результаты опытов должны быть внесены в таблицу;
- выводы.
Рекомендации по составлению письменного отчета о выполненной практической работе.
Для оформления отчета о работе удобно использовать табличную форму.
| ||||
«Ход опыта» записывается кратко, вместо словесного описания последовательности действий используется рисунок. Обязательно указываются условия осуществления химических реакций.
В графе «Наблюдения» рисунок или схема поясняются следующими обозначениями:
- образование осадка: ↓ Указывается цвет осадка и его характер (мучнистый, творожистый, студенистый); - выделение газообразного вещества: ↑ Указывается цвет газа, запах.
В графе «Уравнения реакций» учащиеся могут выражать только сущность реакций ионного обмена, т. е. записывать только сокращенные ионные уравнения реакций. Для окислительно-восстановительных реакций записываются молекулярное уравнение реакции, выражается ее сущность методом электронного баланса. Указываются названия процессов и функции веществ.
Особого внимания требует заполнение графы «Вывод». Вывод должен соответствовать условию задачи, быть полным и обоснованным.
Инструкционная карта № 1.
Тема: Составление строения атомов по заданным схемам.
Характеристика формул.
Теория: Вещество-это то из чего состоят предметы. Вещество имеет сложное строение. Вещество состоит из молекул. Молекулы - это мельчайшие частицы, которые находятся в непрерывном движение: между ними существует взаимное притяжение и отталкивание. Скорость движения молекул зависит от агрегатного состояния веществ. Они отвечают за все свойства данного вещества, при физических явлениях состав молекул остаётся неизменимым, при химических - они претерпевают качественные и количественные изменения и из одних молекул образуются другие, способные к самостоятельному существованию.
Молекулы состоят из атомов - это мельчайшие неделимые частицы. При химических реакциях атомы, в отличие от молекул не претерпевают качественных изменений.
ВЕЩЕСТВО → МОЛЕКУЛЫ → АТОМЫ
1. Молекула может состоять из одного атома, характерно для металлов и некоторых неметаллов / Al, S,Si, Na, Pb, P/.
2. Молекула может состоять из нескольких атомов одного вида. И в первом и во втором случае речь идет о простых /N2/C2/Br2/H/ веществах.
Простое вещество - это вещество, состоящие из атомов одного вида.
3. Молекула может состоять из атомов разного вида и в этом случае речь идет о сложных веществах /Na2O, H2O, K2S, Na2SO4/.
Сложное вещество – это вещество, состоящее из атомов различного вида.
Атом –это электронейтральная частица имеющая сложное строение. Строение можно представить следующим образом: в центре располагается ядро, а вокруг ядра вращаются электроны. Ядро состоит из положительно заряженных протонов. Условно заряд одного протона равен + 1, а нейтроны зарядом частицы не обладают, число протонов в атоме данного элемента определяют по периодической системе – порядковым номером.
Число протонов = порядковому номеру элемента = заряд ядра
Na = +11, Al = + 13 ,Ca= +20,S= +16
Число нейтронов определяется по разнице между атомной массой и порядковым номером элемента.
Число нейтронов = Атомная масса – порядковый номер
Al=14, Na =12,Si=1
Заряд одного электрона условно принимается -1,число электронов в атоме любого элемента равно числу протонов и определяется порядковым номером элемента в периодической системе.
Число протонов = число электронов = порядковому номеру элемента.
Электроны в атоме вращаются по разным электронным слоям или энергетическим уровням, их число определяется номером периода где располагается данный элемент.
Число электронных слоев = номеру периода, где располагается элемент
Максимально число электронов на электроном слое рассчитывается по формуле N=2n2 , Где n-номер слоя.
На электронных слоях или энергетических уровнях электроны образуют подуровни, т. е. вращаются по орбиталям различной нормы. Число подуровней определяется номером уровня.
1 уровне – 1 Подуровень – S
2 уровне - 2 Подуровень –S, P
3 уровне - 3 Подуровень – S, P,d
4 уровне - 4 Подуровень –S, P,d, f
S - подуровень всегда 1 орбиталь шарообразной формы /O/.на котором может расположиться только 2 электрона с противоположными стенами / вращаются в противоположных направлениях/.
Графически обозначаются одной ячейкой
Электр. ф-ла S2.P – подуровень всегда 3 орбитали восьмеркообразной формы, на которой может располагаться 6 электронов по 2 на каждой орбитали. Графически изображается тремя ячейками электр. ф-ла р6
d – подуровень всегда 5 орбиталей более сложной конфигурации на котором могут располагаться 10 электронов, графически изображается пятью ячейками
f-подуровень всегда 7 орбиталей очень сложной конфигурации, на котором может располагаться 14 электронов, графически изображается 7 ячейками.
Записывается химический знак элемента Справа сверху записывается заряд ядра /порядковый номер периодич. системы/ Определяем число электронов электронная формула 1S2 2S2P6 3S1/ порядк. номер/ и распределяем их по уровням / номер периода/ с учетом формулы максимального числа электронов на слое.
Записываем уровни и подуровни, которые на нем имеются и распределяем электроны. При этом необходимо помнить, что каждый подуровень заполняется отдельно, сначала по одному электрону в каждую орбиталь, а затем происходит спаривание.
Проверка - на внешнем уровне у элементов главных подгрупп число электронов
соответствует номеру группы.
Помнить, что на внешнем электронном слое 2 электрона, заполняется d - подуровень предвнешнего слоя, его рассчитывают по разнице.
Помнить, что один электрон на внешнем слое объясняется правилом « черной дыры» - на предвнешнем слое /обычно d - подуровень / не может одна ячейка быть совсем пустая или заполненная не полностью/Cr, Cu, Ag, Me, Au/, а также др. влияния Nb/41/,Ru/44/Rh/45/,Pd/46/,Pt/78/.
ХИМИЧЕСКАЯ ФОРМУЛА
Это условная запись состава молекул вещества с помощью символов химических элементов и индексов, указывающих число атомов данного элемента, г
Формула несет информацию:
1. Качественную - какие элементы входят в состав данного вещества / из азота и кислорода/.
2. Количественную – сколько атомов каждого элемента входит в состав молекулы вещества -2 атома азота и 1 атом кислорода.
Расчеты по формуле:
1. Расчет относительной молекулярной массы Mr – сумма атомных масс элементов входящих в молекулу с учетом числа атомов каждого элемента.
Mr / N2O / = 2*14 + 1*16=44 / нет ед. измерения/
2. Запись молярной массы которая нужна для решения задач:
Mr=M Они численно равны, но М имеет ед. измерения г/моль
M/ N2O/ =44 г/ моль
3. Расчет массовой доли элемента в веществе /W / N2O
![]() где W(v)-массовая доля эл-та в %
где W(v)-массовая доля эл-та в %
![]()
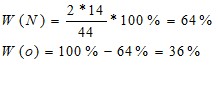
n – число атомов эл-та
Ar – атомноя масса эл-та
M - молярная масса вещества.
ЗАДАНИЯ.
Вариант 1.
1.Написать графические и элетронные формулы строения атомов следующих элементов: Al, N,V, Cu, AS
2. Вещество имеет формулу Al(NO3)3 дать качественную и количественную характеристику.
3. Рассчитать молекулярную массу след. вещ-вам : Ca SO4,Al2(SO4)3,AlCl3,Co(OH)2,P2O5.Записать их молярную массу.
4. Рассчитать массовую долю каждого эл-та в формулах
Al2(SO4)3,Ca(OH)2,P2O5
5.Что означает след. запись: 4H, 2H2, 5H2O, 10O2, 3HNO3.
6. Напишите химические формулы веществ, если известно, что в их состав входит:
А) атом железа и 3 атома хлора
Б) 2 атома алюминия и 3 атома кислорода
В) атом кальция, атом углерода и 3 атома кислорода.
Инструкционная карта № 2
Тема : Способы очистки веществ от примесей
Теория: Растворы – это однородные системы, состояшие из растворенного вещества и растворителя. Их обычно подразделяют на истинные, коллойдные и взвеси. Различают растворы водные и неводные в зависимости от растворителя. Неводные обычно в качестве растворителя содержат спирт, бензин и другие вещества.
Растворы занимаю промежуточное положение между механическими смесями / поваренная соль и уличный песок / и химическими соединениями.
M/ раствора /=М/ растворенного / +М/ растворителя/
В зависимости от количества растворенного вещества растворы классифицируются:
Насыщенные растворы – В растворе растворено столько вещества сколько может раствориться при данной температуре Ненасыщенные растворы – В растворе растворено меньше вещества чем может раствориться при данной температуре. Перенасыщенные растворы – В растворе растворено вещества больше чем может раствориться при данной температуре.Концентрация раствора – это количество растворенного вещества в определенном количестве раствора.
Способы выражения концентрации:
1. Процентная – количество растворенного вещества в 100 гр. Раствора. 5%-5 гр. Вещества в 100 гр. Раствора
Задача. Сколько грамм хлорида меди и воды потребуется для приготовления 500г. 5% раствора.
1/ Какое количество вещества потребуется :
5 гр.- в 100 гр. Раствора
Х-гр. В 500гр. Раствора
![]()
2/ Какое количество растворителя потребуется:
2. Какое количество г - эквивалентов вещества в 1 литре раствора. /Н/
1 М - однонормальный раствор.
0,1 М – децинормальный раствор.
0,01 М – сантинормальный раствор.
0,001 М – миллинормальный раствор.
Задача. Сколько гр. Сульфата меди потребуется для приготовления 1 л 0,2 М раствора.
Рассчитать молярную массу сульфата меди:М=64+32+64=169 г/моль
Рассчитать г-экв соли :![]()
1 М содержит -80 г. Вещества
0,2 содержит - х г. Вещества
![]()
![]()
1М-одномолярный
0,1М-децимолярный
0,01М-сантимолярный
0,001М-миллимолярный
Задача. Определит процентную концентрацию раствора если 30 г. Вещества растворили в 150г. Растворителя.
Определять массу раствора :
30+150=180
Определяют процентную концентрацию или массовую долю растворенного вещества:
![]()
Реактивы : поваренная соль, уличный песок, вода
Оборудование: колбы конические на 100мл. воронки, филтры, тигели, тигелние щипцы.
Ход работы:
В колбу в которой находится смесь уличного песка и поваренной соли прилить воды и перемешать. Отметить, что вы наблюдайте.
Собрать фильтровальную установку и профильтровать приготовленный раствор. Приготовленный профильтрованный раствор называется фильтратом. Вещество которое оседает на фильтре называется осадком. Отметить, что вы наблюдайте?
В фарфоровый тигель наливают фильтрат объемом Ѕ и ставят на плитку. Проводят выпаривание раствора.
ТИГЕЛЬ СТАВИТЬ И СНИМАТЬ С ПЛИТКИ ТОЛЬКО С ПОМОЩЬЮ ТИГЕЛЬНЫХ ЩИПЦОВ!!!
Не допускать прокаливания осадка!
ВЫВОД: Какие процессы можно использовать для очистки веществ от примесей.
Задание:
1. Определить массу раствора и массовую долю растворенного вещества если 20 г. Вещества растворили в 50 г. Растворителя.
2. Сколько гр. Вещества и растворителя потребуется для приготовления 200гр. 15% раствора.
3. Определить концентрацию раствора, если в 180 гр. Раствора находится 10 г. растворенного вещества.
4. Определить г-эквивалент: M2SO4, KOH, NA2CO3
5. Сколько вещества потребуется для приготовления 200мл 1н раствора серной кислоты.
6. Сколько вещества потребуется для приготовления 1л0,15н раствора щелочи калия.
Инструкционная карта № 4
Тема: Гидролиз солей
Теория : Гидролизом солей называется взаимодействия солей с водой, которое приводит к образованию слабого электролита и изменению реакции среды. Слабыми электролитами могут быть все нерастворимые соли, основания и слабые кислоты : угольная, сернистая, сероводородная, уксусная.
Реакции среды может быть : кислая, щелочная, нейтральная. Кислая среда определяется наличием ионов водорода(Н +), щелочная – наличием ионов гидроксида(ОН-), нейтральная среда может быть, когда ионов водорода и гидроксида одинаковое количество или они полностью отсутствуют.
Вещества, которые могут помочь определить реакцию среды, называются индикаторами.
Кислая Щелочная Нейтральная
Лакмус красная синяя фиолетовая Фенолфталеин бесцветный малиновая бесцветный Метиловый оранж. Розовая желтая оранжеваяПРИ ГИДРОЛИЗЕ СОЛИ ВСЕГДА ОБРАЗУЮТ ОСНОВАНИЯ И КИСЛОТЫ.
Три случая гидролиза солей:
Соль образованная сильным основанием и слабой кислотой, гидролизуется с образованием слабой кислоты, а реакция среды щелочная: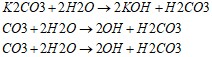
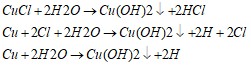
Реактивы: сульфат меди, карбонат калия, сульфит натрия, хлорид железа III, лакмусовая бумага - фиолетовая и розовая
Оборудование: пробирки.
Ход анализа:
В раствор с сульфатом меди отпустить сначала фиолетовую лакмусовую бумажкой, а затем розовую и записать как изменился цвет каждой индикаторной бумажки. Какую среду они указывают?Написать уравнение реакции в молекулярной, полной и сокращенной ионной формах.
В раствор с карбонатом калия опустить сначала фиолетовую лакмусовую бумажку, а затем розовую и записать как изменился цвет каждой индикаторной бумажки. Какую среду они указывают?Написать уравнения реакции в молекулярной, полной и сокращенной ионной формах.
В раствор с сульфитом натрия опустить сначала фиолетовую лакмусовую, а затем розовую бумажку и записать как изменился цвет каждой бумажки. Какую среду они указывают?Написать уравнения реакции в молекулярной, полной и сокращенной ионной формах.
В раствор с хлоридом железа III отпустить сначала фиолетовую лакмусовую бумажку, а затем розовую и записать как изменился цвет каждой лакмусовой бумажки. Какую среду они указывают?Написать уравнения реакции в молекулярной, полной и сокращенной ионной формах.
Вывод: Что такое гидролиз солей?
Задание:
Даны формулы: Na2SO4,Fe(NO3)2,Na2S, написать уравнения гидролиза тех веществ, где идет реакция в молекулярной, полной и сокращенной ионной формах. Указать реакцию среды в каждом случае Какую среду будут иметь растворы следующих солей:K2S, KNO
Имеются уравнения реакций(гидролиза) в сокращенной ионной форме:![]()
Напишите уравнения гидролиза в молекулярной форме.
Какова концентрация раствора хлорида железа, если 20 гр. соли растворили 100гр. воды.Инструкционная карта №6
Тема: Составления уравнений реакций, характеризующих химические свойства металлов и неметаллов.
Вариант 1.
1.Даны растворы веществ: карбоната натрия и серной кислоты. С помощью каких реактивов можно распознать в какой пробирке находится какое вещество. Ответ подтвердить уравнением реакции в молекулярной, полной и сокращенной ионной формах.
2. Даны вещества: HCl, Li OH, Ca CO3. Какие из них могут реагировать друг с другом, уравнения писать с точки зрения ионного обмена
3. Даны уравнения реакции, определить которое из них является окислительно-восстановительным и разобрать ее с точки зрения окисления-восстановления:
4. Написать уравнения гидролиза солей в молекулярной, полной и сокращенной тонной формах, указать реакцию среды:
A) Al (NO3)3 B) Na2CO3 C) CaS
5. Сколько грамм карбоната кальция образуется при взаимодействии 22 грамм оксида углерода и оксидом кальция.
6. Сколько грамм оксида цинка образуется из 20 грамм цинка, если в нем 10% примесей
7. Сколько грамм сульфата магния образуется из 120 грамм магния, если выход продукции 85%
8. Сколько грамм сульфида магния образуется, если с серой вступает в реакцию 100 грамм магния, содержащего 15% примесей, а выход продукции 90%
Вариант 2
Даны растворы: сульфата калия(К2SO4) и хлорида натрияПробирке находится какое вещество.
Ответ подтвердить уравнением реакции в молекулярной, полной и сокращенной ионной формах.
Даны вещества, какие из них могут реагировать друг с другом, уравнения реакции писать с точки зрения ионного обмена:HNO3, KOH, K2CO3, AL(NO3)3
Даны уравнения реакции, определить, которое из них является окислительно-восстановительным и разобрать его с точки зрения окисления-восстановления:![]()
Написать уравнение реакции гидролиза солей в молекулярной, полной и сокращенной ионной формах, указать реакцию среды:
А) CuSO4 б)K2S в)CuSO3
Сколько грамм оксида кальция образуется из 200 грамм кальция Сколько грамм оксида магния образуется из 100 грамм магния если в нем 15% примесей Сколько гамм хлорида цинка образуется при взаимодействии 260 грамм цинка с соляной кислотой, если выход продукции 75% Сколько грамм оксида углерода образуется из 100 грамм углерода, если в нем 10% примесей, а выход продукции 90%Вариант 3
![]()
Fe Cl2 b) Na2 SO3 c) Al2S3
Сколько грамм оксида магния образуется при разложении 60 грамм карбоната магния Сколько грамм оксида алюминия образуется из 80 грамм алюминия, если в нем содержится 12% примесей Сколько грамм нитрата цинка образуется, если в реакцию вступает 150грамм цинка, а выход продукции 85% Сколько грамм сульфида натрия образуется из 80 грамм натрия, если в нем 10% примесей, а выход 90%Вариант 4
Даны растворы веществ: хлорида калия и нитрата аммония. С помощью каких реактивов можно распознать в какой пробирке находится какое вещество. Ответ подтвердить уравнением реакции в молекулярной, полной и сокращенной ионной формах Даны вещества, какие из них могут взаимодействовать друг с другом. Уравнения писать с точки зрения ионного обмена:K3 PO4, Ca (OH)2, Na2 CO3, Fe Cl3
Даны уравнения реакции, определить, какое из них является окислително-восстановительным и разобрать его с точки зрения окисления-восстановления:![]()
K2CO3, Al2(CO3)3
Сколько грамм оксида алюминия образуется из 40 грамм алюминия. Сколько грамм сульфида алюминия образуется из 120 грамм алюминия, если в нем 10% примесей. Сколько грамм хлорида алюминия образуется, если в реакцию с соляной кислотой вступает 100 грамм алюминия, а выход продукции 95%
Инструкционная карта № 7
Тема: Свойства металлов и их соединений.
Оборудования: пробирки
Реактивы: гидроксид натрия, свежеприготовленный сульфат железа, хлорид железа, соляная кислота, серная кислота, железные опилки.
Ход работы:
Опыт 1. Взаимодействия железа с разбавленными кислотами.
В пробирку всыпать немного железных опилок и влить немного соляной кислоты. Что вы наблюдайте? Написать уравнения реакции и разобрать его с точки зрения окисления-восстановления.
Опыт 2. Получения гидроксида железа и взаимодействия его с кислотами.
А) Налейте в пробирку 2-3 мл свежеприготовленного сульфата железа и прилейте немного гидроксила натрия. Что вы наблюдайте? Написать уравнения реакции в молекулярной, полной сокращенной и ионной формах.
В) К полученному осадку добавить немного соляной кислоты. Что вы наблюдайте? Написать уравнения реакций в молекулярной, полной и сокращенной ионной формах.
Опыт 3. Получения гидроксида железа и взаимодействия его с кислотами.
А) Налить в пробирку 2-3 мл хлорида железа и добавить немного гидроксида натрия.
Что вы наблюдайте?
Написать уравнения реакции в молекулярной, полной и сокращенной ионной формах.
В) К полученному осадку добавить немного серной кислоты.
Что вы наблюдайте?
Написать уравнения реакции в молекулярной, полной и сокращенной ионной формах.
Вывод: С чем реагирует железо?
Как можно получить гидроксиды железа и с чем они взаимодействуют
Задания :
1. Написать уравнение электролиза:
А) расплава хлорида калия.
В) водного раствора нитрата меди, сульфида калия.
2. Разберите уравнения реакции с точки зрения окисления-восcтановления:
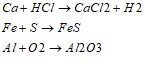
3. Из 200 грамм известняка, содержащего 4 % примесей, получили120 грамм оксида кальция: определить % выхода продукции.
4. На алюминий массой 10 грамм подействовали избытком раствора соляной кислоты, какой газ и в каком количестве выделился при этом.



