Федеральное агентство по образованию
Бийский технологический институт (филиал)
государственного образовательного учреждения
высшего профессионального образования
«Алтайский государственный технический университет им. »,
Эквивалент химических веществ
Методические рекомендации по выполнению лабораторной работы по дисциплине «Химия» для студентов специальностей 151001, 160302, 190603, 080401, 170104, 230201, 260204, 240901, 240701, 240702, 240706, 260601, 200106 всех форм обучения
Бийск
Издательство Алтайского государственного технического
университета им.
2010
УДК 546 (075.5)
Рецензент: профессор, к. х.н. БТИ АлтГТУ
Макрушина, Т. И.
Эквивалент химических веществ: методические рекомендации по выполнению лабораторной работы по дисциплине «Химия» для студентов специальностей 151001, 160302, 190603, 170104, 230201, 080401, 080502, 260204, 240901, 240701, 240702, 240706, 260601, 200106 всех форм обучения / , ; Алт. гос. техн. ун-т, БТИ. – Бийск : Изд-во Алт. гос. техн. ун-та, 2010. – 36 с.
Методические рекомендации содержат теоретические сведения по теме основные законы химии, описание методики и правил проведения лабораторной работы, задачи и примеры их решения, тесты, а также примерный перечень вопросов и рекомендации по защите лабораторной работы.
УДК 546 (075.5)
Рассмотрены и одобрены на заседании
кафедры общей химии и экспертизы товаров.
Протокол № 4 от 02 марта 2010 г.
© , 2010 © БТИ АлтГТУ, 2010 |
СОДЕРЖАНИЕ
Введение | 4 |
1 Теоретическая часть | 5 |
1.1 Атомно-молекулярное учение | 5 |
1.2 Закон сохранения массы вещества | 6 |
1.3 Закон постоянства состава вещества | 7 |
1.4 Стехиометрические расчеты в химии | 9 |
1.5 Закон эквивалентов | 11 |
1.6 Закон кратных отношений | 16 |
1.7 Закон Авогадро | 17 |
2 Экспериментальная часть | 18 |
2.1 Методика эксперимента | 18 |
2.2 Обработка экспериментальных данных | 20 |
2.3 Примерный перечень вопросов для получения допуска к лабораторной работе | 21 |
2.4 Примеры решения задач | 21 |
2.5 Задачи для самостоятельного решения | 25 |
2.6 Тесты | 29 |
2.7 Примерный перечень вопросов на защиту работы | 32 |
2.8 Общие методические рекомендации по подготовке и защите лабораторной работы | 32 |
3 Техника безопасности | 34 |
авление насыщенного водяного пара | 35 |
Литература | 36 |
ВВЕДЕНИЕ
Историк, риторик, механик, химик,
металлург, художник и стихотворец,
он все испытал и все проник
Эти слова посвятил великому русскому ученому , который открыл один из основных законов химии «Закон сохранения массы вещества». С помощью этого закона он объяснил превращения металлов, происходящие при их горении. использовал количественные методы исследования. Он заложил фундамент новой науки − физической химии. развил основы атомно-молекулярной теории. Он стремился к передаче своих знаний народу.
К основным законам химии относятся: атомно-молекулярное учение, закон сохранения вещества и энергии, закон постоянства состава, закон эквивалентов, закон Авогадро, закон кратных отношений, учение о строении атома и периодический закон, законы термодинамики.
1 ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1 Атомно-молекулярное учение
Все химические вещества состоят из частиц, классификация которых в химии достаточно сложна; химические превращения связывают, прежде всего, с такими частицами, как атом, молекула, электрон, атомные и молекулярные ионы, радикалы.
Основные положения атомно-молекулярного учения.
1. Все вещества состоят из молекул. Молекула − наименьшая частица вещества, обладающая его химическими свойствами.
2. Молекулы состоят из атомов. Атом − наименьшая частица химического элемента, сохраняющая все его химические свойства. Атомы одного вида одинаковы между собой и отличаются от атомов другого вида массой и свойствами.
Атом − электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра (образованного протонами и нейтронами) и электронов.
3. Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
4. Между молекулами существуют силы взаимного притяжения и отталкивания.
5. Существуют вещества с молекулярным и немолекулярным строением.
Вещества с молекулярным строением – это такие вещества, у которых в твердом состоянии в узлах кристаллических решеток находятся молекулы.
Вещества с немолекулярным строением – это такие вещества, у которых в твердом состоянии в узлах кристаллических решеток находятся другие частицы (атомы, ионы).
6. При взаимодействии атомов образуются молекулы: простых веществ или сложных веществ.
7. При физических явлениях молекулы сохраняются, при химических – разрушаются, атомы же и при физических, и при химических реакциях остаются неизменными.
8. Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состоят первоначальные вещества.
1.2 Закон сохранения массы вещества
Рассмотрим в свете атомно-молекулярного учения основные законы химии: сохранения массы веществ, постоянства состава, закон эквивалентов, объемных кратных отношений и закон Авогадро. Эти законы подтверждают атомно-молекулярное учение − основу химии. В свою очередь, атомно-молекулярное учение объяснило основные законы химии.
Закон сохранения массы веществ впервые сформулирован в 1748 г. . Позднее (в 1756 г.) он экспериментально обосновал этот закон. Современная формулировка закона такова: масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции.

Рисунок 1.1 −
Независимо от Ломоносова этот закон сформулировал в 1789 г. французский химик Лавуазье. Он также получил экспериментальные доказательства закона, изучив многие реакции окисления металлов. Закон сохранения массы веществ может быть объяснен так: при химических реакциях атомы не исчезают и не могут возникнуть из ничего; общее число атомов остается постоянным до и после реакции. Например, при взаимодействии двухатомных молекул водорода и хлора должно образоваться столько молекул НСl, чтобы число атомов водорода и хлора осталось равным двум, т. е. две молекулы:
Н2 + Cl2 = 2HCl
Поскольку атомы имеют постоянную массу, не меняется и масса веществ до и после реакции. Закон сохранения массы веществ связывал с законом сохранения энергии (количества движения). Законы сохранения массы веществ и сохранения энергии − это две стороны единого закона природы — закона вечности материи и ее движения. Взгляды подтверждены современной наукой.
Взаимосвязь массы и энергии (она рассматривается в физике) выражается уравнением Эйнштейна:
Е = m·c2, (1.1)
где Е − энергия;
m − масса;
c − скорость света в вакууме.
Закон сохранения массы веществ дает материальную основу для составления уравнений химических реакций. Опираясь на него, можно производить расчеты по химическим уравнениям.
1.3 Закон постоянства состава вещества
К основным законам химии относится закон постоянства состава, который был открыт в 1799–1808 гг. Ж. Прустом.

Рисунок 1.2 − Жозеф луи Пруст
Всякое чистое вещество независимо от способа его получения всегда имеет постоянный качественный и количественный состав.
Рассмотрим, например, состав оксида углерода (IV) СО2 . Он состоит из углерода и кислорода (качественный состав). Содержание углерода в углекислом газе СO2 − 27,27 %, кислорода — 72,73 % (количественный состав). Получить углекислый газ можно многими способами: синтезом из углерода и кислорода, из оксида углерод (II) и кислорода, действием кислот на карбонаты и др. Во всех случаях чистый оксид углерода (IV) будет иметь приведенный выше состав независимо от способа получения. Атомно-молекулярное учение позволяет объяснить закон постоянства состава. Поскольку атомы имеют постоянную массу, то и массовый состав вещества в целом постоянен.
Закон постоянства состава впервые сформулировал французский ученый-химик Ж. Пруст в 1808 г. Развитие химии показало, что наряду с соединениями постоянного состава существуют соединения переменного состава. Первые названы дальтонидами (в память английского химика и физика Дальтона), вторые — бертоллидами (в память французского химика Бертолле, предвидевшего такие соединения). Состав дальтонидов выражается простыми формулами с целочисленными стехиометрическими индексами, например, молекулы хлороводорода НС1, четыреххлористого углерода CCl4, углекислого газа CO2. Состав бертоллидов изменяется и не отвечает стехиометрическим отношениям. Например, состав оксида урана (VI) обычно выражают формулой UOз. На самом деле он имеет состав от UO2,5 до UO3. Бертоллиды встречаются среди оксидов, гидридов, сульфидов, нитридов, карбидов (соединения с углеродом), силицидов (соединения с кремнием) и других неорганических веществ, имеющих кристаллическую структуру. В связи с наличием соединений переменного состава в современную формулировку закона постоянства состава следует внести уточнение.
Состав соединений молекулярной структуры, т. е. состоящих из молекул, является постоянным независимо от способа получения.
Состав же соединений с немолекуляриой структурой (с атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения.
Например, состав оксида ванадия (II) зависит от температуры и давление кислорода, применяемого при синтезе. Надо также учитывать изотопный состав элементов: обычная вода, например, содержит 11,19 % водорода, а тяжелая вода – 20 % .
1.4 Стехиометрические расчеты в химии
Слово «стехиометрия» – изобретение немецкого химика Иеремии Вениамина Рихтера (1762–1807). Рихтер произвел его от греческих слов stoicheion – основание, элемент и metreo – измеряю, что должно было означать измерение соотношений, в которых химические элементы реагируют друг с другом.
Стехиометрия − раздел химии, в котором рассматриваются массовые или объемные соотношения между реагирующими веществами. Исключительное значение для развития химии имело установление основных стехиометрических законов.
Стехиометрическими расчетами называют нахождение значений количества, масс и объемов веществ (реагентов и продуктов), участвующих в химических реакциях.
Реальные частицы – это атомы, молекулы, ионы, электроны, радикалы и т. д.
Условные частицы – это какая-то часть реальной частицы, например, 1/5 молекулы.
Международная единица атомных масс равна 1/12 массы изотопа 12C − основного изотопа природного углерода.
1 а. е.м. = 1/12 ∙ m (12C) = 1,66057 ∙ 10-27 кг.
Относительная атомная масса (Ar) - безразмерная величина, равная отношению средней массы атома элемента (с учетом процентного содержания изотопов в природе) к 1/12 массы атома 12C.
Средняя абсолютная масса атома (m) равна относительной атомной массе, умноженной на а. е.м.
Ar(Mg) = 24,312
m (a)(Mg) = 24,312 ∙ 1,66057 ∙ 10-27 = 40,37 ∙ 10-27 кг.
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода 12C.
Mr (B) = m(a)(B) / (1/12 mа(12C)),
где ma(B) − масса молекулы данного вещества;
mа(12C) − масса атома углерода 12C.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а. е.м. Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения − моль.
Моль – количество вещества, содержащего столько реальных или условных частиц, сколько атомов содержится в 12 граммах изотопа углерода 12C.
Молярная масса M(B) – это масса одного моля вещества. По абсолютному значению она равна для простых веществ относительной атомной массе Ar(B), для сложных веществ – относительной молекулярной массе Mr(B), но выражена в г/моль или кг/моль.
Формульное количество вещества B (nB) и масса этого вещества (mB) связаны между собой соотношением:
nB = mB /M (B), (1.2)
где M(B) – молярная масса данного вещества.
Единица формульного количества вещества – моль. Буквой В обозначена формульная единица вещества, которой может быть химическая формула атома (Na, Ca), молекулы (Cl2, H2O2), катиона (K+, Al3+), аниона (CN-, NO3-, Cr2O72-), электронейтральной группы катионов и анионов (AlCl3, K2Cr2O7), радикала (-OH, - NO2) или любой другой точно определенной и реально существующей совокупности указанных частиц.
Если вещество B – газ, то его формульное количество и объем (VB) соотносятся между собой так:
nB = V(B) /VM, (1.3)
где V(B) - объем, занимаемый газообразным веществом;
VM – молярный объем идеального газа при при нормальных условиях (н. у.) – атмосферном давлении p = 1,01325 . 105 Па = 1 атм и термодинамической температуре T = 273,15 K – значение VM принимается равным 22,4 л/моль.
Масса находящегося в любом агрегатном состоянии вещества B определяется объемом этого вещества по выражению
m(B) = с(B) ·V(B) (1.4)
где с(B) − плотность данного вещества.
Для необратимой химической реакции, определяемой стехиометрическим уравнением
нАА + нВВ+ …= нСС + нDD + …,
формульные количества реагентов и образовавшихся продуктов пропорциональны соответствующим стехиометрическим коэффициентам нА, нВ, …, нС, нD, …:
пА / нA = п В / нB = …=пС /нC =пD / нD = … (1.5)
Если формульное количество одного из веществ (реагента или продукта) задано условием задачи, то вышеприведенное выражение позволяет рассчитать формульные количества (а, следовательно, массы и объемы) участвующих в данной реакции всех остальных веществ в соответствии с их стехиометрией.
1.5 Закон эквивалентов
Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН–, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества. Например, рассмотрим следующую реакцию:
H3PO4 + 2KOH → K2HPO4 + 2H2O.
В ходе этой реакции только два атома водорода замещаются на атомы калия, иначе, в реакцию вступают два иона Н+ (кислота проявляет основность 2). Тогда по определению эквивалентом H3PO4 будет являться условная частица 1/2H3PO4, т. к. если одна молекула H3PO4 предоставляет два иона Н+, то один ион Н+ дает половина молекулы H3PO4.
С другой стороны, на реакцию с одной молекулой ортофосфорной кислотой щелочь отдает два иона ОН–, следовательно, один ион ОН– потребуется на взаимодействие с 1/2 молекулы кислоты. Эквивалентом кислоты является условная частица 1/2Н3РО4, а эквивалентом щелочи частица КОН.
(1/2) H3PO4, (1)КОН, …(1/zB) B
Параметр zВ − эквивалентное число, показывающее, какое число эквивалентов вещества B условно «содержится» в одной формульной единице этого вещества (следовательно, zВ всегда больше или равно 1).
Эквивалентное число может быть приписано веществу только тогда, когда оно участвует в конкретной химической реакции, причем для одних веществ значение zВ меняется от реакции к реакции, а для других – остается постоянным.
Число, показывающее, какая часть молекулы или другой частицы вещества соответствует эквиваленту, называется фактором эквивалентности (fЭ). Фактор эквивалентности – это безразмерная величина, которая меньше либо равна 1.
Фактор эквивалентности равен обратному значению эквивалентного числа:
fЭ(В) = 1/zВ(В). (1.6)
Например, между H3PO4 и КОН также могут происходить следующие реакции. При этом кислота будет иметь разные значения фактора эквивалентности:
H3PO4 + 3KOH → K3PO4 + 3H2O fЭ(H3PO4) = 1/3
H3PO4 + KOH → KН2PO4 + H2O fЭ(H3PO4) = 1.
Таким образом, сочетая фактор эквивалентности и формульную единицу вещества, можно составить формулу эквивалента какой-либо частицы, где фактор эквивалентности записывается как химический коэффициент перед формулой частицы:
Эквивалент ≡ fЭ формульная единица вещества. (1.7)
Молярная масса эквивалента вещества В (МэB) (эквивалентная масса) в конкретной реакции всегда в zB раз меньше молярной массы этого вещества:
Мэ(B) = M(B)/zB = fЭ(В) · M(B), (1.8)
Единица эквивалентной массы – г/моль.
Эквивалентное количество вещества, пэ(B) − количество вещества в молях, в котором частицами являются эквиваленты.
Для некоторого вещества В в конкретной реакции между эквивалентным количеством вещества (пэ(B)) и формульным количеством вещества существует простая зависимость:
пэ (B) = zB · п(В) = п(В)/fЭ(В). (1.9)
Так, если в некоторой реакции эквивалентное число дихромата калия равно шести 6, то формульному количеству этого вещества, равному один моль, соответствует эквивалентное количество вещества шесть 6 моль. Другими словами, в реакции участвует число Авогадро NА формульных единиц K2Cr2O7, которым отвечает число 6NА эквивалентов дихромата калия.
Для газообразного вещества В его эквивалентный объем определяется так:
Vэ(В) =VМ / zВ = VМ· fЭ(В). (1.10)
Единица эквивалентного объема − л/моль.
Так, если в некоторой реакции fЭ(Сl2) = 1/2, то эквивалентный объем (н. у.) газообразного дихлора равен:
Vэ(Cl2) = VM ⋅f(Cl2) =22,4/2 = 11,2 л/моль.
Значения массы некоторого вещества В и объема некоторого газа В при известном значении пeq(B) определяют по выражениям:
т(B) = пэ(B) · Мэq(B) и V(B) =пэ(B) · Vэ(B). (1.11)
Следует учитывать, что эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно вступает. Эквивалент элемента также может быть различным в зависимости от вида соединения, в состав которого он входит. Эквивалентом может являться как сама молекула или какая-либо другая формульная единица вещества, так и ее часть.
Формулы расчета фактора эквивалентности приведены в таблице 1.1.
Молярная масса эквивалента сложного вещества обладает свойством аддитивности и равна сумме молярных масс, эквивалентных его составляющих частей:
Mэ(AxBy) = Mэ(A) + Mэ(B). (1.12)
Таблица 1.1 – Формулы расчета фактора эквивалентности
Частица | Фактор эквивалентности | Примеры |
Элемент | fЭ(В) = 1/В(Э), где В(Э) – валентность элемента | Фактор эквивалентности хрома в оксиде хрома (III) |
Простое вещество | fЭ(В) = 1/n(Э)·В(Э), где n(Э) – число атомов элемента (индекс в химической формуле); В(Э) – валентность элемента | fЭ(H2) = 1/(2Ч1) = 1/2; fЭ(O2) = 1/(2Ч2) = 1/4; fЭ(Cl2) = 1/(2Ч1) = 1/2; fЭ(O3) = 1/(3Ч2) = 1/6 |
Оксид | fЭ(В) = 1/n(Э)·В(Э), где n(Э) – число атомов элемента (индекс в химической формуле оксида); В(Э) – валентность элемента | fЭ(Cr2O3) = 1/(2Ч3) = 1/6; fЭ(CrO) = 1/(1Ч2) = 1/2; fЭ(H2O) = 1/(2Ч1) = 1/2; fЭ(P2O5) = 1/(2Ч5) = 1/10 |
Кислота | fЭ(В) = 1/n(Н+), где n(H+) – число отданных в ходе реакции ионов водорода (основность кислоты) | fЭ(H2SO4) = 1/1 = 1 (основность равна 1) или fЭ(H2SO4) = 1/2 (основность равна 2) |
Основание | fЭ(В) = 1/n(OН-), где n(ОH–) – число отданных в ходе реакции гидроксид-ионов (кислотность основания) | fЭ(Cu(OH)2) = 1/1 = 1 (кислотность равна 1) или fЭ(Cu(OH)2) = 1/2 (кислотность равна 2) |
Соль | fЭ(В) = 1/n(Me)·В(Me)= 1/n(А)·В(А), где n(Ме) – число атомов металла (индекс в химической формуле соли); В(Ме) – валентность металла; n(А) – число кислотных остатков, В(А) – валентность кислотного остатка | fЭ(Cr2(SO4)3) = 1/(2Ч3) = 1/6 (расчет по металлу) или fЭ(Cr2(SO4)3) = 1/(3Ч2) = 1/6 (расчет по кислотному остатку) |
Частица в окислительно-восстановительных реакциях | fЭ(В) = 1/ где | Fe2+ + 2e - → Fe0 fЭ(Fe2+) =1/2; |
Ион | fЭ(В) = 1/z, где z – заряд иона | fЭ(SO42–) = 1/2 |
Молярная масса эквивалента сложного вещества обладает свойством аддитивности и равна сумме молярных масс, эквивалентных его составляющих частей:
Mэ(AxBy) = Mэ(A) + Mэ(B). (1.12)
Электрохимический эквивалент показывает массу вещества, которая выделяется на электроде при протекании через электролит заряда в 1 Кл.
Электрохимический эквивалент (k) вещества прямо пропорционален его химическому эквиваленту:
k =Mэ(В)/F, (1.13)
где F = 96480 Кл/моль – постоянная Фарадея.
В результате работ И. Рихтера был открыт закон эквивалентов (1793 г.): все вещества реагируют друг с другом в количествах, пропорциональных их эквивалентам.

Рисунок 1.3 −
Это означает, что эквивалентные количества всех веществ, участвующих в реакции, одинаковы. Для необратимой химической реакции
νАА + νВВ+ …= νСС + νDD + …
в соответствии с законом эквивалентов всегда будут справедливы равенства:
пэ(A) = пэ(В) = …= пэ(С) = пэ (D) = …
или ![]() =
=![]() =
=![]() =
=![]() (1.14)
(1.14)
т. е. эквивалентные количества вступивших в реакцию реагентов и образовавшихся продуктов одинаковы. Если в реакции участвуют газообразные вещества, то вместо массы и эквивалентной массы вещества подставляются объемы и эквивалентные объемы. Поэтому если эквивалентное количество одного из веществ (реагента или продукта) известно по условию задачи, то определены и эквивалентные количества всех остальных веществ, участвующих в данной реакции, а необходимость их расчета отпадает. В этом состоит преимущество проведения стехиометрических расчетов по закону эквивалентов.
1.6 Закон кратных отношений
Закон кратных отношений был открыт Д. Дальтоном в 1804 г.
Если два элемента образуют между собой несколько различных соединений, то на одну и ту же массу одного из них приходятся такие же массы другого, которые относятся между собой как простые числа.

Рисунок 1.4 − Джон Дальтон
N2O N2O3 NO2(N2O4) N2O5
Число атомов кислорода в молекулах этих соединений, приходящиеся на два атома азота, относятся между собой, как 1 : 3 : 4 : 5.
1.7 Закон Авогадро
А. Авогадро открыл в 1811 г. закон, который был назван в его честь:
В равных объемах газа при одинаковых условиях содержится одинаковое число молекул.

Рисунок 1.5 − Амедео Авогадро ди Кваренья
Количество молей вещества n(В) находят как отношение массы вещества m к его молярной массе M(В):
n(B) =![]() . (1.15)
. (1.15)
Следствия из закона Авогадро:
1. Один моль газообразного вещества при нормальных условиях занимает объем, равный 22,4 л.
2. Один моль газообразного вещества содержит одно и то же число молекул, равное 6,023·1023 (число Авогадро)
3. Зная массы или молярные массы газообразного вещества можно найти относительную плотность.
![]() , (1.16)
, (1.16)
где сА, сВ – плотность вещества А и В, г/см3;
![]() – относительная плотность вещества А по В.
– относительная плотность вещества А по В.
2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Цель работы:
− изучить основные законы химии;
− опытным путем определить эквивалентную массу металла методом вытеснения водорода;
− научиться производить стехиометрические расчеты по уравнению реакции (с применением формульных величин) и по закону эквивалентов (с применением эквивалентных величин).
2.1 Методика эксперимента
Для проведения опыта соберите прибор, изображённый на рискнке 2.1, тщательно соединяя части прибора в местах стыковки, чтобы обеспечить его герметичность (рисунок 2.1).
Уравнение химической реакции, происходящей в опыте:
Me + нНCl = MeClн + yH2↑
Взвесьте 0,2−0,3 г металла с точностью до 0,01 г. В колбу 4 (см. рисунок 2.1) налейте разбавленной (1:2) соляной кислоты столько, чтобы она при горизонтальном положении колбы не вылилась в горло колбы. Внутреннюю поверхность горла колбы вытрите полоской фильтровальной бумаги, закрепите колбу на штативе, придав ей горизонтальное положение. Поместите взвешенный металл (навеску) в горлышко колбы, соблюдая осторожность, так, чтобы он не упал в кислоту до начала опыта. Цилиндр заполните доверху водой, переверните и быстро опустите в кристаллизатор, заполненный водой наполовину. (Как перевернуть цилиндр с водой, не пролив из него воду?) Закрепите цилиндр в штативе и подведите под него газоотводную трубку от колбы. Проверить герметичность.
До начала опыта необходимо произвести замеры температуры, при которой производится опыт, записать показания барометра, давление насыщенных паров воды.
Затем осторожным постукиванием колбы перенесите металл в кислоту. По окончании реакции дайте колбе охладиться 5−6 мин. И проведите замеры объема водорода в цилиндре и высоту столба воды в цилиндре от поверхности воды в кристаллизаторе.

Рисунок 2.1 − Прибор для измерения эквивалента металла
1 − мерный цилиндр на 250 мл, 2 − лабораторный штатив, 3 − кристаллизатор, 4 − колба на 20–25 мл, 5 − газоотводная трубка
Экспериментальные данные запишите в таблицу 2.1.
Таблица 2.1 – Таблица экспериментальных данных
Измеряемые величины | Ед. изме- рения | Условные обозначения | Данные опыта |
Навеска металла | г | m | |
Температура опыта |
| t | |
Давление насыщенных паров воды (Приложение А1) | Па |
| |
Атмосферное давление | Па |
| |
Объем водорода в цилиндре | мл |
| |
Высота столба воды в цилиндре от поверхности воды в кристаллизаторе после опыта (давление столба воды) | мм. вод. ст. | h |
2.2 Обработка экспериментальных данных
Рассчитайте давление водорода, который выделился в опыте по уравнению
![]() , (2.1)
, (2.1)
где 9,81 – коэффициент пересчёта для перевода мм. вод. ст. в паскали (Па).
Приведите опытный объем водорода к нормальным условиям. С этой целью можно воспользоваться уравнением объединенного газового закона:
![]() =
= ![]() , (2.2)
, (2.2)
где ![]() ,
, ![]() ,
, ![]() - давление, объем и температура выделившегося водорода в условиях опыта;
- давление, объем и температура выделившегося водорода в условиях опыта;
![]() ,
, ![]() ,
, ![]() - давление, объем и температура водорода при н. у.
- давление, объем и температура водорода при н. у.
По закону эквивалентов рассчитайте опытную молярную массу эквивалента металла:
![]()
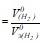 , (2.3)
, (2.3)
где ![]() − эквивалентный объем водорода при н. у., равный 11,2 ·103 мл;
− эквивалентный объем водорода при н. у., равный 11,2 ·103 мл;
![]() − масса навески металла, г.
− масса навески металла, г.
Зная опытную эквивалентную массу металла и молярную массу атома металла, рассчитайте опытный фактор эквивалентности и эквивалент металла.
![]() , (2.4)
, (2.4)
![]() . (2.5)
. (2.5)
Определите теоретическую эквивалентную массу металла:
![]() . (2.6)
. (2.6)
Рассчитайте относительную погрешность эксперимента:
![]() . (2.7)
. (2.7)
2.3 Примерный перечень вопросов для получения допуска
к лабораторной работе
1. Молярная и молекулярная масса вещества.
2. Эквивалент и молярная масса эквивалента вещества.
3. Эквивалентное число и фактор эквивалентности.
4. Формульное и эквивалентное количество вещества.
5. Эквивалентный объем.
6. Электрохимический эквивалент.
7. Как определить эквивалент сложного вещества, используя свойство аддитивности эквивалентов?
8. Расчет фактора эквивалентности.
9. Закон эквивалентов.
10. Первая помощь при несчастных случаях.
11. Методика проведения работы.
2.4 Примеры решения задач
Пример 1. Определите значение формульного количества вещества (моль) в оксиде хрома(III), затраченном на получение 21,4 г хромита (III) натрия по реакции
Cr2O3 + Na2CO3 =2NaCrO2 + CO2 .
Рассчитайте также объем (л, н. у.) выделившегося газа.
Решение
Дано: т (NaCrO2) = 21,4 г М(NaCrO2) =106,98 г/моль VМ = 22,4 л/моль Найти: п(Cr2O3) V(СО2) | n 0,2 моль Cr2O3 + Na2CO3 = 2NaCrO2 + CO2 1 моль 2 моль 1 моль Находим формульное количество хромита (III) натрия: n(NaCrO2) = 21,4/106,9 = 0,2 моль. Находим формульное количество оксида хрома (III): п(Cr2O3) = п(NaCrO2) н(Cr2O3) / н(NaCrO2) = 0,2 · 1 / 2 = 0,1 моль. Находим объем углекислого газа: V(CO2) = VМ · п(CO2) = VM · п(Cr2O3) · н(CO2) / н(Cr2O3) = 22,4 · 0,1 · 1 / 1 = = 2,24 л. |
Ответ. В данной реакции участвует 0,1 моль Cr2O3 и образуется 2,24 л СО2. |
Пример 2. Рассчитайте объем (мл) воды, необходимый для проведения реакции
Al4C3 + 12H2O = 4Al(OH)3 + 3CH4 ,
если имеется 99,85 г трикарбида тетраалюминия. Плотность воды принять равной 0,9982 г/мл
Решение
Дано: т(Al4C3)= 100 г с(H2O) = 1 г/мл М(H2O) = 18 г/моль М(Al4C3)= 144 г/моль Найти: V(H2O) | 0,69 моль n Al4C3 + 12H2O = 4Al(OH)3 + 3CH4 1 моль 12 моль Находим формульное количество Al4C3: n(Al4C3) = 100/144=0,69 моль. Находим формульное количество воды: п (H2O)= п(Al4C3)· н(H2O) /н(Al4C3) = = 0,69·12/1 = 8,28 моль. Рассчитываем объем воды: V(H2O) = m(H2O) / с( H2O) = = п (H2O) · М(H2O) / с( H2O)= = 8,28 · 18,02 / 0,9982 = = 149 мл. |
Ответ. Для проведения данной реакции надо взять 149 мл Н2О. |
Пример 3. Из 3,85 г нитрата металла получено 1,60 г его гидроксида. Вычислите молярную массу эквивалента металла Мeq(Ме).
Решение
При решении задачи следует иметь в виду: а) молярная масса эквивалента гидроксида равна сумме молярных масс эквивалентов металла и гидроксильной группы; б) молярная масса эквивалента соли равна сумме молярных масс эквивалентов металла и кислотного остатка. Вообще молярная масса эквивалента химического соединения равна сумме молярных масс эквивалентов составляющих его частей.
Учитывая сказанное, подставляем соответствующие данные в уравнение (1.14):
![]()
![]() .
.
Получаем Мэ(Ме)=15 г/моль.
Ответ. Молярная масса эквивалента металла 15 г/моль.
Пример 4. В какой массе Ca(OH)2 содержится такое же количество эквивалентов, сколько в 312 г Al(OH)3?
Решение
Молярная масса эквивалента равна Мэ(Al(OH)3) = М(Al(OH)3)/3 = 78/3 = 26 г/моль. Следовательно, в 312 г Al(OH)3 содержится 312/26 = 12 моль эквивалентов. Молярная масса эквивалента Ca(OH)2 равна Мэ(Са(OH)2) = М(Са(OH)2)/2 = 37 г/моль. Отсюда 12 молей эквивалентов составляют 37 г/моль · 12 моль = 444 г.
Ответ. В 444 г Ca(OH)2.
Пример 5. Определите значение эквивалентного количества вещества (моль) для окислителя в реакции между перманганатом калия и иодидом калия в кислотной среде (Н2SO4), если в реакцию вступило 0,075 моль KI. Рассчитайте также формульное количество вещества (моль) в образовавшемся диоде I2.
Решение
Дано: n(KI)= 0,075 моль f(KI) = 1 f(I2) =1/ 2 Найти: пэ(KMnO4) п(I2) | MnO4- + 8H+ + 5e - = Mn2+ + 4H2O 2I - - 2e - = I2 По закону эквивалентов количество эквивалентов окислителя равно количеству эквивалентов восстановителя. По уравнению (1.9) рассчитываем эквивалентное количество окислителя: пэ(KMnO4) = пэ(KI) = п(KI)/ f(KI) = = 0,075/1 = 0,075 моль. Находим формульное количество диода: п(I2) = пэ(I2)· f(I2) = пэ(KI) ·f (I2)= = 0,038моль. |
Ответ. В данной реакции участвует 0,075 моль KMnO4 (экв.) и образуется 0,038 моль I2. |
Пример 6. Рассчитайте массу (г) алюминия, вступившего в реакцию с серной кислотой (разб.), если собрано 10,24 л газа (н. у.). В решении используйте закон эквивалентов.
Решение
Дано: V(H2) = 10,24 л М(Al) = 27 г/моль VМ = 22,4 л/моль f(H2) = 1/2 т(Al) = ? | Al – 3e - = Al3+ 2H+ + 2e - = H2 По закону эквивалентов пeq(Al) = пeq(H2). Массу алюминия можно рассчитать по уравнению (1.11): т(Al) = пэ(Al) · Мэ(Al) = =пэ(H2) · Мэ(Аl). Рассчитываем количество эквивалентов водорода: пэ(H2) = V(H2) / Vэ(H2) = 10,24/{1/2·22,4}=0,91 моль. Рассчитываем молярную массу эквивалента алюминия: Мэ(Al) = f(Al)·M(Al) = 1/3×27 = 9 г/моль. Находим массу алюминия: т(Al) = 0,91·9 = 8,2 г. |
Ответ. В данную реакцию вступило 8,2 г Аl. |
2.5 Задачи для самостоятельного решения
1. В стратосфере на высоте 20−30 км находится слой озона O3, защищающий Землю от мощного ультрафиолетового излучения Солнца. Если бы не «озоновый экран» в атмосфере, то фотоны с большой энергией достигли бы поверхности Земли и уничтожили на ней все живое. Подсчитано, что в среднем на каждого жителя Москвы в воздушном пространстве над городом (вплоть до верхней границы стратосферы) приходится по 150 моль озона. Сколько молекул O3 и какая масса озона приходится в среднем на одного москвича? Ответ: N(O3) = 9,03 . 1025, m(O3) = 7,2 кг.
2. В школьном химическом кабинете пролили на пол немного соляной кислоты, и к концу урока она полностью испарилась. Хотя хлороводород сильно токсичен и при вдыхании оказывает раздражающее действие, ученики не почувствовали никакого постороннего запаха. Много ли молекул HCl оказалось в воздухе, если масса хлороводорода, перешедшего в газообразное состояние, равна 1 г? Ответ: N(HCl) = 1,65 . 1022.
3. Масса 200 см3 ацетилена при нормальных условиях равна 0,232 г. Определите молярную массу ацетилена. Ответ: 26,0 г/моль.
4. При производстве серы автоклавным методом неизбежно выделяется около 3 кг сероводорода на каждую тонну получаемой серы. Сероводород − чрезвычайно ядовитый газ, вызывающий головокружение, тошноту и рвоту, а при вдыхании в большом количестве - поражение мышцы сердца и судороги, вплоть до смертельного исхода. Какой объем сероводорода (при н. у.) выделится при получении 125 т серы на химзаводе? Ответ: 247 м3 H2S.
5. Грузовой автомобиль загрязняет воздух вредными выбросами: на каждые 10 км пути с его выхлопными газами в атмосферу попадает 700 г монооксида углерода и 70 г монооксида азота. Каким будет объем (при н. у.) этих вредных веществ при перевозке груза на расстояние 250 км четырьмя автомобилями? Ответ: 56 м3 CO и 5,2 м3 NO.
6. Природный газ (метан CH4) не имеет никакого запаха. Чтобы легче обнаруживать его утечку из бытовых нагревательных приборов и газопроводов, к нему добавляют немного фосфина PH3, запах которого ("запах газа") ощущается, если в 10 м3 природного газа находится всего 0,01 мл фосфина. Рассчитайте число молекул фосфина в 0,01 мл (н. у.) этого газа. Ответ: 2,69 . 1017 молекул PH3.
7. Оконные стекла и дверцы вытяжных шкафов в химической лаборатории часто бывают покрыты белым налетом, состоящим из кристаллов хлорида аммония. Причина этого явления - постоянное присутствие в воздухе лабораторий аммиака и хлороводорода. Рассчитайте количество и объем (при н. у.) этих газов, если образовалось 5 г хлорида аммония. Ответ: 0,093 моль (2,09 л) NH3 и 0,093 моль (2,09 л) HCl.
8. Природный газ содержит главным образом метан CH4, но в нем присутствуют и примеси, например, ядовитый сероводород H2S − до 50 г на 1 кг метана. Чтобы удалить примесь сероводорода, можно провести его окисление перманганатом калия в кислой среде до серы. Рассчитайте количество серы, которую можно таким образом выделить из 1 т природного газа. Определите также, какая масса серной кислоты может быть получена, если всю выделенную серу направить в цех производства H2SO4. Ответ: 50 кг серы и 153 кг H2SO4.
9. Толщи известняка на земной поверхности и под землей медленно "размываются" под действием почвенных вод, где растворен диоксид углерода. Какую массу карбоната кальция CaCO3 может перевести в растворимый гидрокарбонат кальция состава Ca(HCO3)2 вода, в которой растворено 10 моль CO2? Практический выход для реакции химического растворения считайте равным 90 %. Ответ: 900 г CaCO3.
10. Предельно допустимая среднесуточная концентрация монооксида углерода в воздухе составляет 3,0 мг/м3. Простейший газоанализатор, позволяющий определить наличие в воздухе ядовитой примеси СО, содержит белый порошок оксида иода(V), нанесенный на пемзу и помещенный в стеклянную трубочку. При взаимодействии I2O5 c CO идет окислительно-восстановительная реакция с выделением иода, который окрашивает содержимое трубочки в черный цвет. Какое количество монооксида углерода вызовет выделение 0,1 г иода в трубке газоанализатора? Какой объем воздуха (при н. у.), содержащего 3,0 мг/м3 CO, надо будет пропустить через трубку, чтобы в ней выделилось 0,1 г иода? Ответ: 0,0020 моль CO; 18 м3 воздуха.
11. Коррозия железа на воздухе в присутствии большого количества воды приводит к образованию метагидроксида железа состава FeO(OH). Рассчитайте, какая масса железа подверглась коррозии, если количество полученного в результате этого процесса FeO(OH) составило 11,5 моль. Определите также объем (при н. у.) кислорода, участвовавшего в реакции. Ответ: 644 г железа,193,2 л O2.
12. При выпечке печенья в качестве разрыхлителя теста используют пищевую соду (гидрокарбонат натрия) с добавкой уксусной кислоты. Эта смесь при нагревании разлагается, выделяя углекислый газ. Рассчитайте объем (при н. у.) CO2, который выделится при использовании 1 чайной ложки (5 г) NaHCO3 и избытка CH3COOH.
Ответ: 1,33 л CO2.
13. Взаимодействие минерала магнетита (оксида железа состава Fe3O4) с монооксидом углерода CO приводит к получению железа и выделению углекислого газа CO2. В результате реакции было выделено 65,3 кг железа. Рассчитайте практический выход железа, если масса исходного магнетита составляла 110 кг. Определите объем (при н. у.) полученного газа. Ответ: Практический выход 82%.
14. Жженую известь, применяемую в строительстве, получают прокаливанием известняка. Определите массовую долю основного вещества (карбоната кальция) в известняке, если прокаливание его образца массой 5,0 кг привело к выделению 1,0 м3 углекислого газа (при н. у.). Ответ: 0,893, или 89,3 % карбоната кальция в известняке.
15. Карл-Вильгельм Шееле в 1774 году получил кислород термическим разложением перманганата калия KMnO4. Помимо кислорода, при этом получаются оксид марганца(IV) и манганат калия K2MnO4. Кислород, выделенный при разложении 33,5 г перманганата калия, использовали для сжигания серы и при этом получили 2,1 л (при н. у.) диоксида серы SO2. Определите практический выход кислорода при разложении перманганата калия. Рассчитайте массу серы, затраченной на сжигание. Ответ: Практический выход 88,4 %, масса серы 3,0 г.
16. Разбитый термометр, в котором было 20,5 г ртути, выбросили в пруд. Прошло 4 месяца, и вследствие сложных биохимических процессов около 5 % этого опасного металла перешло в раствор в виде солей ртути(II) типа нитрата ртути(II) Hg(NO3)2. Определите количество и массу катионов ртути(II) в пруду. Определите, представляет ли опасность прудовая вода, если объем воды в пруду 80 м3, а санитарная норма предусматривает содержание не более чем 0,01 г Hg2+ в 1 м3. Ответ: 0,051 моль (1,025 г) Hg2+; вода опасна для здоровья, так как в ней содержится 0,013 г/м3 Hg2+ (выше нормы).
17. В какой массе NaOH содержится такое же количество эквивалентов, сколько в 140 г КОН? Ответ: 100 г.
18. Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите молярную массу эквивалента этого металла. Ответ: 32,5 г/моль.
19. Из 1,3 г гидроксида металла получается 2,85 г его сульфата. Вычислите молярную массу эквивалента этого металла. Ответ: 9 г/моль.
21. Чему равен при н. у. эквивалентный объем водорода? Вычислите молярную массу эквивалента металла, если на восстановление 1,017 г его оксида израсходовалось 0,28 дм3 водорода (н. у.). Ответ: 32,68 г/моль.
22. В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите молярные массы эквивалентов металла и его оксида. Чему равна молярная и атомная массы этого металла? Ответ: 23 г/моль.
23. Из 3,31 г нитрата металла получается 2,78 г его хлорида. Вычислите молярную массу эквивалента этого металла. Ответ: 103,6 г/моль.
24. При окислении 16,74 г двухвалентного металла образовалось 21,54 г оксида. Вычислите молярные массы эквивалентов металла и его оксида. Чему равна молярная и атомная массы металла? Ответ: 55,8 г/моль.
25. При взаимодействии 3,24 г трехвалентного металла с кислотой выделяется 4,03 л водорода (н. у.). Вычислите молярную, атомную массы и молярную массу эквивалента металла. Ответ: 9 г/моль.
26. Исходя из молярной массы углерода и воды, определите абсолютную массу атома углерода и молекулы воды в граммах.
Ответ: 2,0 · 10-23 г; 3,0 · 10-23 г.
27. На нейтрализацию 9,797 г ортофосфорной кислоты израсходовано 7,998 г NaOH. Вычислите число эквивалентности, молярную массу эквивалента и основность H3PO4 в этой реакции. На основании расчета напишите уравнение реакции. Ответ: 0,5 моль; 49 г/моль; 2.
28. На нейтрализацию 0,943 г фосфористой кислоты H3PO4 израсходовано 1,291 г КОН. Вычислите число эквивалентности, молярную массу эквивалента и основность кислоты. На основании расчета напишите уравнение реакции. Ответ: 0,5 моль; 41 г/моль; 2.
29. При сгорании 5,00 г металла образуется 9,44 г оксида металла. Определить молярную массу эквивалента металла. Ответ: 9,01 г/моль.
30. Вычислите молярную массу двухвалентного металла и определите, какой это металл, если 8,34 г металла окисляются 0,680 л кислорода (н. у.). Ответ: 137,4; Ва.
31. 1,00 г некоторого металла соединяется с 8,89 г брома и с 1,78 г серы. Найдите молярные массы эквивалентов брома и металла, зная, что молярная масса эквивалента серы равна 16,0 г/моль. Ответ: 79,9 г/моль; 9,0 г/моль.
32. Для растворения 16,8 г металла потребовалось 14,7 г серной кислоты. Определите молярную массу эквивалента металла и объем выделившегося водорода (н. у.). Ответ: 56,0 г/моль; 3,36 л.
33. 1,60 г кальция и 2,61 г цинка вытесняют из кислоты одинаковые количества водорода. Вычислите молярную массу эквивалента цинка, зная, что молярная масса эквивалента кальция равна 20,0 г/моль. Ответ: 32,6 г/моль.
34. На нейтрализацию 2,45 г кислоты идет 2,00 г гидроксида натрия. Определите молярную массу эквивалента кислоты.
Ответ: 49,0 г/моль.
35. 0,376 г алюминия при взаимодействии с кислотой вытеснили 0,468 л водорода (н. у.). Определите эквивалентный объем водорода, зная, что молярная масса эквивалента алюминия равна 8,99 г/моль.
Ответ: 11,2 л/моль.
36. Проводят следующую реакцию в водном растворе:
KMnO4 + H2SO4 + KNO2 = KNO3 + MnSO4 + K2SO4 + H2O
Определите значения эквивалентного количества вещества (моль) и молярные массы эквивалентов (г/моль) для прореагировавшего восстановителя, если известно формульное количество вступившего в реакцию окислителя
Вариант | а | б | в | г | д | е |
пОк, моль | 0,13 | 0,55 | 0,27 | 0,09 | 0,31 | 0,67 |
37. Рассчитайте эквивалентные объемы (л/моль, н. у.) газообразных веществ в следующих обменных реакциях (предварительно подберите коэффициенты):
а) FeS + HCl → FeCl2 + H2S(г)
б) Ba(OH)2 + CO2(г) → Ba(HCO3)2
в) NH4Cl + LiOH → LiCl + NH3(г) + H2О
г) H2SO4 + NaCl → NaHSO4 + HCl(г)
д) Na2SO3 + H2SO4 → Na2SO4 + SO2(г) + H2O
е) CaF2 + H2SO4 → CaSO4 + HF(г)
Рассчитайте также эквивалентное количество вещества (моль) в 2,8 л (н. у.) каждого газа.
38. Определите массу (г) серной кислоты, необходимую для проведения следующих реакций:
а) осаждение сульфата свинца(II) из раствора, содержащего 0,28 моль Pb2+ (экв.);
б) нейтрализация раствора гидроксида лития, содержащего 0,14 моль ОН - (экв.), с образованием сульфата лития;
в) нейтрализация раствора, содержащего 0,07 моль Са(ОН)2 (экв.), с образованием сульфата кальция;
г) осаждение сульфата бария из раствора, содержащего 0,35 моль Ва2+ (экв.);
д) полная реакция обмена с 0,21 моль K2CO3 (экв.) в растворе;
е) полная реакция обмена с 0,42 моль NaHCO3 (экв.) в растворе.
Согласно заданному варианту выберите задачи по таблице 2.2 и предоставьте их решение преподавателю.
Таблица 2.2 – Варианты задач для самостоятельного решения
Вариант | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
Номера задач | 1, 38а, 17 | 2, 38б,18 | 3,38в,19 | 4,38г, 21 | 5, 38д, 21 | 6, 38е, 22 | 7,37а,23 | 8,37б,24 | 9,37в,25 |
Вариант | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
Номера задач | 10,37г,26 | 11, 37д,27 | 12, 37е,28 | 13,36а,29 | 14,36б,30 | 15,36в,31 | 16,36г,32 | 36д,33,34 | 36е,35,17 |
2.6 Тесты
1. Эквивалент перманганата калия, если MnO4- восстанавливается до Mn+2, равен _____моль.
а) 1/2;
б) 1/3;
в) 1/4;
г) 1/5.
2. Определите фактор эквивалентности и молярную массу эквивалента олова в реакциях:
Sn4++2е→Sn2+
Sn4+ + 4OH-→Sn (OH)4
a) f = 1/4 , Mэ(Sn4+) = 29,7 г/моль. экв,
f = 1/2, Mэ(Sn4+) = 59,3 г/моль. экв;
б) f = 1/2, Mэ(Sn4+) = 59,3 г/моль. экв,
f = 1/4, Mэ(Sn4+) = 29,7 г/моль. экв;
в) f = 1/2, Mэ(Sn4+) = 59,3 г/моль. экв,
f = 1, Mэ(Sn4+) = 118,7 г/моль. экв;
г) f = 1/4, Mэ(Sn4+) = 29,7 г/моль. экв,
f = 1/4, Mэ(Sn4+) = 59,3 г/моль. экв;
д) f = 1/2, Mэ(Sn4+) =59,3 г/моль. экв,
f = 1/2, Mэ(Sn4+) =29,7 г/моль. экв.
3. На нейтрализацию 9,797 г ортофосфорной кислоты израсходовано 7,998 r NaOH. Вычислите количество вещества эквивалента, молярную массу эквивалента и основность Н3РО4 в этой реакции:
а) 0,4, 17 г/моль. экв, 1;
б) 0,5, 49 г/моль. экв, 2;
в) 1, 27 г/моль. экв, 2;
г) 3, 32 г/моль. экв, 2.
4. Чему равен фактор эквивалентности и молярная масса эквивалентов ионов Fe3+ в реакциях его восстановления?
Fe3+ + e = Fe2+
Fe3+ + 3e = Fe0
а) f = 1; Мэ = 55,85 г/моль. экв,
f = 1/3; Мэ = 18,62 г/моль. экв;
б) f = 1/3; Мэ = 18,62 г/моль. экв,
f = 1; Мэ = 55,85 г/моль. экв;
в) f = 1; Мэ = 55,85 г/моль. экв,
f = 1; Мэ = 55,85 г/моль. экв;
г) f = 1/3; Мэ = 18,62 г/моль. экв,
f = 1/3; Мэ = 18,62 г/моль. экв.
5. Определить фактор эквивалентности H3PO4 в реакциях с КОН при образовании следующих соединений: KH2PO4, K2HPO4, K3PO4
а) f = 1, 1, 1;
б) f = 1, 1/2, 1/3;
в) f = 1/3, 1/2, 1;
г) f = 1/2, 1/2, 1/2;
д) f = 1, 1/3, 1.
6. Определите процентное содержание металла в оксиде, если молярная масса эквивалента металла составляет 56,2 г/моль.
а) 90,5%;
б) 85,4%;
в) 87,5%;
г) 77,5%;
д) 67,5%.
7. Изотоны – это:
а) атомы с различным числом протонов и нейтронов, но с одинаковым числом нуклонов;
б) атомы с одинаковым числом протонов, но разным массовым числом;
в) атомы с одинаковым числом нейтронов, но разным массовым числом;
г) атомы с одинаковым числом протонов и нейтронов, но имеющие различное пространственное строение;
д) конкретное ядро с заданным массовым числом и данным зарядом:
е) общее название протона и нейтрона.
8. Закон Бойля−Мариотта можно записать с помощью выражения:
а) p/T = const;
б) v/T = const;
в) pv = const;
г) pV=(m/M)RT;
д) pV/T=p0V0/T0.
9. Дальтониды – это вещества:
а) с одинаковой молекулярной массой;
б) с разной молекулярной массой;
в) с одинаковым количественным составом;
г) с различным количественным составом.
10. Закон Авогадро и следствия из него можно записать следующими выражениями:
а) E = m·c2;
б) n = m/M(x);
в) pV=(m/M)RT;
г) V = n·VM
д) ) pv = const.
11. Закон постоянства состава был открыт:
а) ;
б) А. Авогадро;
в) ;
г) И. Рихтером;
д) Ж. Прустом.
12. Фактор эквивалентности для солей в кислотно-основных реакциях определяется по формуле
а) f = ![]()
![]() ;
;
б) f = ![]()
![]() ;
;
в) f = ![]()
![]() ;
;
г) f = ![]()
![]() ;
;
д) f = ![]()
![]() ;
;
е) f = ![]()
![]() .
.
2.7 Примерный перечень вопросов на защиту работы
1. Приведите понятия, классификацию кислот, солей, оснований и оксидов.
2. Предмет и задачи химии.
3. Атомно-молекулярное учение.
4. Стехиометрические расчеты в химии.
5. Сформулируйте законы сохранения массы, энергии и материи веществ? Всегда ли они выполняются?
6. Кем и когда был открыт закон эквивалентов? Сформулируйте закон эквивалентов. Какова математическая запись этого закона?
7. Приведите понятия моля, эквивалента, фактора эквивалентности, молярной массы эквивалента вещества, эквивалентного объема, эквивалентного количества, электрохимического эквивалента.
8. По каким формулам определяют фактор эквивалентности различных веществ? Примеры.
9. Как формулируется закон постоянства состава? Приведите первоначальную и современную формулировки этого закона. Какие вещества называют дальтонидами, а какие бертоллидами?
10. Как формулируется закон Авогадро и следствия из него?
11. Закон кратных отношений.
12. Методика проведения работы.
13. По каким уравнениям рассчитывали фактор эквивалентности и молярную массу эквивалента металла, опытную и теоретическую?
14. Какую технику безопасности необходимо соблюдать при выполнении данной лабораторной работы?
2.8 Общие методические рекомендации по подготовке и
защите лабораторной работы
Подготовка к выполнению лабораторной работы заключается в изучении теоретической части работы по учебному пособию, конспекту лекций и методическим рекомендациям.
На лабораторные занятия студент также должен подготовить предварительно бланк отчета, который выполняется в тетради и включает указания наименования и целей работы, зарисовку лабораторной установки и химической посуды, а также формы экспериментальных таблиц.
Форма контроля − проверка отчетов, индивидуальный устный опрос по контрольным вопросам для получения допуска к работе.
Выполнение лабораторных работ сопровождается записью опытных данных и наблюдаемых явлений в отчете. После проведения лабораторной работы студент обрабатывает экспериментальные данные, заполняет отчетные таблицы и пишет заключение (выводы), используя теоретическую часть методических рекомендаций и результаты полученных опытов.
Защита лабораторной работы проводится индивидуально и состоит из ответов на теоретические вопросы, выполнения тестовых заданий и решения задач.
3 ТЕХНИКА БЕЗОПАСНОСТИ
Перед началом проведения лабораторных опытов студент должен
надеть хлопчатобумажный халат, при работе с токсичными и агрессивными веществами подготовить к использованию средства индивидуальной защиты (резиновые перчатки, защитные очки, противогазы).
Опыты всегда необходимо проводить в чистой посуде. Не загромождайте свое рабочее место письменными принадлежностями и другими посторонними предметами. После опытов остатки металлов в раковину не выбрасывать, а собрать в отдельную посуду. Битую посуду, обрывки бумаги, спички выбрасывают в урну.
Не включайте без разрешения преподавателя рубильники электрических приборов. Нельзя пробовать вещества на вкус. При приливании реактивов нельзя наклоняться над отверстием сосуда во избежание попадания брызг на лицо и одежду. Нельзя наклоняться над нагреваемой жидкостью, так как ее может выбросить.
В случае пожара немедленно выключите все электронагревательные приборы. Горящие жидкости прикройте асбестом, засыпьте песком, но не заливайте водой.
При ранении стеклом удалите осколки из раны, смажьте края раны раствором йода и перевяжите бинтом.
При химическом ожоге рук или лица смойте реактив большим количеством воды, затем либо разбавленной уксусной кислотой в случае ожога щелочью, либо раствором соды в случае ожога кислотой, а затем опять водой.
При ожоге горячей жидкостью или горячим предметом обожженное место обработайте свежеприготовленным раствором перманганата калия, смажьте обожженное место мазью от ожога или вазелином. Можно присыпать ожог содой и забинтовать.
При химических ожогах глаз обильно промойте глаза водой, используя глазную ванночку, а затем обратитесь к врачу.
ПРИЛОЖЕНИЕ А
Давление насыщенного водяного пара
Таблица А1 – Давление насыщенного водяного пара
Температура oC | Давление | |
КПа | мм. рт. ст. | |
13 | 1,49 | 11,22 |
14 | 1,58 | 11,9 |
15 | 1,68 | 12,6 |
16 | 1,81 | 13,6 |
17 | 1,93 | 14,5 |
18 | 2,07 | 15,5 |
19 | 2,20 | 16,5 |
20 | 2,33 | 17,5 |
21 | 2,49 | 18,7 |
22 | 2,64 | 19,8 |
23 | 2,81 | 21,1 |
24 | 2,99 | 22,4 |
25 | 3,17 | 23,8 |
26 | 3,36 | 25,4 |
27 | 3,56 | 26,7 |
28 | 3,75 | 28,1 |
29 | 3,97 | 29,8 |
30 | 4,21 | 31.6 |
ЛИТЕРАТУРА
1. Коровин, химия / . – М.: Высшая школа, 2002. − 558 с.
2. Глинка, химия: учебное пособие для вузов / ; под. ред. . – М.: Интеграл-Пресс, 2003. – 728 с.
3. Ефимов, неорганических соединений: справочник / , , ; под ред. . – Л.: Химия, 1983. – 389 с.
4. Макрушина, . Модуль 1. Строение атома и вещества: учебное пособие для модульно-рейтинговой технологии обучения / . – Бийск: БТИ Алт ГТУ, 2007. – 2002 с.
Учебное издание
Эквивалент химических веществ
Методические рекомендации по выполнению лабораторной работы по дисциплине «Химия» для студентов специальностей 151001, 160302, 190603, 080401, 170104, 230201, 260204, 240901, 240701, 240702, 240706, 260601, 200106 всех форм обучения
Редактор …….
Корректор …..
Подписано в печать …… Формат …..
Усл. п. л. ….. Уч.-изд. л. ….
Печать — ризография, множительно-копировальный
Аппарат «RISO TR-1510»
Тираж …. экз. Заказ ….
Издательство Алтайского государственного
технического университета
656038, г. Барна
Оригинал-макет подготовлен ИИО БТИ АлтГТУ
Отпечатано в ИИО БТИ АлтГТУ
659305, 7
Федеральное агентство по образованию
Бийский технологический институт (филиал)
государственного образовательного учреждения
высшего профессионального образования
«Алтайский государственный технический университет им. »,
Эквивалент химических веществ
Методические рекомендации по выполнению лабораторной работы по дисциплине «Химия» для студентов специальностей 151001, 160302, 190603, 080401, 170104, 230201, 260204, 240901, 240701, 240702, 240706, 260601, 200106 всех форм обучения
……………………………………………………
…………………………………………………….
Зав. кафедрой……………………...…………....
Заместитель МКФ………………..……………..
Нормоконтролер………………............………...
Зав. библиотекой……………………….……….
Редактор…………………….…………………....
Зам. директора по УР……………………..………….
Бийск 2010



