Лабораторная работа №2: Определение меди в электролите латунирование дифференциально-фотометрическим методом.
Электролит латунирования содержит компоненты CuSO4 и ZnSO4 ионы меди определяют фотометрическим методом в виде аммиакатов, окрашивающих раствор в интенсивный сине-фиолетовый цвет. Ионы Zn, образующие с аммиакатом бесцветные комплексы, определению не мешают. Определение проводят в присутствии избытка NН4. В этих условиях в растворе образуются комплексы меди Cu(NН3)42+.
Ввиду относительно большого содержания меди в образце определение выполняют методом дифференциальной фотометрии.
Реактивы и оборудование: сульфат меди CuSO4∙5Н2О, аммиак NН3, раствор 5 % концентрации, Н2SO4 1 М раствор (2н), колбы мерные (50 и 100 мл), бюретка (25 мл), пипетка 10 м, фотоэлектроколориметр.
Ход работы:
1. Приготовление стандартных растворов меди и выбор светофильтра.
Точную навеску CuSO4∙ 5Н2О массой около (0,78±0,04) г количественно переносят в мерную колбу вместимостью 100 мл, растворяют в 5 мл Н2SO4 и доводят раствор до метки дистиллированной водой (раствор 1). Из раствора 1 готовят 6 стандартных растворов, содержащих от 5-30 г меди в 50 мл. Для этого используя бюретку, в мерные колбы вместимостью 50 мл переносят от 2,5 до 15 мл раствора 1. Добавляют в каждую колбу по 2 мл раствора NН4 и объём растворов доводят до метки дистиллированной водой. Оптическую плотность каждого раствора измеряют не ранее чем через 10 мин в кювете с толщиной слоя 2 см.
Первым фотометрируют раствор, имеющий наиболее интенсивную окраску, изменения его оптической плотности относительно воды в диапазоне длин волн 400-750 нм и строят кривую светопоглощения в координатах оптическая плотность-длина волны. Выбирают светофильтр, при котором наблюдается максимальное светопоглощение раствора. Этот светофильтр используется для дальнейшей работы.
2.Построение градуировочного графика.
С выбранным светофильтром (п.1) поочередно фотометрируют растворы аммиакатов меди, полученные по п.1, относительно стандартного раствора, содержащего 5 мг Cu в 50 мл. По результатам измерений строят график (относительная плотность-концентрация меди).
3.Анализ исследуемого раствора.
Анализируемый раствор, состоящий из смеси CuSO4 и ZnSO4 , помещают в мерную колбу, объемом 50 мл, добавляют 2 мл раствора NН3, доводят до метки водой и через 10 минут фотометрируют при выбранном по п.1светофильтре относительно стандартного раствора меди, содержащего 5 мг Cu в 50 мл. Измерения повторяют несколько раз и, используя среднее значение оптической плотности меди по градуировочному графику находят концентрацию меди в пробе анализируемого раствора. Рассчитывают массу меди в анализируемом растворе, учитывая произведенные разбавления.
Таблица 1.
№ | Сульфосалициловая к-та 10% | Железо(стандарт) | NH4OH – 10 % | T (%) | D |
1 | 10 мл | 2,5 мл | 10 мл | 26 | 0,57 |
2 | 10 мл | 5 мл | 10 мл | 27 | 0,55 |
3 | 10 мл | 7,5 мл | 10 мл | 28 | 0,54 |
4 | 10 мл | 10 мл | 10 мл | 29 | 0,53 |
5 | 10 мл | 12,5 мл | 10 мл | 31 | 0,51 |
6 | 10 мл | 15 мл | 10 мл | 32 | 0,50 |
7 | Х мл | 10 мл | 15 мл | 30 | 0,52 |
Обработка результатов:
Найдем титр по меди![]() г/мл
г/мл
![]()
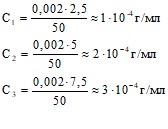
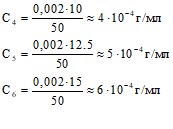
График зависимости T от С
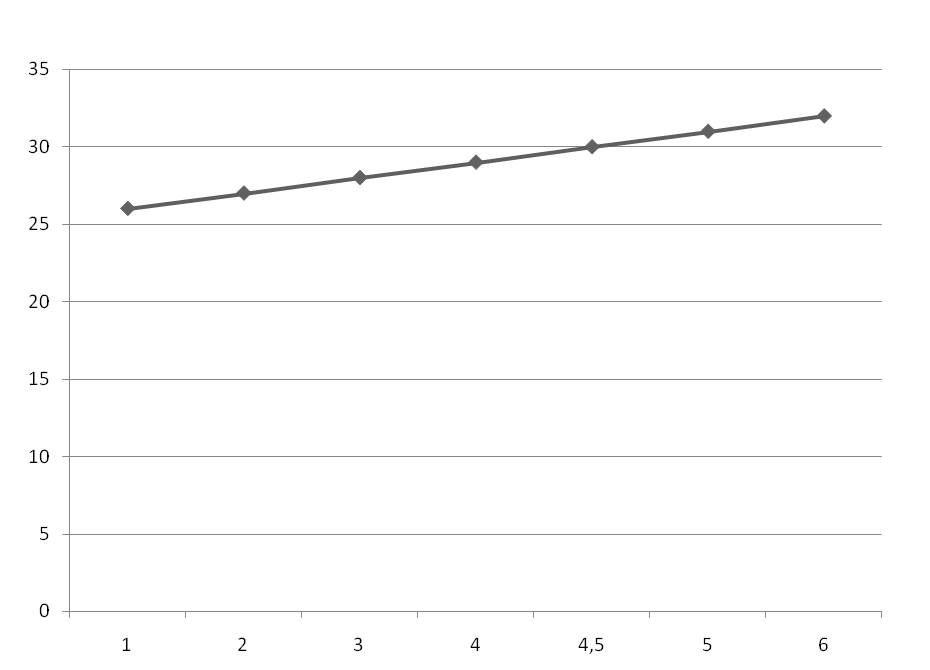
График зависимости D от С
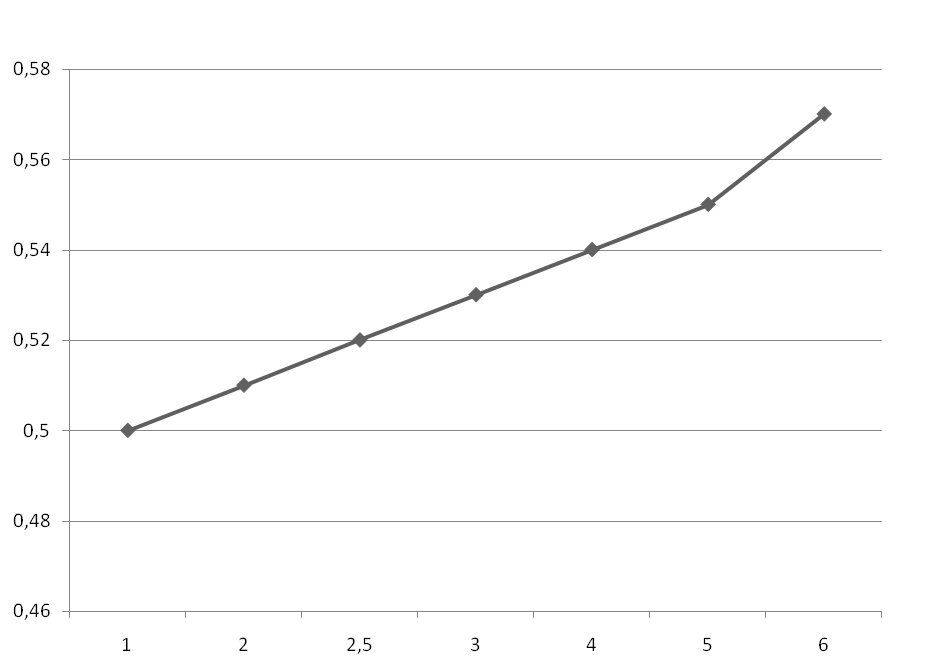
График зависимости D от T
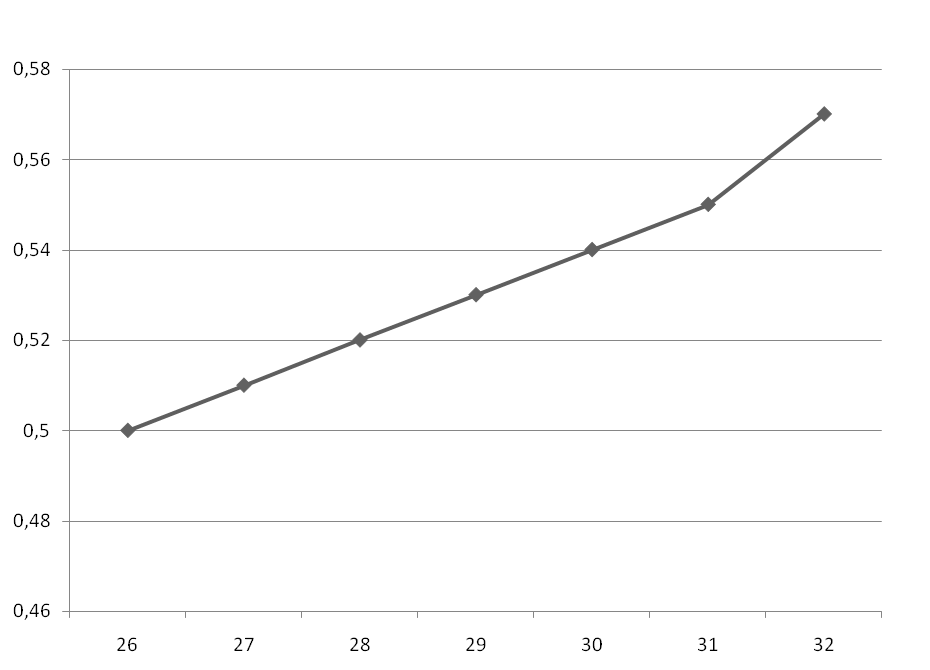
Вывод: произвели необходимые расчеты, построили графики зависимостей и, используя метод градуировочного графика, количественно определили содержание меди в электролите.
Также вычислили объем анализируемой пробы “X”:
![]()
![]()




