Цель:
Изучив данный элемент. Вы сможете:
- правильно проверить работу аккумулятора (свинцового типа).
Эти знания должны быть основными для каждого водителя и для каждого человека, занимающегося автоделом. Только соответствующая осведомленность о том, что происходит, когда аккумуляторная батарея становится разряженной, или что случается, когда электролит разбавлен или имеет повышенную концентрацию кислоты и т. д., может изменить существующее в настоящее время положение во многих странах, где автомобильные аккумуляторные батареи имеют срок службы только полтора года или меньше. При регулярном обслуживании срок службы аккумуляторной батареи может удвоиться, но при этом очень важно следовать советам, изложенным в этом Учебном элементе.
Оборудование, материалы и вспомогательные средства:
- два литра электролита;
- два литра кислоты;
- три литра дистиллированной воды;
- один пластмассовый контейнер, размером около 250х200х150 мм;
- одна 12-ти вольтовая лампочка на 18 ватт с патроном;
- одна отвертка с 3 мм наконечником;
- четыре зажима - «крокодильчика»;
- около четырех метров однофазного провода диаметром около 0,8 мм;
- два медных штырька в качестве электродов;
- одна 12-ти вольтовая автомобильная аккумуляторная батарея, полностью заряженная;
- несколько старых аккумуляторных батарей в различной плотностью электролитов;
- один денсиметр;
- один термометр;
- одну шкалу в диапазоне от 0° до 75°С;
- одну модель аккумуляторной батареи (секционную);
- одну аккумуляторную батарею с сульфатированными пластинами, а также несколько отдельных сульфатированных пластин, если возможно;
- одно зарядное устройство аккумуляторных батарей.
Сопутствующие учебные элементы и пособия:
- «Устройство аккумуляторной батареи».
Замечание: Очень важно, чтобы обучаемый уже освоил вышеприведенный Учебный элемент до начала изучения данного Учебного элемента.
1. Закончив изучение Учебного элемента «Устройство аккумуляторной батареи». Вы хорошо представляете, что такое гальванический эффект и как работает первичный элемент батареи.
2. Автомобильная аккумуляторная батарея - это уже вторичное устройство, и давайте называть его аккумулятором, это означает, что он не только выдает ток, пока не разрядится, и затем заменяется, как первичный элемент батареи;
аккумулятор способен поглощать ток и выдавать его опять, когда требуется.
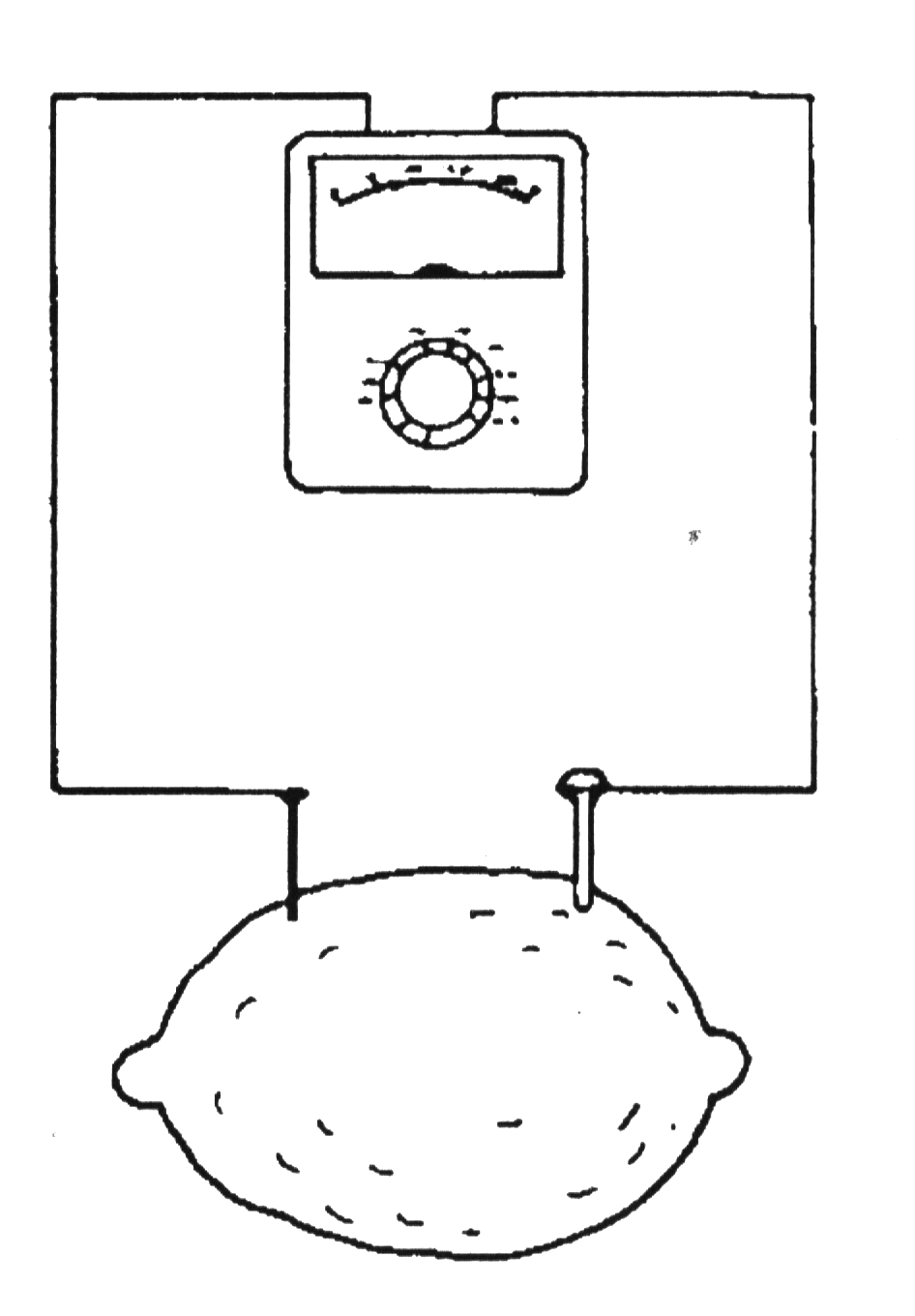
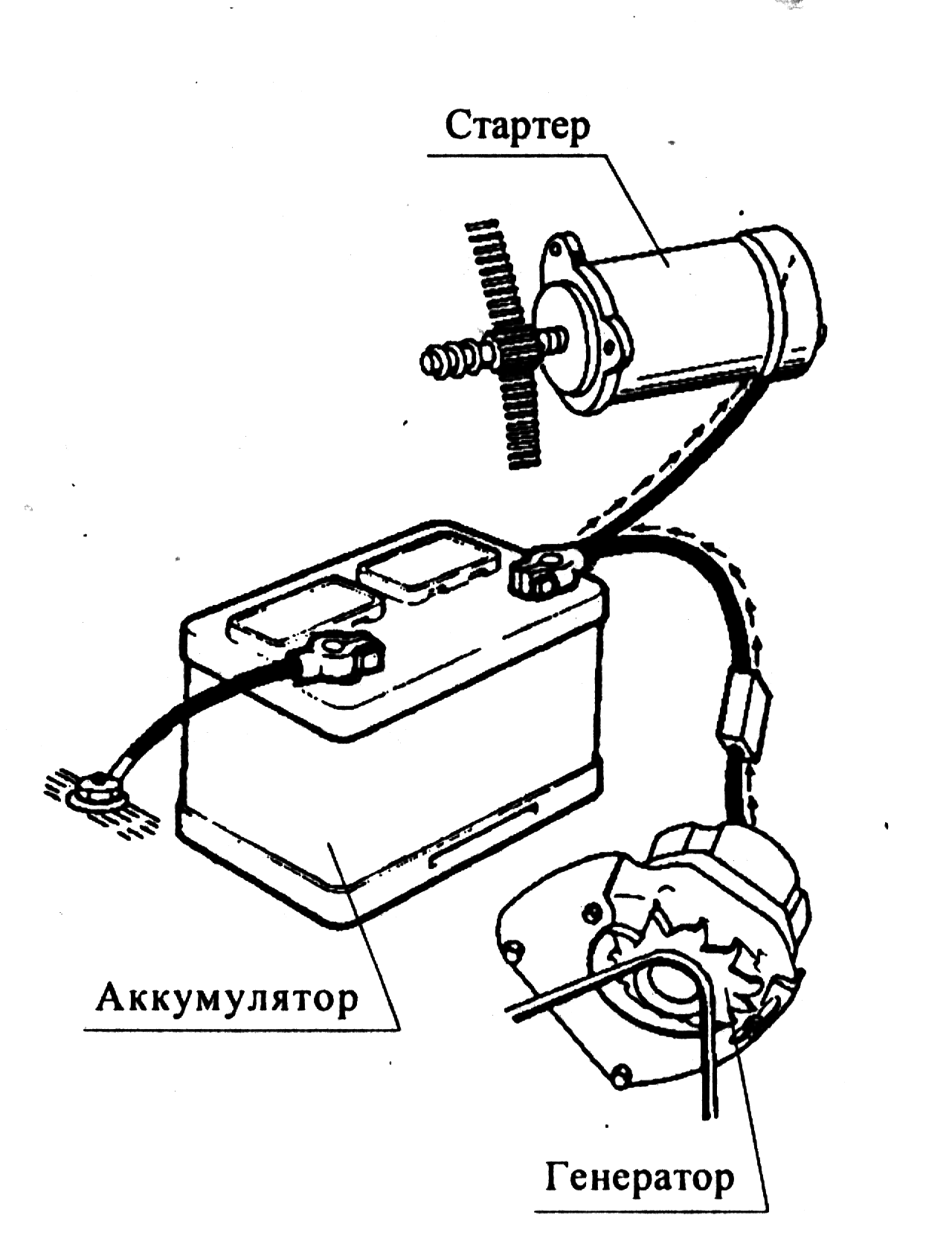
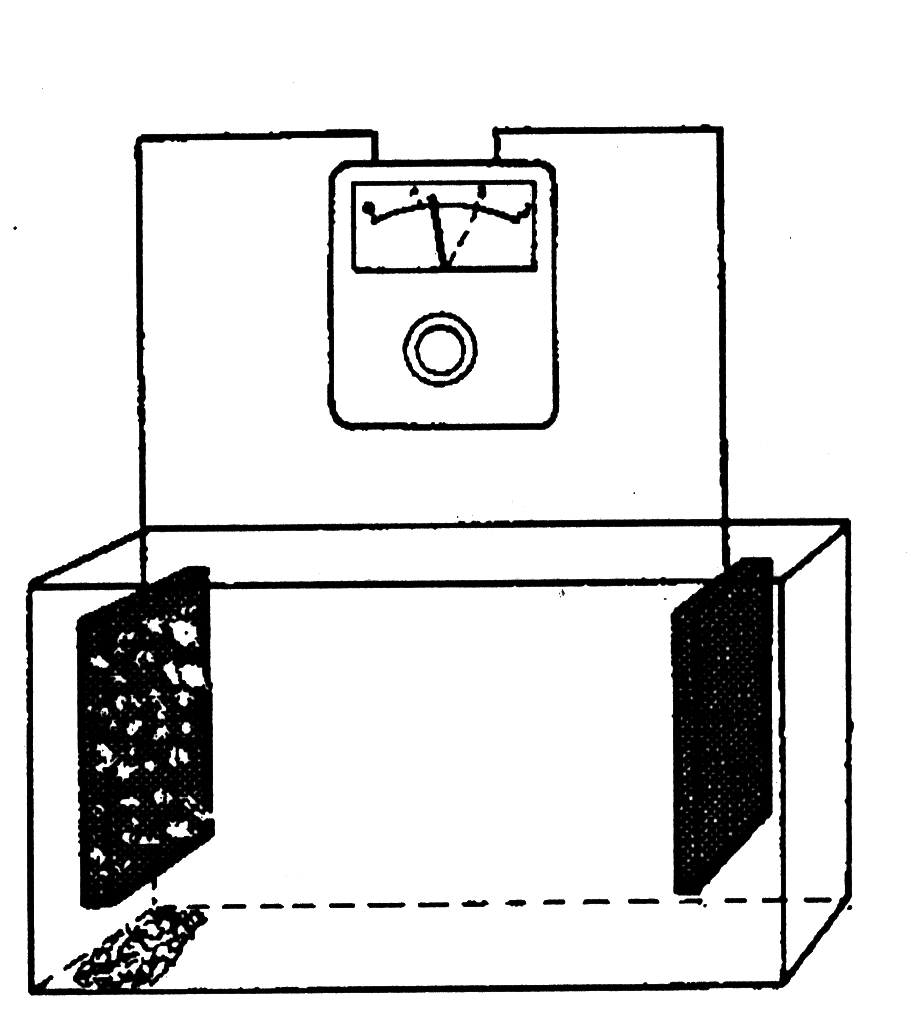
3. Проведите следующий опыт. Возьмите контейнер из пластика размером около 250х200 мм и высотой около 150 мм и заполните его наполовину дистиллированной водой.
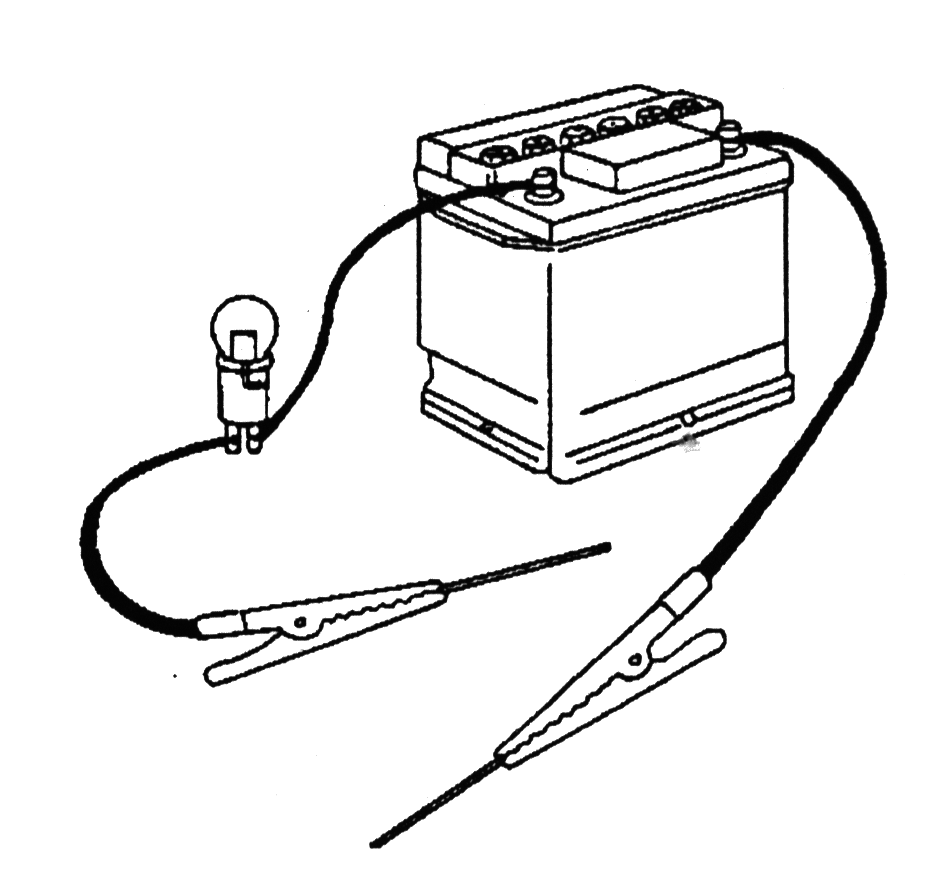
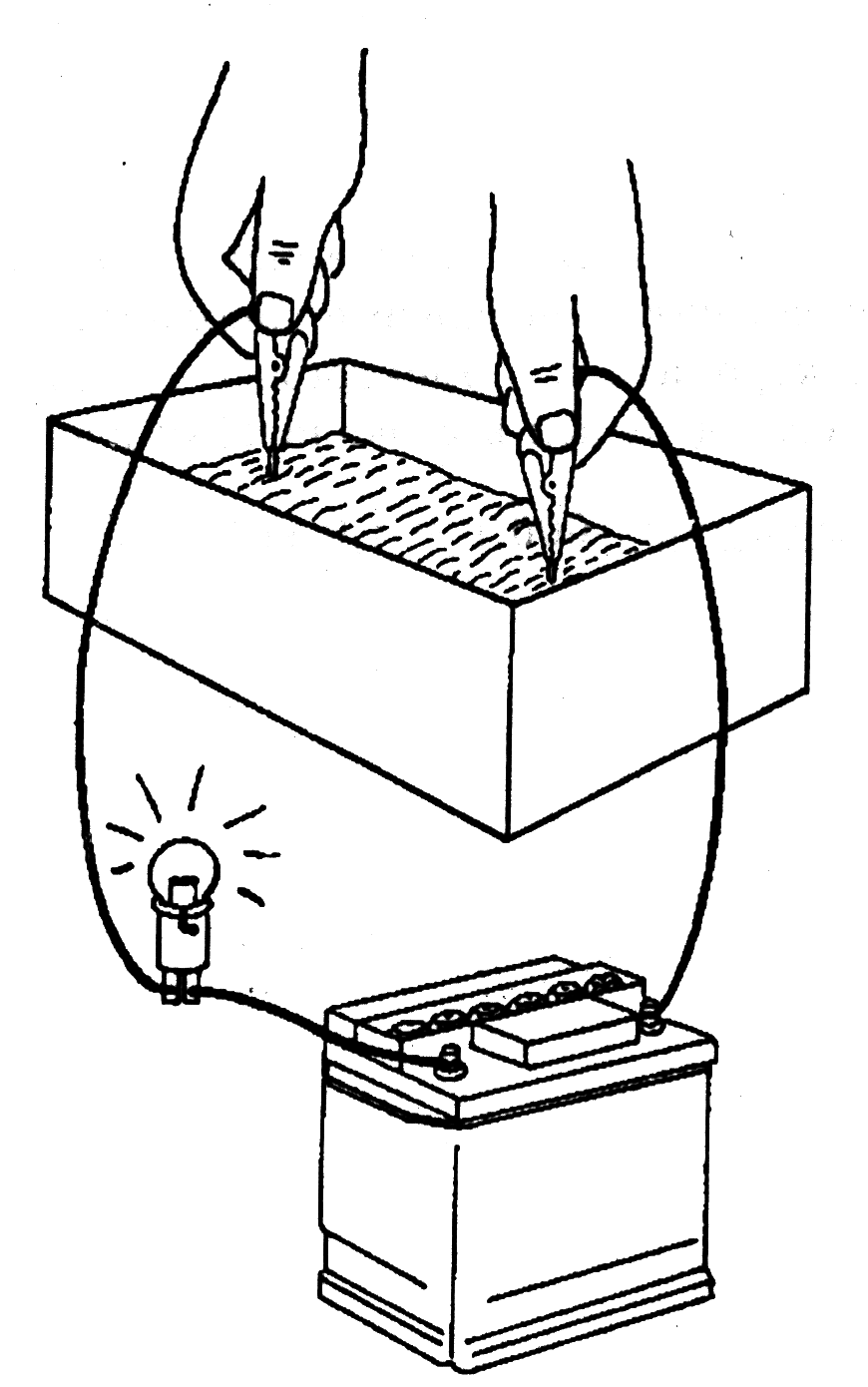
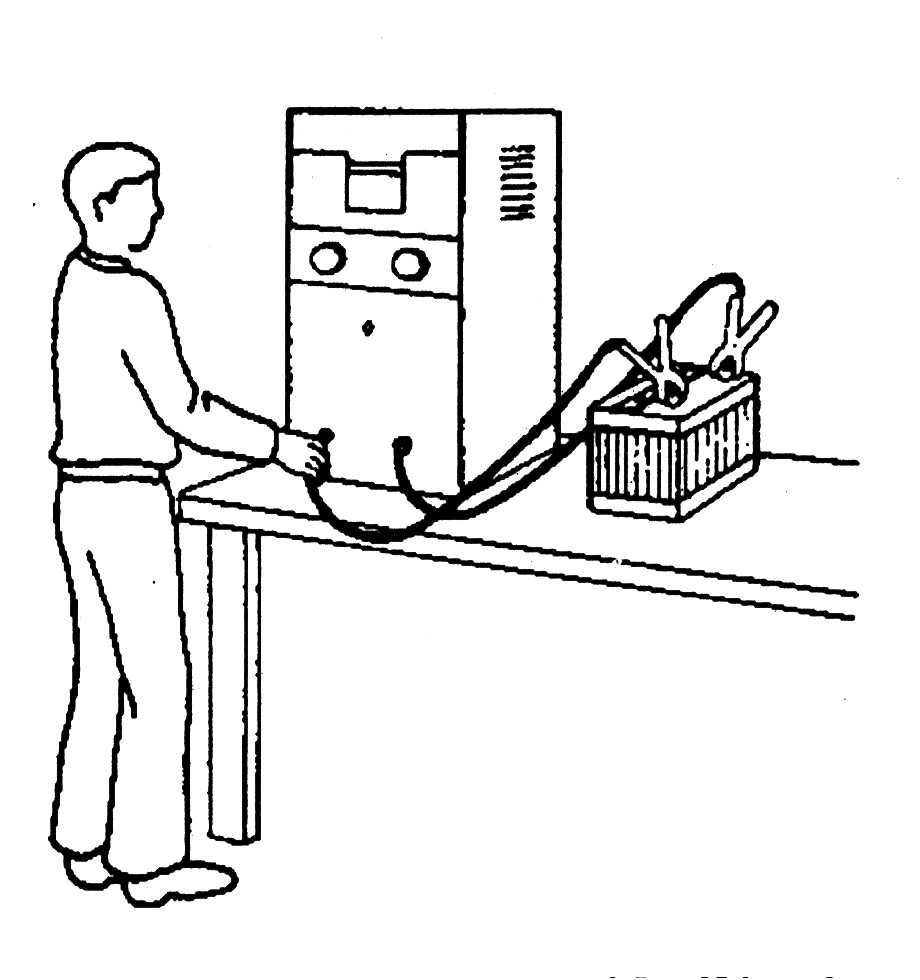
4. Затем соберите схему, приведенную на рисунке.
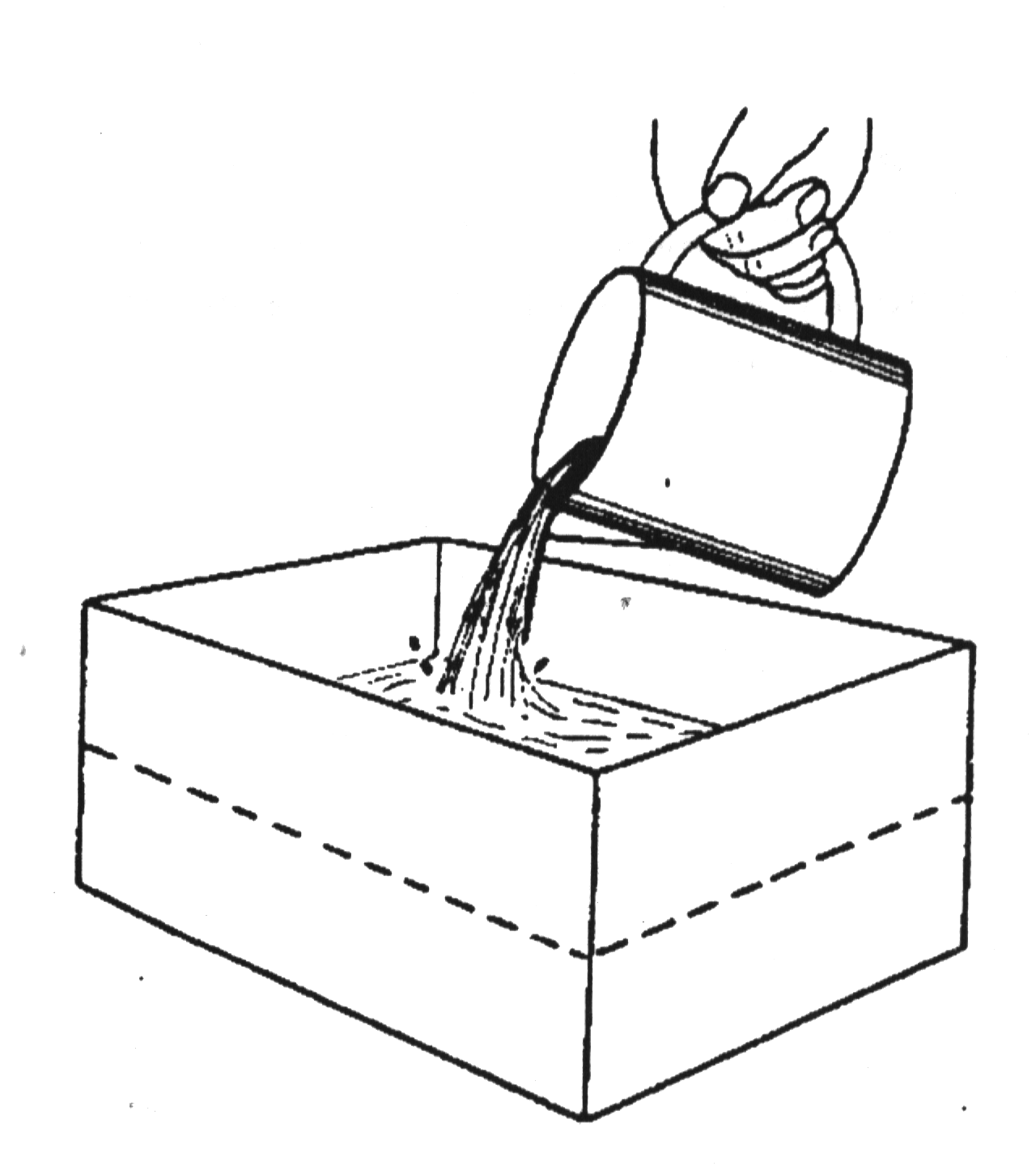
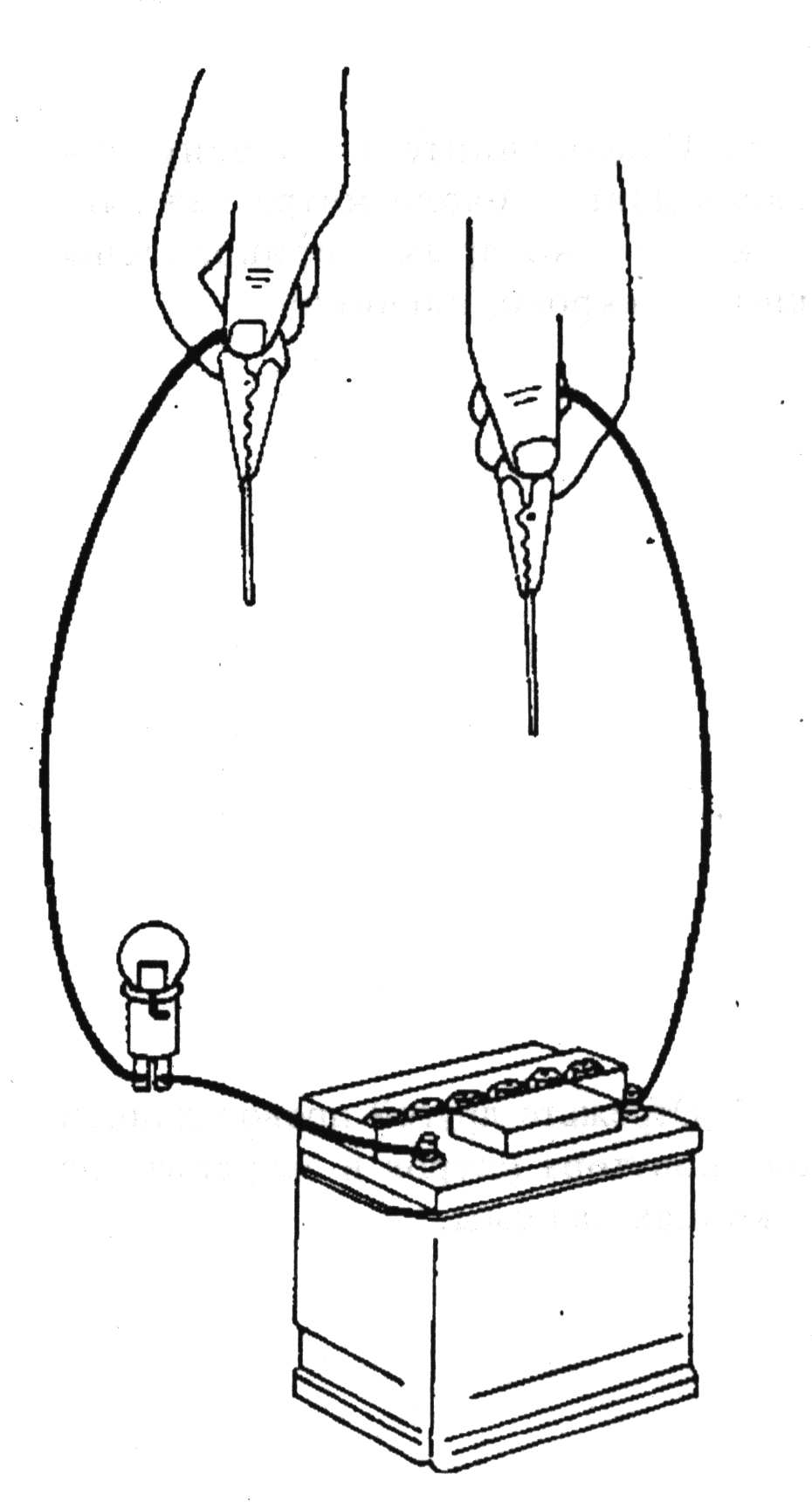
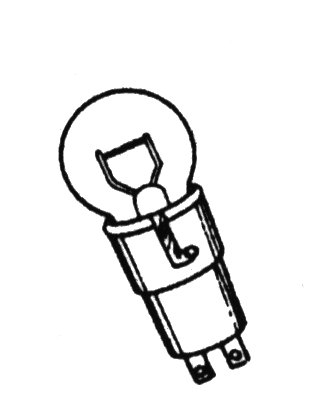
5. Возьмите 12-ти вольтовую лампочку на 18 или 21 ватт и вставьте ее в патрон.
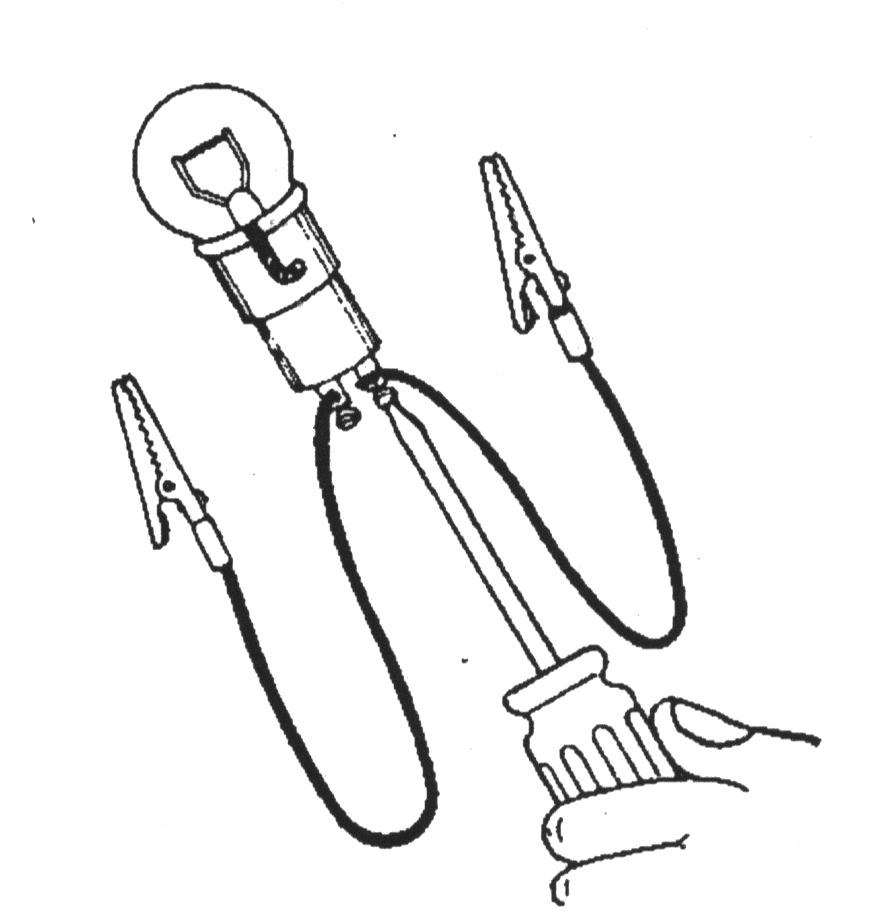
6. Подсоедините к патрону два провода длиной около метра каждый, на конце которых прикреплены зажимы - «крокодильчики».
7. Отрежьте другой провод длиной около полутора метров и закрепите на его концах зажимы.
8. Подсоедините один провод от лампочки к положительной клемме 12-ти вольтового аккумулятора. Затем возьмите отдельный провод (самы длинный) и подсоедините один из его зажимов к отрицательной клемме аккумулятора.
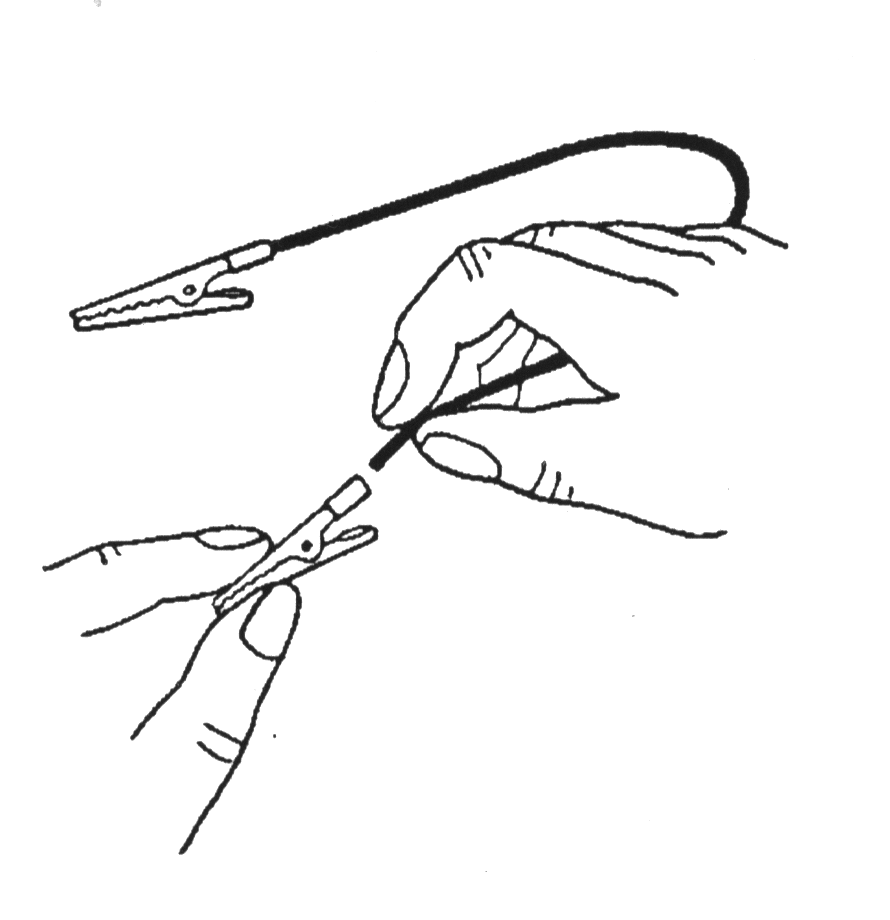
9. Теперь закрепите в оставшихся двух зажимах по отрезку неизолированного медного провода длиной около 50 мм.
10. Наложите один медный наконечник на другой, чтобы убедиться, что все работает нормально. Лампочка должна загореться; если нет, то необходимо проверить соединения и попытаться снова.
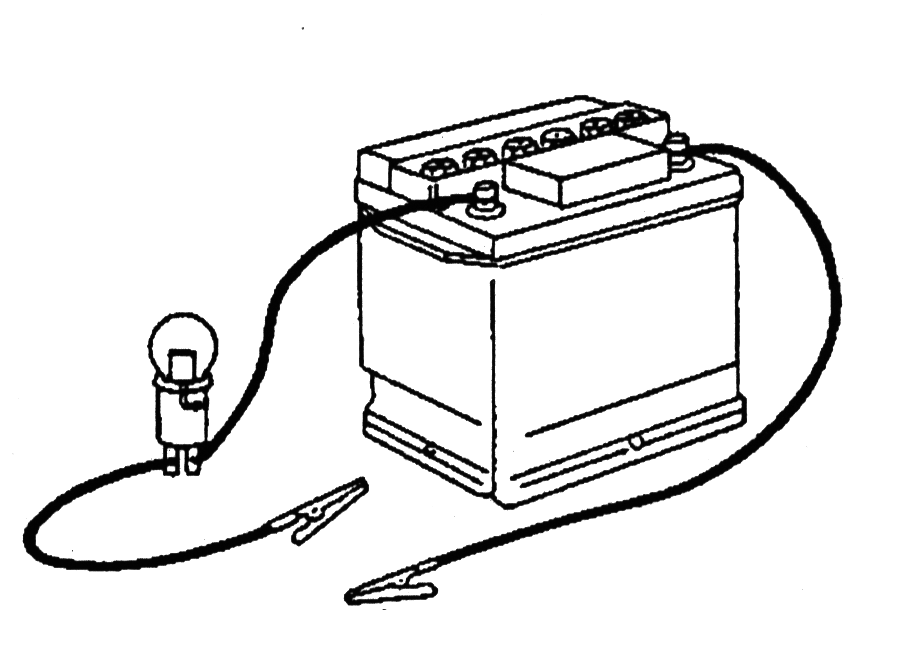

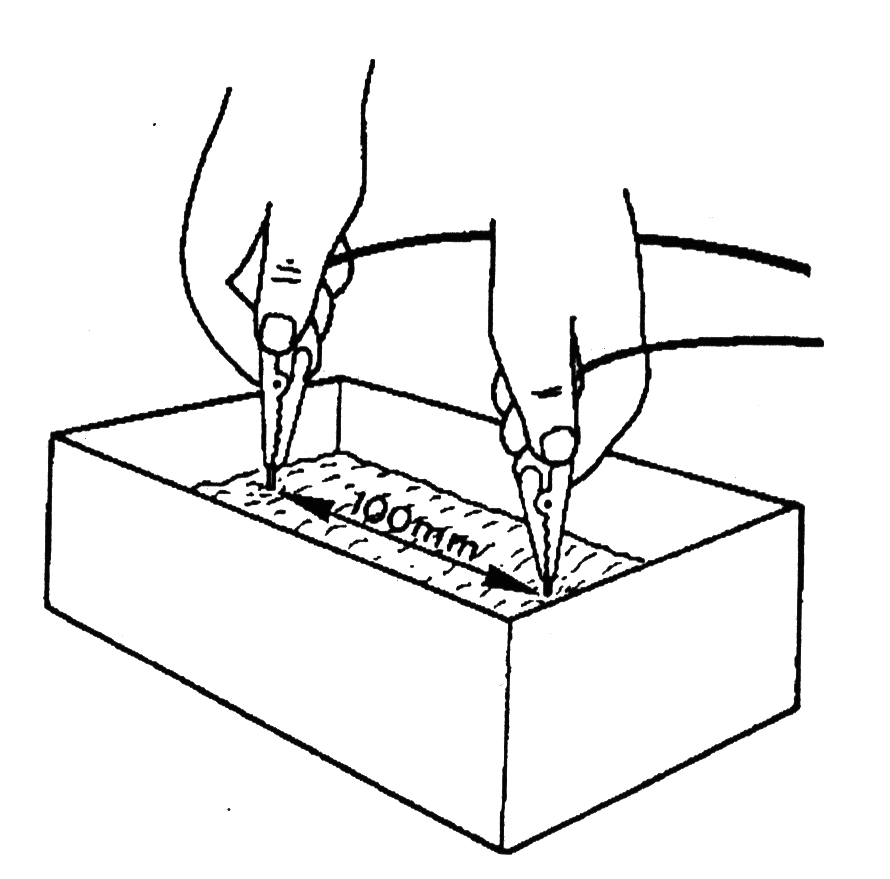
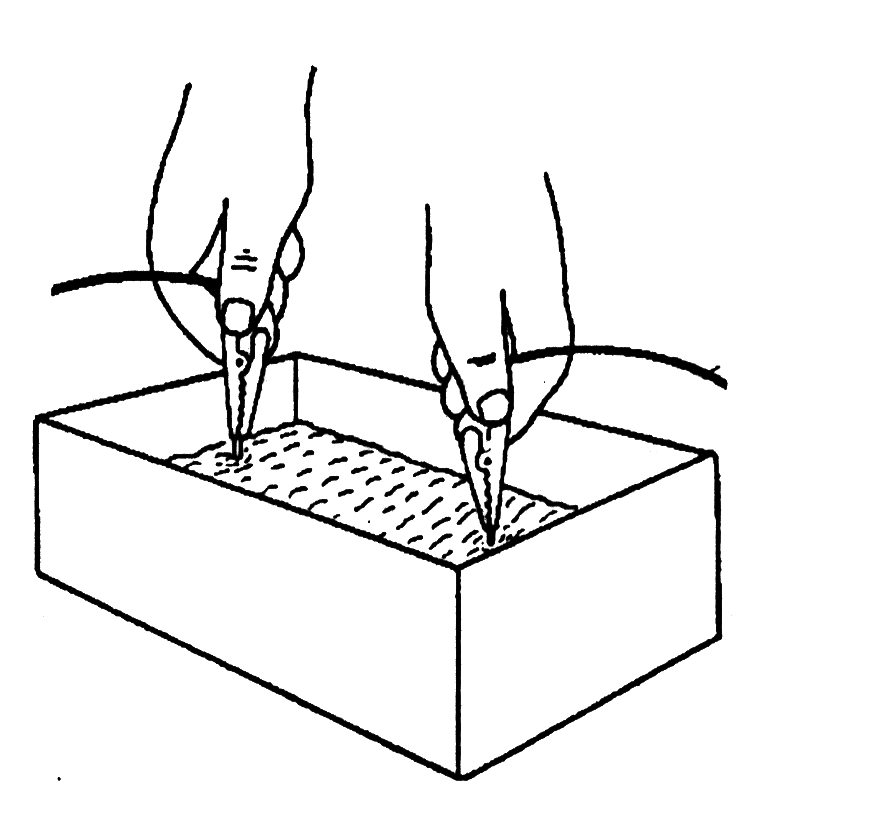
11. Теперь Вы готовы к опыту. Поместите оба конца провода (медные провода) в воду, но держите их на расстоянии около 100 мм друг от друга (смотри рисунок).
12. Вы обнаружите, что лампочка не загорается, так как вода не имеет достаточной проводимости, чтобы перемещать электроны от одного электрода (провода) к другому.
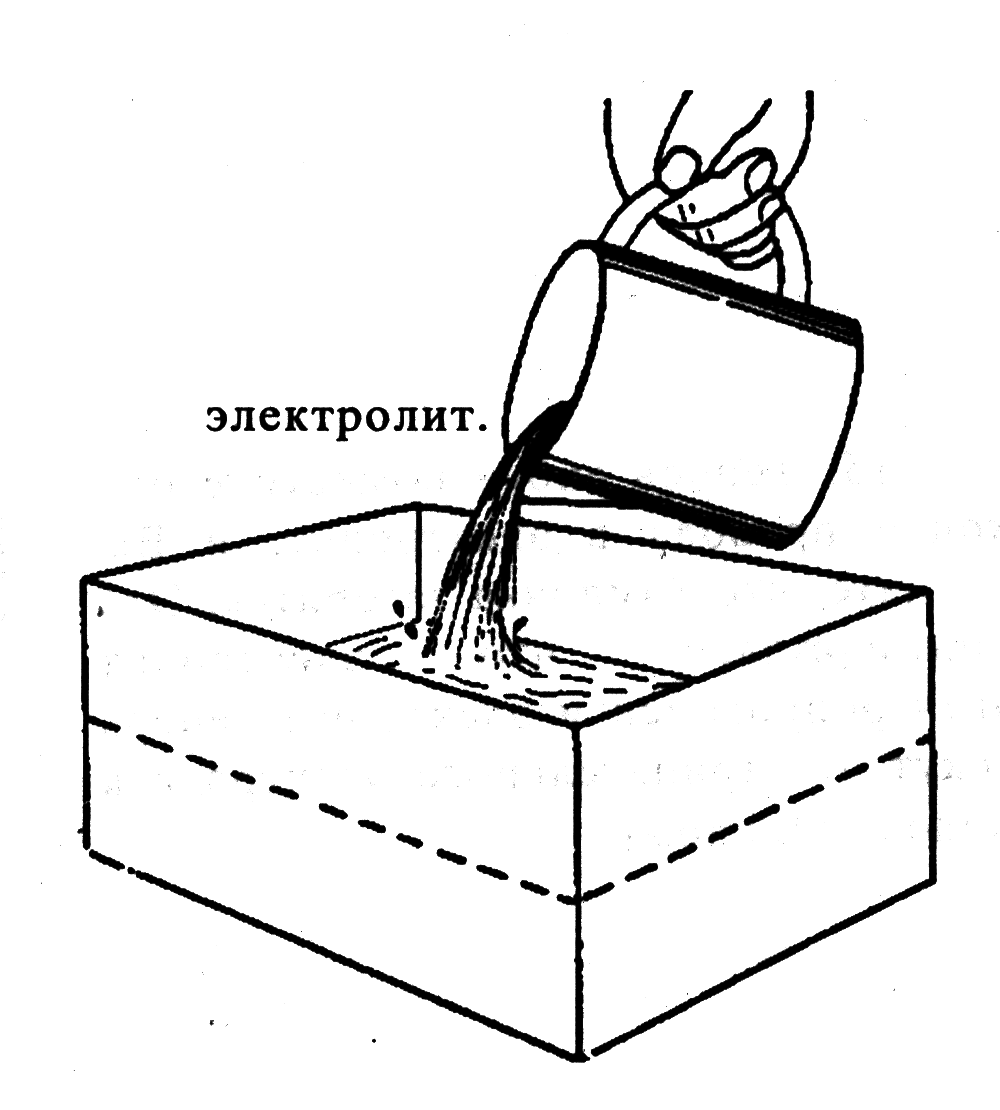
13. Для следующего опыта опорожните контейнер и заполните его электролитом. Электролит должен иметь удельный вес около 1,280 г/см3.
Замечание: 1000 г = 1,0 кг.
14. Предостережение:
Позаботьтесь о том, чтобы капли электролита не попали на глаза, кожу и одежду. Последствия могут быть серьезными.
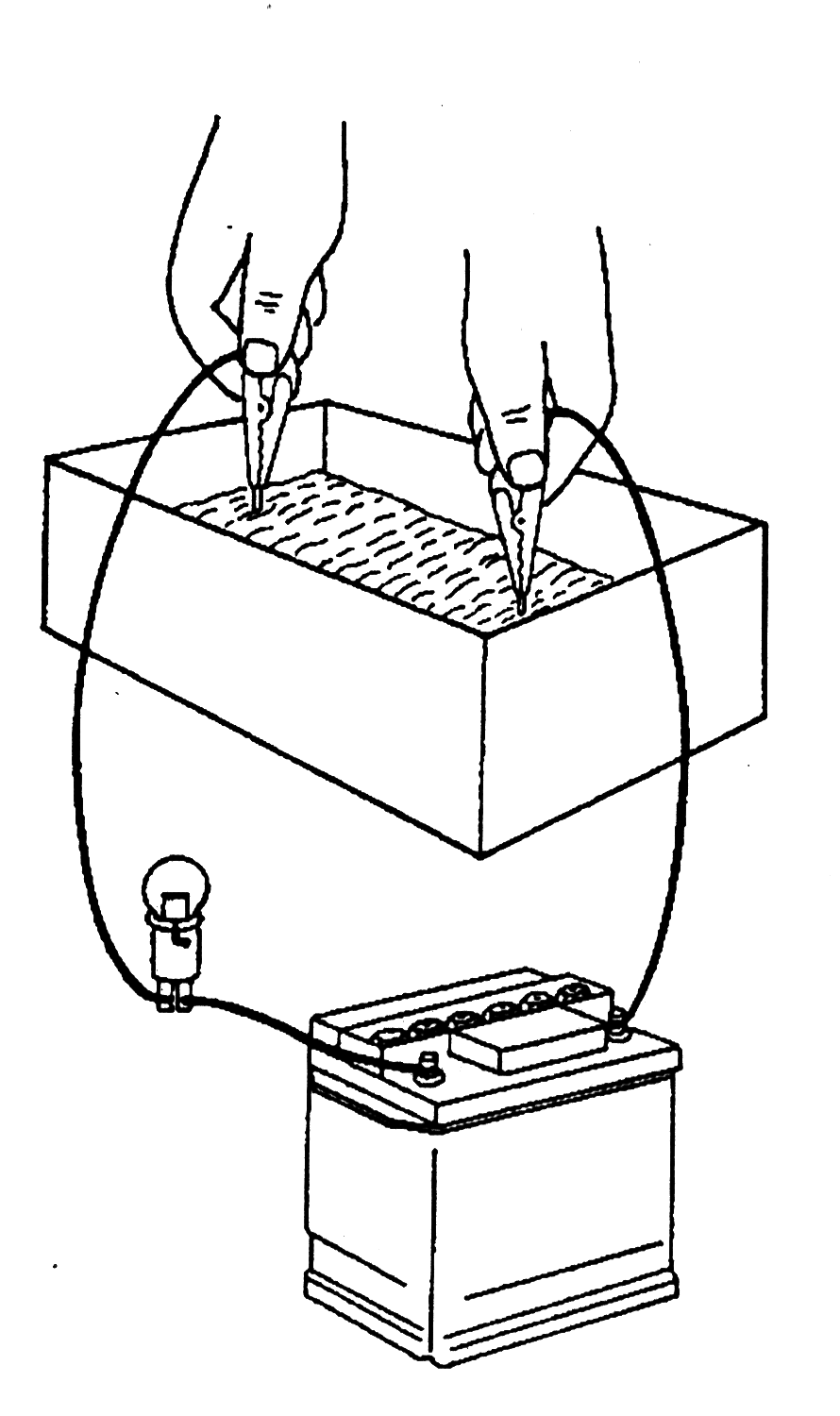
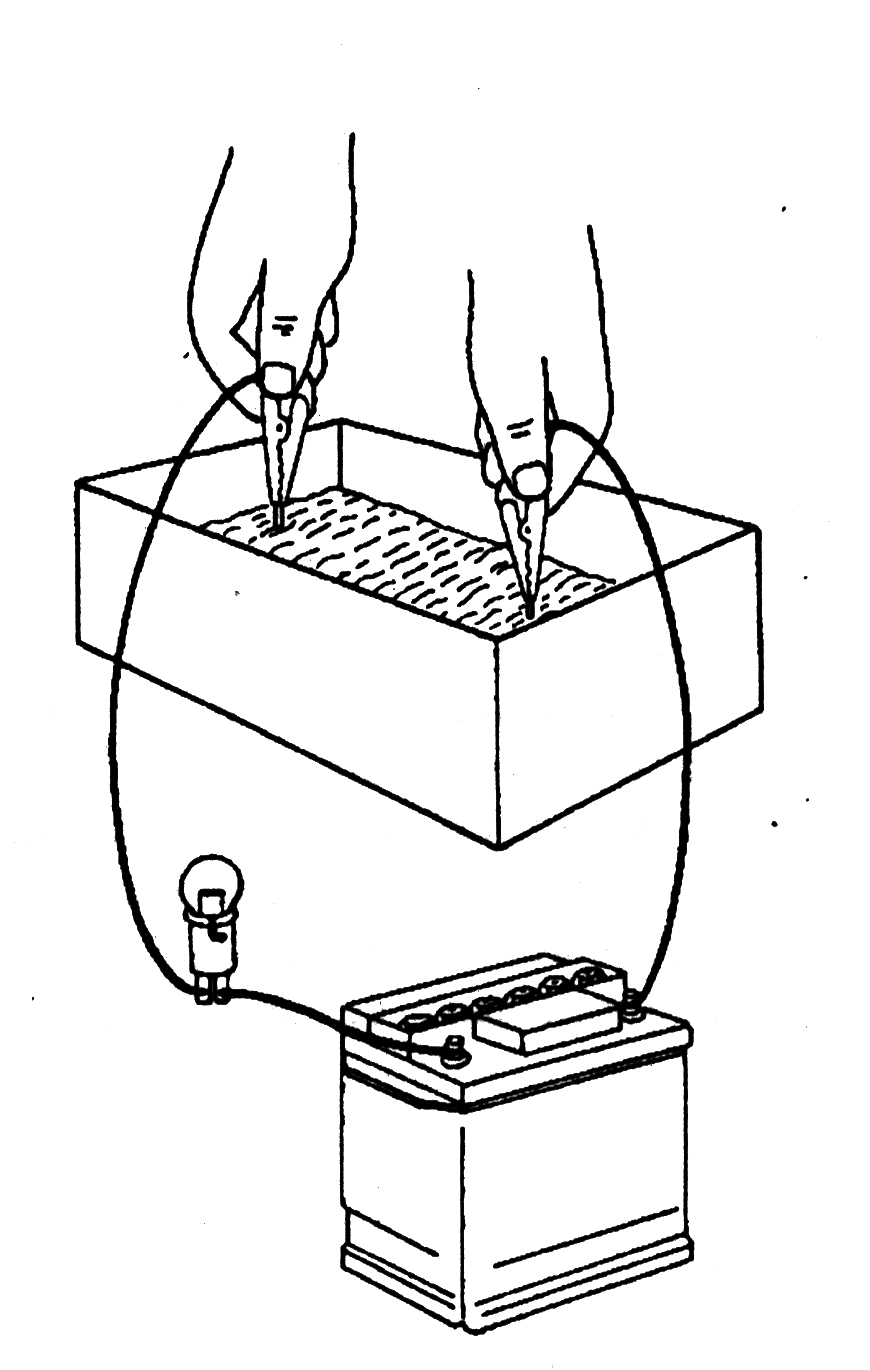
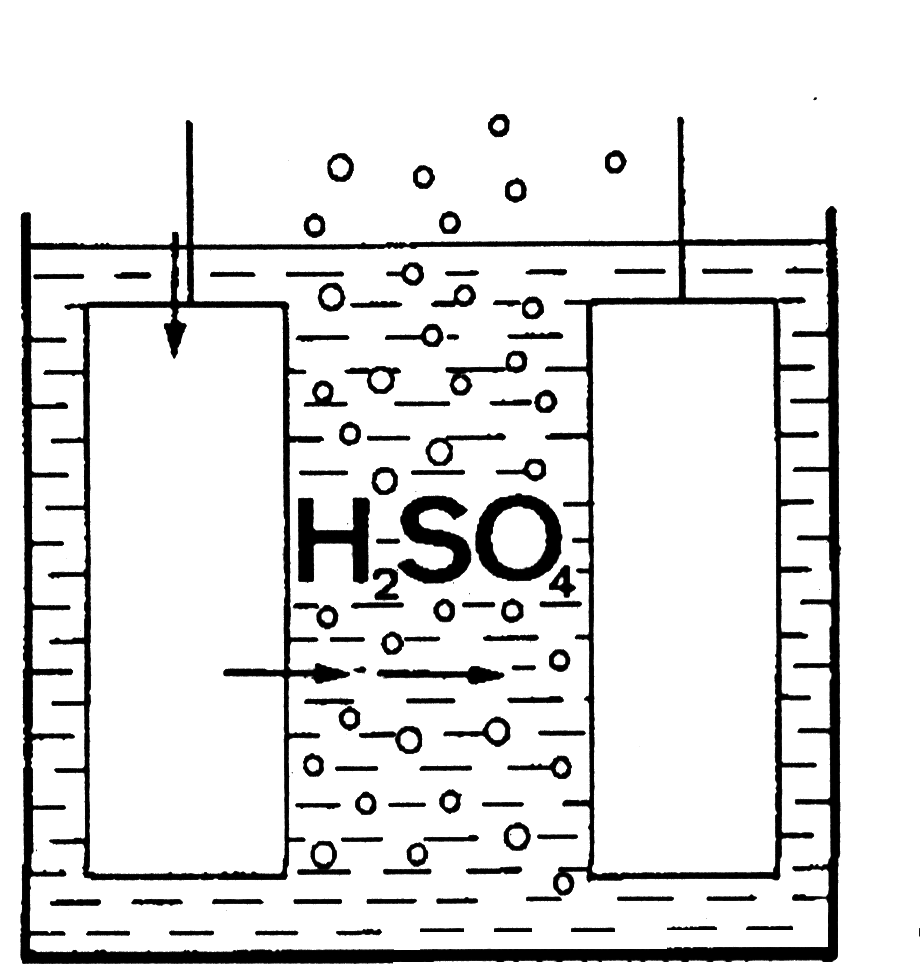
15. Теперь снова поместите оба конца провода в электролит, и Вы увидите, что лампочка загорится. Это подтверждает, что электролит электропроводен и электроны теперь текут от отрицательного электрода к положительному.
16. Увеличьте плотность электролита, добавив в него еще кислоты, или замените электролит чистой кислотой. Будьте очень осторожны, чтобы капли не попали Вам на глаза, кожу, одежду и т. д. Вы имеет дело с кислотой и можете получить серьезные ожоги
17. Опять опустите концы провода в жидкость.
18. Да, все правильно, лампочка не загорается.
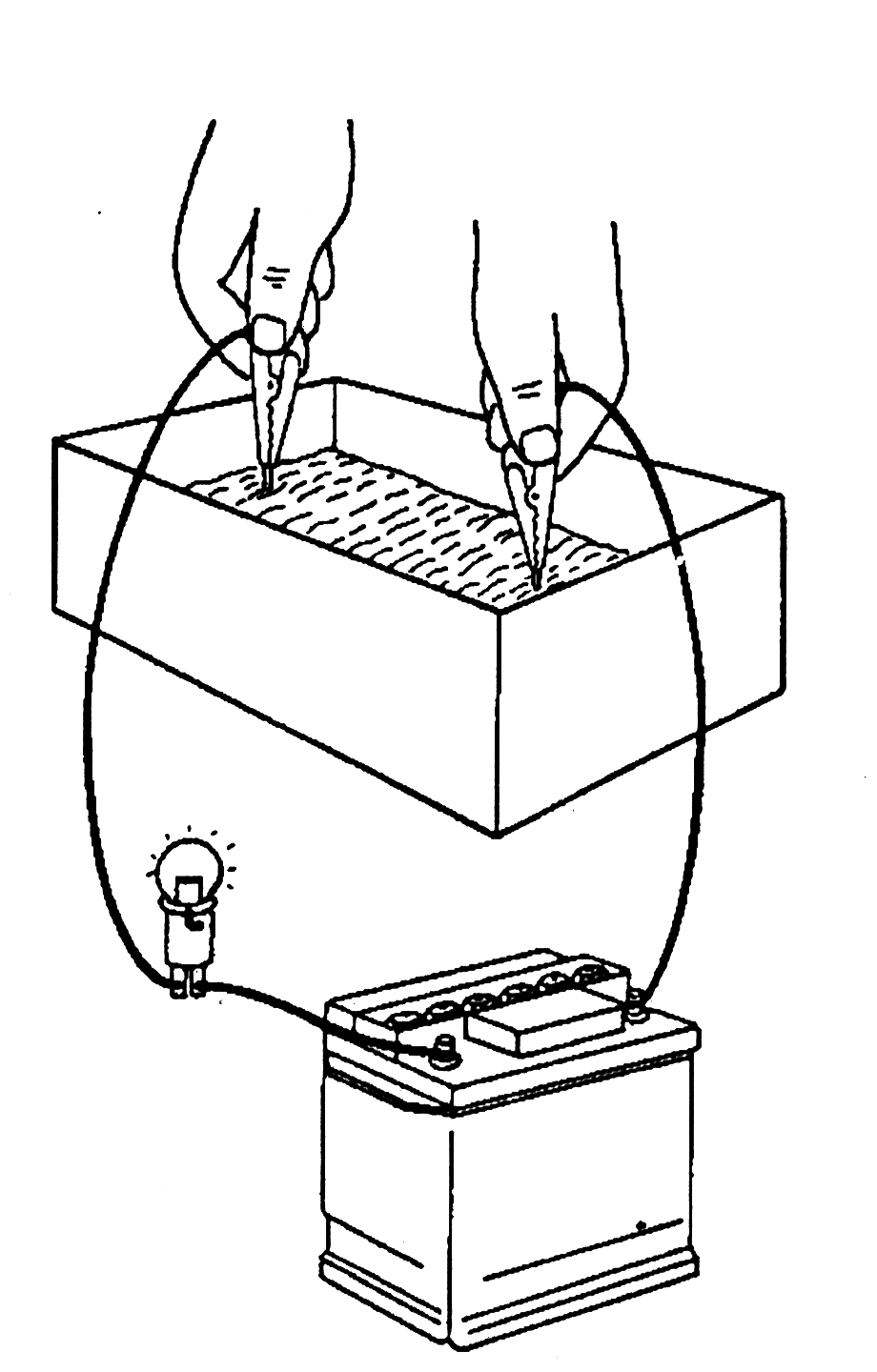
19. Или лампочка дает очень слабый свет. Это происходит, когда концентрация кислоты очень высокая.
20. Вывод: Только электролит с плотностью, примерно, 1,280 г/см3 имеет хорошую электропроводность. Если концентрация кислоты больше или меньше, то электропроводность меньше или даже ее нет совсем.
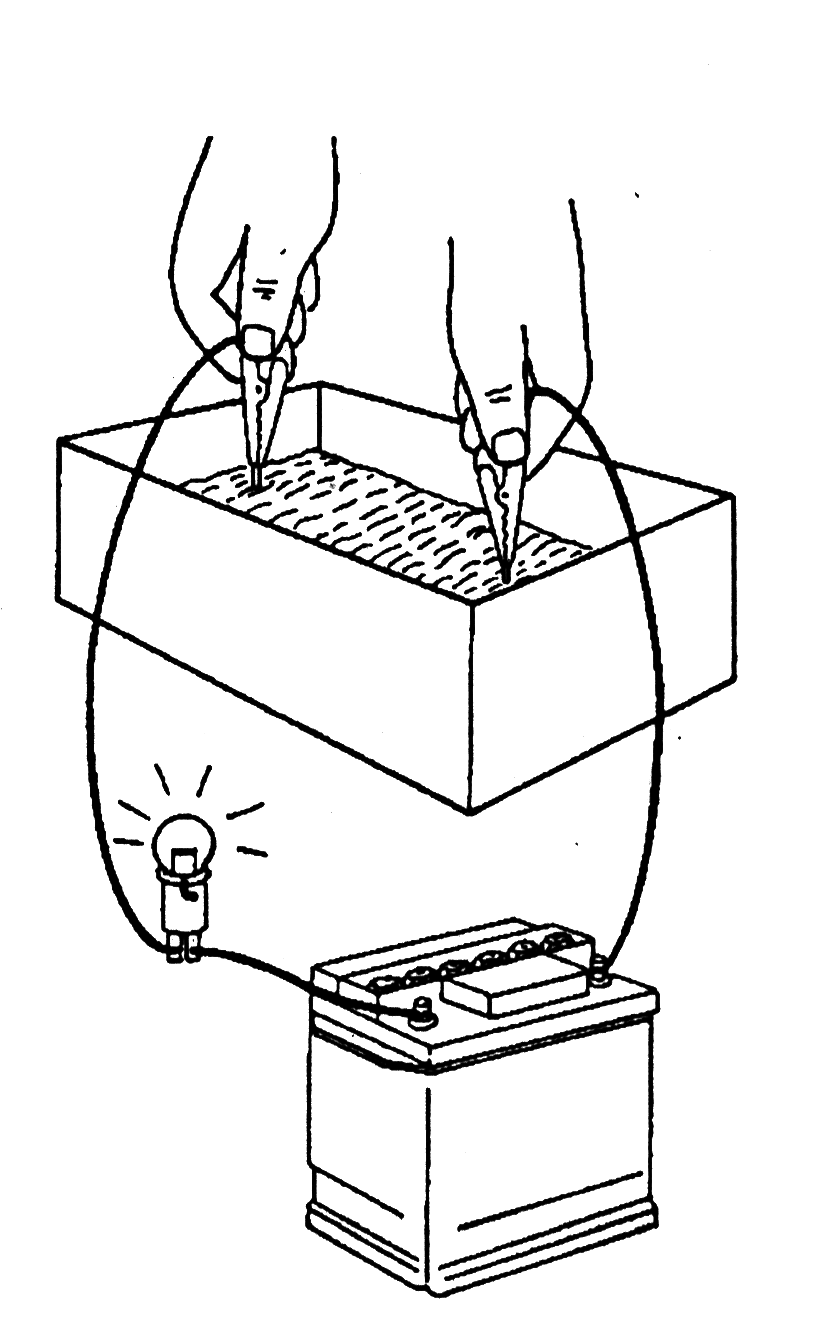
21. Надо помнить, что при более высокой концентрации кислоты, при плотности более 1,280 г/см3 будет разрушаться активный материал секции и срок службы аккумулятора уменьшается.
Замечание: Электролит является проводником второго класса (металлы являются проводниками первого класса). Химическая формула электролита H2SO4. [В одной молекуле серной кислоты содержится два атома водорода (Н)].
22. Как уже отмечалось в Учебном элементе «Устройство аккумуляторной батареи», только постоянный ток можно использовать, чтобы зарядить аккумулятор.
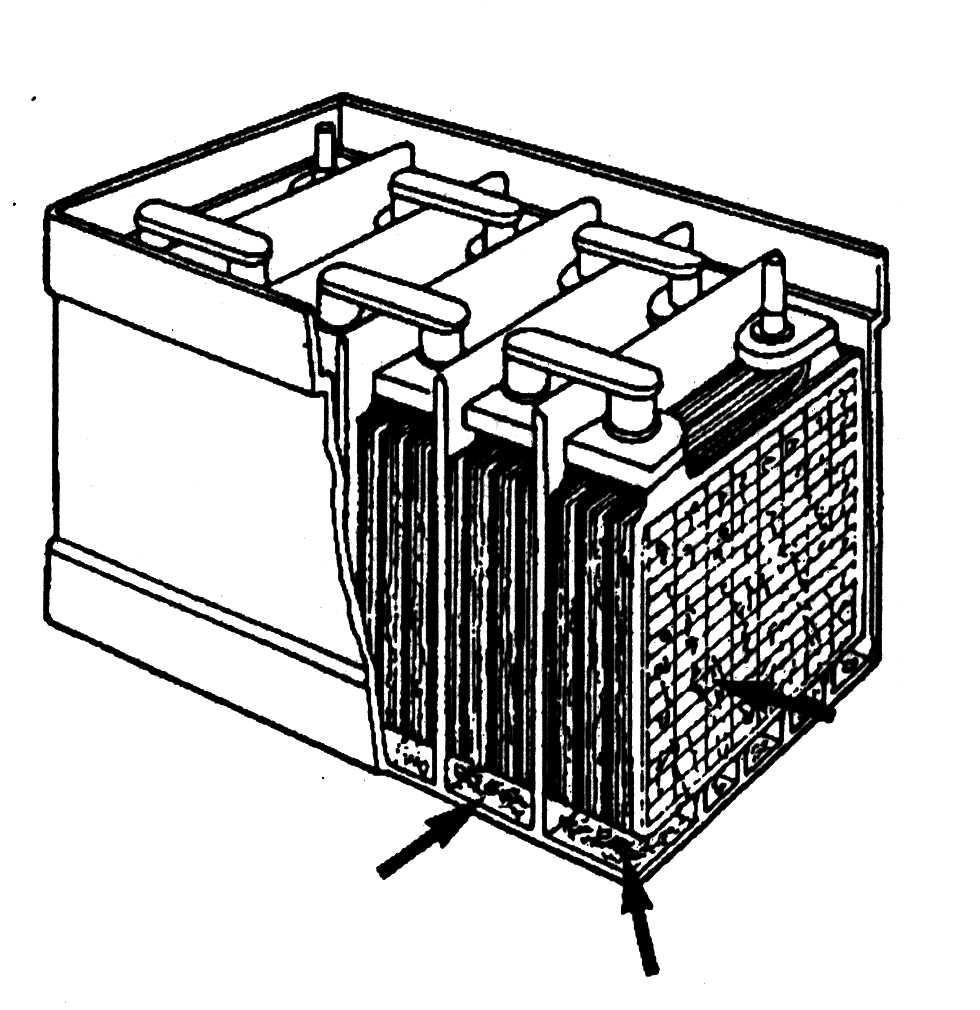

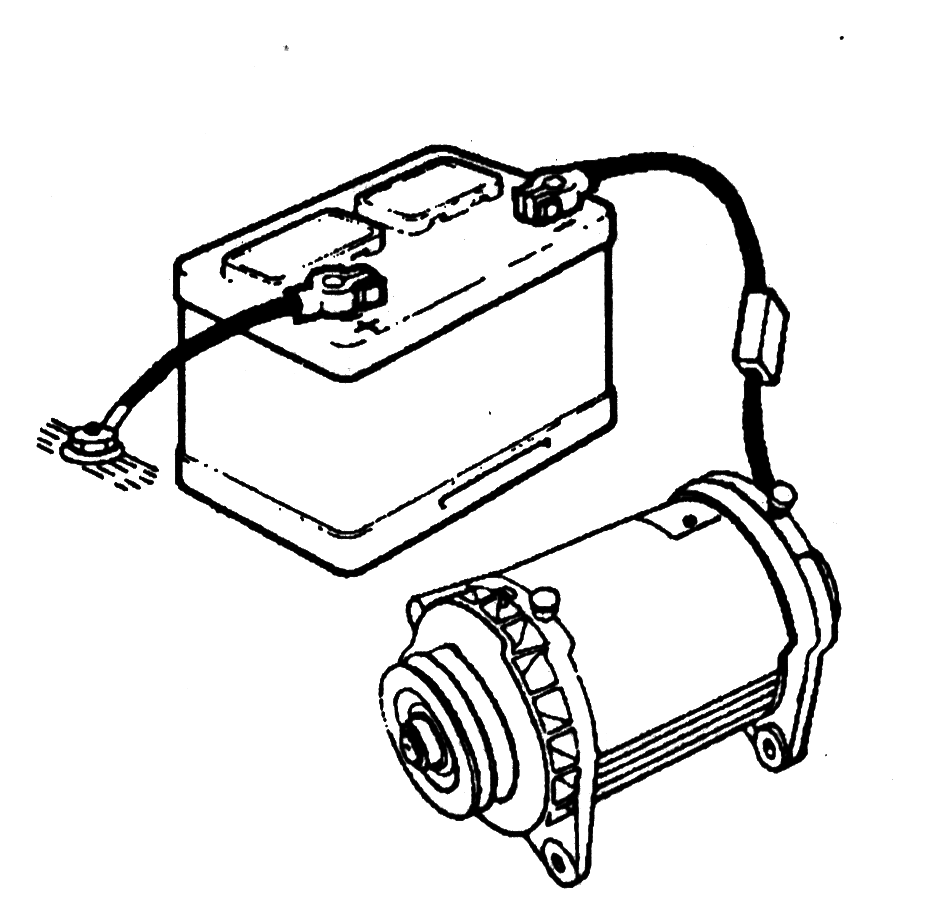
23. Когда постоянный ток течет через положительную свинцовую пластину, через электролит к отрицательной свинцовой пластине, происходит химическая реакция. Сульфаты положительной пластины превращаются в диоксид свинца, а сульфаты отрицательной пластины превращаются в губчатый свинец.
Химические формулы
Положительная пластина: РЬО2 (диоксид свинца)
Отрицательная пластина: РЬ (пористый свинец).
24. Если процесс зарядки остановить, то между положительной и отрицательной пластинами возникает электродвижущая сила, и, если цепь замкнута, то ток зарядки потечет в обратном направлении. Поверхность положительной и отрицательной пластин покрываются при этом сульфатом свинца.
Химические формулы:
Положительная пластина: PbSO4 (сульфат свинца)
Отрицательная пластина: PbSO4 (сульфат свинца)
э. д.с. : электродвижущая сила.
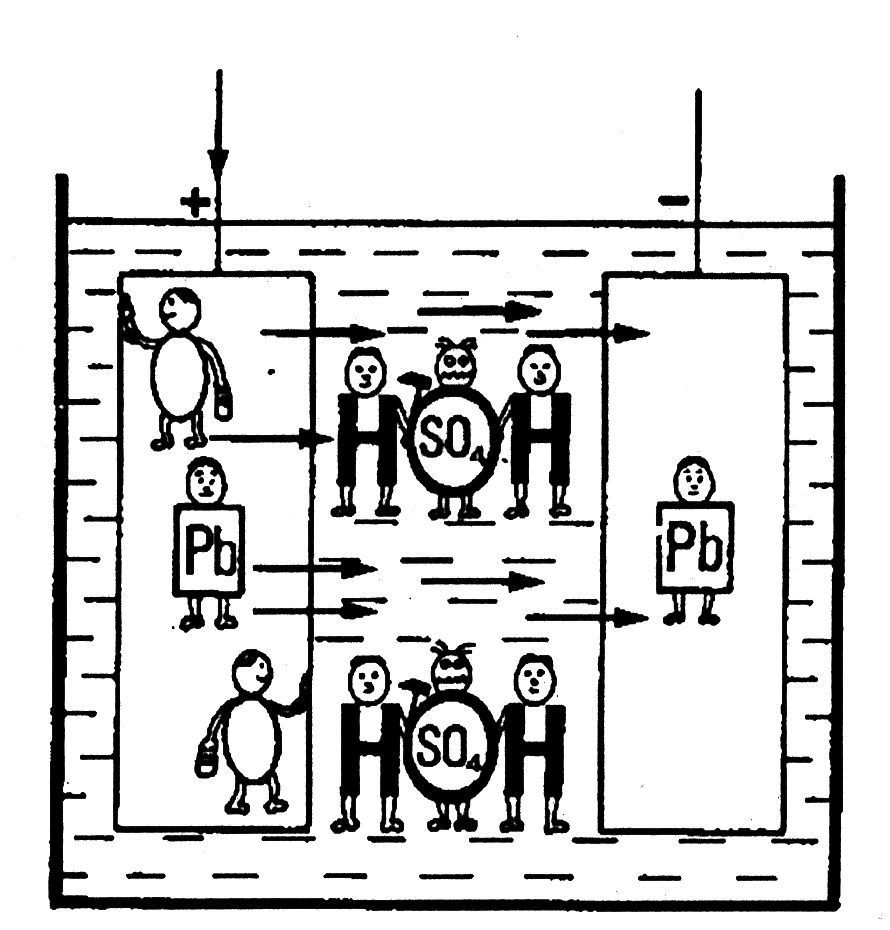
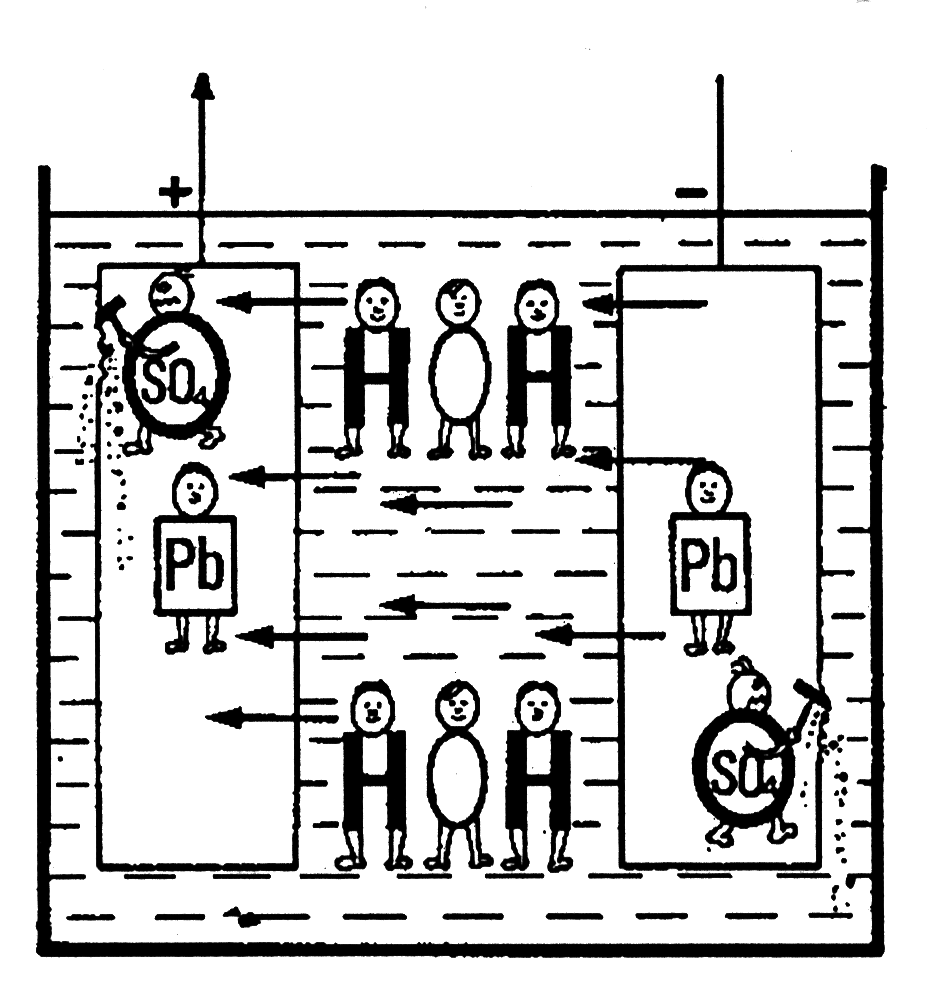
25. Более детально:
генерированный ток отрывает электроны от положительной пластины и закрепляет их в отрицательной пластине. Свинец нулевой валентности образуется на отрицательной пластине из двух валентных положительных ионов свинца, при этом разрушаются молекулы сульфата свинца (PbSO4). В то же время отрицательно заряженные сульфат ионы (SO4) отделяются от отрицательного электрода в электролит и т. д.
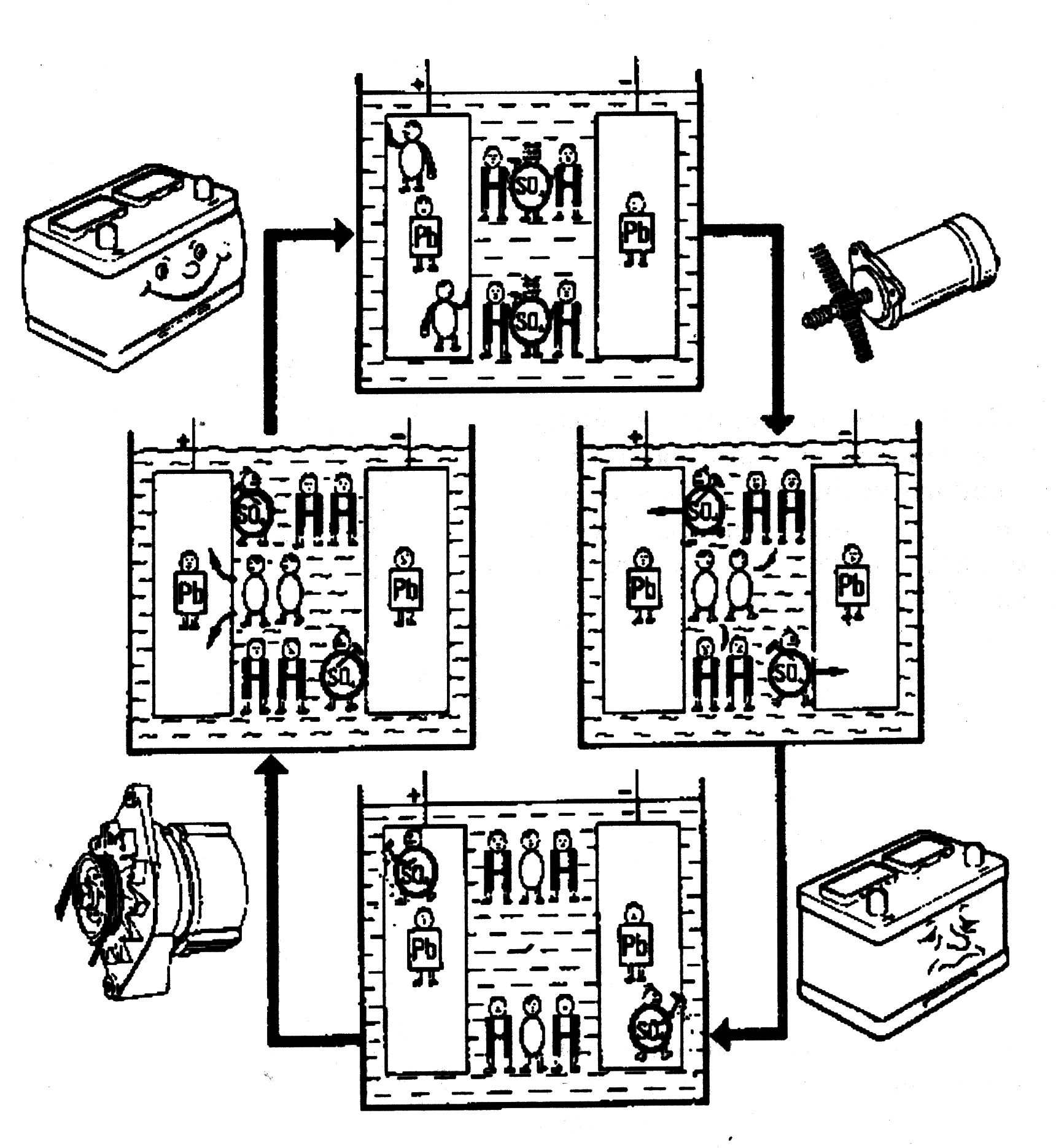
26. Давайте на этом остановимся, чтобы сказать, что на этой стадии нет необходимости объяснять химический процесс более детально. Следующие рисунки покажут Вам в простой форме принцип работы секции аккумулятора.
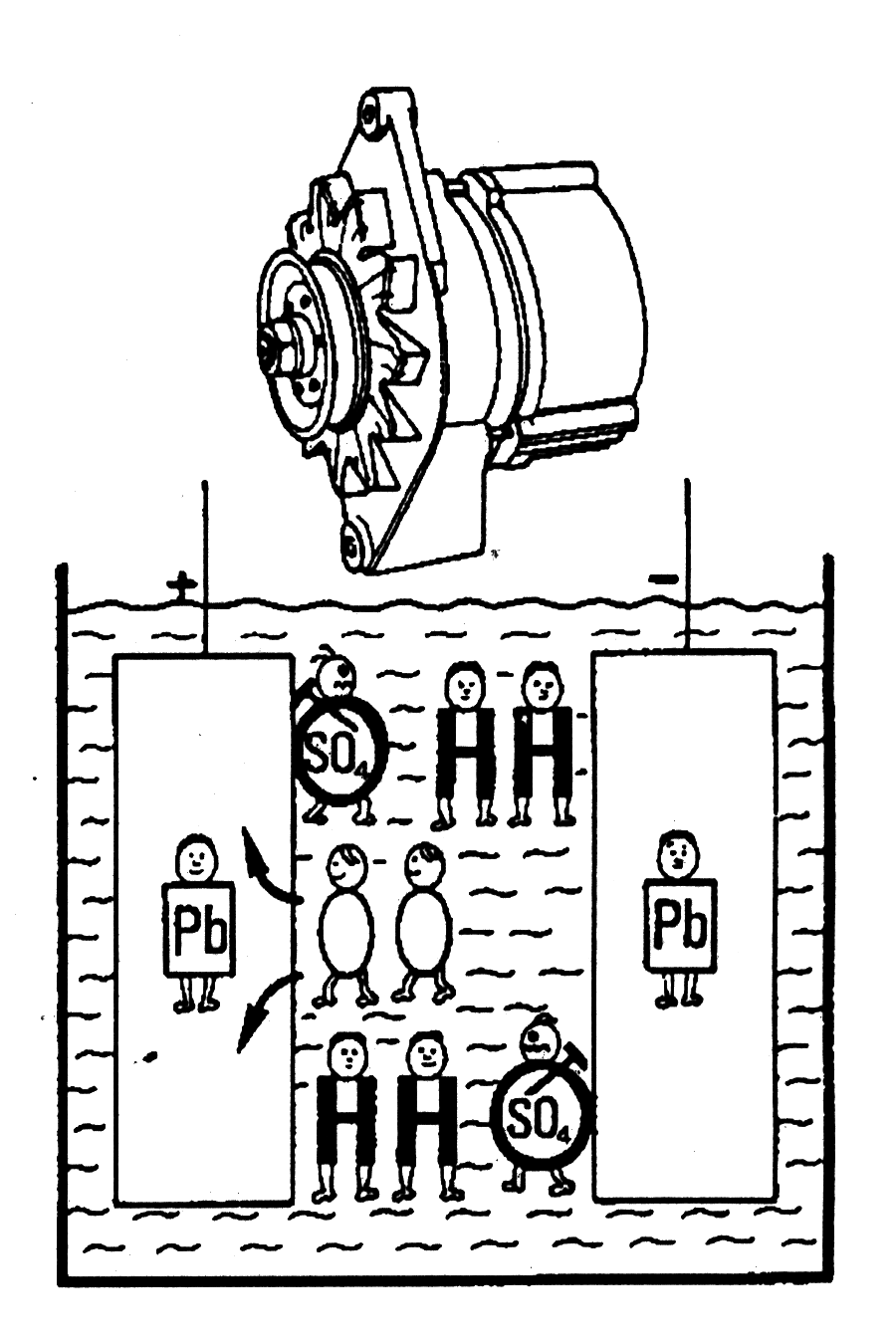
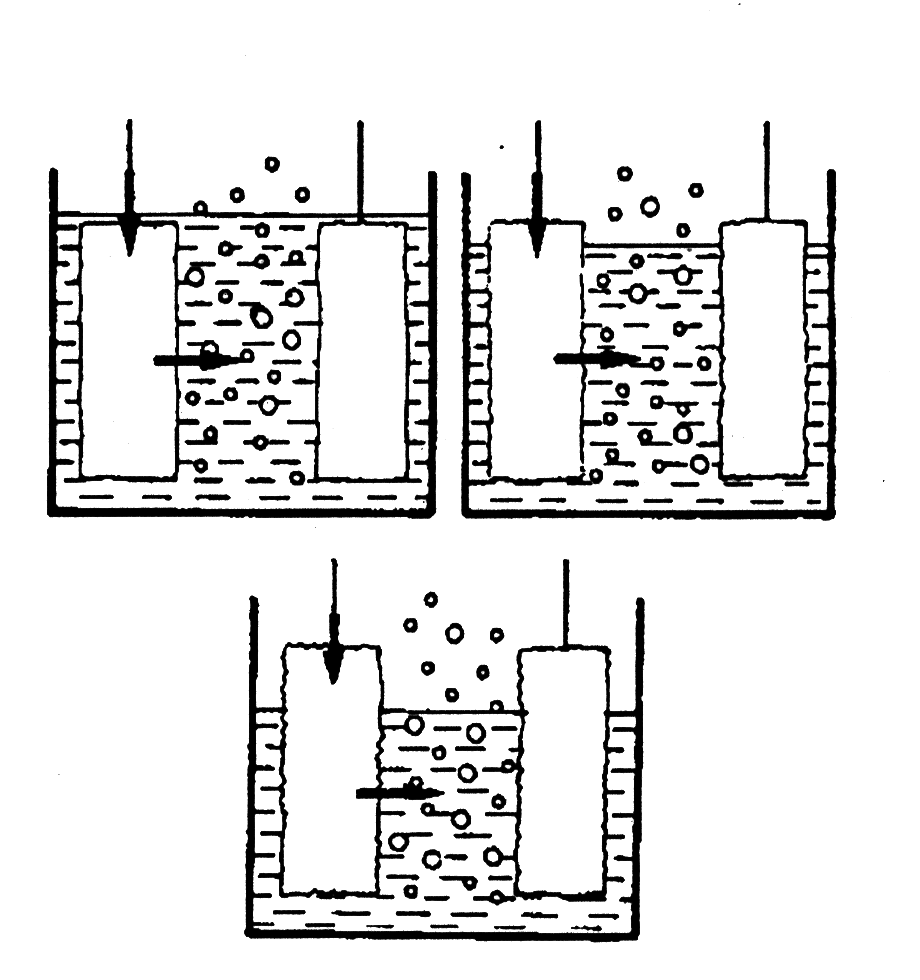
Теперь посмотрите внимательно на эти иллюстрации.
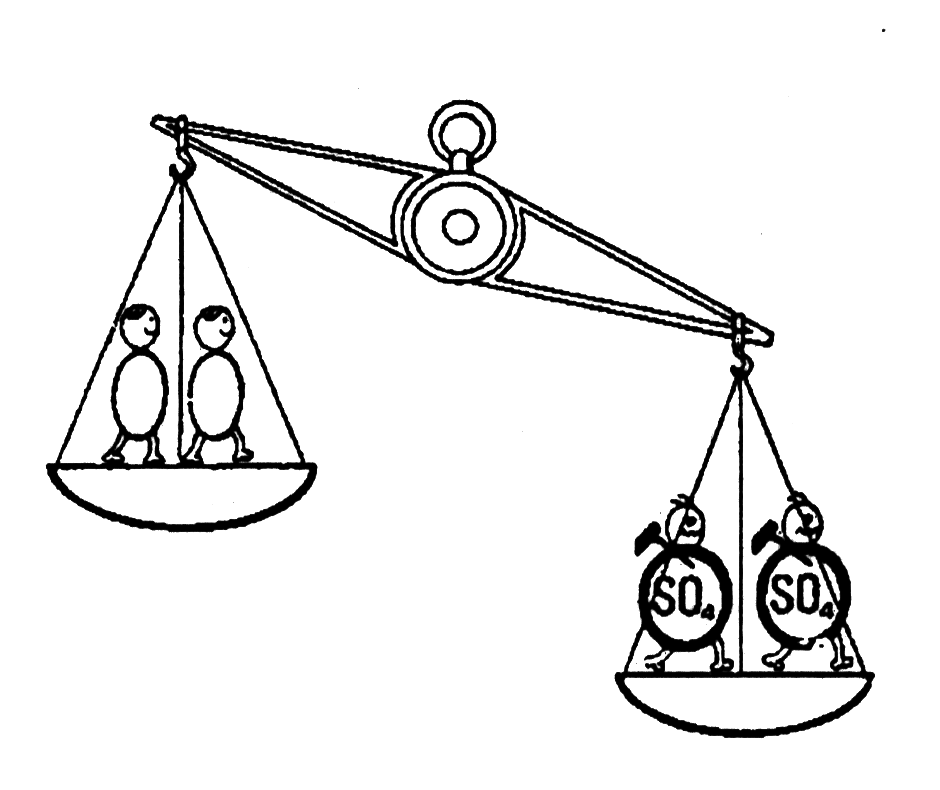
1) Первый рисунок показывает аккумулятор полностью заряженный. Свинец (РЬ) положительной пластины в двумя «О» сохраняет пластину в хорошем состоянии. Отрицательная пластина - только свинец РЬ. В электролите Вы найдете два маленьких парня SO4. Эти два парня делают электролит тяжелым.

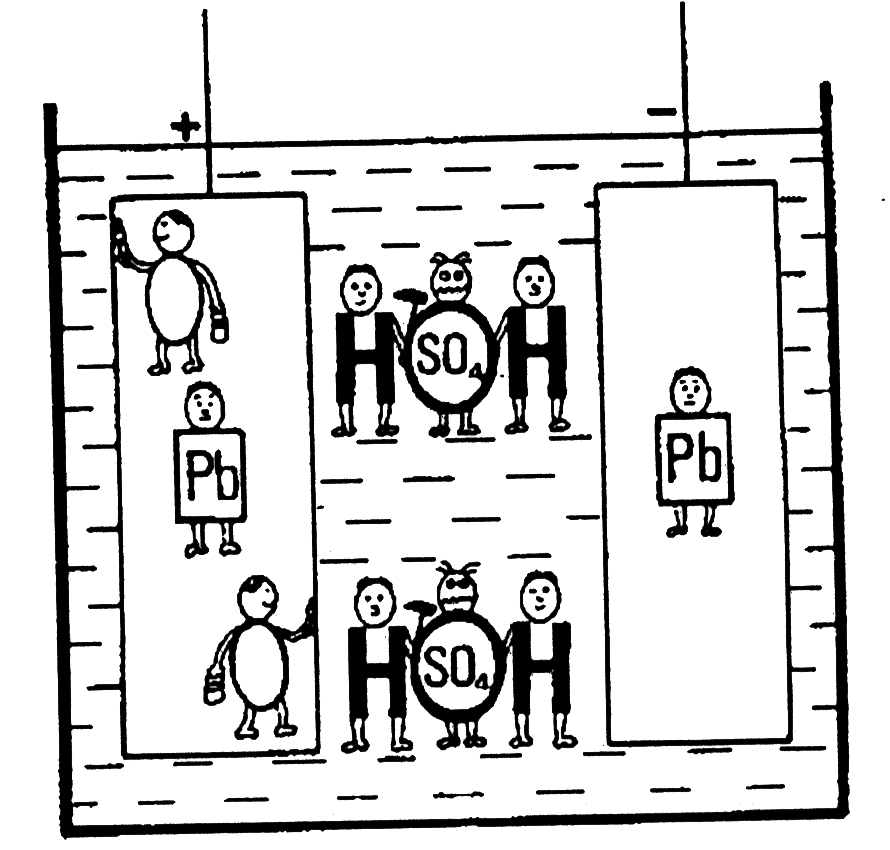
2) Второй рисунок показывает, что происходит, когда заводится двигатель. В процессе разрядки два парня «О» протискиваются с положительной пластины - в электролит. Один из парней SO4 проникает в положительную пластину, другой - в отрицательную. Чем более разряженным становится аккумулятор, тем больше парни SO4 начинают разрушать пластины.
3) На третьем рисунке показан разряженный аккумулятор. Оба парня SO4 заняты разрушением пластин. Чем больше у них времени, тем больше разрушения. Электролит теперь более легкий, так как оба тяжелых парня SO4 заменены двумя легкими парнями «О».
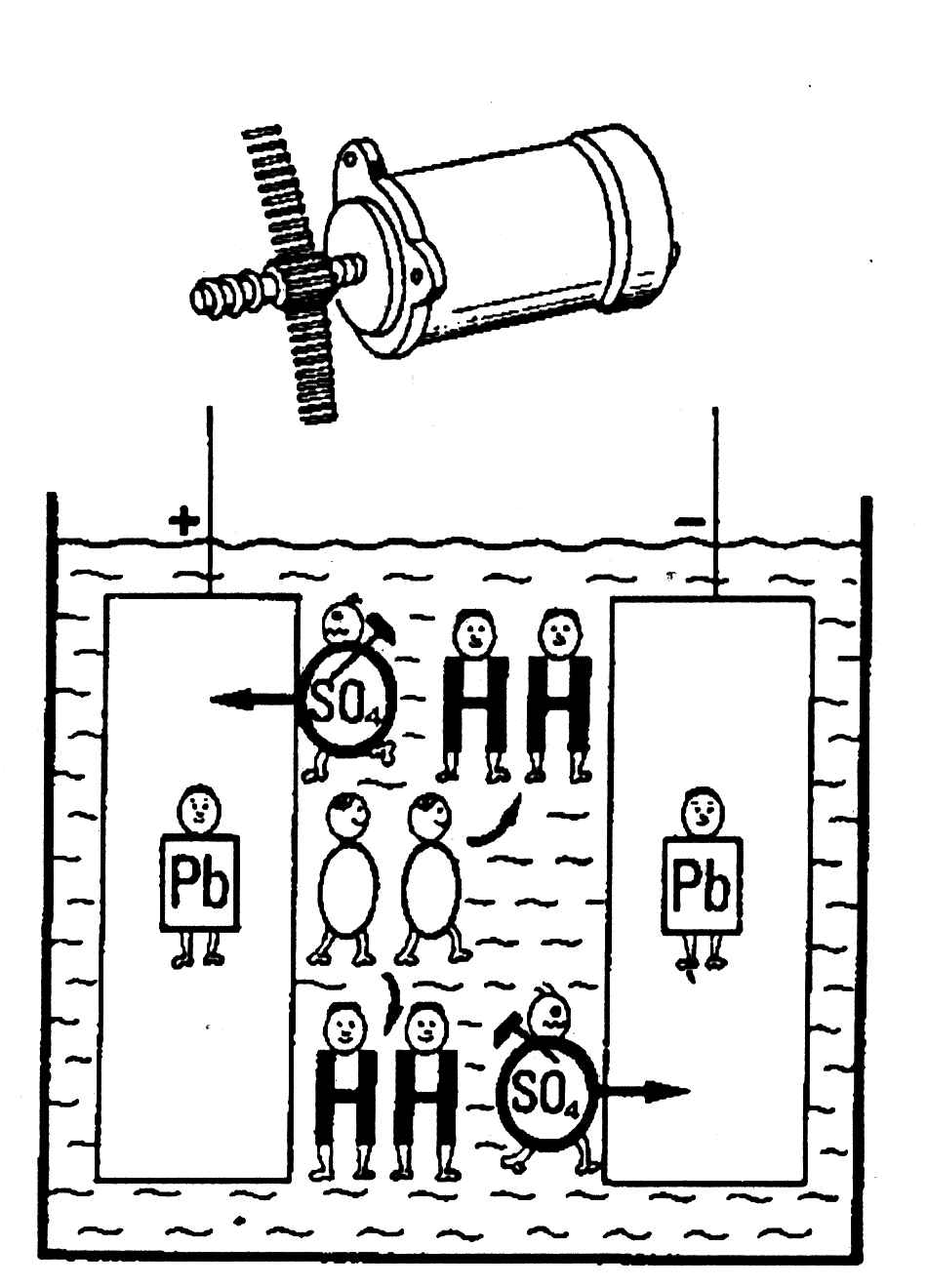
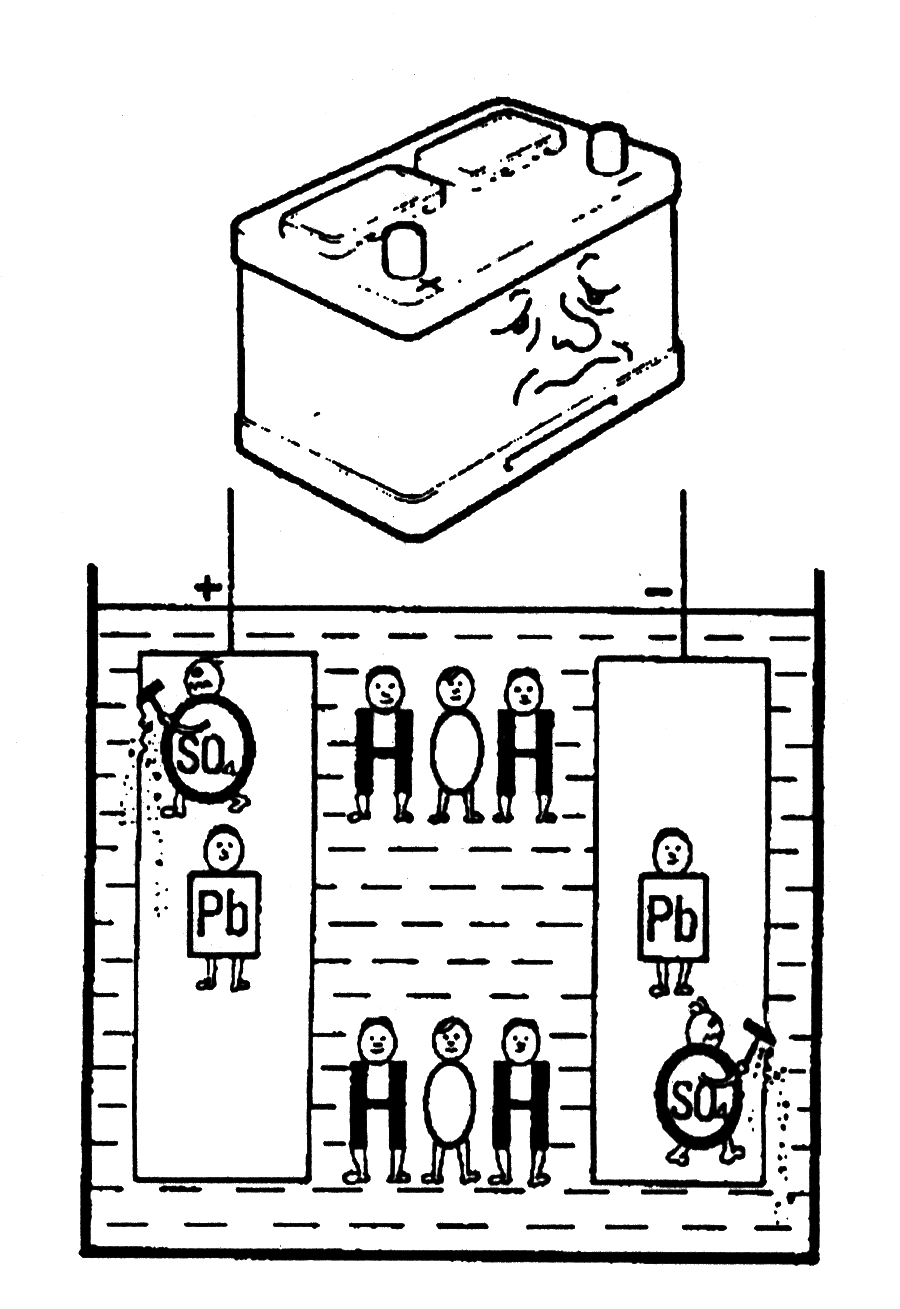
4) На последнем рисунке показано, что аккумулятор опять заряжается. Опять и опять два парня SO4 прекращают разрушение аккумулятора. Они вынуждены покинуть пластины и вернуться обратно в электролит. Это увеличивает вес электролита, и два парня «О» проникают в положительную пластину и стараются восстановить поврежденные пластины. Однако, если повреждение слишком велико, поскольку аккумулятор в разряженном состоянии был слишком долго, тогда ничего уже нельзя сделать. Это значит, что часть секции уже постоянно не работает.
Не продолжайте изучение, пока полностью не поймете параграф 26.
27. Опять в процессе зарядки образуется серная кислота и плотность электролита возрастает. В полностью заряженной секции плотность электролита в нормальных условиях составляет 1,280 г/см3. Это положение делает возможным контролировать зарядку секции или аккумулятора, измеряя плотность электролита. (Смотри Учебный элемент «Обслуживание аккумулятора»).
28. После того как сульфат свинца На положительной пластине будет превращен в диоксид свинца, а сульфат свинца на отрицательной пластине будет превращен в пористый свинец, процесс зарядки закончен, и аккумулятор необходимо отключить от источника тока.
29. По этой причине в цепь последовательно с генератором введен переключатель, который приводится в действие механически или электронно.
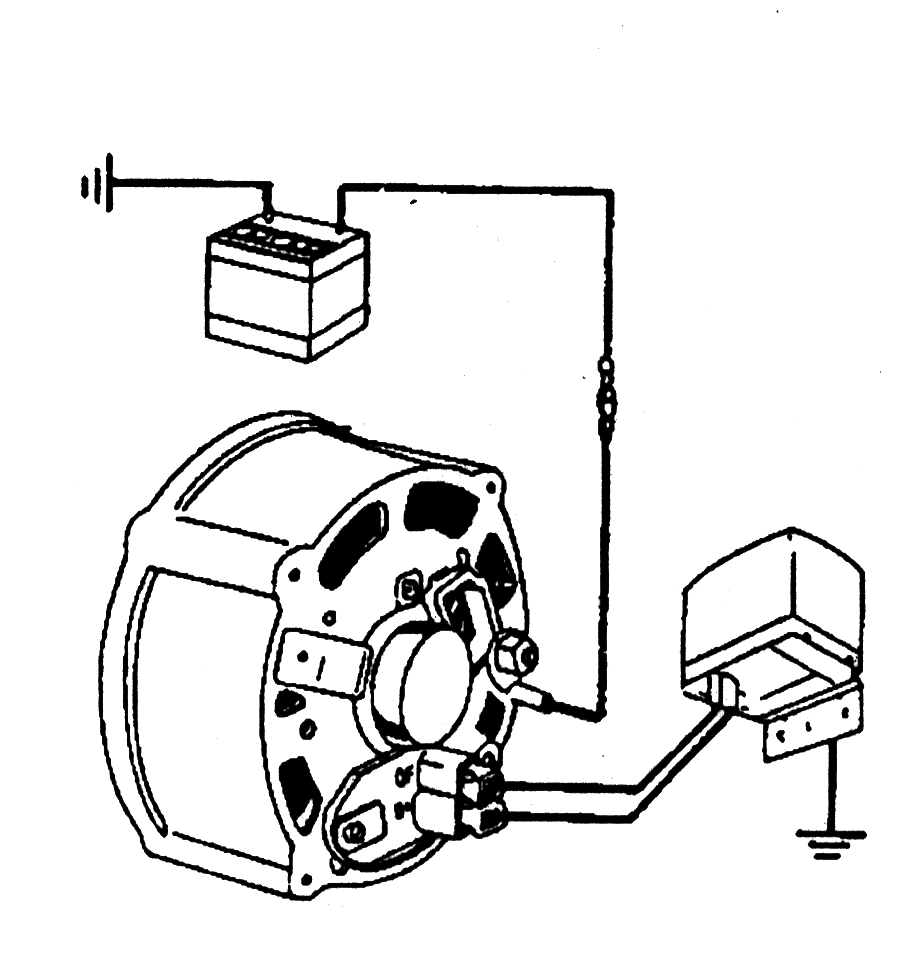
30. Или, когда аккумулятор заряжается от зарядного устройства, то после зарядки он должен быть отсоединен от этого устройства ответственным персоналом.
31. Если аккумулятор не отсоединить и подать больше электронов, то происходят новые нежелательные реакции.
32. Электрическая энергия, все еще поступающая в секцию, не может больше быть использована на химическое превращение материала положительной пластины и поэтому вызывает электрическое разложение воды. Этот процесс известен под названием «аккумулятор газит».
33. Это газовыделение уменьшает содержание воды в электролите. Концентрация серной кислоты повышается сверх нормы.
Замечание: Аккумулятор «газит» - это тогда, когда Вы видите много поднимающихся пузырьков при заглядывании в аккумулятор.
ПОЗОВИТЕ ИНСТРУКТОРА, и он покажет Вам в зарядной комнате разницу между «аккумулятор «газит» нормально» и «аккумулятор «газит» сильно».
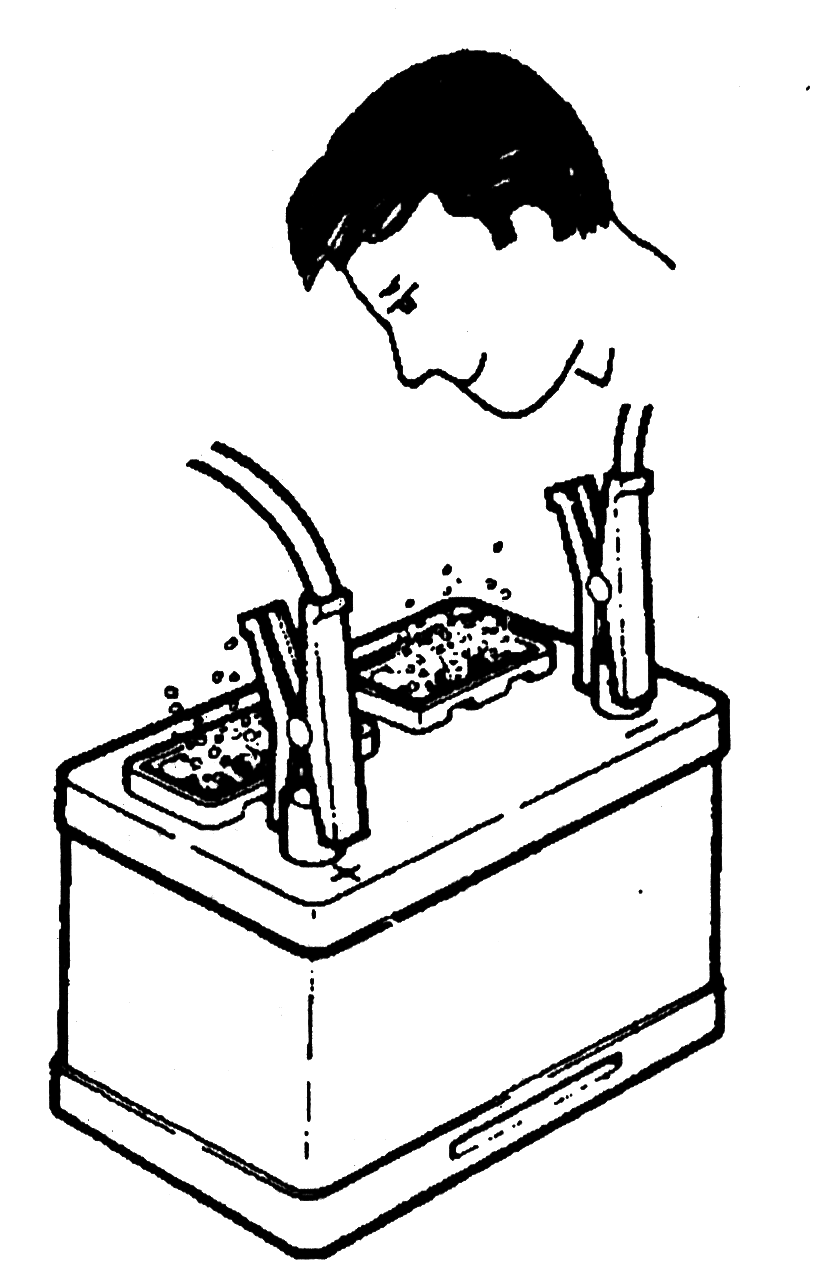
Меры безопасности: Аккумулятор «газит» - это значит, что пузырьки с отрицательной пластины выносят водород, а с положительной пластины кислород. Это очень опасный взрывчатый газ. Никогда не вносите открытый огонь!!! Это может вызвать взрыв.
И НИКОГДА. НИКОГДА НЕ КУРИТЕ ИЛИ ДАЖЕ НЕ ПЫТАЙТЕСЬ ЗАЖЕЧЬ СИГАРЕТУ В ПОМЕЩЕНИИ ДЛЯ ЗАРЯДКИ АККУМУЛЯТОРОВ
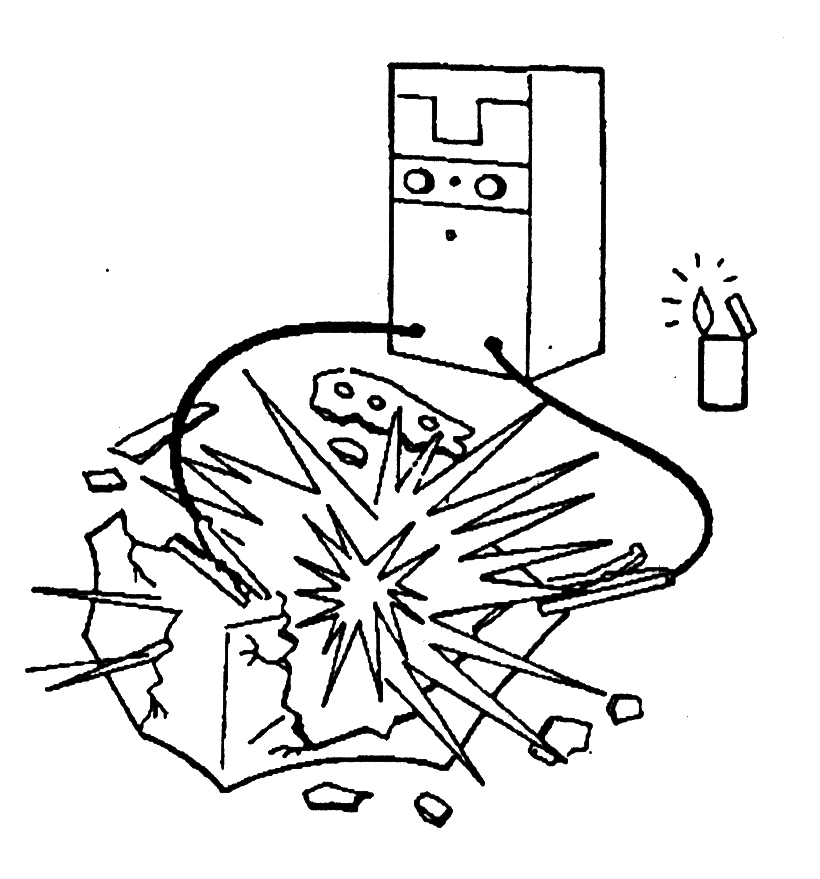

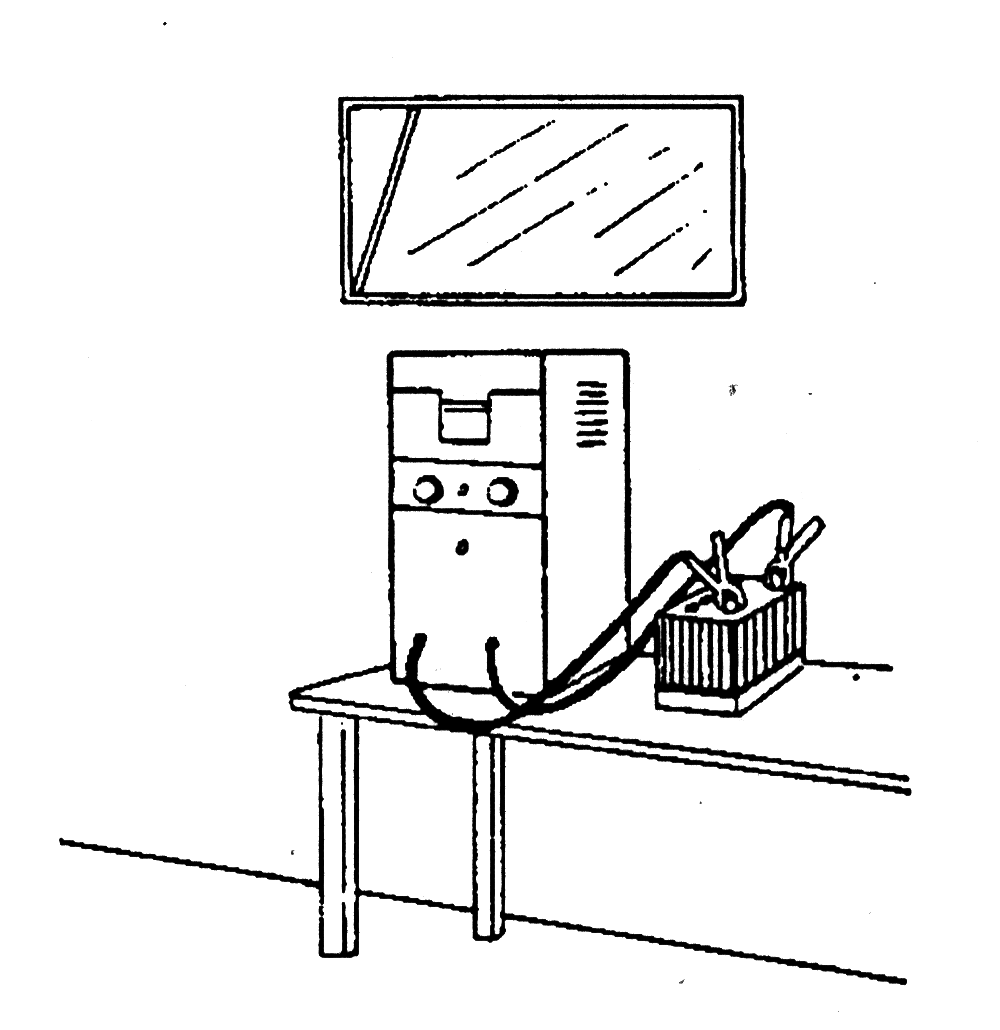
34. Зарядное помещение должно хорошо проветриваться. Должна быть хорошая циркуляция воздуха вверху помещения, так как этот крайне взрывоопасный газ легче воздуха и поднимается вверх.
35. Кроме того, чрезмерная зарядка аккумулятора повышает его температуру, при этом повышается температура активного материала в решетках, происходит нежелательное расширение, в результате чего часть активного материала отщепляется от пластин и падает вниз.
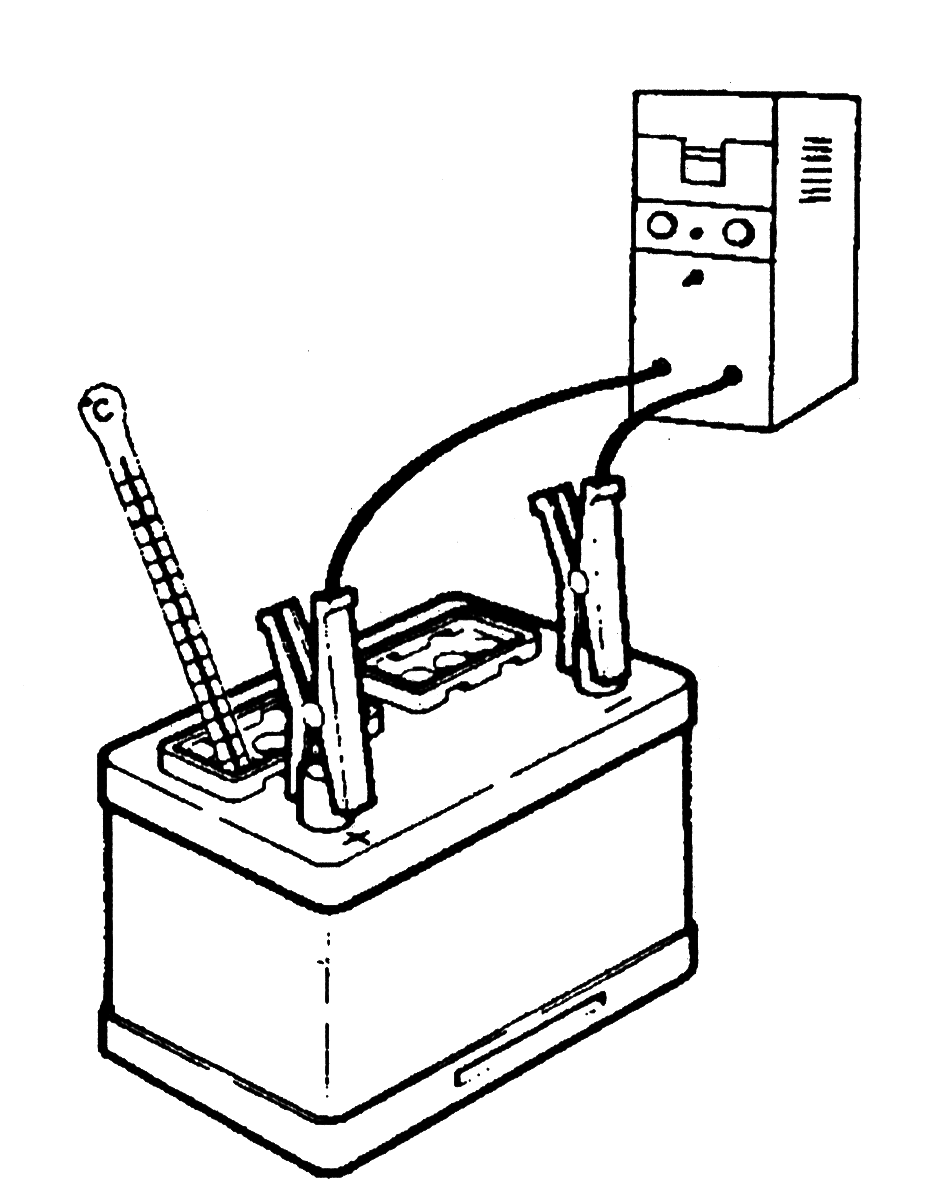
36. Химический процесс разложения воды вызывает некоторое шелушение активного материала отрицательной пластины, в результате гальванический эффект уменьшается. Это означает, что напряжение между положительной и отрицательной пластинами уменьшается, и это старит аккумулятор.
37. Разрядка аккумулятора происходит, когда заводят двигатель или...
38. ... включают радио, свет, стеклоочистители или любые другие электрические приборы, а автомобиль при этом стоит на месте.
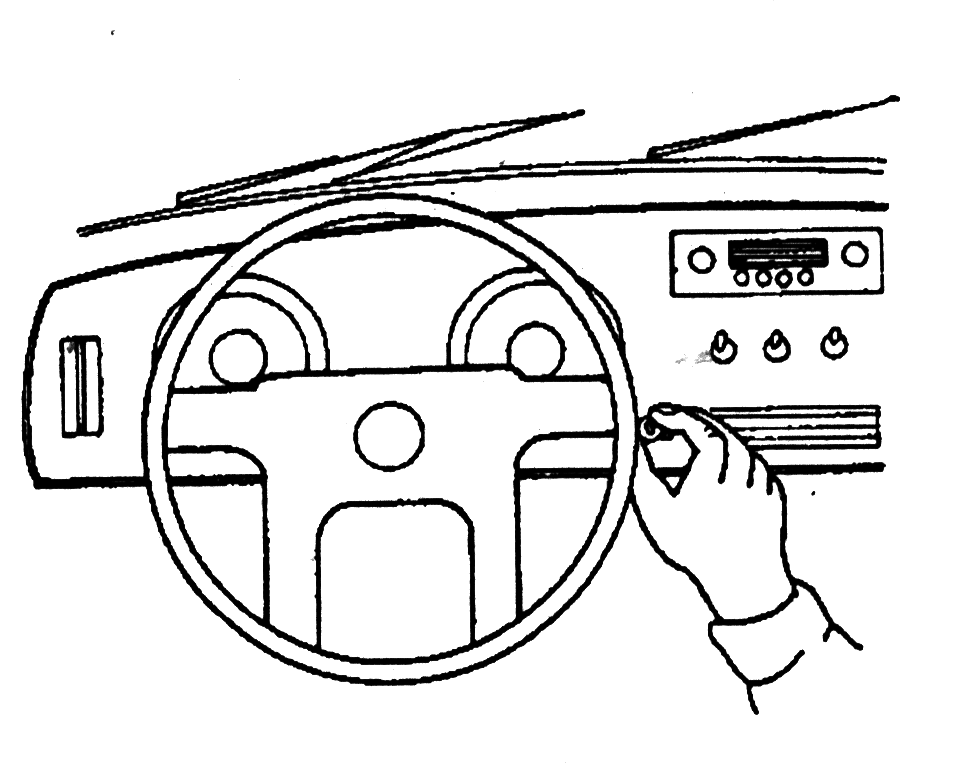
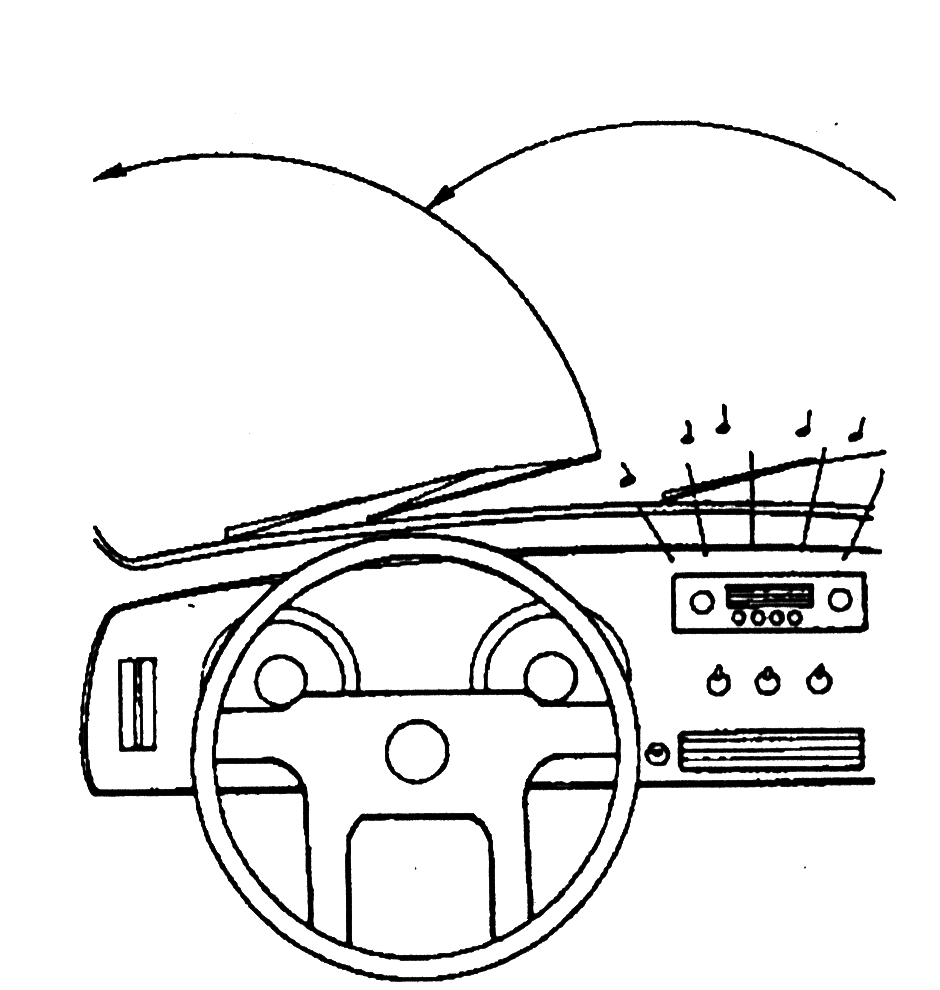
39. Когда автомобиль движется, генератор обеспечивает электричеством все электрические приборы и механизмы, за исключением тех случаев, когда прибор или механизм потребляет больше тока, чем генератор постоянного или переменного тока могут дать.
40. Например, плохо заводится двигатель автомобиля, который работает в тяжелых дорожных условиях, когда приходится очень часто останавливаться и двигаться вновь или когда автофургон выполняет много заказов в центре города, при этом аккумулятор разряжается всегда больше, чем его подзаряженный генератор постоянного тока на коротких участках пути.
41. Установка аккумулятора большего размера, как это рекомендуют некоторые механики, не решает проблемы. Это даже ухудшает положение. Настоящая проблема состоит в том, что из аккумулятора потребляется тока больше, чем его замещают генераторы постоянного и переменного тока при движении на коротких расстояниях.
42. Больший аккумулятор потребует большего времени для полной зарядки, т. е. движения автомобиля на большие расстояния.
43. Ответ на вопрос - более мощные генераторы. Эту проблему так именно и надо решать, когда автомобиль выполняет множество заказов по доставке грузов.
44. Здесь необходимо напомнить о том, что некоторые люди устраивают на автомобилях причудливую иллюминацию, которая дает дополнительную нагрузку на аккумулятор, и он разряжается. Поэтому не следует применять такую иллюминацию.

45. Давайте повторим: в полностью заряженной аккумуляторной батарее, в которой положительные пластины состоят из диоксида свинца РЬО2, а отрицательные пластины состоят из губчатого свинца РЬ, положительные и отрицательные пластины превращаются в сульфат свинца PbSO4, когда аккумулятор разряжается, т. е. при запуске двигателя и т. д.
46. Последующий процесс зарядки будет вновь превращать сульфат свинца (PbSO4) в диоксид свинца на положительных пластинах и в пористый свинец на отрицательных пластинах
47. Однако, если зарядка не происходит, то за короткое время мелкие кристаллы сульфата свинца (PbSO4), образовавшиеся в процессе разрядки, будут превращаться в крупные кристаллы сульфата свинца. Превратить эти крупные кристаллы обратно в мелкие очень трудно, и не все из них могут быть обращены.
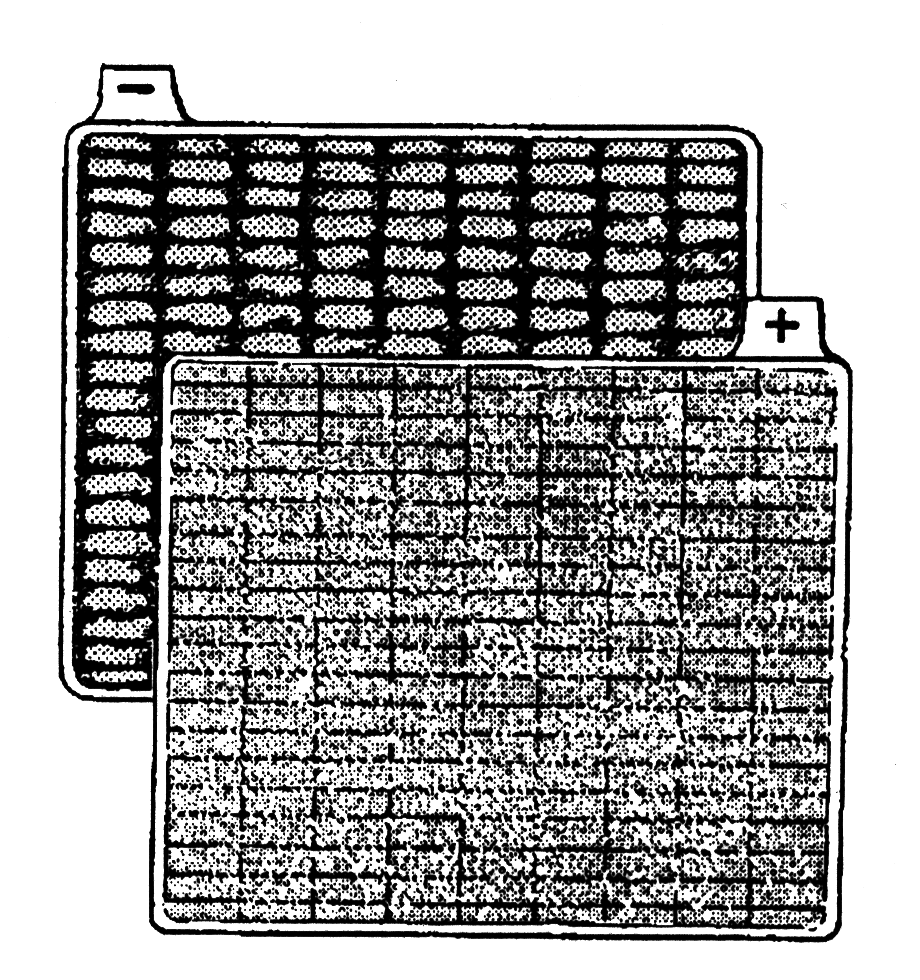
48. Положение становится еще более тяжелым, когда крупным кристаллам уже несколько дней. В этом случае говорят, что аккумулятор сульфатированный. Сульфатированная пластина покрыта крупными кристаллами сульфата свинца и выглядит серовато-белой.
49. Когда сульфатированный аккумулятор заряжается, он очень сильно нагревается.
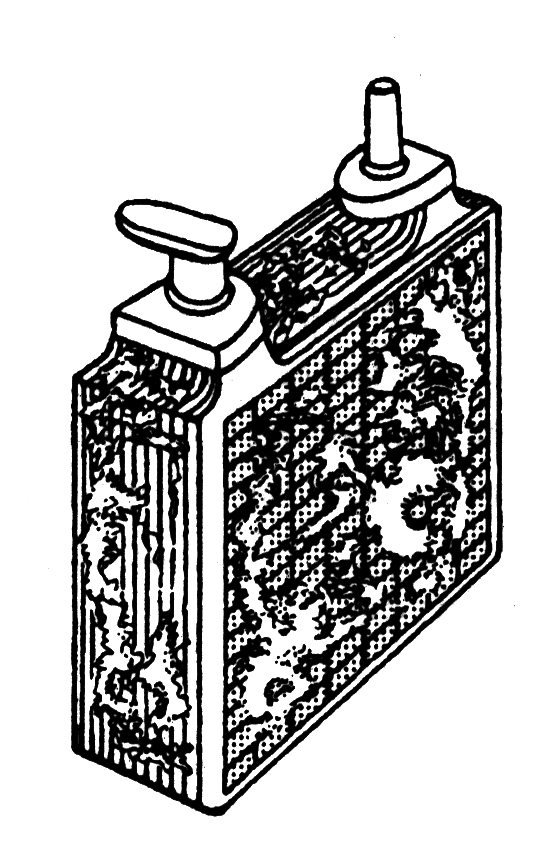
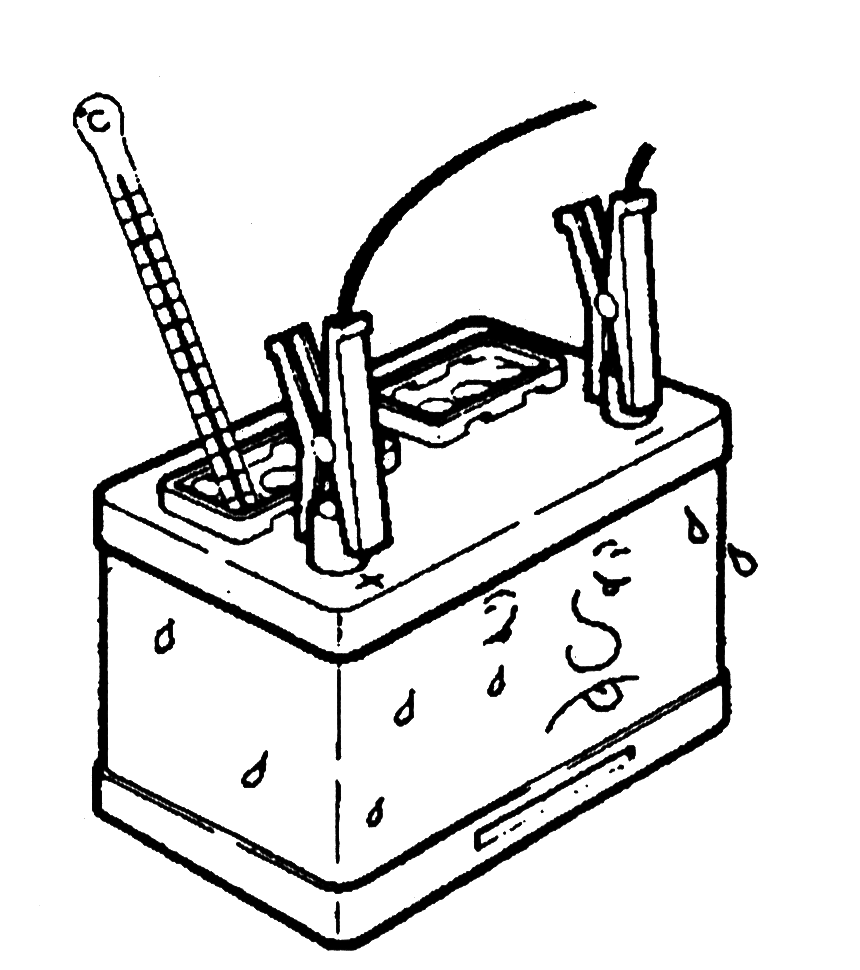
50. При незначительном сульфатировании сульфатирование можно устранить длительной зарядкой при низком уровне зарядного тока; однако, не весь активный материал в пластинах в состоянии сохранять энергию. Емкость аккумулятора снизится.
51. В более тяжелых случаях сульфатирования аккумуляторы становятся непригодными. Если сильно сульфатированный аккумулятор поставить на зарядку в зарядное устройство, напряжение зарядки быстро поднимется и аккумулятор сразу же начнет сильно «газить».
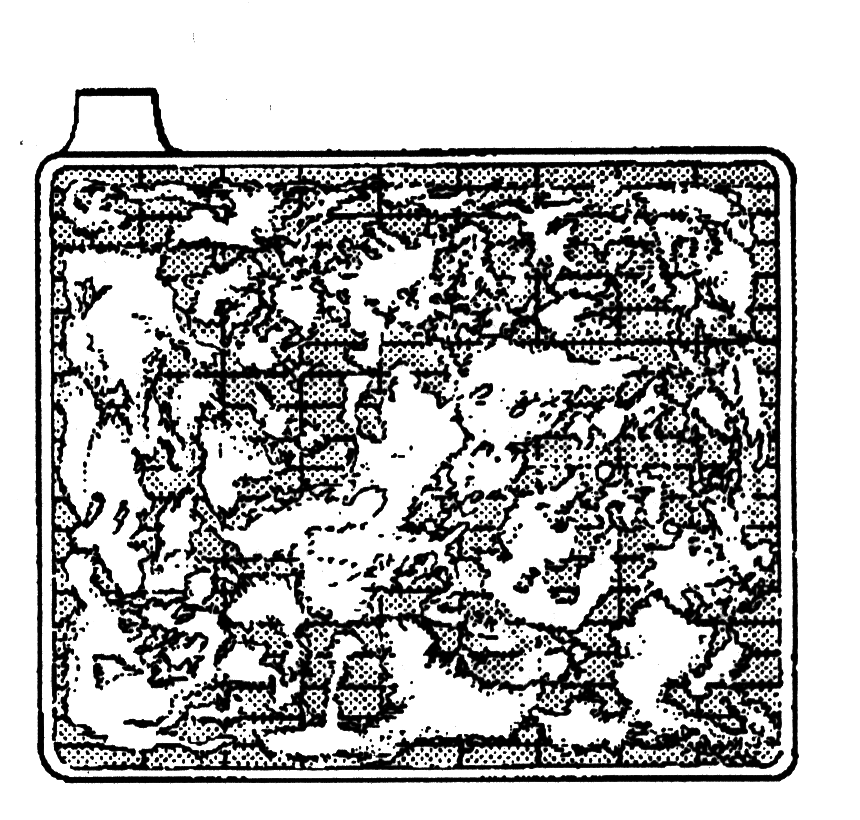
52. Помните, что новый аккумулятор, который оставлен на некоторое время в разряженном или полузаряженном состоянии, теряет свою емкость и даже становится непригодным.
На рисунке - «НОВЫЙ».
53. Аккумулятор должен быть подзаряжен вовремя!!! Следить за аккумулятором стоит дешевле, чем его заменить.
54. Полностью заряженная аккумуляторная батарея может медленно разряжаться сама. Эта «саморазрядка» различна у разных аккумуляторов и зависит от их срока службы и условий.
55. По этой причине полностью заряженную батарею, когда ее не используют, следует заряжать каждые две недели и подзаряжать, когда необходимо.
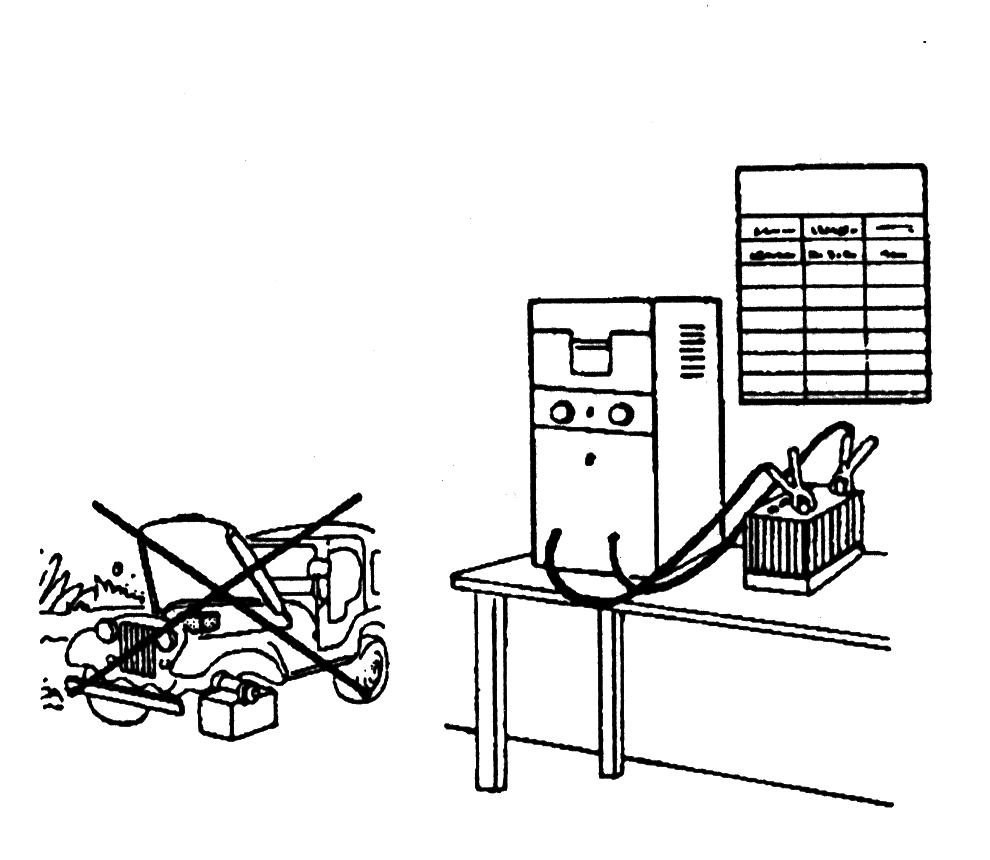
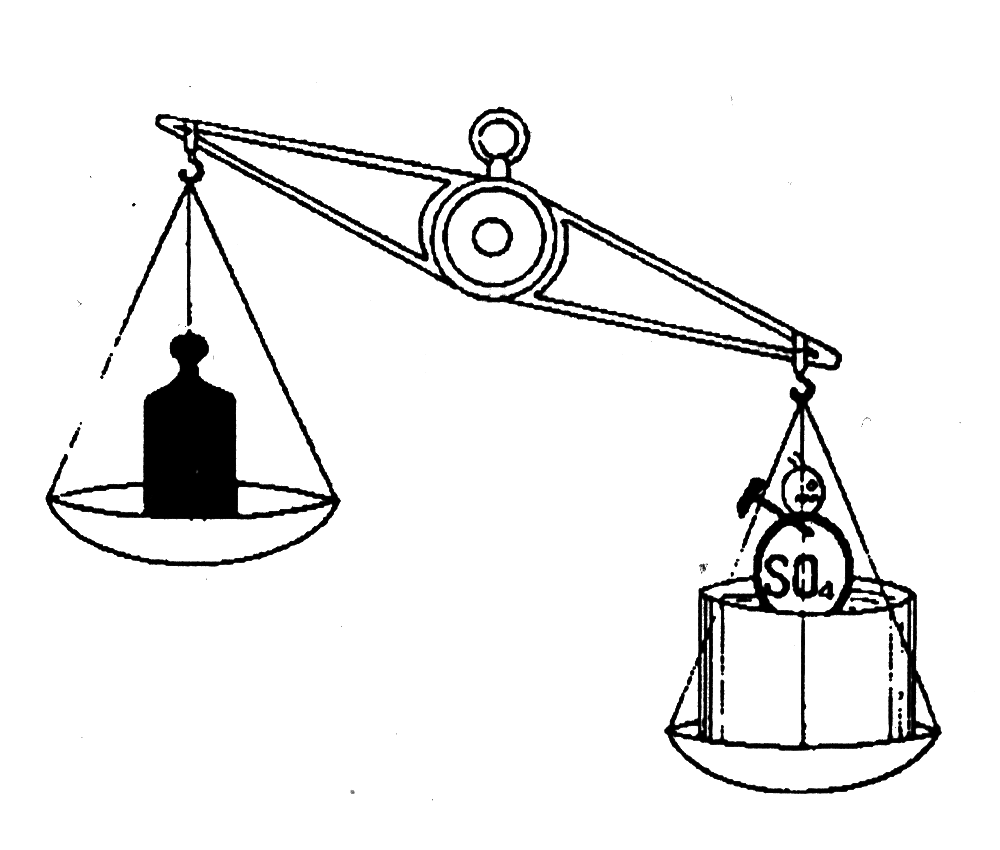
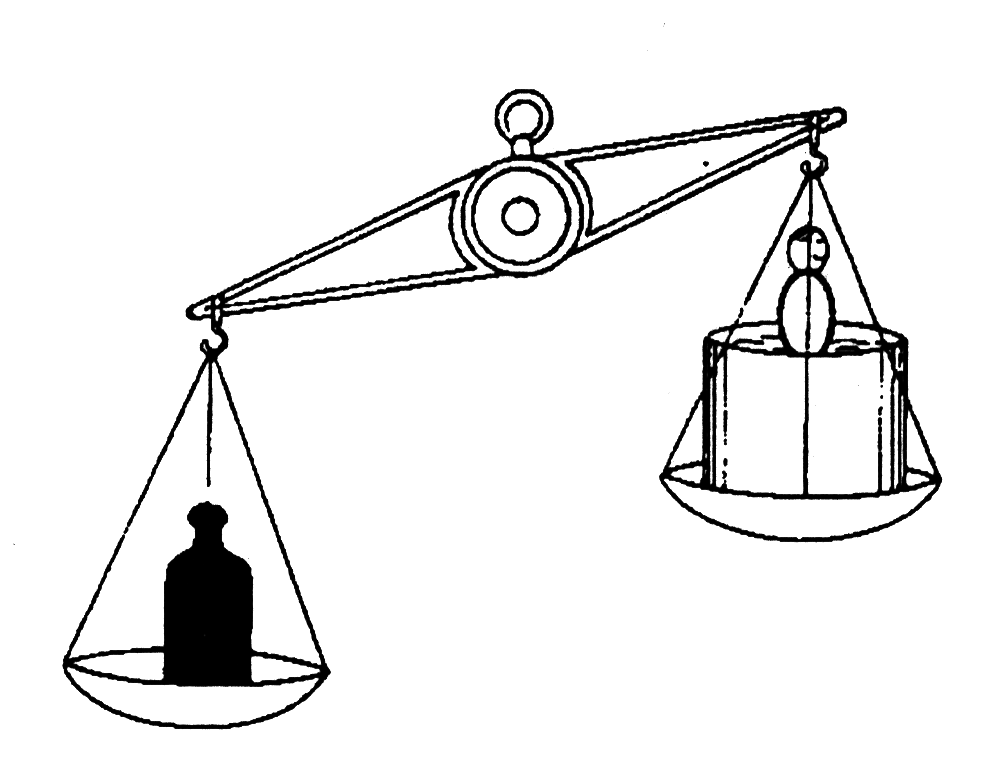
56. Как уже отмечали, зарядка аккумулятора увеличивает вес электролита, а разрядка аккумулятора уменьшает вес электролита.
57. Другими словами, если мы знаем вес электролита, то мы знаем степень зарядки аккумулятора. Вместо весов для проверки веса электролита используют ареометр. Поплавок (со специальной шкалой) в полости денсиметра позволяет определять плотность электролита
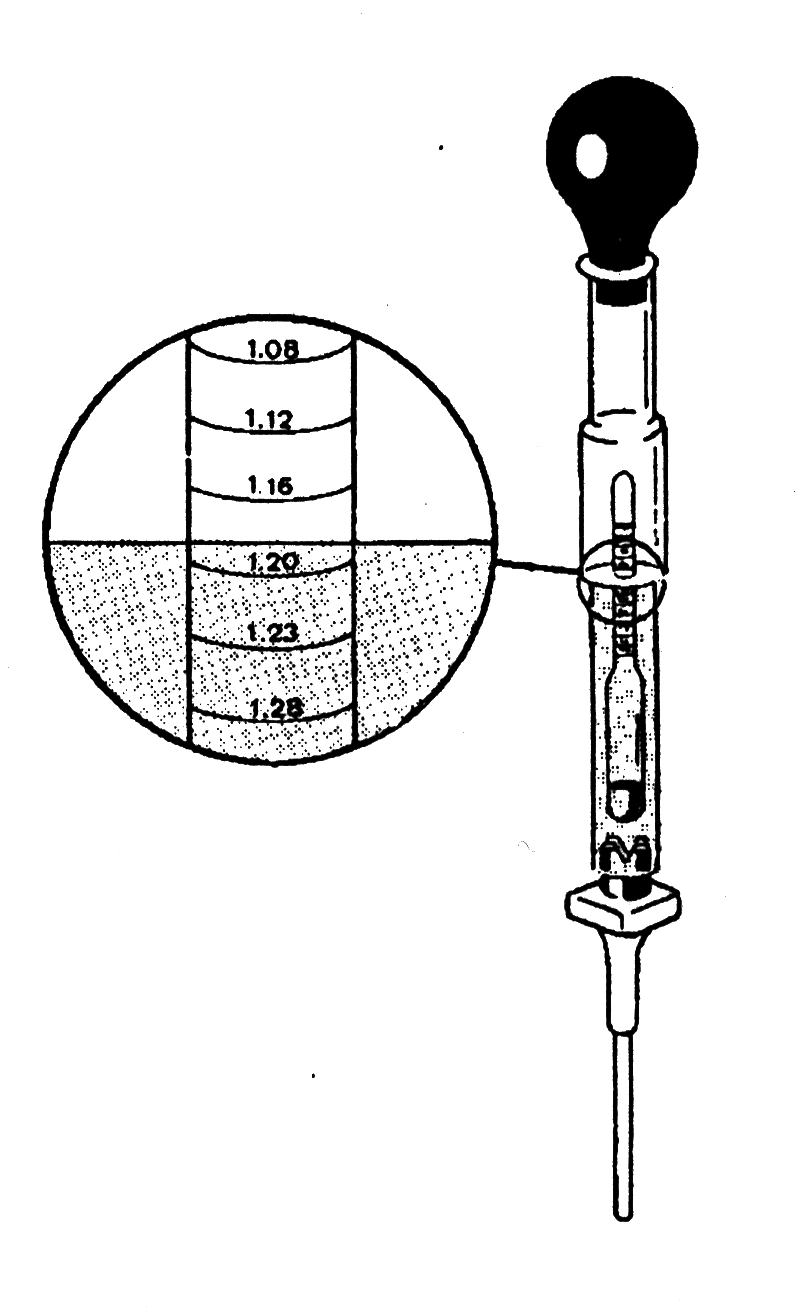
Следующая таблица даёт численные значения плотности электролита аккумулятора для различных стадий его зарядки.
Степень зарядки | Плотность при 20° С, г/см3 |
Заряженная аккумуляторная батарея Полузаряженная аккумуляторная батарея Разряженная аккумуляторная батарея | 1,28*) 1,20 1,12 |
* точность +0,01 г/см3
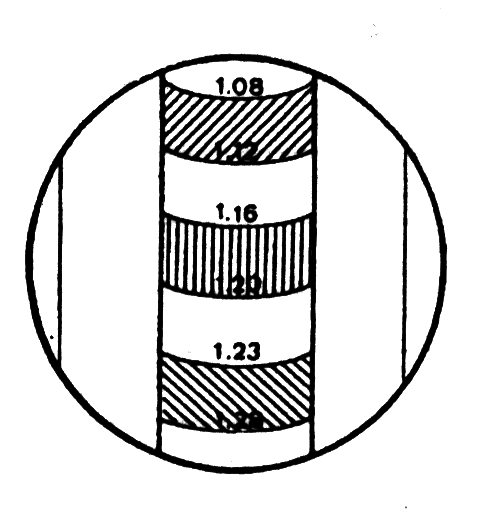
58. Когда плотность ниже 1,200 г/см3 (аккумулятор заряжен только наполовину) аккумулятор в опасности. Образование крупных кристаллов сульфата свинца началось.
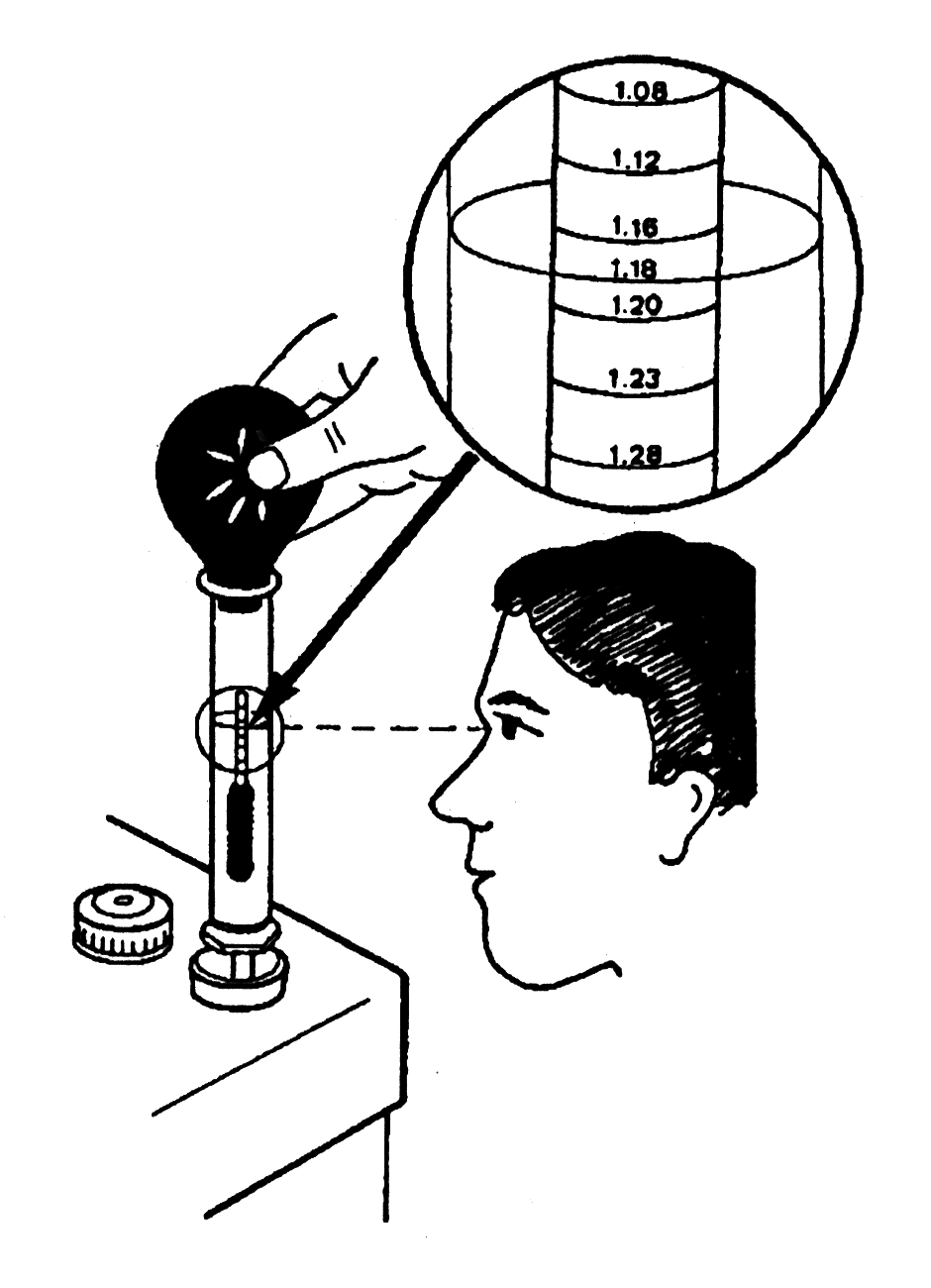
59. Попросите Вашего инструктора дать Вам несколько аккумуляторных батарей с различной степенью зарядки. Проверьте денсиметром каждую секцию и запишите результаты в таблицу, приведённую ниже:
№ аккумуляторной батареи | Плотность электролита в секциях | Комментарии | |||
1 | 2 | 3 | 4 | 5 | 6 |
В колонке «Комментарии» запишите, что Вы думаете о состоянии аккумулятора, например: «полностью заряжен» или «совершенно разряжен» и т. д.
60. Также отметим, что, если вверху пластины сухие, то даже у полностью заряженной батареи на сухой части пластин начинается сульфатирование, так как уровень электролита очень низкий.

61. Если уровень электролита не поправлен вовремя, то сухая часть пластин будет постоянно разрушаться и емкость аккумулятора будет снижаться.
Если Вы закончили чтение этого Учебного элемента и провели практическую работу по проверке плотности электролита в каждой секции различных аккумуляторных батарей и ясно представляете себе, как работают секции аккумуляторной батареи, ПОЗОВИТЕ ИНСТРУКТОРА и объясните ему кратко, что Вы узнали из этого Учебного элемента. Если Ваши объяснения удовлетворят его, то он позволит Вам приступить к Заключительной проверке.

ПРОВЕРКА УСВОЕНИЯ
Контрольные вопросы
Каждый вопрос имеет один или несколько правильных ответов. Выберите правильные.
1. Аккумуляторная батарея (свинцового типа) является вторичным устройством. Как мы можем назвать ее?
2. Какие из этих материалов являются проводниками второго класса?
3. Постоянный ток превращает сульфат свинца положительной пластины в:
4. Постоянный ток превращает сульфат свинца отрицательной пластины в:
5. Что увеличивает вес электролита?
6. Что вызывает сульфатирование пластин аккумулятора?
а) Аккумулятор.
б) Транзистор.
в) Трансформатор.
а) Медь.
б) Стекло.
в) Фарфор.
г) Электролит.
д) Воздух и вода.
а) диоксид свинца;
б) пористый свинец;
в) свинец.
а) диоксид свинца;
б) губчатый свинец;
в) свинец.
а) Процесс зарядки.
б) Процесс разрядки.
а) Чрезмерная зарядка аккумулятора.
б) Разрядка аккумулятора.
в) Оставление в неработающем состоянии разряженного или слабо заряженного аккумулятора в течение длительного периода.
7. Чрезмерная зарядка аккумулятора:
8. Автомобиль в тяжелых условиях уличного движения («остановился, поехал») плохо заводится из-за слабо заряженного аккумулятора. Как бы Вы решите эту проблему?
а) увеличит срок службы аккумулятора;
б) уменьшит срок службы аккумулятора;
в) вызовет электрическое разложение воды;
г) перегреет аккумулятор и вызовет осыпание активного материала;
д) обеспечит более легкий запуск двигателя;
е) уменьшит напряжение между положительными и отрицательными пластинами из-за вытеснения части активного материала;
ж) производит взрывчатый газ, который может взорваться, если вблизи окажется открытое пламя.
а) Уменьшите число запусков, (ненужных остановок и троганий с места).
б) Замените аккумулятор на другой с большей емкостью.
в) Исключите ненужное расходование тока на радио, лишнюю иллюминацию и т. д.
г) Обеспечите зарядку аккумулятора за короткие промежутки времени на подзарядном устройстве (ночью, например).
д) Установите другой генератор с более мощным выходом.
9. Каким образом можно избежать сульфатирования аккумулятора?
10. Что бы Вы порекомендовали сделать, если автомобиль стоит в гараже в ожидании запасных частей и аккумулятор не используется?
11. Когда литр электролита легче?
12. Какова плотность электролита полностью заряженного аккумулятора?
13. Аккумулятор автоматически сульфатируется, если плотность электролита ниже:
а) Поставить новый аккумулятор.
б) Хорошо заряжать аккумулятор.
в) Чрезмерно заряжать аккумулятор.
а) Аккумулятор следует снять с в автомобиля, проверять каждые две д недели и, если необходимо, заряжать.
б) Аккумулятор можно оставить в автомобиле первые три месяца, затем его следует проверить.
в) Это не имеет значения! Важно только, чтобы аккумулятор был хорошо заряжен, когда ставился на автомобиль.
а) Когда аккумулятор заряжен.
б) Когда аккумулятор разряжен.
в) Вес остаётся постоянным.
а) 1,45 г/см3
б) 1,40 г/см3
в) 1, 38 г/см3
г) 1,28 г/см3
д) 1,23 г/см3
е) 1,20 г/см3
ж) 1,16 г/см3
з) 1,12 г/см3
и) 1,08 г/см3
а) 1,45 г/см3
б) 1,40 г/см3
в) 1, 38 г/см3
г) 1,28 г/см3
д) 1,23 г/см3
е) 1,20 г/см3
ж) 1,16 г/см3
з) 1,12 г/см3
и) 1,08 г/см3
14. Что может уменьшить ёмкость аккумулятора?
15. Что следует сделать с сульфатированным аккумулятором
16. Плотность электролита измеряется:
а) Чрезмерная зарядка аккумулятора.
б) Сульфатирование пластин.
в) Применение электролита несоответствующей плотности.
а) Слабое сульфатирование можно уменьшить длительной зарядкой при умеренном токе.
б) Уменьшить содержание кислоты в электролите.
в) Сильно сульфатированный аккумулятор следует заменить.
г) Увеличить содержание кислоты в электролите.
а) вольтметром;
б) амперметром;
в) омметром;
г) денсиметром.



