1. Права и обязанности врача судебно-медицинского эксперта судебно-химического отделения бюро судебно-медицинской экспертизы.
Права и обязанности лиц, допущенных к производству химических судебных экспертиз Государственным судебным экспертом является аттестованный работник государственного судебно-экспертного учреждения, производящий судебную экспертизу в порядке проведения своих должностных обязанностей (ст. 12 ФЗ РФ от 01.01.2001 г. «О государственной судебно-экспертной деятельности в Российской Федерации»).
Должность эксперта в государственных судебно-экспертных учреждениях может занимать гражданин РФ, имеющий высшее профессиональное образование и прошедший последующую подготовку по конкретной специальности в порядке, установленном правовыми актами (ст. 13 ФЗ РФ от 01.01.2001 г. «О государственной судебно-экспертной деятельности в Российской Федерации»).
Обязанности эксперта (ст. 16 ФЗ РФ от 01.01.2001 г. «О государственной судебно-экспертной деятельности в Российской Федерации»):
Эксперт обязан:
- принять к производству порученную ему экспертизу,
- провести полное исследование представленных ему объектов, дать обоснованное заключение по поставленным перед ним вопросам,
- составить мотивированное письменное заключение о невозможности дать заключение, если поставленные вопросы выходят за пределы специальных знаний эксперта,
- не разглашать сведения, которые стали ему известны в связи с производством экспертизы,
- обеспечить сохранность представленных объектов исследований и материалов дела.
Эксперт не вправе:
- принимать поручения о производстве судебных экспертиз от кого-либо, за исключением руководителя государственного судебно-экспертного учреждения,
- осуществлять судебно-экспертную деятельность в качестве негосударственного эксперта,
- вступать в личные контакты с участниками процесса, самостоятельно собирать материалы для производства судебной экспертизы,
- сообщать кому-либо о результатах судебной экспертизы, за исключением органа или лица, её назначивших,
- уничтожать объекты исследований либо существенно изменять их свойства без разрешения органа или лица, её назначивших.
Права эксперта(ст. 17 ФЗ РФ от 01.01.2001 г. «О государственной судебно экспертной деятельности в Российской Федерации»):
Эксперт в праве:
- ходатайствовать перед руководителем государственного судебно-экспертного учреждения о привлечении к производству экспертизы других экспертов, если это необходимо,
- делать заявления по поводу неправильного истолкования участниками процесса его заключения или показаний,
- обжаловать действия органов или лиц, назначивших экспертизу, если они нарушают права эксперта.
Эксперт также исполняет обязанности и имеет права, предусмотренные соответствующим процессуальным законодательством.
2. Основные реакции 2 этапа метаболизма (примеры).
а) Конъюгация с глюкуроновой кислотой:
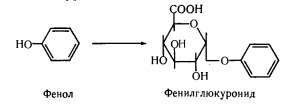
б) Метилирование:
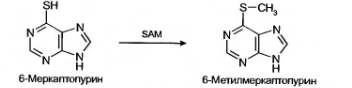
в) Конъюгация с аминокислотами:
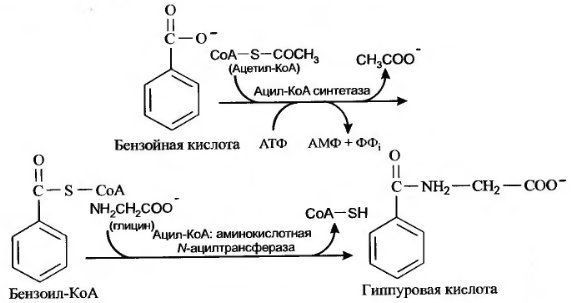
г) Сульфатирование:
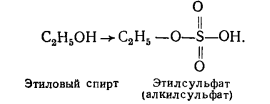
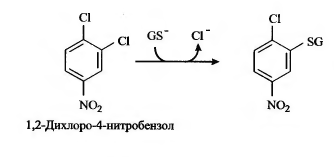
д) Конъюгация с глутатионом:
3. Дробный анализ на наличие ионов мышьяка: основные этапы, химические процессы, количественное определение.
В качестве ориентирующей реакции, имеющей только отрицательное значение, в дробном обнаружении мышьяка введена реакция Зангер – Блека, проведение которой осуществляется в течение 60 мин.
Реакция Зангер – Блека неспецифична для мышьяка, что ограничивает значение её в токсикологической химии, но высокочувствительна. Чувствительность реакции достигает 0,1 мкг мышьяка в исследуемом объёме. При отрицательном результате этой чувствительной реакции отпадает необходимость в проведении реакции Марша. При положительном результате, подтверждение обнаружения мышьяка реакцией Марша является обязательным.
Реакция Зангер – Блека позволяет сочетать качественное обнаружение мышьяка (при его малых количествах) с полуколичественным определением. Метод основан на восстановлении соединений мышьяка до гидрида мышьяка, который затем реагирует с хлоридом или бромидом ртути (II). Реакция выполняется в специальном приборе.
Восстановление соединений мышьяка производится водородом в момент его выделения, который получают при взаимодействии металлического цинка с кислотой серной:
H2SO4 + Zn → ZnSO4 + 2H+
Водород, образовавшийся при взаимодействии кислоты серной и цинка, восстанавливает соединения мышьяка до арсина (AsH3).
AsO2– + 7 H+ → AsH3 + 2H2O
AsO33– + 9 H+ → AsH3 + 3H2O
AsO43– + 11 H+ → AsH3 + 4H2O
Скорость восстановления соединений трёх– и пяти–валентного мышья-ка (арсенитов и арсенатов) водородом различна. Арсениты восстанавливаются водородом легче, чем арсенаты. В присутствии солей железа (II) или олова (II) арсенаты легко восстанавливаются в арсениты.
AsO43– + Sn2+ + 4 H+ ![]()
![]() AsO2– + Sn4+ + 2 H2
AsO2– + Sn4+ + 2 H2
AsO2– + 7 H+ → AsH3 + 2 H2O
Образовавшийся гидрид мышьяка реагирует с хлоридом или бромидом ртути (II), которым пропитана фильтровальная бумага. В результате этой реакции образуется ряд окрашенных соединений, которые окрашивают бумагу в виде жёлтого или коричневого пятна:
AsH3 + HgCl2 → AsH2(HgCl) + HCl
AsH3 + 2 HgCl2 → AsH(HgCl)2 + 2HCl
AsH3 + 3HgCl2 → As(HgCl)3 + 3HCl
AsH3 + As(HgCl)3 → As2Hg3 + 3HCl
Сероводород, выделяющийся при взаимодействии водорода с кислотой серной реагирует с хлоридом или бромидом ртути (II). В результате этой реакции образуется ртути (II) сульфид тёмно–коричневого цвета, который маскирует, имитирует окраску пятен. Для связывания сероводорода применяют вату, пропитанную раствором свинца ацетата:
H2S + Pb(CH3COO)2 → PbS + 2CH3COOH
Реакция Марша основана на восстановлении соединений мышьяка водородом в момент его выделения и на последующем термическом разложе-нии образовавшегося при этом гидрида мышьяка:
AsO2– + 7H+ → AsH3 + 2H2O
2AsH3 → 2 As + 3H2
Обнаружение мышьяка проводится на приборе Марша. Прибор Марша в современном варианте состоит из нескольких частей: конической колбы ёмкостью 150 мл, к горлу которой пришлифована капельная воронка и стеклянная трубка, согнутая под прямым углом; хлор–кальциевой трубки; восстановительной трубки, обычно называемой трубкой Марша. Восстановительная трубка изготавливается из тугоплавкого стекла или кварца и имеет в нескольких местах сужения (диаметр 1,5 мм), при внутреннем диаметре трубки 4 – 5 мм, а конец её согнут почти под прямым углом и оттянут.
Количественное определение мышьяка основано на восстановлении мышьяка в кислом растворе до мышьяковистого водорода и определении его: а) объемным методом или б) колориметрическим методом по Зангер—Блеку. Выбор метода определяется результатами обнаружения мышьяка.
а) Объемный метод — определение по избытку нитрата серебра, не вошедшего в реакцию с AsH3:
АsН3 + 6AgNO3 + 6NH4OH = 6Ag + Н3АsO3 + 6NH4NO3 + 3H2O
титрованием роданидом аммония в присутствии железоаммонийных квасцов.
Метод позволяет определять при содержании 10 мг мышьяка
92% и при I мг — 76% со средней относительной ошибкой 2,9%
и 11% соответственно в 100 г органа.
Гранина определения 1 мг.
б) Колориметрический метод основан на реакции Зангер—
Блека. Определяется при содержании 1 мг мышьяка в органе.
Граница определения 0,04 мг.
4. Основные этапы процесса минерализации биоматериала концентрированными кислотами. Химические превращения белков, жиров и углеводов на каждой стадии минерализации.
Минерализация - это окисление (сжигание) органического вещества (объекта) для освобождения металлов из комплексов с белками и другими соединениями.
Процесс разрушения биологического объекта протекает в 2 стадии:
1. Стадия деструкции, на которой происходит разрушение биологических субстратов организма (белков, жиров, углеводов) на составные части: белки разрушаются до аминокислот, углеводы (полисахариды) до ди - и моносахаридов жиры до глицерина и жирных кислот. Менее всего подвержены разрушению на первой стадии жиры. На первой стадии нагревание не должно быть сильным, чтобы избежать подгорания объекта или сильного пенообразования и выброса частиц объекта из колбы. Поэтому, в начале процесса колбу Къельдаля закрепляют над плиткой на расстоянии 1-2 см. Температура не должна превышать 110°С. Эта стадия непродолжительна по времени, длится от 15 до 40 минут. По окончании деструкции получается прозрачная желтовато-бурая жидкость, иногда с пленкой жира, т. к. на этой стадии все элементы объекта разрушены, кроме жиров.
На стадии деструкции концентрированная H2SO4 выполняет роль водоотнимающего средства, что приводит к нарушению структуры клеток и тканей, деформирует их. При этом она способствует повышению температуры кипения смеси и тем самым повышает окислительное действие концентрированной HNO3.
Роль окислителя на первой стадии выполняет концентрированная HNO3. Кислота азотная, свободная от окислов азота, что наблюдается в самом начале минерализации, почти инертна. Под влиянием индуцирующих веществ в процессе окисления биоматериала часть кислоты азотной разлагается до кислоты азотистой и оксидов азота, которые являются катализаторами окисления. Под их влиянием и с повышением температуры азотная кислота проявляет себя как сильный окислитель. Идет интенсивный автокаталитический процесс окисления органических веществ:
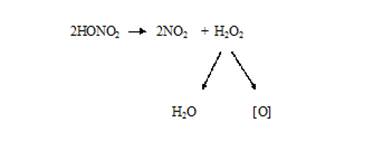
2. Стадия глубокого жидкофазного окисления. Колбу Къельдаля опускают на плитку и усиливают нагревание. На этой стадии происходит окончательное разрушение органических веществ. Полностью разрушаются и жиры, которые на первой стадии почти не пострадали под действием кислоты азотной. В процессе окисления необходимо по каплям постоянно добавлять в колбу разведенную кислоту азотную из капельной воронки, но при этом скорость добавления реактива должна быть такова, чтобы бурые пары окислов азота, образующиеся при минерализации, не выходили из колбы. Эта стадия длится 3-4 часа и считается законченной тогда, когда:
- начинает выделяться белый туман (пары SО2);
- жидкость остается бесцветной;
-минерализат не темнеет в течение 30 минут без добавления кислоты азотной.
Роль окислителя на этой стадии играет концентрированная кислота серная (её концентрация повышается в смеси до 60-70%, температура превышает 110°С). Она разлагается с выделением оксида серы (IV) и активного кислорода.
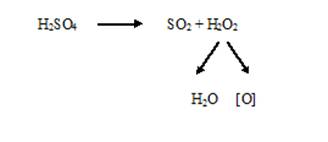
В процессе минерализации происходит не только разрушение органических веществ, но и ряд побочных реакций, имеющих негативное значение:
А) Кислота серная в высоких концентрациях сульфирует органические вещества, а кислота азотная, особенно в присутствии кислоты серной, - нитрует их. Сульфо - и нитросоединения очень прочные, трудно поддаются воздействию окислителей, что влечет за собой неполное разрушение биообъекта. Эти негативные процессы можно значительно уменьшить. Это достигается использованием не концентрированных кислот, а частично разбавленных добавлением в окислительную смесь воды (вспомните соотношение реагентов в окислительной смеси). При разбавлении Н2SO4 и HNO3 водой степень нитрования - сульфирования значительно снижается.
Б) Ещё одна побочная реакция связана с образованием нитрозилсерной кислоты при взаимодействии оксидов азота с концентрированной серной кислотой.
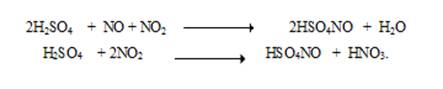
Нитрозилсерная кислота очень устойчива к температуре, однако легко гидролизуется. Реакция гидролиза обратима.
![]()
Нитрозилсерная кислота является источником окислителей в минерализате, что мешает в дальнейшем обнаружению некоторых катионов металлов. Чтобы избавиться от негативного воздействия нитрозилсерной кислоты, её удаляют путем проведение денитрации.
5. Методология ХТА при исследовании на неизвестный "летучий яд ".

Реакция образования берлинской лазури
NaOH + HCN → NaCN + H2O
FeSO4 + 2 NaCN → Fe(CN)2
Fe(CN)2 + 4 NaCN → Na4[Fe(CN)6]
3Na4[Fe(CN)4] + 4 FeCl3 → Fe4[Fe(CN)6]3 ↓ + 12NaCl
Реакция отщепления атома хлора
CHCl3 + 4NaOH → 3NaCl + HCOONa + 2H2O
NaCl + AgNO3 → AgCl ↓ + NaNO3
Реакция образования изонитрила
CHCl3 + C6H5NH2 + 3KOH → C6H5N=C + 3KCl + 3H2O
Реакция с нитропруссидом натрия
СH3СOСH3 + Na2[Fe(CN)5NO] + 2NaOH → Na4[Fe(CN)5ON=CHCOCH3] +
+2H2O интенсивное красное окрашивание
Реакция отщепления атомов хлора (в ампуле)
СH2Сl-CH2Cl + Na2CO3 +H2O → HOCH2-CH2OH + 2NaCl + CO2
HOCH2-CH2OH + KJO4 → 2HCHO + KJO3 + H2O

6. ХТА на группу одноатомных алифатических спиртов. Особенности количественного определения.
Для расчета концентрации спирта и других «летучих» ядов в исследуемой пробе ис - пользуют калибровочный график зависимости концентрации и соотношения высот (площадей) пика этанола («летучего» яда) к пику изопропанола (или пропанола). Калибровочный график строят ежедневно по 3-4 концентрациям анализируемого ядовитого вещества. Удобнее пользоваться величиной fR - фактора чувствительности или калибровочного
коэффициента, который является постоянным для данной пары веществ на каждой колонке и зависит от летучести определяемых веществ в условиях опыта.
Калибровочный коэффициент рассчитывается по формуле:
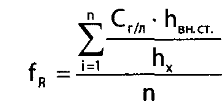
где Сг/л - концентрация спирта («летучего» яда), %о; hвн. ст - высота пика внутреннего стандарта пропанола или изопропанола; hх - высота пика определяемого спирта («летучего» яда); n - число измерений (обычно не менее трех).
Калибровочный коэффициент вводят в формулу расчета концентрации спирта («летучего» яда) в исследуемой пробе.
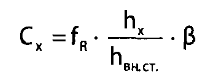
где Сх - концентрация спирта («летучего» яда) в пробе, %о; Лх - высота пика определяемого спирта («летучего» яда); hвн ст - высота пика внутреннего стандарта; fR - коэффициент пересчета водных растворов, на которых проводилось определение fR на исследуемый объект; для крови в=0,95, для мочи в=l,05.
7. Метод изолирования лекарственных веществ подкисленным спиртом /метод Стаса-Отто/.
100 г тщательно измельченного биологического материала вносят в широкогорлую колбу вместимостью 500 мл. заливают этиловым 96% спиртом до покрытия им твердых частиц исследуемого объекта. Смесь биологического материала и этилового спирта подкисляют 10% спиртовым раствором щавелевой кислоты. Содержимое колбы периодически перемешивают стеклянной палочкой. Через некоторое время проверяют рН содержимого колбы и при необходимости прибавляют 10% спиртовой раствор щавелевой кислоты до рН=2...3.
Колбу слегка закрывают пробкой, оставляют на сутки в теплом месте (25—30◦С) при периодическом перемешивании ее содержимого. После этого кислую спиртовую вытяжку сливают с биологического материала. Настаивание биологического материала с новыми порциями этилового спирта, подкисленного 10% раствором щавелевой кислоты до рН= 2...3, производят еще 3—4 раза (в течение суток каждый раз).
Кислые спиртовые вытяжки из биологического материала
соединяют и переносят в фарфоровую чашку. Биологический материал переносят на фильтр и промывают этиловым спиртом.
Этиловый спирт, которым промывают биологический материал,
присоединяют к полученным вытяжкам. Объединенные спиртовые вытяжки упаривают до густоты сиропа на водяной бане, нагретой до 40◦С. К сиропообразной жидкости при перемешивании стеклянной палочкой по каплям прибавляют этиловый спирт (96°) до прекращения выпадания примесей в осадок. Образовавшийся осадок отфильтровывают, фильтр промывают этиловым спиртом. Фильтрат снова упаривают на водяной бане до густоты сиропа, как указано выше. Из сиропообразного остатка примеси
осаждают этиловым спиртом. Упаривание спиртовых фильтратов
и осаждение примесей этиловым спиртом из сиропообразной жидкости проводят многократно (до прекращения осаждения примесей от прибавления этилового спирта).
К очищенной таким образом сиропообразной жидкости при-
бавляют 25 мл воды. Если при этом образуется осадок, его от-
фильтровывают.
Кислую водно-спиртовую жидкость переносят в делительную
воронку, прибавляют 10—15 мл хлороформа и легко взбалтывают
в течение 5 мин, а затем отделяют хлороформную вытяжку. Кислую водно-спиртовую жидкость еще 2—3 раза взбалтывают с новыми порциями хлороформа (по 10—15 мл). Хлороформные вытяжки из кислой водно-спиртовой жидкости соединяют и исследуют на наличие ядовитых соединений, экстрагирующихся органическими растворителями из кислой среды.
Оставшуюся в делительной воронке кислую жидкость подщелачивают 25 % раствором аммиака до рН = 9...10. Из этой подщелоченной жидкости алкалоиды и другие токсические вещества 3—4 раза экстрагируют новыми порциями хлороформа (по 10—15 мл). Хлороформные вытяжки соединяют и исследуют на наличие алкалоидов и некоторых других токсических веществ основного характера.
8. Химико-токсикологический анализ на производные 1,4-бенздиазепина.
При ненаправленном анализе на производные 1,4-бензодиазепина исследование проводится после изолирования из биологического материала подкисленным спиртом или подкисленной водой с хлороформным экстрактом из водной фазы с рН=2 и рН=10.
При рН=2 хлордиазепоксид полностью экстрагируется хлороформом, диазепам - частично, нитразепам и оксазепам экстрагируются хлороформом при рН=10. При проведении общего ТСХ-скрининга производные 1,4-бензодиазепина могут быть обнаружены на хроматографической пластинке в виде светящихся в УФ-свете пятен. При обработке реактивом Драгендорфа светящиеся пятна окрашиваются в оранжевый цвет.
С осадительными реактивами производные 1,4-бензодиазепина дают аморфные осадки. При исследовании извлечений из биологических объектов на производные 1,4-бензодиазепина используют 2 направления в анализе.
Первое направление основано на гидролизе бензодиазепинов до 2-аминобензофенонов. Данный способ позволяет обнаружить и определить в извлечении нативные соединения и их метаболиты. Этому направлению придают судебно-химическое значение при отрицательном результате.
2 направление используется, если в процессе исследования обнаружены бензофеноны по 1 направлению анализа. Этот способ позволяет точно установить природу 1,4-бензодиазепина по нативным соединениям и их метаболитам.
Определение 1,4-бензодиазепинов после гидролиза
Для проведения гидролиза могут быть использованы непосредственно ткани органов, хлороформные экстракты из подкисленных вытяжек и элюаты при применении сорбционного метода.
Определенный объем элюата или экстракта выпаривают досуха. К сухому остатку, навеске ткани органа, к 10 мл мочи или 2 мл крови прибавляют 2 мл 6 М раствора хлороводородной кислоты. Смесь нагревают на кипящей водяной бане в течение 1ч или 5-10 мин на глицериновой (песчаной) бане при 120°С. При наличии в объекте производных 1,4-бензодиазепина раствор окрашивается в желтый цвет за счет образования бензофенонов.
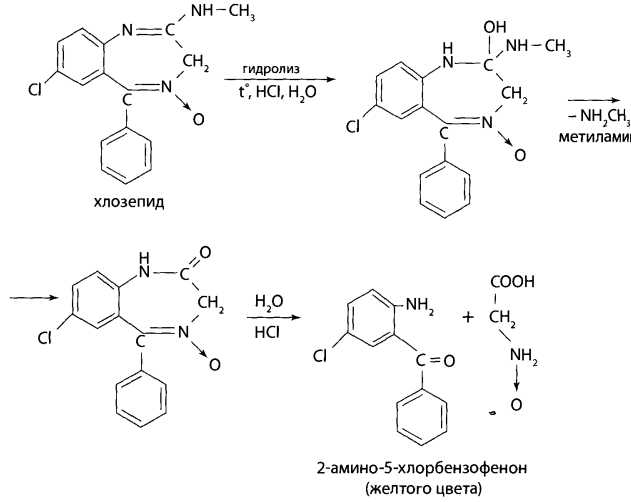
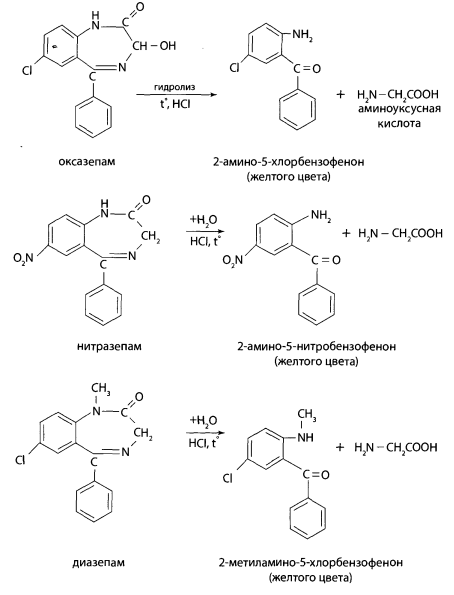
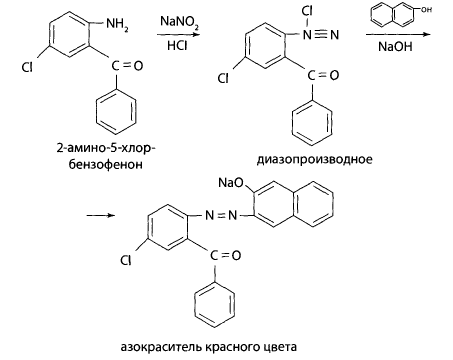
К части гидролизата после охлаждения добавляют каплю 5% раствора нитрита натрия, перемешивают. Несколько капель полученного раствора вносят в 2 мл свежеприготовленного 2% щелочного раствора резорцина или в-нафтола - наблюдают образование вишнево-красного окрашивания или оранжево-красного осадка.
Продукт гидролиза диазепама (2-метиламино-5-хлорбензофенон) не образует азокрасителя, так как имеет заместитель - метальную группу в положении 1. В присутствии диазепама раствор может сохранить желтую окраску.
Вторую часть гидролизата осторожно подщелачивают 50% раствором гидроксида натрия до рН=10-11 и экстрагируют гексаном. Гексановые экстракты выпаривают досуха при комнатной температуре, остаток растворяют в небольшом объеме этанола и исследуют с помощью ТСХ - и УФ-спектрофотометрии.
Хроматографию проводят на пластинках «Силуфол». В качестве подвижной фазы используют бензол, которым предварительно насыщают хроматографическую камеру в течение 10 мин. Раствор экстракта из гидролизата наносят на стартовую линию пластинки и одновременно в качестве «свидетелей» - бензофеноны, полученные при гидролизе стандартных веществ - бензодиазепинов (по 10-15 мкг каждого). После хроматографирования бензофеноны первоначально фиксируют на пластинке по собственному желтому окрашиванию. При просматривании пластинки в УФ-свете бензофеноны обнаруживают характерную флуоресценцию. Затем проводят непосредственно на пластинке реакцию Браттона-Маршалла. Хроматографическую пластинку последовательно опрыскивают 0,1% раствором нитрита натрия, 2 М раствором хлороводородной кислоты.
Через 1-2 мин обрабатывают 2% щелочным раствором в-нафтола. Флуоресцирующие пятна на пластинке окрашиваются в оранжево-красный цвет. Пятна 2-метиламино-5-хлорбензофенона не переходят в красно-оранжевый цвет, но при обработке хроматограммы 10% раствором хлорной кислоты дают яркую флуоресценцию в УФ-свете при
254 и 360 нм.
Предел обнаружения производных бензодиазепина составляет 1-5 мкг исследуемого вещества в пробе, нанесенной на пластинку.
УФ-спектрофотометрия используется после проведения ТСХ и элюирования бензофенонов с пластинки спиртом или ацетоном. Бензофеноны имеют характерную абсорбцию в области 230-240 и 390-410 нм.
Описанное исследование по 1 направлению имеет судебно-химическое значение при получении отрицательного результата. При получении положительных испытаний по 1 направлению проводят дальнейший анализ.
Задачи
1. В загородном доме через несколько часов после начала застолья была обнаружена компания молодых людей в невменяемом состоянии. Родители одного из участников «пира» вызвали «скорую помощь». К приезду врача двое молодых людей, наиболее крепкого телосложения, пришли в себя и от госпитализации отказались, остальные были доставлены в клинику и через две недели выписаны.
Отказавшиеся от госпитализации молодые люди вечером следующего дня всё же попали в больницу, где скончались через неделю, несмотря на интенсивное лечение по поводу отравления …../?/.
Для судебно-химического исследования доставлены внутренние органы, кровь, моча пострадавших, а также остатки прозрачной, без запаха жидкости в бутылке. Проведено судебно-гистологическое исследование тканей трупов, результаты которого были идентичны результатам химико-токсикологического исследования: отравление технической жидкостью -……/?/. Результаты анализа технической жидкости, находящейся в бутылке, следующие. При реакции с Cu(OH)2 образуется прозрачный раствор ярко синего цвета, не изменяющийся при нагревании; при окислении этого вещества перманганатом калия в кислой среде образуется кислота. Кальцевые соли этой кислоты обнаружены как при судебно-гистологическом исследовании тканей трупов, так и в ходе химико-токсикологического исследования.
• Представьте схему химико-токсикологического исследования внутренних органов трупов.
2. В суд.-химическое отделение поступили объекты (печень с желчным пузырем, почка, желудок, кровь, моча) трупа гр. А. Рядом с трупом обнаружена пустая упаковка таблеток Нозепам. Представить формулу вещества, описать физ.-хим. свойства. Выбрать объекты и описать изолирование. Предложить схему ХТА.
3. В клинико-токсикологическую лабораторию Центра лечения отравлений поступили объекты (кровь, моча) гр. В. Предполагается отравление аминазином. Представить формулу вещества, описать физ.-хим. свойства. Выбрать объекты и описать изолирование. Предложить схему ХТА.
4. В суд.-химическое отделение поступили объекты (печень с желчным пузырем, почка, желудок, кровь, моча) трупа гр. А. Диагноз – отравление неизвестным лекарственным веществом. Предложить схему ХТА.
В результате ХТА обнаружен кофеин в печени, почке, крови и моче.



