Публикация доступна для обсуждения в рамках функционирования постоянно
действующей интернет-конференции “Бутлеровские чтения”. http:///readings/
УДК 546.05.543.4.548.54. Поступила в редакцию 12 июня 2017 г.
Биомиметические композиты на основе карбонатапатита, альбумина и желатина биомедицинского назначения
© Герк+ Светлана Александровна, Голованова* Ольга Александровна
и
Кафедра неорганической химии. Омский государственный университет им. . Проспект Мира, 55-А, г. Омск, 644077. Россия. Тел.: (3812) 268-199.
E-mail: *****@***ru, *****@***ru
_______________________________________________
*Ведущий направление; +Поддерживающий переписку
Ключевые слова: композиты, биоматериалы, гидроксиапатит, белок, альбумин, желатин, кристаллизация, термодеструкция, резорбция, изоморфизм.
Аннотация
В настоящей работе получены биокомпозиты методом осаждения из прототипа биожидкости человека при варьировании концентрации альбумина и желатина. Материалы, синтезированные из сред с альбумином и желатином ( 7 г/л) представлены карбонатгидроксиапатитом и биополимером, а из растворов содержащих > 7 г/л желатина, включают 10 % масс. витлокита и состоят из кристаллитов меньшего размера. Показано, что присутствие белков приводит к осаждению композитов с меньшей степенью кристалличности и площадью удельной поверхности. Исследована кинетика растворения композитов в нейтральной и слабокислых средах. Установлено, что резорбируемость в 0.9% NaCl биокомпозитов не зависит ни от природы биополимера, ни от его концентрации в растворе. Порошки, полученные из вязко-упругих сред растворяются с большей скоростью в ацетатном буферном растворе.
Объём аннотации посылаемой в печать статьи должен быть 200-250 слов. Количество слов в аннотации можно узнать в MS Word 2003 выделив текст, войти в информационной панели в Сервис и затем в Статистику. В MS Word 2007, выделяют весь текст аннотации и на нижней информационной панели нажимают на секцию “Число слов”, в возникшем статистическом окошке смотрят численное значение.
Введение
В последние годы интенсивно развивающимся направлением науки и техники является создание биоадекватных имплантатов для восстановления структуры и целостности кости человека. Первоначально главной была идея прямого замещения костного дефекта биомате-риалом, в настоящее время определяющим стал подход регенеративной медицины, базирую-щийся на использовании биорезорбируемых материалов, способных инициировать регене-рацию костной ткани и замещаться вновь образованной [1-4]. Перспективными в этом плане являются композиты на основе фосфатов кальция и естественных биополимеров, сочетающих в себе структуру и свойства кости человека [5, 6]. Известно, что костная ткань помимо опорной функции, выполняет роль биоактивной матрицы, внутри которой протекают различ-ные сложные биохимические процессы с участием живых клеток. Она представляет собой композит, неорганическая фаза которого представлена нанокристаллами карбонатгидрокси-апатита (КГА) пластинчатой формы (с размером 5-10 нм), кристаллизующимися на волокнах коллагена из внеклеточной жидкости, в состав которой входят неорганические ионы (Са2+. РО43-, CO32-, K+, Na+ так далее,), белки, моно - и полисахариды, жиры и так далее [7-11]. Органическая компонента кости состоит из белка коллагена I типа (≈95%), неколлагеновых белков (альбумина – основная часть, протеогликанов, гликопротеинов), гликозаминогликанов, органических и нуклеиновых кислот и тому подобное. В рамках регенерационного подхода применение органических веществ для получения биоматериалов особенно актуально, поскольку, позволяет улучшить не только их биосовместимость, механические свойства, но и довольно часто резорбируемость биорезистивной неорганической компоненты кости – ГА, то есть компоненты, сложно растворяющейся в организме при имплантации [10, 12]. В настоя-щее время перечень органических веществ, применяемых для решения данной проблемы достаточно разнообразен: белки (коллаген, желатин, неколлагеновые белки), полисахариды (хитин, хитозан, гиалуроновую кислоту, альгинат, крахмал, хондроэтин), синтетические полимеры (полилактиды, поликапролактон, полиэтилен и другие) [10, 11, 13-18]. Однако, до сих пор не найдено оптимального сочетания между природой биополимера, способом получения композита и его свойствами.
Цель работы: биомиметический синтез композитов КГА-белок путем варьирования концентраций альбумина и желатина в прототипе синовиальной суставной жидкости человека (синовии).
Экспериментальная часть
В основе методик получения композитов материалов лежит термодинамическая модель осаждения малорастворимых соединений из прототипов синовиальной биожидкости (синовия) [19]. Синтез композитов, проведен из раствора, соответствующего по ионно-электролитному составу, рН (рН = 7.40±0.05) и ионной силе синовии человека при пятидесятикратном пересыщении по ионам Са2+ и НРО42- относительно физиологического значения. Проведено три серии модельных экспериментов. В первой серии синтезов получены образцы без органического полимера (контрольные); во второй – в исходный раствор, содержащий анионы (HPO42-, HCO3-, Cl-, SO42-) добавлялся альбумин (сывороточ-ный бычий альбумин марки А, БСА, диапазон концентраций от 2.5 до 12 г/л), в третьей – желатин (высокомолекулярный, диапазон концентраций – от 5 до 10 г/л). При выборе альбумина руководст-вовались его содержанием в биожидкостях (синовии и плазме крови) [20-22]. Поскольку осаждение кристаллического карбонатгидроксиапатита в живом организме происходит на коллагеновых волокнах [4, 23, 24]. В качестве наиболее доступного реагента выбрана нерастворимая форма коллагена – желатин [10-11]. Раствор, содержащий анионы и органическое вещество, проливали к раствору с катионами кальция и магния со скоростью 5 мл/мин. Корректировка кислотности среды осущест-влялась 10%-ным раствором HCl. Время кристаллизации твердых фаз составляло 7 суток. По чего, осадки отделяли от раствора фильтрованием, трехкратно декантировали и высушивали при 80 °С до постоянной массы.
Фазовый состав порошков исследовали на дифрактометре D8 Advance (Bruker). Съёмку проводили с использованием Cu-kб излучения с позиционно-чувствительным детектором Lynxeye при следующих режимах измерения: шаг сканирования – 0.05о, время накопления сигнала – 4 сек/точке, div. slit = 0.5, напряжение и ток накала 40 kV и 40 mA, соответственно; область сканирования 2и: 5-80о. Расшиф-ровка полученных дифрактограмм проведена с использованием базы данных по порошковой дифрак-ции ICDD PDF-2 (2006 г., программный пакет EVA, Bruker). Кристаллохимические параметры определены по методу наименьших квадратов (метод ЛеБэйля, программный пакет TOPAS 4.2., Bruker). Содержание присутствующих фаз в образцах определяли по методу корундовых чисел (метод Чанга, программа CrystallographicaSearch-Match). Оценка величины областей когерентного рассеяния (ОКР или D, минимальных размеров кристаллитов) осадков была произведена по формуле Дебая-Шеррера по рефлексу (002) в соответствии с формулой:
D = k λ /βm cosΘ, (1)
где D – средняя величина кристаллита (Е), которая зависит от его формы и направления [hkl]
и связана с истинным размером через константу k ≈ 0.9, λ – длина волны рентгеновского излучения (Cu Kб1.2 = 1.5406 Е),), βm – интегральная ширина линии рефлекса; и – брегговский угол дифракционной линии (002) [25, 26].
ИК-спектры осадков регистрировали на спектрофотометре ФСМ-2202 (Инфраспек, Россия) в диапазоне 400-4000 см-1 с шагом сканирования 1 см-1. Образцы готовились методом прессования таблеток с КВr (осч.). Исследование микроструктуры и микротекстуры порошков проведено с помощью оптической микроскопии (бинокулярный микроскоп XSP-104, видеоокуляр ToupCam UCMOS03100KPA) и скани-рующей электронной микроскопии с применением детектора вторичных электронов при ускоряющем напряжении 10 кВ (СЭМ, микроскопа JSM-6610LV, “JEOL”). Термический анализ проводился на синхронном термическом анализаторе STA-449C «NETZSCH». Количественные данные массовых потерь при отжиге получены с помощью программного обеспечения Proteus 7.10. Удельная поверх-ность образцов исследована на анализаторе Сорбтометр (, Россия) по методике одноточечной адсорбции азота при 77.4 К. Расчет полученных величин Sуд. (м2/г) выполнен по методу БЭТ.
Моделирование пассивной («медленной») и активной («быстрой», при участии остеокластов) фаз резорбции полученных порошков осуществлялось путем динамического растворения образцов «статическим» методом при постоянном перемешивании в растворе 0.9 %-ного хлорида натрия (рН ≈ 7) и ацетатном буфере (pH = 5.5) [27, 28]. С помощью прямой потенциометрии фиксировали значение рН и рСа в растворе.
Результаты и их обсуждение
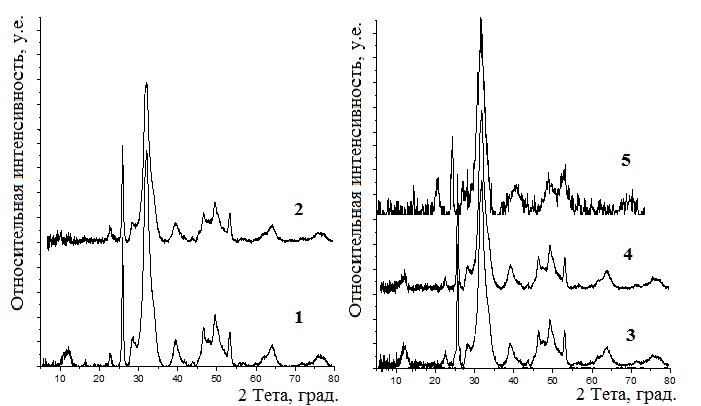
Установлено, что присутствие альбумина и желатина (менее 7 г/л) в модельном растворе не оказывает влияния на фазовый состав полученных осадков (рис. 1). Оценка содержания фаз по методу корундовых чисел показала, что основной фазой всех полученных осадков является плохоокристаллизованный или/и высокодисперсный гидроксиапатит (ГА, Ca10(PO4)6(OH)2, JCPDS, №73-293). В составе образцов присутствует рентгеноаморфная компонента в виде аморфного фосфата кальция. Уширение основных максимумов (002), (121) и (112) ГА в области 25-30 градусов по 2и на дифрактограммах композитов ГА-альбумин, свидетельствует о формировании фазы с меньшей степенью кристалличности. Для желатинсодержащих образцов характерна наибольшая аморфность (наименьшая степень кристалличности). Композиты, синтезированные при концентрации желатина в растворе 7 г/л и более являются двухфазными. Помимо компоненты ГА содержат до 10 % масс. витлокита (Ca18Mg2H2(PO4)14, Card 70-2064). Можно предположить, что в среде желатина из-за высокой вязкости затруд-нены диффузионные процессы, и как следствие, замедляются процессы роста частиц и перекристаллизации метастабильной фазы фосфата кальция в ГА.
|
Рис. 1. Дифратограммы контрольного образца (1), синтезированных в присутствии 5 г/л (2), 7 г/л (3), 10 г/л (4) альбумина; 10 г/л желатина (5). |
Показано, что наличие белков в модельной среде менее 7 г/л не влияет на кристалло-химические параметры полученных агрегатов (табл. 1). Композиты, как и контрольные образцы близки к нестехиометричным карбонатсодержащим кальцийдефицитным гидрокси-апатитам (JCPDS №46-0905), в том числе, составляющим минеральную основу костной ткани человека. Для таких апатитов характерен смешанный АБ-тип замещения структурных анионов карбонатными группировками (А-тип: 2OH - = VOH + CO32-.; В-тип: Са2+ + 2РО43- = VCa + 2CO32-; [10, 27]. При максимальных концентрациях белков в растворе (альбумина – 12 г/л, желатина – 10 г/л) в структуре композитов можно отметить небольшое расширение элементарной ячейки вдоль оси а, при этом параметр с, величина с/а и объем самой ячейки не изменяются. Возможно, происходит формирование карбонатгидроксиапатита преимущественно А-типа, что сопровождается сменой пространственной группы P63/m на P21/b [10].
Табл. 1. Кристаллографические параметры решетки, размеры кристаллитов ГА
ГА | Ось а, Е | Ось с, Е | с/а | V, Е | D, нм |
Контрольный образец | 9.459±0.002 | 6.874±0.002 | 0.726 | 532.6±0.726 | 2.57 |
С альбумином, г/л: 5 7 12 | 9.461±0.002 9.460±0.002 9.473±0.002 | 6.878±0.002 6.879±0.002 6.877±0.002 | 0.727 0.727 0.726 | 533.2 ±0.715 533.1±0.725 534.4±0.721 | 2.34 3.00 3.51 |
С желатином, г/л 5 7 10 | 9.455±0.001 9.463±0.001 9.466±0.002 | 6.870±0.002 6.872±0.001 6.873±0.002 | 0.727 0.726 0.726 | 532.71 ±0.725 533.33±0.725 533.35 ± 0.725 | 2.15 1.35 1.03 |
Са9HРO4(PO4)5OH (JCPDS №46-0905) | 9.441 | 6.881 | 0.729 | 531.2 | - |
Костная ткань [29] | 9.410 | 6.891 | 0.732 | 528.4 | 5-10 |
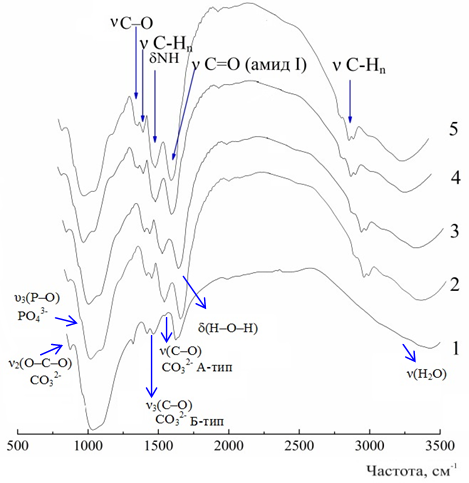
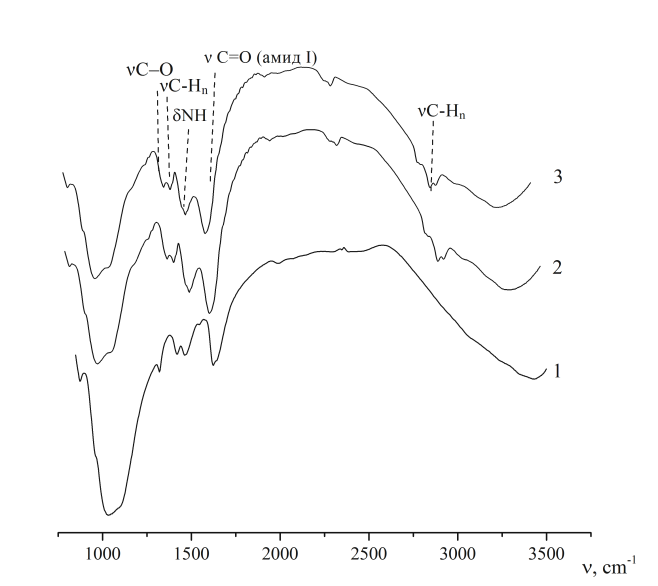
Полученные данные обоснованы с помощью ИК-спектроскопии. Доказано, что во всех случаях образуется карбонатсодержащий гидроксиапатит (КГА) преимущественно Б-типа (рис. 2, 3). На ИК-спектрах осадков присутствуют дублет асимметричных валентных колебаний связи н3(С–О) 1410-1480 см-1 и деформационного колебания н2(О–С–О) 875-879 см-1 в СО32-, указывающих на механизм замещения фосфатных тетраэдров карбонат-ионами в структуре полученных КГА по Б-типу; асимметричные валентные колебания н(С–О) в СО32- А-типа; валентные и деформационные колебания в Н2О – н(Н2О) 3400-3440 см-1 и δ(Н–О–Н) 1610-1650 см-1; асимметричные валентные и деформационные колебания в РО43- – х3(Р–О) 1030-1090 см-1.
|
|
Рис. 2. ИК-спектры контрольного образца (1); и синтезированных в присутствии альбумина, г/л: 5 (2); 7 (3); 10 (4); 12.5 (5) | Рис. 3. ИК-спектры контрольного образца (1) и синтезированных в присутствии 5 и 7 г/л желатина (2) и (3) |
Подтверждением предположения присутствия органической добавки в составе твердой фазы являются наличие на ИК-спектрах мод колебаний органических групп: –СНn (д); СОО - (н); - NH2 (д); амида I С=О (н); –СН2 (н). С увеличением содержания органического вещества в полученных композитах (более чем 10 г/л альбумина и 7 г/л – желатина), характеристика неорганических группировок, в том числе и механизма замещения карбонат-ионами гидроксогрупп и фосфат ионов, становится проблематичной, так как в интервале частот 1300-1700 см-1 отмечается наложение пиков минеральных и органических группировок. Однако, в ИК-области где отсутствует такое наложение мод (2800-3000 см-1), отмечается рост интенсивности моды С-Н метиленовых групп с увеличением концентрации белков в модельном среде, и, следовательно, в составе твердой фазы. Возможно, это связано с тем, что в водном растворе функциональные группы органических веществ (NH2+, OH - и др.) обладают адсорбционной активностью по отношению к поверхности КГА за счет водородных связей, электростатических и координационных взаимодействий заряженных центров. Это предполо-жение согласуется с участием белковой компоненты в минерализации, описанной работах [30, 31]. При формировании минеральной фазы в среде, содержащий биополимер, первоначаль-ный гомогенный механизм образования зародышей кристаллов сменяется гетерогенным. Зарождение новой фазы инициируется активными центрами, входящими в состав органи-ческой молекулы. Первоначально ионы кальция взаимодействуют с карбоксильными группами белка, далее к формирующимся кальциевым комплексам присоединяются фосфат-ионы. Таким образом, образуются зародыши новой кристаллической фазы, и наибольшая часть поверхности твердой фазы связана с биополимером. В среде с высокой вязкостью при содержании желатина более 7 г/л замедляется скорость массопереноса осадкообразующих ионов, вследствие чего происходит формирование менее окристаллизованных образцов, в составе которых содержатся кристаллиты меньшего размера. Размеры кристаллитов данных композитов ГА-желатин меньше в 1.5-2 раза по сравнению с другими образцами (табл. 1).
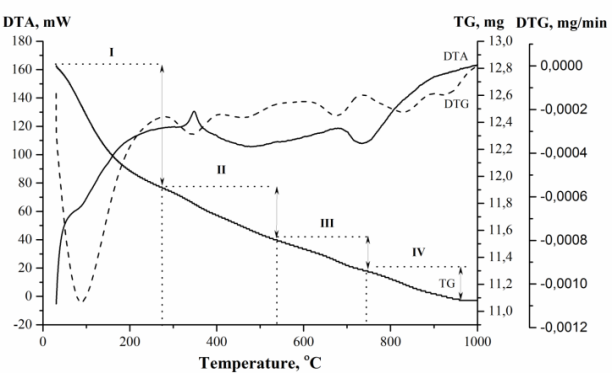
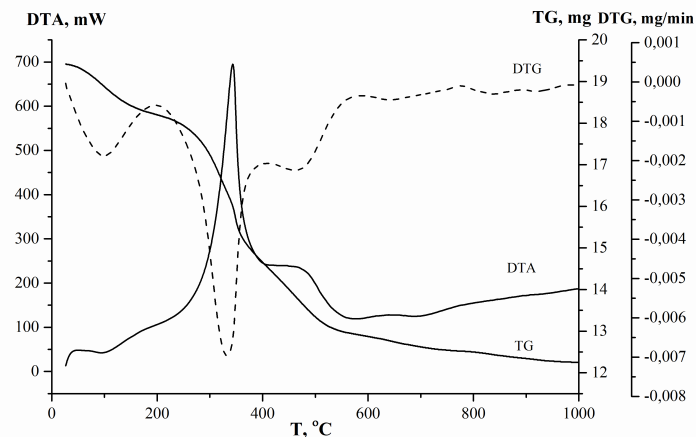
С помощью термического анализа проанализированы термопревращения порошков в интервале температур 25-1000 °С. Можно выделить пять этапов термопреобразования КГА-белок (рис. 3, схемы превращений в табл. 2, [11, 31-35].
|
|
1 | 2 |
Рис. 3. Термограммы образцов: контрольного (1); синтезированных в присутствии альбумина (2) |
На первом этапе (I) при 25-280 °С происходит удаление химически не связанной воды, разложение легколетучих примесей. На втором этапе (II) при 200…280-470 °С – потеря адсорбированной воды или/и начинается термическая деструкция белков. Основная стадия разрушения полипептидных цепей альбумина, связанных с поверхностью КГА, происходит при 200-400 °С (этап II, максимум на ДТА при 250-340 °С, рис. 3б). Температурный интервал термодеструкции желатина характеризуется более высокой температурой начала разложения компоненты (280-400…450 °С). Вероятно, это связано с более сложным аминокислотным составом и сложной структурной организацией. Термическое превращение желатина про-текает через последовательные стадии дезорганизации спиральной структуры коллагеновых волокнах, распада цепей, сгорания органических молекул, карбонизации и окисления углерода до СО2. На третьем этапе (III) при 400-750 °С отмечается полная деструкция белков, дегидратация хемосорбированной и кристаллизационной воды. Заключительные IV и V этапы при 600…750-900 °С и 800…900-1000 °С (пики при 830 и 940 °С) связаны с преобразованием КГА (первый пик и второй пики ДТА).
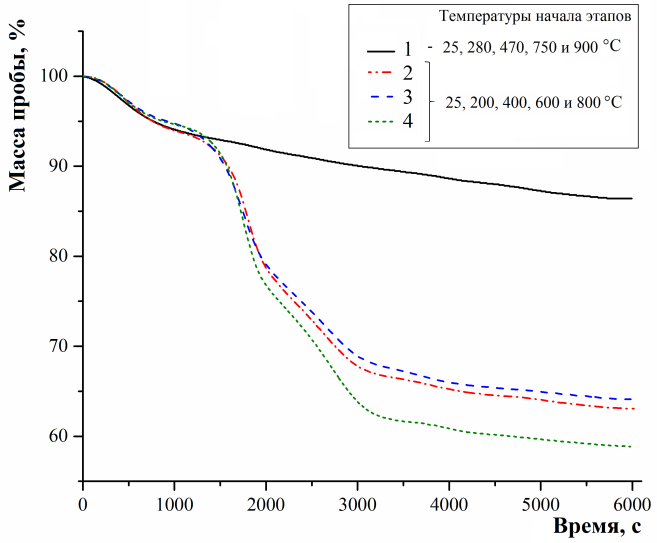
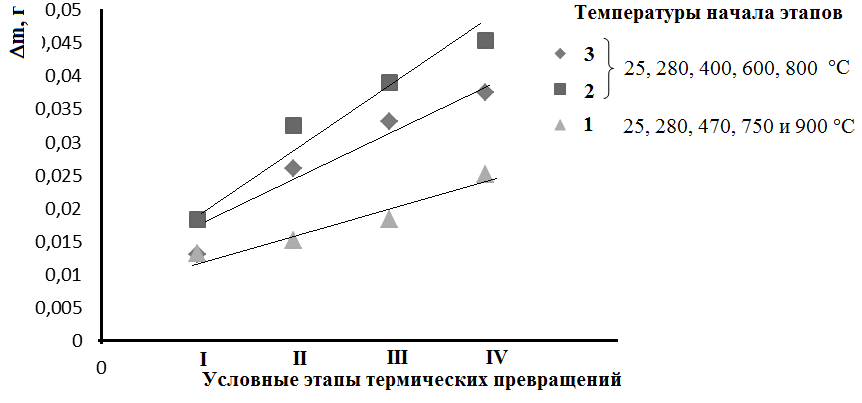
Выявлено, что при отжиге порошки, синтезированные при наличии биополимера в модельном растворе, характеризуются наибольшими суммарными потерями массы и их разложение начинается при более низких температурах (I-IV, рис. 4-5), что свидетельствует о низкой кристалличности образцов. Показано, что убыль массы композитов КГА-альбумин (рис. 4) в основном происходит за счет повышения массовых потерь белка и кристаллизационной воды и не зависит от содержания альбумина в модельном растворе при содержаниях ≤ 7 г/л.
Образец, синтезированный при больших концентрациях белка (10 г/л) отличается наибольшими потерями массы данных компонентов и структурных СО32-, что косвенно может указывать, как на низкую степень кристалличности композита, так и малую упорядоченность структуры КГА. Наболее термостабильными оказались желатинсодержащие композиты (рис. 5). Наибольшая убыль массы фиксируется на этапах удаления белковой компоненты, кристаллизационной воды, а также карбонат ионов, изоморфно входящих в позиции ОН - и РО43- в структуре КГА осадков. Показано, что с увеличением концентрации желатина в растворе, уменьшается степень кристалличности и термическая стабильность композитов. Полученные данные хорошо согласуются с результатами РФА и ИК-спектроскопии.
Табл. 2. Схемы процессов, характеризующих
массовые потери компонентов образцами при отжиге
Этап | Tнач. разложения компонентов * | Процесс |
I | 25 | - удаление химически не связанной воды: [КГА ⋅ nH2O] ⋅ mН2O(тв.) → КГА⋅ n H2O(тв.) + mН2O(г.) ; - легколетучих примесей (например, адсорбированного CO2). |
II | 200 (280) | - потери адсорбированной воды, - начало термической деструкции белков. |
III | 400 (470) | - дегидратация хемосорбированной и кристаллизационной воды : КГА⋅ nH2O(тв.) → КГА(тв.) + mН2O(г.), - окончание термической деструкции белков. |
V | 600 (750) 800 (900) | - преобразование КГА, а именно удаление карбонат-ионов из его структуры в виде СО2 при переходе нестехиометричного КГА в стехиометричную фазу ГА или в-Са3(РО4)2: Са10(РО4,СО3)6(ОН)2 → Са10(РО4)6(ОН)2 + 6СО2↑; Са9(РО4)6-x-y(НРО4)у(СО3)x(ОН)2-у(тв.) - преобразование гексагональной сингонии ГА в моноклинную форму и/или стехиометричного ГА в оксигидроксиапатит согласно реакции: Са10(РО4)6(ОН)2 → Са10(РО4)6(ОН)2-2xOxnx + xH2O |
* Начальная температура разложения компонентов композитов
|
|
Рис. 4. Кривые ТГ образцов, синтезированных при содержании альбумина в модельном растворе, г/л: 0 (1); 5 (2); 7 (3); 10 (4) | Рис. 5. Поэтапные массовые потери при отжиге образцов, синтезированных при содержании желатина в модельном растворе, г/л: 0 (1); 5 (2) и 7 (3) |
Исследование текстуры и морфологии проведено методами БЭТ, сканирующей и оптической микроскопии. Установлено, что присутствие биополимера в модельной среде приводит к формированию композитов с меньшей удельной поверхностью (табл. 3). Можно предположить, что снижение Sуд. происходит за счет адсорбционных взаимодействий заряженных участков белка с поверхностью нестехиометричного КГА [29, 30].
При содержании альбумина более 7 г/л образуется образец значение Sуд., которого в 5 раз меньше удельной поверхности контрольного образца. На микрофотографиях образцов, полученных с помощью сканирующего электронного микроскопа (СЭМ), видно, что частицы чистого КГА имеют чешуйкоподобную форму и образуют агрегаты размером до 100 мкм (рис. 1, 2). С увеличением содержания альбумина в модельном растворе частицы приобретают округлую форму, поверхность самих осадков становиться более однородной. Для двухфазных осадков, полученных в среде с 7 г/л желатина и более характерна наибольшая аморфность, вследствие чего отдельные частицы располагаются близко друг к другу и образуются непрозрачные сферические агрегаты.
Табл. 3. Площадь удельной поверхности композитов КГА-белок
Характеристика КГА | Без добавки | Содержание альбумина в модельной среде, г/л | ||
5 | 7 | 10 | ||
Sуд., м2/г | 130±7 | 44±2 | 48±2 | 25±2 |
|
|
|
|
Рис. 6. Микрофотографии КГА, полученные на синтезированные без добавки (1), в присутствии 10 г/л альбумина (2) – сканирующий микроскоп JSM-6610LV; 7 г/л альбумина и желатина (3) и (4) – оптический микроскоп XSP-104, 160 кратное увеличение |
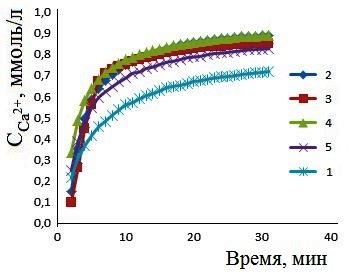
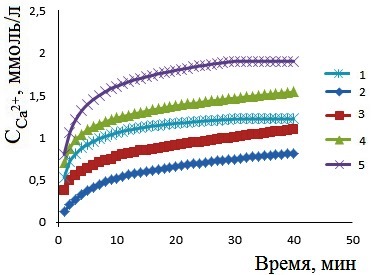
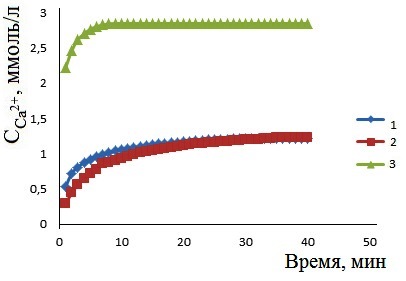
Для характеристики биоактивности образцов проведено их растворение в растворителях, подобранных с учетом условий резорбции in vivo [27, 28]. Установлено, что наличие белка в составе композита улучшает их растворимость, как в слабокислой среде, так и в средах близких к нейтральным (рис. 7.1, 8.1). При моделировании пассивной фазы резорбции путем растворения в 0.9% NaCl, показано, что альбумин - и желатинсодержащие образцы растворяются примерно с одинаковой скоростью, причем содержание белков в составе твердых фаз не влияет на их растворимость. На стадии «активной» резорбции при растворении в ацетатном буферном растворе (рН = 5.5) по сравнению с фазой КГА, с большей скоростью растворяются менее кристалличные композиты, полученные при осаждении из среды, содержащей более 10 г/л альбумина и 7 г/л желатина (рис. 7.2, 8.2). При этом растворяется в 2 и 3 раза больше композита КГА-альбумин и КГА-витлокит-желатин. Построены ряды, характеризующие резорбируемость композитов в ацетатном буферном растворе: желатин (более 7 г/л) > альбумин (более 10 г/л) > КГА ≈ желатин (менее 7 г/л) > альбумин (менее 10 г/л).
|
|
а) | б) |
Рис. 7. Зависимости концентрации ионов Ca2+ от времени растворения в 0.9% NaCl (1) и в ацетатном буферном растворе композитов (2) композитов, полученных при содержании альбумина в модельном растворе г/л:0 (1); 5 (2); 7 (3); 10 (4); 12.5 (5) |
|
|
а) | б) |
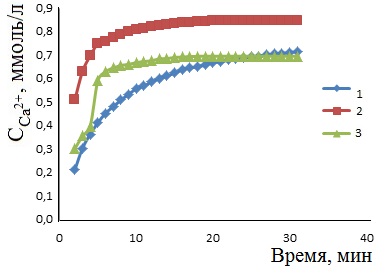
Рис. 8. Зависимости концентрации ионов Ca2+ от времени растворения в 0.9 % NaCl (1) и в ацетатном буферном растворе композитов (2) композитов, полученных при содержании желатина в модельном растворе г/л: 0 (1); 5 (2); 7 (3) |
Полученные результаты по кинетике растворения образцов в разных растворителях можно пояснить, учитывая поведение биополимеров в растворе. Как желатин, так и альбумин являются полиамфолитами, так как содержат остатки различных аминокислот (глицина, лизина, глутаминовой кислоты и так далее) [36]. Заряд белков завит от рН раствора. Их изоэлектрическая точка. при которой амфолиты обладают минимальной вязкостью находится примерно при рН 4.7. В более кислой среде (рН 4.7) группы - NH2 протонируются в - NH3+ и молекулы белка приобретают положительный заряд (свойства основания). В более щелочных средах происходит –COOH групп, в растворе доминируют СОО - ионы, за счет чего биополимеры приобретают отрицательный заряд (свойства кислоты). Подобные электроста-тические взаимодействия приводит к деформации гибких макромолекул, что сказывается на повышении вязкости среды, что негативно отрицательно на растворимости белков. В связи с чем, для достижения изоэлектрической точки биополимеров, следовательно, улучшения их растворимости необходимо подавлять диссоциацию –COOH групп. Это становиться возмож-ным при добавлении избытка H+ (рН 7). Поэтому в слабокислых условиях (ацетатном буферном растворе или активной стадии резорбции) полученные композиты КГА-альбумин и КГА-желатин будут лучше резорбироваться.
Заключение
На основании результатов теоретического моделирования осаждения малорастворимых соединений из прототипов синовиальной биожидкости (синовия) проведена серия синтезов композитов, состоящих из карбонатапатита низкой степени кристалличности, белков альбу-мина и желатина. Исследованы термические свойства и биорезорбируемость образцов. Показано, что присутствие органического полимера приближает свойства композита к характеристикам живой костной ткани и улучшает растворимость материалов на стадии активной фазы резорбции, которая протекает in vivo с участием остеокластов.
Выводы
Синтезированы модифицированные белками (альбумином и желатином) кальций-фосфатные композиты. Полученные осадки представлены плохоокристаллизованным карбонатсодер-жащим гидроксиапатитом (КГА) и аморфной компонентой. Композиты КГА-альбумин и КГА-желатин (7 г/л) однофазны, а КГА-желатин (>7 г/л) двухфазны (содержат 10 % масс. витлокита). Наличие белков в модельной среде менее 7 г/л не влияет на кристаллохими-ческие параметры КГА, при большем содержании биополимеров, происходит небольшое расширение элементарной ячейки КГА вдоль оси а.Показано, что наличие белков в модельной среде ухудшает степень кристалличности кальций-фосфатных композитов, а при концентрациях биополимеров более 7 г/л в структуре КГА содержится больше карбонат-ионов. Наиболее термостабильными являются желатин-содержащие композиты.
Установлено, что присутствующие в растворе низкомолекулярный белок альбумин и высокомолекулярный желатин при содержании менее 7 г/л в кальций-фосфатных композитах не оказывает влияния на размеры формирующихся кристаллов карбонатсодержащего гидроксиапатита (КГА), а способствуют изменению площади удельной поверхности образцов. При увеличении концентрации желатина в среде более чем 7 г/л на процесс кристаллизации оказывает влияние вязкость среды, и происходит формирование аморфизированных двух-фазных композитов, состоящих из кристаллитов КГА меньшего размера. Установлено, что скорость растворения в 0.9% NaCl композитов карбонатсодержащего гидроксиапатита – белок не зависит ни от природы биополимера, ни от его концентрации в растворе. В ацетатном буферном растворе с большей скоростью растворяются порошки, синтезированные из среды, в которой содержится > 7 г/л альбумина и ≥ 7 г/л желатина.
Получены результаты, которые могут быть использованы для создания композитных материалов, позволяющих ускорить процесс остеоинтеграции системы имплант-костная ткань, востребованных в разных областей медицины (ортопедии, костной пластики, стоматологии).
Благодарности
Исследование выполнено при частичной финансовой поддержке Российского фонда фундаментальных исследований (проект №16-33-0053 мол_а и №15-29-04839 офи_м).
Литература
Леонтьев активные кальций фосфатсодержащие материалы для стоматологии. Стоматология. 1996. №5. С.4-6. , Григорьян как субстрат для костной пластики: теоретические и практические аспекты проблемы. Стоматология. 1996. Т.75. №5. С.7-12. , Путляев неорганическое материаловедение в России: кальцийфосфатные материалы. Наносистемы: физика, химия, математика. 2013. №4(1). С.24-47. , , Григорьев композиты медицинского назначения. Медицинская техника. 2014. №1. С.30-33. Е. Bourgeat-Lami. Organic-inorganic nanostructured colloids. Journal Nanoscience and Nanotechnology. 2002. Vol.2. №1. P.1-24. A. Stein, B. J. Melde, R. C. Schroden. Hybrid inorganic-organic mesoporous silicates nanoscopic reactors coming of age. Advanced Materials. 2000. Vol.12. No.19. P.1403-1419. A. L. Boskey. Mineralization of Bones and Teeth. Elements. 2007. Vol.3. P.387-393. C. Rey, bes, C. Drouet, M. J. Glimcher. Bone mineral: update on chemical composition and structure. Osteoporosis International. 2009. No.20(6). Р.1013-1021. R. Murugan, S. Ramakrishna. Crystallografic study of hydroxyapatite bioceramics derived from varios sources. Crystal Growth and Design. 2005. Vol.5. P.111-112. Баринов и композиционные материалы на основе фосфатов кальция для медицины. Успехи химии. 2010. №1. С.15-32. , , Скубишевска- , Туров костной ткани композитными системами на основе гидроксиапатита - альбумина – желатина. Поверхность. 2010. Вып.2 (17). С.244-265. , , Альмяшев и композиционные наноматериалы на основе ортофосфатов кальция. Наносистемы: физика, химия, математика. 2012. №3 (5). С.84-102. Пат. 2516921. Российская Федерация. МПК A61K 35/32 (2006.01) Композиция для костной пластики (варианты). , , 2013115516/15, заяв. 08.04.2013, опубл. 20.05.2014. , , Киченко применения в стоматологии полифункциональных биополимеров хитозана и альгината. Российская стоматология. 2008. №2. Р.66-73 ndaram, T. D. Durance, R. Wang. Porous scaffold of gelatine – starch with nanohydroxyapatite composite processed via novel microwave vacuum drying. Acta Biomaterialia. 2008. Vol.4. P.932-942. M. Chen, J. Tan, Y. Lian, D. Liu. Preparation of Gelatin coated hydroxyapatite nanorods and the stability of its aqueous colloidal. Applied Surface Science. 2008. Vol.254. P.2730-2735. M. Li, X. Xiao, R. Liu, C. Chen, L. Huang. Structural characterization of zinc-substituted hydroxyapatite prepared by hydrothermal method. Journal of Materials Science: Materials in Medicine. 2008. No.19. Р.797-103. H. C. Kroese-Deutman, J. van den Dolder, P. H. Spauwen, J. A. Jansen. Influence of RGD-loaded titanium implants on bone formation in vivo. Tissue Engineering. 2005. No.11. Р.1867-1875. Пат. 2496150. Российская Федерация. МПК G09B 23/28 (2006.01) / Способ моделирования костной минерализации коксартроза in vitro. , Лемешева (Герк) С. А., 2012115045/14, заяв. 16.04.2012, опубл. 20.10.2013. , , Гасанова состав синовиальной жидкости коленного сустава людей в норме. Успехи современного естествознания. 2015. №9(1). С.122-125. Павлова среда суставов. М.: Медицина. 1980. 296с. Базарный жидкость (клинико-диагностическое значение лабораторного анализа). Екатеринбург: УГМА. 1999. 62с. , , Клушин , элементный, аминокислотный и структурный состав физиогенных минералов. Бутлеровские сообщения. 2012. Т.32. №12. С.80-89. ROI: jbc-01/12-32-12-80; S. A. Gerk, O. A. Golovanova, and V. A. Klushin. Phase, elemental, amino acid and structural composition of physiogenic minerals. Butlerov Communications. 2012. Vol.32. No.12. P.80-89. ROI: jbc-02/12-32-12-80 D. W. Green, T. K. Goto, K. S. Kim, H. S. Jung. Calcifying tissue regeneration via biomimetic materials chemistry. Journal of the Royal Society Interface. 2014. No.11. P.1-11. , Черепанова в структурный анализ нанокристаллов. Новосибирск: Новосибирский гос. университет. 2008. 92с. , , Домашевская нанокристаллического гидроксиапатита метом химического осаждения с использованием биогенного источника кальция. Конденсированные среды и межфазные границы. 2011. Т.13. №4. С.427-441. Климашина , структура и свойства карбонатзамещенных гидроксиапатитов для создания резорбируемых материалов. Автореф. дис. … к. х.н. М.: МГУ им. . 2011. 23с. , Голованова гранулированного композита на основе карбонатгидроксилапатита и желатина в средах с различными значениями рН. Вестник Омского университета. 2015. №2. С.61-65. Лосев кристаллических фаз, образующихся в системах «глицин - карбоновая кислота» и «серин - карбоновая кислота». Дис. … к. х.н.. Новосибирск. 2014. 116с. , , Тураева гидроксилапатит, синтезированный осаждением в растворе желатина. Доклады академии наук. 2006. Т.411. №3. С.348-351. , Голованова на основе фосфатов кальция и желатина, полученные при варьировании рН среды. Вестник Омского университета. 2013. №4. С.152-158. , , Межевой исследование аминокислот и алифатических пептидов. Жидкие кристаллы и их практическое использование. 2014. Т.14. №3. С.43-52. , Рудченко свойств композита на основе гидроксиаптита и хитозана путем вариации состава и режимов термообработки. Вестник Харьковского университета. 2010. Вып.14. С.35-39. V. C. Chang. Organic-inorganic interaction and the growth mechanism of hydroxyapatite crystals in gelatin matrices between 37 and 80 °C. Journal of Materials Science. 2006. No.17. P.387-396. Баринов на основе фосфатов кальция. М.: Наука. 2005. 204с. Ляндзберг практикум по физической и коллоидной химии. Петропавловск-Камчатский: КамчатГТУ. 2004. 75с.In the English version of this article, the Reference Object Identifier – ROI: jbc-02/17-50-6-66
Biomimetic composites based on carbonatation,
albumin and gelatin for biomedical applications
© Svetlana A. Gerk,+ Olga A. Golovanova,* and Viktoria N. Odajiu
Inorganic Chemistry Division. F. M. Dostoevsky Omsk State University.
Mir Ave. 55a. Omsk, 644077. Russia. Phone: +7 (3812) 268-199.
E-mail: *****@***ru, *****@***ru
____________________________________
*Supervising author; +Corresponding author
Keywords: composites, biomaterials, hydroxyapatite, protein, albumin, gelatin, crystallization, thermal degradation, resorption, isomorphism.
Abstract
In the present work, biocomposites obtained by the method of deposition from a prototype bioliquids person while varying the concentration of albumin and gelatin. Materials synthesized from environments with albumin and gelatin (7 g/l) is represented by carbonatisation and a biopolymer, and from solutions containing >7 g/l gelatin, inclusive of 10 % wt. whitlock and consist of crystallites of a smaller size. It has been shown that the presence of proteins results in the deposition of composites with a lower degree of crystallinity and a specific surface area. The kinetics of dissolution of composites in neutral and weakly acidic media was studied. It was found that the resorption in 0.9% NaCl of biocomposites does not depend either on the nature of the biopolymer or on its concentration in solution. Powders obtained from viscoelastic media dissolve at a higher rate in an acetate buffer solution.
Объём аннотации посылаемой в печать статьи должен быть 200-250 слов. Количество слов в аннотации можно узнать в MS Word 2003 выделив текст, войти в информационной панели в Сервис и затем в Статистику. В MS Word 2007, выделяют весь текст аннотации и на нижней информационной панели нажимают на секцию “Число слов”, в возникшем статистическом окошке смотрят численное значение.