Автор: ,
Учитель химии и биологии, социальный педагог
МОУ Силикатненская СШ имени Ульяновской области
Использование модульной технологии на уроках химии.
Современные жизненные условия диктуют применение такой системы обучения, которая бы обеспечивала образовательные потребности каждого обучающегося в соответствии с его склонностями, интересами и возможностями. Для достижения этой цели необходимо, чтобы учащиеся добывали знания самостоятельно, а учитель осуществлял управление его учением, т. е. мотивировал, организовывал, консультировал, контролировал. Для решения этой задачи актуальна технология модульного обучения.
Элементом модульной технологии обучения является модульный урок. Составляется модульный урок по следующему алгоритму:
• формулировка темы урока;
• определение и формулировка цели урока и конечных результатов обучения;
• деление учебного содержания на отдельные логически завершенные
учебные элементы (УЭ) и определение цели каждого из них;
• подбор необходимого фактического материала;
• определение способов учебной деятельности учащихся;
• отбор методов и форм преподавания и контроля;
• составление модуля данного урока;
• подготовка необходимого количества копий текста урока (1)
Каждый учебный элемент в модульном уроке – это шаг к достижению интегрирующей цели урока, без овладения содержания которого, цель не будет достигнута. Каждый УЭ должен иметь свою цель. Учебных элементов не должно быть много, но обязательны следующие:
УЭ-0 - определяет интегрирующую цель по достижению результатов обучения;
УЭ-1- включает, как правило, задания по выявлению уровня исходных знаний;
УЭ-2 –n - задания по овладению новым материалом и отработку учебного материала.
УЭ-n (где n - номер последнего учебного элемента) – включает выходной контроль знаний, подведение итогов занятия, выбор домашнего задания, рефлексию (5)
Модульный подход имеет большие преимущества..
Преимущества для учащихся:
• каждый точно знает, что он должен усвоить, в каком объёме и что должен уметь после изучения модуля;
• каждый может самостоятельно планировать своё время, эффективно использовать свои возможности;
• учебный процесс сконцентрирован на ученике, а не на учителе.
Преимущества для учителя:
• возможность концентрировать своё внимание на индивидуальных проблемах, обучающихся;
• своевременная идентификация проблем в обучении, выполнение творческой работы, заключающейся в стимулировании мышления учащихся, активизации их внимания, мышления и памяти, активизации нужных реакций, оказании им возможной помощи.
Модульное обучение ориентировано, прежде всего, на активную учебную деятельность детей, освоение приемов которой способствует быстрому и качественному усвоению содержания учебных предметов и развитию у учащихся самостоятельного изучения, самоанализа, самоконтроля.
Мною разработан модульный урок по теме «Фенолы. Строение, свойства, применение. Взаимное влияние атомов в молекулах» по учебнику Кузнецова :10 класс: профильный уровень: учебник для учащихся общеобразовательных организаций/ , , /- М.: Вентана-Граф. 2014г
№УЭ | Учебный материал с указанием заданий. | Рекомендации по выполнению задании, |
УЭ-0 | Цель: А - уровень Знать: понятие «фенолы», строение, физические и химические свойства фенола: а) взаимодействие с активными металлами, б) со щелочами; в.) бромирование; г) нитрование; д) с хлоридом железа (III); Действие фенола на живые организмы. Мероприятия по охране окружающей среды от промышленных отходов, содержащих фенол. Применение фенола. Получение фенола. Уметь записывать формулу фенола. Составлять уравнения реакции характеризующих химические свойства фенола. (Кроме качественной реакции c хлоридом железа (III)) В - уровень. Знать -понятие «фенолы», строение, физические и химические свойства фенола: а) взаимодействие с активными металлами, б) со щелочами; в.) бромирование; г) нитрование; д) с хлоридом железа (III). Действие фенола на живые организмы. Мероприятия по охране окружающей среды от промышленных отходов, содержащих фенол. Применение фенола. Генетическую связь с другими классами органических соединений, взаимное влияние атомов в молекулах. Получение фенола. Знать условия проведения химических реакций, характеризующих свойства и получение фенола Название полученных веществ. Уметь записывать формулу фенола. Составлять уравнения реакций, характеризующих химические свойства фенола. (Кроме качественной реакции c хлоридом железа (III)) Осуществлять с помощью уравнений генетическую связь Объяснять взаимное влияние атомов в молекуле фенола, определять фенол. Уметь составлять уравнения реакций взаимодействия фенола с солями трехвалентного железа записывать условия проведения химических реакций. С - уровень. Знать понятие «фенолы», строение, физические и химические свойства фенола: а) взаимодействие с активными металлами; б) со щелочами; в.) бромирование; г) нитрование; д) с хлоридом железа (III). Действие фенола на живые организмы. Мероприятия по охране окружающей среды от промышленных отходов, содержащих фенол. Применение фенола. Генетическую связь с другими классами органических соединений, взаимное влияние атомов в молекулах. Получение фенола. Знать условия проведения химических реакций, характеризующих свойства и получение фенола Название полученных веществ. Знать дешевые способы получения фенола из бензола (кумольный способ). Уметь записывать формулу фенола. Составлять уравнения реакции, характеризующие химические свойства фенола. Осуществлять с помощью уравнений генетическую связь. Объяснять взаимное влияние атомов в молекуле фенола, определять фенол. Уметь составлять уравнения реакций взаимодействия фенола с солями трехвалентного железа, записывать условия проведения химических реакций. Уметь составлять уравнения реакций получения дешевого фенола из бензола | Внимательно прочитайте цель урока (5 мин.) А - оценивается на 3 балла Б-4 балла С-5 баллов |
УЭ-1 | Цель: проверить знания по теме «Спирты» и готовность к основному этапу занятий 1. На листе бумаги напишите уравнения реакций, отражающие химические свойства одноатомных спиртов: А. на примере этилового спирта Б. на примере пропилового спирта С. На примере бутилового спирта 2. Выполните задание и сдайте учителю на проверку | Работайте индивидуально. Следите за временем 15 минут А - оценивается на 3 балла Б-4 балла С-5 баллов |
УЭ-2 | Цель: восстановить знания учебного материала Если Вы не смогли выполнить задание, то повторите еще раз тему «Спирты» и ответьте на вопросы учителя. (Приложение 2) Если Вы успешно справились с вопросами, то приступайте к изучению УЭ -3 | «Химия» -10 класс, стр. 151-152 |
УЭ-3 | Цель: Знать определение понятия «фенолы». Строение, физические и химические свойства фенола: взаимодействие с активными металлами; со щелочами; бромирование; нитрование; с хлоридом железа (III). 1. Изучите какие вещества относятся к фенолам, строение молекулы фенола (с.163) 2. В тетрадях изобразите структурные формулы двух - трех представителей принадлежащих к фенолам (с.164) 3. Составьте электронную формулу фенола и поясните, почему атом водорода в гидроксильной группе более подвижен, чем в молекуле одноатомного спирта (с.164-165) 4. Составьте уравнения химических реакций, характеризующие химические свойства фенолов: взаимодействие с активными металлами; со щелочами; бромирование (в результате реакции образуется 2,4,6-трибромфенол); нитрование (в результате реакции образуется 2,4,6-тринитрофенол). 5. расскажите друг другу 6.Оцените свою работу в пятибалльной системе. | Пользуйтесь стр.163-167 учебника Проверьте правильность написания химических уравнений. Работайте 10 минут Оценку поставьте в приложение 1 УЭ-3 |
УЭ-4 | Цель; закрепить знание химических свойств фенолов. Лабораторная работа «Взаимодействие фенола с йодной водой, раствором щелочи и хлоридом железа (III). Вспомните правила техники безопасности при работе в химическом кабинете.Приложение Выданную Вам водную эмульсию фенола разделите на 3 пробирки.К первой порции эмульсии фенола прибавьте несколько капель раствора щелочи и взболтайте. Что наблюдаете. Объясните это явление. Ко второй порции эмульсии фенола добавьте йодную воду. Что наблюдаете? Составьте уравнения реакций в тетради. К третьей порции эмульсии фенола добавьте хлорид железа (III). Что наблюдаете? 3С6 Н5 ОН+FeCl3 = (С6 Н5 О)3 Fe +3HCl Фенолят железа(III) фиолетового цвета Качественная реакция | Выполните Лабораторную работу. Следите за временем, работайте 7 минут. После опыта с фенолом руки тщательно вымойте. |
УЭ-5 | Цель: знать действия фенола на живые организмы, мероприятия по охране окающей среды от промышленных отходов, содержащих фенол. Применение фенола. 1. Изучите по учебнику, а) действие фенола на живые организмы, мероприятия по охране окружающей среды от промышленных отходов, содержащих фенол: б) применение фенола, в) получение фенола 2.расскажите друг другу 3. В тетрадь запишите уравнения реакций, при помощи которых можно получить фенол. 4. оцените свою работу в пятибалльной системе. | Пользуйтесь учебником химии стр. 169. Работайте в парах (10 минут) Оценку поставьте в приложение№1. графа УЭ - 5. |
УЭ-6 | Цель: знать взаимное влияние атомов в молекуле фенола 1. прочитайте приложение №4 2.Расскажите друг другу о взаимном влиянии атомов в молекуле 3. Оцените ответы в пятибалльной системе. Оценку поставьте в Приложении 1 графе УЭ-6 | Работайте в парах (работайте 10 минут) |
УЭ-7 | Выходной контроль приложение №5 Цель: Проверить усвоение теоретического материала. Выполните задания приложения №5, для этого надо выбрать свой вариант и указать номер вопроса и вариант ответа. Например, 1а; б; Помните, что на один вопрос может быть несколько правильных ответов. | Работайте индивидуально 10 минут, выберите свой вариант ответа А - оценивается на 3 балла Б-4 балла С-5 баллов |
УЭ-8 | Рефлексия. Вернитесь к цели урока. Достигли вы ее? Оцените свою работу в пятибалльной системе! | Оцените свою работу в пятибалльной системе в приложении №1 графе УЭ-8 |
УЭ-9 | Домашнее задание. Химия 10 §26 упражнение А-№6 с.171; Б-№8 с.171; С -№9 с.171 | Запишите домашнее задание. |
Приложение
ФИ | УЭ-1 | УЭ-3 | УЭ-5 | УЭ-6 | УЭ-8 | Оценка учителя |
Приложение
1. Дайте определение предельных одноатомных спиртов и приведите примеры.
2. Что такое функциональная группа? Почем гидроксильная группа спирта называется функциональной?
3. Как изменяется состав и физические свойства спиртов в гомологическом ряду метанола?
4.Приведите примеры, подтверждающие влияние функциональной группы —ОН на свойства углеводородного радикала в молекуле спирта.
5. Какие органические соединения называются многоатомными спиртами?
6. Охарактеризуйте важнейших представителей многоатомных спиртов.
Приложение
1. Работайте с малыми количествами веществ
2. Следите, чтобы растворы фенола, щелочи, соли не попали на руки.
3. Все опыты выполняйте над ящиком.
4. После работы вымойте руки
Помните фенол яд!
Приложение
Почему же фенол является более сильной кислотой, чем спирты? р - электронная система бензольного ядра может притягивать к себе не поделённую (свободную) пару р-электронов тех атомов, которые соединены с ним одной у - связью. Таким атомом в данном случае является кислород. Перемещение р-электронов кислорода в сторону бензольного ядра понижает электронную плотность на атоме кислорода. Для компенсации этой потери он усиливает перемещение в свою сторону электронной плотности у - связи О-Н, что создает условия для относительно легкого отрыва протона.
Атом кислорода гидроксильной группы спирта подобной электронной потери не несет, и поэтому он дополнительно не перемещает в свою сторону электроны у - связи О-Н. Сказанное графически выразим таким образом;
R O Н
Вспомним, что бензол не реагирует с бромной водой. Если же бромную воду прилить к раствору фенола, то легко образуется белый осадок три - бром фенола:
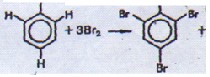
ЗНВг
Очевидно, причину большей реакционной способности бензольного ядра следует искать в наличии гидроксильной группы в молекуле, так как в остальном строение фенола и бензола одинаково. Неподеленная пара электронов атома кислорода, притягиваясь к бензольному ядру, повышает в нем электронную плотность, что и увеличивает его реакционную способность. Особенно сильно возрастает активность в положениях 2,4,6. Подобную картину мы наблюдали на примере бромирования толуола.
Здесь мы, следовательно, вновь встречаемся с проявлением взаимного влияния атомов: в молекуле фенола не только бензольное ядро влияет на гидроксильную группу, повышая ее кислотность, но и гидроксильная группа влияет на бензольное ядро, обусловливая более легкое замещение в нем атомов водорода.
Приложение№5
А.
1. Укажите формулы фенолов:
а)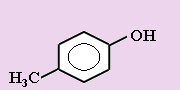 б)
б) 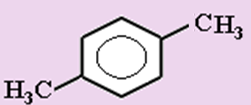 в)
в) 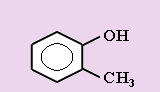
г)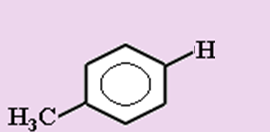 д)
д) 

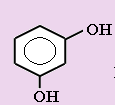
2.Влияние гидроксильной группы на свойства фенола состоит в том, что:
а) фенол в отличие от метанола реагирует со щелочами
б) повышается электронная плотность в положении 2,4,6 бензольного кольца
в) реакции замещения в бензольном кольце фенола протекают легче, чем у бензола
г) фенол в отличие от метанола реагирует со щелочами
3. Для обнаружения фенола используются:
а) хлороводород в) свежеприготовленный Сu(OH)2
б) FeCl3 г) бромная вода
4. Какое вещество используется как антисептик
а) бензол в) диметиловый эфир
б) толуол г) фенол
5. Укажите окраску фенолфталеина в водном растворе фенола:
а) малиновая в) желтая
б) розовая г) бесцветная
6.Фенол в промышленности используется для получения:
а) пластмасс в) красителей
б) лекарственных препаратов г) этанола
В
1.С какими веществами реагируют как фенол, так и бензол:
а) бром в) нитрующая смесь
б) натрий г) водный раствор гидроксида натрия
2. Укажите схемы реакций, в которых образуется фенол:
а) фенолят калия + соляная кислота
б) хлорбензол + NаОН
в) фенолят натрия + водный раствор СО2
г) фенолят натрия + разбавленная серная кислота
3. В отличие от этанола фенол реагирует с:
а) калием в) водным раствором КОН
в) хлороводородом г) гидросульфатом калия
4. Фенолят натрия образуется при взаимодействии фенола с:
а) натрием в) нитратом
б) гидроксидом натрия г) хлоридом натрия.
5. Какие два органических вещества используются для получения фенола в промышленности:
а) т толуол в) этилен
б) бензол г) пропилен
6. Охарактеризуйте реакцию взаимодействия фенола с бромной водой:
а) является реакцией замещения;
б) сопровождается образованием белого осадка;
в) продуктами являются кислота и 2,4,6 - трибромфенол;
г) является качественной реакцией на фенол,
С.
1.Укажите схемы реакций, в результате которых получается фенол:
а) С6Н5- ОК + НС1 в) С6Н5-СН3 +KMnO4
б) С6Н5- Вr + NаОН г) С6Н5-СН(СН3) + О
2.При взаимодействии каких пар веществ можно получить фенолят калия?
а) фенол и калий в) ацетат калия и фенол
б) фенол и гидроксид калил. г) фенол и хлорид калия
3. С какими веществами реагирую как фенол, так и бензиловый спирт?
а) хлороводород в) водный раствор гидроксида калия
б) калий г) гидрокарбонат натрия
4. Сколько веществ изображено с помощью формул:
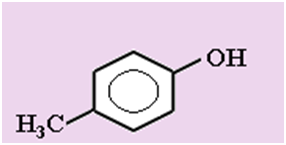
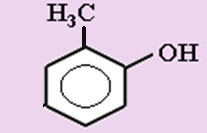
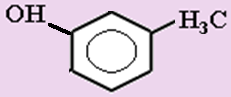
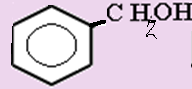
а) 1 б) 2 в) 3 г) 4
5. Различить пробирки с бензольными растворами фенола и этанола можно с помощью:
а) натрия; в) бромной воды;
б) гидроксида калия; г) хлороводорода.
6. В чем проявляется влияние бензольного кольца на свойства фенола?
а) повышается электронная плотность в положениях 2,4,6 ароматического кольца;
б) атом водорода гидроксильной группы фенола более подвижен, чем атом водорода гидроксильной группы в метаноле;
в) фенол в отличие от предельных одноатомных спиртов реагирует со щелочами;
г) фенол в отличие от бензола реагирует с бромной водой.
Литература:
1.Гульчевская модульного обучения: проблема внедрения в массовый опыт отечественной школы//www. ipkpro. aaanet. ru или *****@***ru-от18 февраля2003г.
2.Данилина обучение как средство реализации компетентностного подхода в развитии иноязычной профессиональной компетенции. [Текст]/ // Вектор науки/ Тольяттинский Государственный Университет. – Тольятти, 2012. - №1 (8). – с.109-111.
3.Мордасова модульного обучения. Режим доступа: //http://www. detskiysad. ru/.html
4. «Перспективные школьные технологии». // Завуч. – 2005 – № 5.
5.Шамова обучение: сущность, технологии / Биология в школе. 1994. – №5


