Модуль 3. Занятие 8.
Лабораторная работа. Итоговая УИРС.
(на занятии выполняются пункты 1 и 2)
Спектрофотометрическое определение равновесных концентраций сопряженных кислотно-основных форм метилового оранжевого в растворе
кислотная форма основная форма
Реагенты и аппаратура.
Метиловый оранжевый, водный раствор, С(НА)=1,5∙10-4 моль/дм3.
Серная кислота, С(H2SO4)=1,0000 моль/дм3.
Гидроксид натрия, С(NaOH)=0,0100 моль/дм3.
Спектрофотометр.
Выполнение определения. I. Выбор рабочих длин волн.
1. В двух мерных колбах объемом 100,0 см3 готовят растворы:
№ 1: С(НА)=1,8·10-5 моль/дм3, растворитель С(H2SO4)=0,0050 моль/дм3;
№ 2: С(А)=1,8·10-5 моль/дм3, растворитель С(NaOH)=0,0050 моль/дм3.
Измеряют спектры поглощения растворов в диапазоне длин волн
390-560 нм. Результаты измерений заносят в таблицу 1 и представляют в виде графика А = f(л).
Таблица 1. Светопоглощение кислотной и основной форм метилового оранжевого.
л, нм | 420 | 460 | 510 | 540 | 600 |
АНА | |||||
АА | |||||
АНА – АА |
По полученным результатам рассчитывают разности АНА – АА и результат записывают в таблицу 1. Строят график зависимости АНА – АА от л и выбирают рабочие длины волн л1 и л2 в области максимума и минимума этой кривой с учетом условия АНА, АА ≥ 0,08-0,1.
Oпределение коэффициентов молярного погашения сопряженных кислотно-основных форм метилового оранжевого при выбранных длинах волн л1 и л2.
1. Готовят две серии растворов метилового оранжевого в соответствии с таблицами 2 и 3.
2. Измеряют оптическую плотность растворов при двух выбранных длинах волн и рассчитывают коэффициенты молярного погашения обеих форм красителя, занося результаты расчетов в таблицы 2 и 3.
Таблица 2. Определение молярных коэффициентов погашения кислотной формы
метилового оранжевого(л1=… нм, л2=... нм, С(H2SO4) = 0,0050 моль/дм3)
С(НА), моль/дм3 | 6,0·10-6 | 9,0·10-6 | 1,2·10-5 | 1,5·10-5 | 1,8·10-5 | 2,1·10-5 | 2,4·10-5 |
| |||||||
| |||||||
| |||||||
|
![]() = ε ± Дε,
= ε ± Дε, ![]() = ε ± Дε
= ε ± Дε
Таблица 3. Определение молярных коэффициентов погашения (основной формы метилового оранжевого при л1 =…нм, л2=… нм, C(NaOH)=0,0050 моль/дм3)
С(А), моль/дм3 | 6,0·10-6 | 9,0·10-6 | 1,2·10-5 | 1,5·10-5 | 1,8·10-5 | 2,1·10-5 | 2,4·10-5 |
| |||||||
| |||||||
|
![]() = ε ± Дε,
= ε ± Дε, ![]() = ε ± Дε
= ε ± Дε
Значения е представляют в нормальном виде как целую степень десяти е =(ε ± Дε)∙10n.
III. Определение равновесных концентраций сопряженных кислотно - основных форм метилового оранжевого в анализируемом растворе.
1. Измеряют оптические плотности исследуемого раствора (задача, выданная преподавателем) при выбранных длинах волн л1 и л2. Результаты повторяют не менее трех раз и рассчитывают средние значения.
2. По формулам (1) вычисляют концентрации кислотной и основной форм красителя.
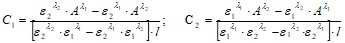 (1)
(1)
Аналогично можно провести измерения и расчеты и в тех случаях, когда в анализируемом растворе одновременно присутствуют более двух определяемых веществ.
Рассматриваемым методом можно определять медь, кобальт и никель при их совместном присутствии в виде комплексонатов фотометрированием раствора при трех длинах волн (436; 367 и 328 нм); амидопирин и кофеин – при 272 и 255 нм; дикаин и новокаин – при 311 и 290 нм.



