Задание №1
Физико-химические процессы в атмосфере:
оценка направления самопроизвольного протекания реакции,
расчет равновесного выхода продукта
Любые превращения – абиотические (химические) или биотические (биохимические) могут быть рассмотрены с точки зрения химической термодинамики и с точки зрения химической кинетики.
Химическая термодинамика на основе сведений об изменении термодинамических функций позволяет:
1) рассчитать тепловой эффект химической реакции;
2) определить возможность самопроизвольного протекания химических реакций в том или ином направлении;
3) определить условия, при которых устанавливается химическое равновесие.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Пример 1. Для реакции N2 + O2 = 2NO вычислите температуру, выше которой процесс протекает самопроизвольно. Определите содержание NO в равновесной смеси и равновесный выход NO при температурах 298К, 2500К и равновесной температуре, если исходная смесь – воздух. Давление равно стандартному (1атм.).
Решение:
Воспользуемся уравнением изотермы Вант-Гоффа для стандартных условий с целью вычисления константы равновесия Ка.
![]() ,отсюда
,отсюда ![]() .
.![]()
![]() ;
;
![]() ;
;
![]() .
.
Следовательно, процесс не может протекать самопроизвольно в прямом направлении (∆G°298 < 0).
При низких давлениях газы можно считать идеальными, и Ka ≈ Kp.
В общем случае ![]() для гипотетической реакции аА + вВ ↔ сС + dD:
для гипотетической реакции аА + вВ ↔ сС + dD:
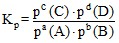 ,
,
где p(С) = P·N(С); p(D) = P·N(D); p(A) = P·N(A); p(B) = P·N(B);
Р – общее давление в системе;
а, в,с, d – cтехиометрические коэффициенты в уравнении реакции.
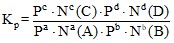 = =
= =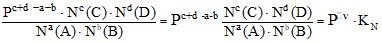
Здесь ∆н = с + d – a – b – изменение количества газов в ходе химической реакции;
![]() – константа равновесия, выраженная через мольные доли компонентов равновесной смеси:
– константа равновесия, выраженная через мольные доли компонентов равновесной смеси:
![]() .
.
Если давление выражено в атмосферах и равно 1 атмосфере, то Kp = ![]() и
и
![]() =
= ![]() .
.
Для данной реакции ∆н = с + d – a – b = 2 – 1 – 1 =0, поэтому Kp = ![]() при любых давлениях:
при любых давлениях:
![]() =
=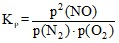 =
= ![]() =
= 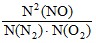 ,
,
где p(NO) = P·N(NO); p(O2) = P·N(O2); p(N2) = P·N(N2);
Р – общее давление в системе;
N(NO), N(O2),·N(N2) – мольные доли компонентов равновесной смеси.
Один моль воздуха содержит 0,79 моль азота и 0,21 моль кислорода.
Пусть к моменту становления равновесия в реакцию вступило х моль азота. Тогда в реакцию вступило столько же моль азота и образовалось 2х моль оксида азота (II).
Содержание – равновесные количества – N2, O2, NO в системе и их равновесные мольные доли мольные доли равны:
N2 O2 NO
но, моль 0,79 0,21 0
нравн, моль 0,79 – х 0,21 – х 2х
Nравн 0,79 – х 0,21 – х 2х*
* 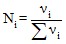 ; Унi = 0,79 – х + 0,21 – х + 2х = 1
; Унi = 0,79 – х + 0,21 – х + 2х = 1
T = 298K
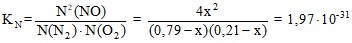 ;
;
4х2 = (0,79– х)(0,21 – х)·1,97·10-31
4х2 ≈ 0 ⇒ х ≈ 0
Равновесный выход продукта равен отношению количества продукта в равновесной смеси к общему количеству реагентов входящих в состав равновесной смеси:
зi = ![]() .
.
Равновесный выход оксида азота (II) равен:
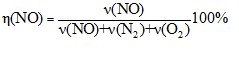 ;
;
![]() ≈ 0.
≈ 0.
T = 2500K
Согласно уравнению Гиббса-Гельмгольца: ![]() .
.
Принимаем, что ![]() и
и ![]() , тогда
, тогда
![]() .
.
![]()
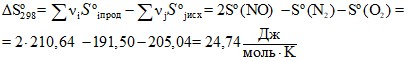
![]() = 182,52·103 – 2500·24,74 = 120670
= 182,52·103 – 2500·24,74 = 120670![]() = 120,67
= 120,67![]() .
.
![]() ;
;
![]() .
.
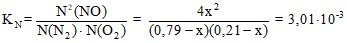
4х2 = (0,79– х)(0,21 – х)·3,01·10-3
4х2 = (0,1659 – 0,21х·–0,79х –3,01·10-3 + х2)·3,01·10-3
4х2 – 0,003х2 + 3,01·10-3х – 5·10-4 = 0
3,997 х2 + 3,01·10-3х – 5·10-4 = 0
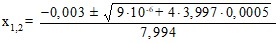
![]()
![]() =
=
= 2·0,0108 100% = 1,08%.
В состоянии равновесия ΔG°Т =0 и Ka = 1.
![]() , отсюда
, отсюда 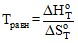 .
.
Полагаем, что ![]() и
и ![]() , тогда
, тогда 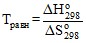 .
.
![]()
Процесс образования NO из азота и кислорода будет протекать самопроизвольно при T > 7378 K. При этой температуре Ka = 1.
T = 7378K
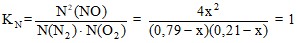
4х2 = (0,79– х)(0,21 – х)
3х2 + х – 0,1659 = 0
![]()
![]()
![]() =
=
= 2·0,1216·100% = 24,32%.
Ответ: При 298К реакция не может протекать самопроизвольно, т. к. ∆G°298 > 0. ![]() ; з298(NO) = 0; При 2500К реакция также не может протекать самопроизвольно, т. к. ∆G°2500 >0.
; з298(NO) = 0; При 2500К реакция также не может протекать самопроизвольно, т. к. ∆G°2500 >0. ![]() ; з2500(NO) = 1,08%. Реакция будет протекать самопроизвольно при температуре выше Травн = 7378K; з7378(NO) = 24,3%.
; з2500(NO) = 1,08%. Реакция будет протекать самопроизвольно при температуре выше Травн = 7378K; з7378(NO) = 24,3%.
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
Для заданной реакции вычислите:
изменение энергии Гиббса ΔG0298 и константу равновесия реакции Ка при температуре 298 К. температуру, при которой устанавливается равновесие в системе (∆G0T = 0). равновесный выход продукта (или продуктов) реакции при 298К и при равновесной температуре.
По результатам расчетов сделайте выводы о направлении самопроизвольного протекания реакции при Т=298К. Установите, при какой температуре (выше или ниже равновесной температуры) возможно самопроизвольное протекание реакции.
Давление равно 1 атмосфере. Вещества взяты в стехиометрических количествах.
Таблица вариантов
№ варианта | Уравнение реакции |
1 | 2NO + O2 = 2NO2 |
2 | 2NO2 = N2O4 (г) |
3 | 2N2 + O2 = 2N2O |
4 | N2O5(г) = N2O + 2O2 |
5 | N2O5(г) + H2O(г) = 2HNO3(г) |
6 | NO + O3 = NO2 + O2 |
7 | N2O + CO = N2 + CO2 |
8 | CH4 + O2 = CH2O(г) + H2O(г) |
9 | 2CH2O(г) + O2 = 2HCOOH(г) |
10 | 2CO + O2 = 2CO2 |
11 | CO + O3 = CO2 + O2 |
12 | CH2O(г) + O2 = CO2 + H2O(г) |
13 | 2SO2 + O2 = 2SO3 |
14 | SO2 + O3 = SO3 + O2 |
15 | SO2 + NO2 = SO3 + NO |
16 | SO2 + N2O = SO3 + N2 |
17 | SO3 + H2O(г) = H2SO4(ж) |
18 | 2H2S + O2 = S2(г) + 2H2O(г) |
19 | H2S(г) + O3 = SO2 + H2O(г) |
20 | 2H2S = 2H2 +S2(г) |




