Министерство образования Пензенской области
Государственное автономное профессиональное образовательное учреждение
Пензенской области
«Пензенский многопрофильный колледж»
МЕТОДИЧЕСКАЯ РАЗРАБОТКА ОТКРЫТОГО УРОКА
«Скорость химических реакций»
Разработал преподаватель высшей категории |
2014
Технологическая карта занятия «Скорость химических реакций»
№ | Основные пункты технологической карты | Обязательная общая часть | |||
1 | Наименование дисциплины | Химия | |||
2 | Тема урока | Скорость химических реакций | |||
3 | Тип и вид занятия | Комбинированный урок Повторение, лекция | |||
4 | Цели занятия (как ожидаемые результаты обучения) | В результате проведённого урока учащиеся: продолжают формирование понятия «скорость химических реакций», выясняют, от каких факторов зависит скорость химических реакций; продолжают учиться обрабатывать и анализировать экспериментальные данные; выяснять взаимосвязь между скоростью химических реакций и внешними факторами; продолжают развитие коммуникативных умений в ходе парной и коллективной работы; акцентировать внимание на важности знаний о скорости химической реакции протекающих в быту (коррозия металла, прокисание молока, гниение и др.) закрепляют умение работать с электронным пособием, таблицами, справочным материалом, дополнительной литературой | |||
5 | Методы обучения | Частично - поисковый (репродуктивный) | |||
6 | Формируемые компетенции (общие компетенции (ОК) и профессиональные компетенции (ПК)) | Общие: формулировать свои ценностные ориентиры по отношению к изучаемым дисциплинам и сферам деятельности; уметь принимать решения, брать на себя ответственность за их последствия; осуществлять индивидуальную образовательную траекторию с учётом общих требований и норм; владеть разными видами речевой деятельности. Профессиональные: владеть навыками работы с различными источниками информации (электронное пособие, Интернет, словари, справочники, книги, учебники); самостоятельно искать, извлекать, анализировать и отбирать необходимую для решения учебных задач информацию; ориентироваться в информационных потоках, уметь осознанно воспринимать информацию; владеть навыками использования информационных устройств (ПК, принтер); применять для решения учебных задач информационные и телекоммуникационные технологии: аудио и видеозапись, электронную почту, Интернет; уметь применять на практике полученные знания. | |||
7 | Тезаурусное поле занятия | Химическая кинетика – раздел химии, в котором изучаются скорости и механизмы химических реакций. Система в химии – рассматриваемое вещество или совокупность веществ. Фаза - часть системы, которая отделена от других частей поверхностью раздела. Гомогенная (однородная) система – система, состоящая из одной фазы. Гетерогенная (неоднородная) система – система, состоящая из двух или нескольких фаз. Скорость гомогенной химической реакции – количество вещества, вступающего в реакцию или образующегося в результате реакции в единицу времени в единице объёма системы. Скорость гетерогенной химической реакции – количество вещества, вступающего в реакцию или образующегося в результате реакции в единицу времени на единице поверхности раздела фаз. Факторы, влияющие на скорость реакции: - природа реагирующих веществ; - концентрация реагирующих веществ; - температура; - присутствие катализаторов. Катализатор – вещество, которое изменяет (увеличивают) скорость реакции, но не расходуется в результате реакции. Ингибитор - вещество, которое изменяет (замедляют) скорость реакции, но не расходуется в результате реакции. Ферменты (энзимы) – биологические катализаторы. Закон действующих масс. | |||
8 | Используемые средства, в т. ч. средства ИКТ | Компьютерный терминал, мультимедийный проектор, демонстрационный экран, ноутбук, колонки, 15 персональных компьютеров, диск с презентациями и показом опытов по гидролизу солей; основная и дополнительная литература | |||
9 | Междисциплинарные и межкурсовые связи | Межпредметные: биология (химические реакции в живом организме), физика (понятие о тепловом эффекте реакций, влияние физических факторов на скорость химической реакции) | |||
10 | Образовательные ресурсы (в т. Ч. Интернет) | Система электронного обучения «Академия-Медиа», химические сайты XuMuk. ru, Alhimik. ru, Полезная информация по химии, основная и дополнительная литература | |||
Этапы занятия | Длительность этапа | Результаты | Критерии и способ оценки | Функция преподавателя | Организация деятельности учащихся |
1 | Организация начала занятия | 5 мин | Приветствие Проверка подготовки студентов к занятию Готовность оборудования Запуск системы ЭО Определение отсутствующих студентов | Приветствие Дежурный называет отсутствующих студентов | |
2 | Проверка домашнего задания | 10 мин | Выдача карточек с индивидуальным заданием, вывод на экран заданий для всей группы | Выполнение заданий, самопроверка и проверка в паре | |
3 | Этап подготовки студентов к активному и сознательному усвоению нового материала | 3 мин | Объявление темы урока и определение его задач | Запись темы в тетрадь Поиск соответствующей темы в системе ЭО | |
4 | Актуализация знаний, мотивационный этап | 12 мин | Фронтальная беседа Постановка вопросов Управление дискуссией | Ответы на вопросы, дополнение ответов друг друга | |
5 | Этап усвоения новых знаний | 20 мин | Выдача заданий в электронном пособии, консультации | Работа с электронным пособием | |
6 | Первичная проверка усвоения знаний | 10 мин | Выдача заданий, контроль выполнения | Выполнение заданий | |
7 | Первичное закрепление знаний | 15 мин | Демонстрация опытов по теме с помощью проектора и экрана | Наблюдение Составление уравнений реакций | |
8 | Контроль и самопроверка знаний. Рефлексивно-контролирующий этап | 7 мин | Контроль написания уравнений, оценка, обобщение | Самопроверка, выводы | |
9 | Подведение итогов занятия | 3 мин | Проведение анализа успешности достижения цели занятия Оценка перспективы последующей работы | ||
10 | Информация о домашнем задании, инструктаж по его выполнению | 5 мин | Выдача домашнего задания Проведение инструктажа по его выполнению | Запись домашнего задания, вопросы по его уточнению |



Ход урока:
I. Организация начала занятия.
II. Подготовка к основному этапу занятия.
III. Конкретизация знаний, закрепление способов действий, систематизация знаний о закономерностях, с помощью которых можно управлять химическими реакциями.
IV. Подведение итогов занятия, информация о домашнем задании.
I. Организация начала занятия
Задача этапа: подготовить учащихся к работе на занятии.
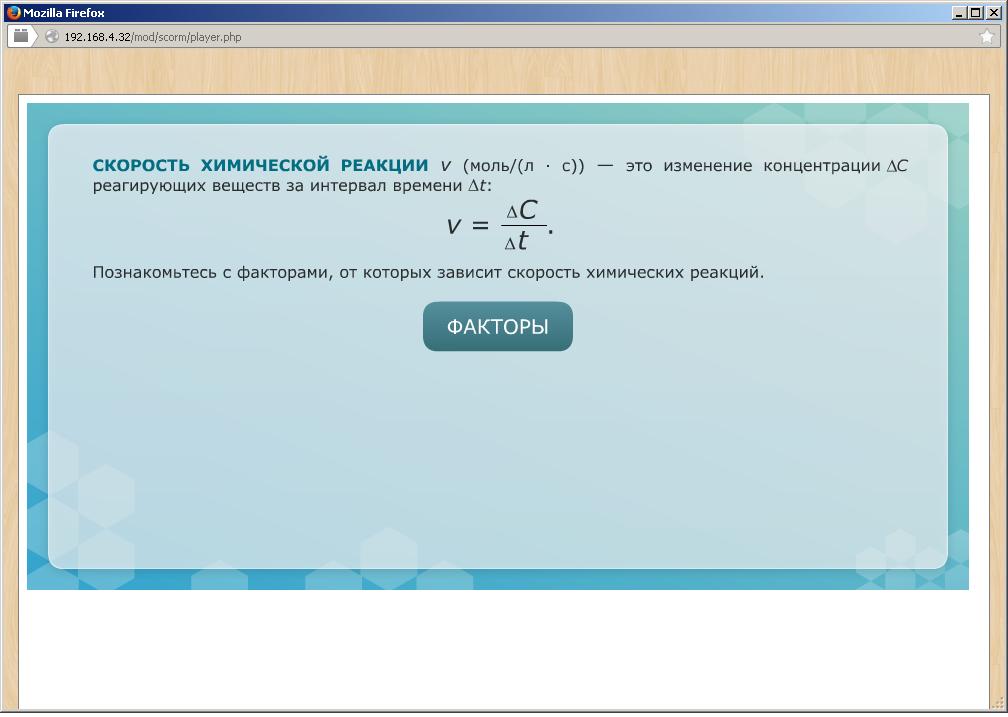
Учитель: сегодня мы продолжим изучение темы «Скорость химической реакции» и выясним, может ли человек, обладая определенными знаниями, управлять химической реакцией. Для решения этой проблемы мы отправляемся в виртуальную лабораторию. Чтобы войти в нее, необходимо показать свои знания о скорости химической реакции.
II. Подготовка к основному этапу занятия
Задачи этапа: актуализация опорных знаний и умений, обеспечение мотивации и принятия учащимися цели урока.
Актуализация знаний учащихся
Учитель организует фронтальную беседу:
Вопрос 1: что изучает химическая кинетика?
Предполагаемый ответ: химическая кинетика – наука о закономерностях протекания химических реакций во времени.
Вопрос 2: на какие две группы можно разделить реакции в зависимости от состояния химических веществ?
Предполагаемый ответ: если химические реакции происходят в однородной среде, например в растворе или газовой фазе, их называют гомогенными. А если реакция идет между веществами, находящимися в разных агрегатных состояниях, их называют гетерогенными.
Вопрос 3: как определить скорость гетерогенной реакции?
Предполагаемый ответ: скорость гетерогенной реакции определяется как изменение количества вещества в единицу времени на единице поверхности (учащийся записывает формулу на доске)

Вопрос 4: как определить скорость гомогенной реакции?
Предполагаемый ответ: Скорость гомогенной реакции определяется как изменение концентрации одного из веществ в единицу времени (учащийся записывает формулу на доске).

Учитель: теперь, используя свой жизненный опыт, предположите:
Вопрос 5: что сгорит быстрее: деревянная доска или древесные стружки?
Предполагаемый ответ: древесные стружки сгорят быстрее.
Вопрос 6: где быстрее сгорит уголь: на воздухе или в кислороде?
Предполагаемый ответ: быстрее уголь сгорит в кислороде.
III. Конкретизация знаний, закрепление способов действий, систематизация знаний о закономерностях, с помощью которых можно управлять химическими реакциями.
Задача этапа: обеспечить усвоение знаний и способов действий, организовав активную продуктивную деятельность учащихся.
Вводный рассказ учителя (сопровождается компьютерной презентацией):
Учитель: используя свой жизненный опыт, вы правильно предположили. Действительно, скорость химической реакции зависит от многих факторов. Основными из них являются: природа и концентрация реагирующих веществ, давление, температура, поверхность соприкосновения реагирующих веществ, действие катализаторов.
По мере работы мы также будем использовать информацию учебника.
Учащиеся под руководством учителя решают каждую экспериментальную задачу, и учитель, используя компьютерную презентацию, подводит учащихся к обоснованным заключениям.
Результат работы:
Фактор, влияющий на скорость | Вывод о влиянии фактора на скорость реакции | Обоснование влияния |
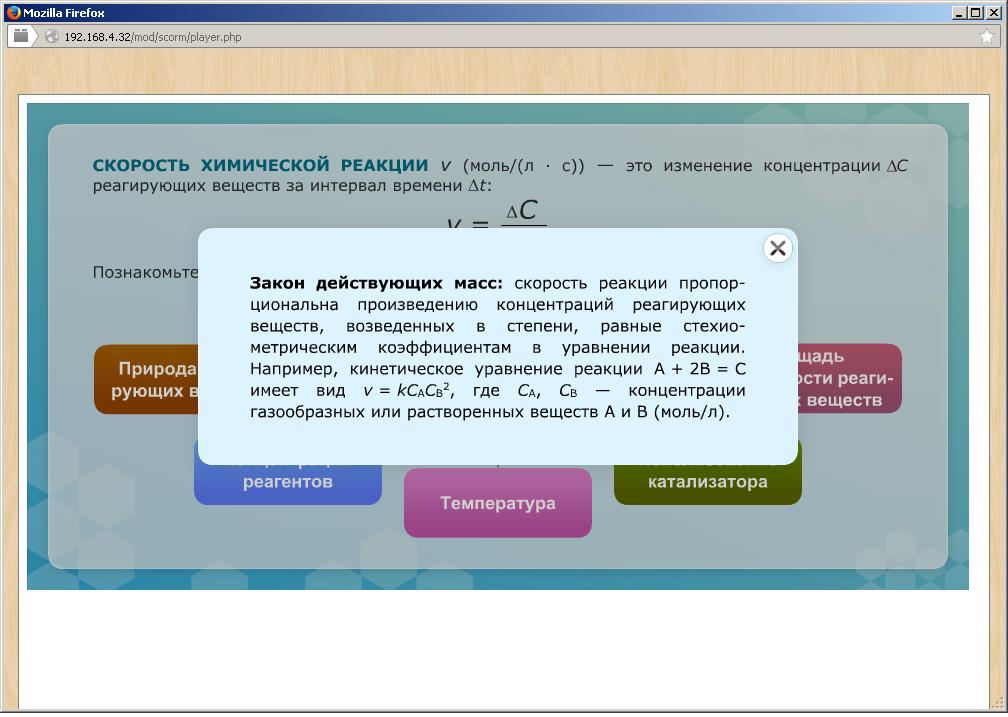
Концентрация реагирующих веществ | Прямая зависимость: чем выше концентрация, тем быстрее протекает реакция. Скорость химической реакции пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных их коэффициентам в уравнении реакции (закон действующих масс) v = k[A]a[B]b[C]c. | Чтобы осуществилось химическое взаимодействие между частицами, они должны столкнуться. Чем больше концентрация реагирующих веществ, тем больше столкновений и соответственно скорость реакции. |
Природа реагирующих веществ | Значение энергии активации определяет влияние природы вещества на скорость реакции. Например, энергия активации соляной кислоты меньше, чем уксусной и поэтому скорость реакции цинка с соляной кислотой выше. | Энергия активации - минимальный избыток энергии, который должна иметь частица, чтобы произошло эффективное соударение |
Температура | При повышении температуры скорость реакции увеличивается согласно правилу Вант – Гоффа: повышение температуры на каждые 10 градусов приводит к увеличению скорости реакции в 2-4 раза.
| Повышение температуры увеличивает долю «активных» молекул, способных преодолеть энергетический барьер реакции. |
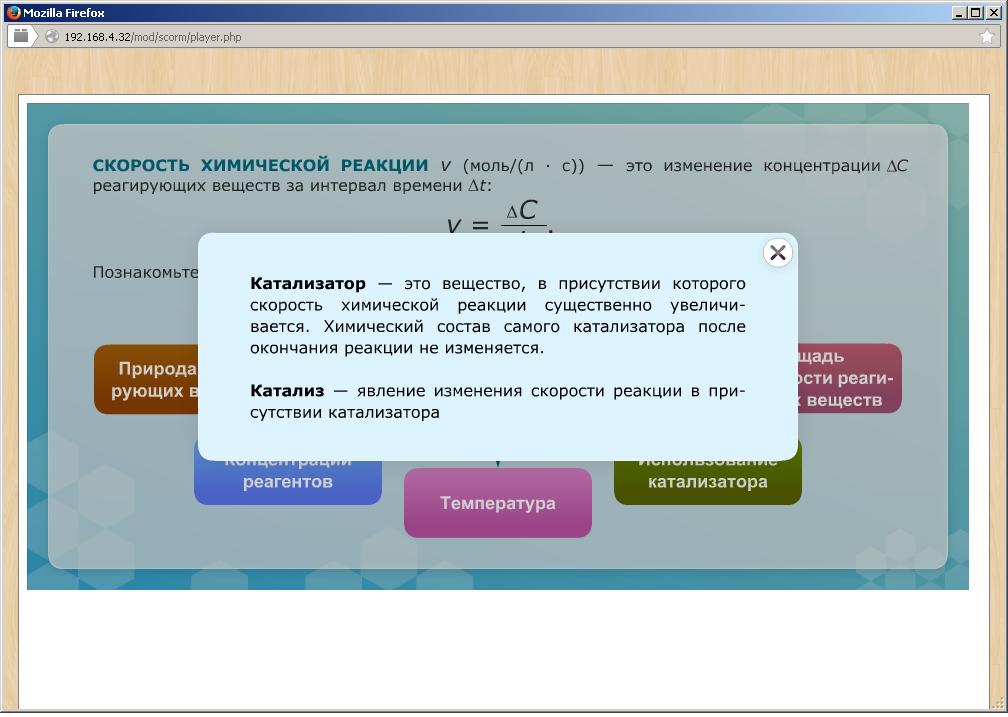
Действие катализатора | Катализатор – вещество, ускоряющее химическую реакцию, и остающееся неизменным по окончании реакции. Например, оксид ванадия, оксид марганца, ферменты. Ингибитор – вещество, замедляющее скорость реакции. | Катализатор изменяет механизм реакции, направляя ее по энергетически более выгодному пути с меньшей энергией активации. |
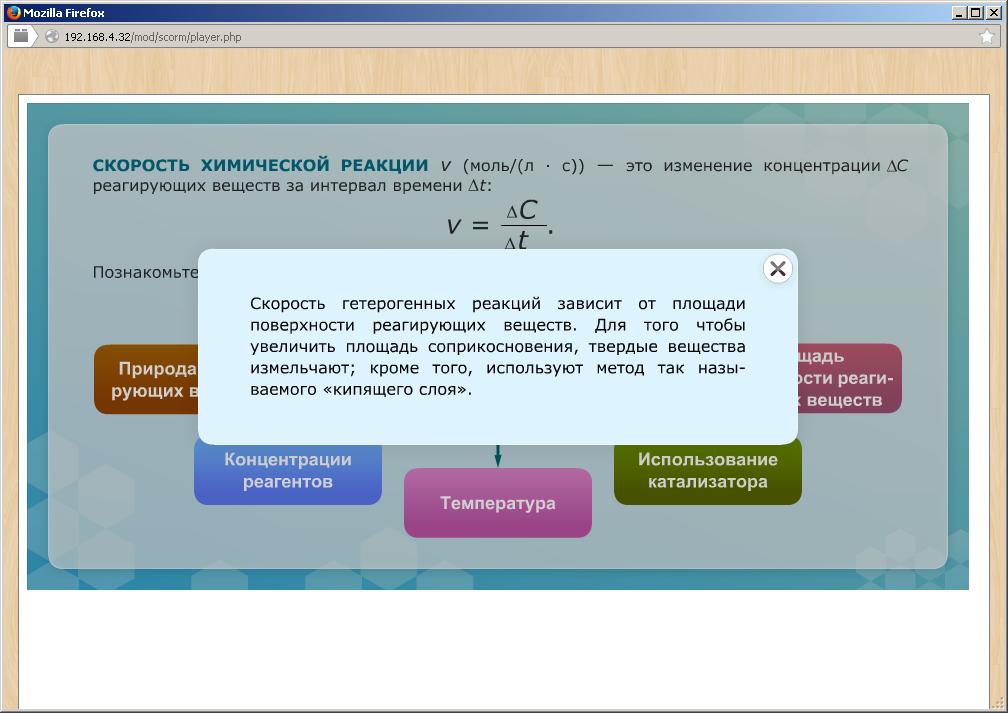
От поверхности соприкосновения | При измельчении веществ, при растворении их в воде перед реакцией, скорость ее будет выше | Измельченные или растворенные вещества имеют больше площадь контакта для молекул |
Закрепление материала.
Задача: для реакции были взяты вещества при температуре 40 С, затем их нагрели до 70 С. Как изменится скорость химической реакции, если температурный коэффициент ее равен 2?
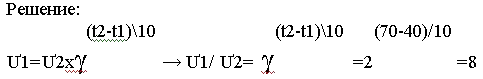
Ответ: в 8 раз увеличится скорость химической реакции.
Учитель: итак, какой вывод мы можем сделать: может ли человек управлять скоростью реакций?
Предполагаемый ответ: да, может, если обладает знаниями о химической кинетике.
IV. Подведение итогов занятия, информация о домашнем задании
Задачи этапа: оценить работу на уроке и показать значение проделанной работы для последующего изучения темы.
Учитель: давайте вспомним ход урока, что мы сегодня узнали, чему научились?
Рефлексия. Высказывания учащихся.
Учитель: домашнее задание: параграф 6.1, выучить информацию таблицы. Выполнить упражнения 5, 6, 8 на стр. 108-109.




