Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего образования «Алтайский государственный университет»
Кафедра физической и неорганической химии
ФОНД
ОЦЕНОЧНЫХ СРЕДСТВ
по дисциплине
Физическая химия
для направления подготовки 04.03.01 Химия
профиль: Физическая химия и нанотехнологии функциональных материалов
Разработчики:
доцент кафедры физической и неорганической химии___________
должность
____________//
подпись
доцент кафедры физической и неорганической химии___________
должность
____________//
подпись
Барнаул 2017
Визирование ФОС для исполнения в очередном учебном году Фонд оценочных средств пересмотрен, обсужден и одобрен для исполнения | |
Внесены следующие изменения дополнения: | Протокол от июня 2017 г. №____ Зав. кафедрой , д. ф.-м. н., профессор фио, должность |
Визирование ФОС для исполнения в очередном учебном году Фонд оценочных средств пересмотрен, обсужден и одобрен для исполнения | |
Внесены следующие изменения и дополнения: | Протокол от___________ №____ Зав. кафедрой , д. ф.-м. н., профессор фио, должность |
Визирование ФОС для исполнения в очередном учебном году Фонд оценочных средств пересмотрен, обсужден и одобрен для исполнения | |
Внесены следующие изменения и дополнения: | Протокол от___________ №____ Зав. кафедрой , д. ф.-м. н., профессор фио, должность |
Визирование ФОС для исполнения в очередном учебном году Фонд оценочных средств пересмотрен, обсужден и одобрен для исполнения | |
Внесены следующие изменения и дополнения: | Протокол от___________ №____ Зав. кафедрой , д. ф.-м. н., профессор фио, должность |
Перечень компетенций, с указанием этапов их формирования в процессе освоения образовательной программы
Перечень формируемых компетенций:
Компетенции/контролируемые этапы | Показатели | Наименование оценочного средства |
Начальный этап формирования компетенций осуществляется в период освоения учебной дисциплины и характеризуется освоением учебного материала | ||
ОПК-1: способностью использовать полученные знания теоретических основ фундаментальных разделов химии при решении профессиональных задач | Знает: знать теоретические основы дисциплины физическая химия Умеет: уметь выполнять стандартные действия (классификация веществ, составление схем процессов, систематизация данных и т. п.) с учетом основных понятий и общих закономерностей, формулируемых в рамках дисциплины физическая химия Владеет: владеть навыками работы с учебной литературой по дисциплине физическая химия | |
ОПК-2: владением навыками проведения химического эксперимента, основными синтетическими и аналитическими методами получения и исследования химических веществ и реакций | Знает: знать стандартные методы получения, идентификации и исследования свойств веществ и материалов, правила обработки и оформления результатов работы, нормы ТБ Умеет: уметь проводить простые химические опыты по предлагаемым методикам Владеет: владеть базовыми навыками проведения химического эксперимента и оформления его результатов | |
Базовый этап формирования компетенции (ий) (формируется по окончании изучения дисциплины (модуля)) | ||
ОК-6: способностью работать в коллективе, толерантно воспринимать социальные, этнические, конфессиональные и культурные различия | Знает: психологию делового общения Умеет: толерантно воспринимать социальные, этнические, конфессиональные и культурные различия Владеет: приемами взаимодействия с сотрудниками, выполняющими различные профессиональные задачи и обязанности | |
ОПК-1: способностью использовать полученные знания теоретических основ фундаментальных разделов химии при решении профессиональных задач | Знает: знать теоретические основы традиционных и новых разделов химии и способы их использования при решении конкретных химических и материаловедческих задач Умеет: решать типовые учебные задачи по дисциплине физическая химия Владеет: владеть навыками работы с научной литературой по дисциплине физическая химия | |
ОПК-2: владением навыками проведения химического эксперимента, основными синтетическими и аналитическими методами получения и исследования химических веществ и реакций | Знает: знать методы получения, идентификации и исследования свойств веществ (материалов) Умеет: уметь проводить многостадийный синтез Владеет: владеть навыками проведения эксперимента и методами обработки его результатов | |
ОПК-6: знанием норм техники безопасности и умением реализовать их в лабораторных и технологических условиях | Знает: знать основные требования к представлению результатов работ в профессиональной сфере деятельности Умеет: уметь анализировать и обобщать результаты эксперимента, формулировать выводы Владеет: владеть навыками планирования, анализа и обобщения результатов эксперимента |
Сопоставление шкал оценивания
4-балльная шкала (уровень освоения) | Отлично (повышенный уровень) | Хорошо (базовый уровень) | Удовлетворительно (пороговый уровень) | Неудовлетворительно (уровень не сформирован) |
100-балльная шкала | 85-100 | 70-84 | 50-69 | 0-49 |
Бинарная шкала | Зачтено | Не зачтено |
Оценивание выполнения практических заданий
4-балльная шкала (уровень освоения) | Показатели | Критерии |
Отлично (повышенный уровень) | Полнота выполнения практического задания; Своевременность выполнения задания; Последовательность и рациональность выполнения задания; Самостоятельность решения; | Студентом задание решено самостоятельно. При этом составлен правильный алгоритм решения задания, в логических рассуждениях, в выборе формул и решении нет ошибок, получен верный ответ, задание решено рациональным способом. |
Хорошо (базовый уровень) | Студентом задание решено с подсказкой преподавателя. При этом составлен правильный алгоритм решения задания, в логическом рассуждении и решении нет существенных ошибок; правильно сделан выбор формул для решения; есть объяснение решения, но задание решено нерациональным способом или допущено не более двух несущественных ошибок, получен верный ответ. | |
Удовлетворительно (пороговый уровень) | Студентом задание решено с подсказками преподавателя. При этом задание понято правильно, в логическом рассуждении нет существенных ошибок, но допущены существенные ошибки в выборе формул или в математических расчетах; задание решено не полностью или в общем виде. | |
Неудовлетвори-тельно (уровень не сформирован) | Студентом задание не решено. |
Оценивание выполнения лабораторных работ
Бинарная шкала (уровень освоения) | Показатели | Критерии |
Зачтено (базовый уровень) | Полнота выполнения лабораторной работы; Правильность ответов при получении допуска к лабораторной работе; Своевременность оформления отчета по лабораторной работе; Последовательность и рациональность действий при выполнении лабораторной работы; Качество оформления отчета по лабораторной работе ; | Лабораторная работа выполнена студентом в полном объеме, при получении допуска к лабораторной работе возможно наличие несущественных ошибок. Отчет сдан вовремя и оформлен надлежащим образом. |
незачтено (уровень не сформирован) | Лабораторная работа студентом не выполнена. |
Оценивание ответа на экзамене
4-балльная шкала (уровень освоения) | Показатели | Критерии |
Отлично (повышенный уровень) | Полнота изложения теоретического материала; Полнота и правильность решения практического задания; Правильность и/или аргументированность изложения (последовательность действий); Самостоятельность ответа; Культура речи; | Студентом дан полный, в логической последовательности развернутый ответ на поставленный вопрос, где он продемонстрировал знания предмета в полном объеме учебной программы, достаточно глубоко осмысливает дисциплину, самостоятельно, и исчерпывающе отвечает на дополнительные вопросы, приводит собственные примеры по проблематике поставленного вопроса, решил предложенные практические задания без ошибок. |
Хорошо (базовый уровень) | Студентом дан развернутый ответ на поставленный вопрос, где студент демонстрирует знания, приобретенные на лекционных и семинарских занятиях, а также полученные посредством изучения обязательных учебных материалов по курсу, дает аргументированные ответы, приводит примеры, в ответе присутствует свободное владение монологической речью, логичность и последовательность ответа. Однако допускается неточность в ответе. Решил предложенные практические задания с небольшими неточностями. | |
Удовлетворительно (пороговый уровень) | Студентом дан ответ, свидетельствующий в основном о знании процессов изучаемой дисциплины, отличающийся недостаточной глубиной и полнотой раскрытия темы, знанием основных вопросов теории, слабо сформированными навыками анализа явлений, процессов, недостаточным умением давать аргументированные ответы и приводить примеры, недостаточно свободным владением монологической речью, логичностью и последовательностью ответа. Допускается несколько ошибок в содержании ответа и решении практических заданий. | |
Неудовлетвори-тельно (уровень не сформирован) | Студентом дан ответ, который содержит ряд серьезных неточностей, обнаруживающий незнание процессов изучаемой предметной области, отличающийся неглубоким раскрытием темы, незнанием основных вопросов теории, несформированными навыками анализа явлений, процессов, неумением давать аргументированные ответы, слабым владением монологической речью, отсутствием логичности и последовательности. Выводы поверхностны. Решение практических заданий не выполнено. Т. е студент не способен ответить на вопросы даже при дополнительных наводящих вопросах преподавателя. |
ПРАКТИЧЕСКИЕ ЗАДАНИЯ Перечень заданий /вопросов | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 1. Первый закон термодинамики. Вычисление работы и теплоты при различных процессах. Теоретические вопросы. 1. Понятия химической термодинамики: изолированная система, обратимый и равновесный процесс. 2. Изобарная и изохорная теплоемкость, их взаимосвязь для любого вещества и для идеального газа. 3. Зависимость теплоемкости от температуры, взаимосвязь истинной и средней теплоемкости. 4. Математические выражения первого закона термодинамики для элементарного и конечного процесса. 5. Формулы для вычисления теплоты и работы в различных процессах с идеальным газом. Задачи. 1. Какое количество теплоты потребуется для нагревания 1 м3 воздуха от 0 до 1°С при постоянном объеме и начальном давлении р = 1,013·105 Па? Плотность воздуха при нормальных условиях 1,29 кг/м3, удельная теплоемкость при постоянном давлении Ср = 1,01 Дж/(г·К). 2. Какое количество теплоты потребуется, чтобы нагреть 10 г паров ртути на 10° при постоянном давлении? (Пары ртути одноатомны). 3. Найти изменение внутренней энергии при испарении 0,2 кг этанола при температуре его кипения под давлением 1,013·105Па. Теплота парообразования спирта при температуре кипения равна 857,7 Дж/г, а удельный объем пара равен 0,607 м3/кг. Объемом жидкости пренебречь. 4. При 0°С и начальном давлении 5065 гПа 0,002 м3 азота расширяются изотермно до давления 1013 гПа. Вычислить работу и количество поглощенной теплоты. 5. Определить работу адиабатного сжатия 1 моль двухатомного идеального газа при повышении температуры от 15 до 25 °С. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 2. Первый закон термодинамики. Термохимия. Закон Гесса. Методы приближенного расчета тепловых эффектов. Теоретические вопросы. 1. Понятие теплового эффекта химической реакции. Экзотермические и эндотермические реакции. Теплота образования и теплота сгорания. 2. Закон Гесса. Следствия из закона Гесса. 3. Методы расчета тепловых эффектов реакций. 4. Приближенные методы расчета теплот образования и сгорания. Задачи. 1. Рассчитать теплоту образования жидкого сероуглерода по следующим данным: S(мон) + O2(г) = SO2(г) – 296,9кДж CS2(ж) + 3O2(г) = CO2(г) + 2SO2(г) – 1109,0 кДж C(графит) + О2(г) = СO2(г) – 393,5 кДж 2. Вычислить теплоты образования органических веществ по методу поправок и по энергиям связей при 25°С. По полученным значениям теплот образования для газов вычислить теплоты образования для указанного агрегатного состояния и рассчитать расхождение между вычисленными и табличными данными.
| ||||||||||||||||||||||||||||||||||||||
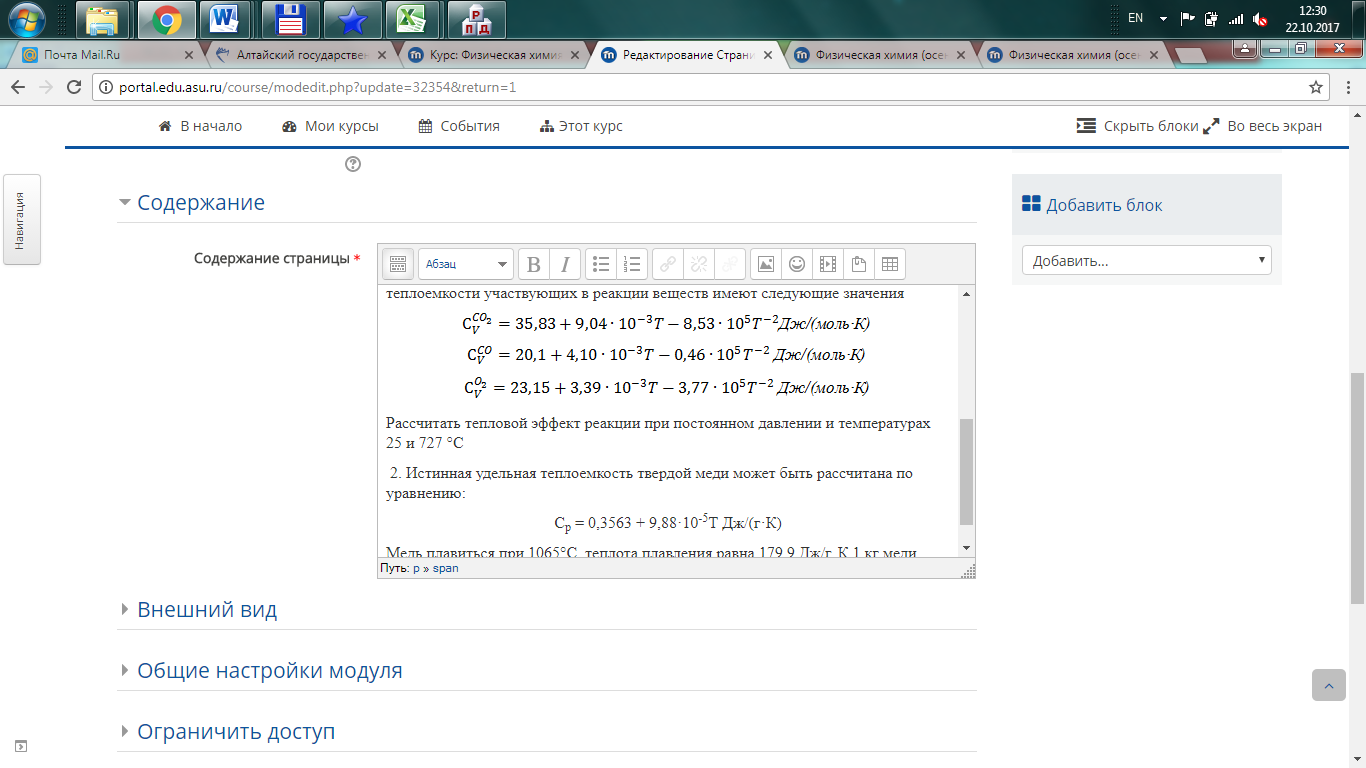
Практическое занятие № 3. Закон Кирхгофа. Теплоемкость. Теоретические вопросы. 1. Теплоемкость. Виды теплоемкости. 2. Зависимость теплоемкости от температуры. 3. Закон Кирхгофа. 4. Анализ уравнения Кирхгофа. Задачи. 1. Тепловой эффект реакции CO (г) + 1/2O2 (г) = CO2 (г) При 0°С и постоянном давлении составляет -284,5 кДж/моль, а молярные теплоемкости участвующих в реакции веществ имеют следующие значения
Рассчитать тепловой эффект реакции при постоянном давлении и температурах 25 и 727 °С 2. Истинная удельная теплоемкость твердой меди может быть рассчитана по уравнению: Сp = 0,3563 + 9,88·10-5T Дж/(г·К) Медь плавиться при 1065°С, теплота плавления равна 179,9 Дж/г. К 1 кг меди, взятому при 15°С, подведено 541,2кДж. Какое количество меди расплавилось. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 4. Второй закон термодинамики. Вычисление энтропии, энергии Гиббса и Гельмгольца в различных процессах. Теоретические вопросы. 1. Второе начало термодинамики. 2. Вычисление КПД. 3. Цикл Карно. 4. Принцип Каратеодори. 5. Энтропия. Расчет энтропии в различных процессах. Задачи. 1. Смешаны 0,002 м3 гелия и 0,002 м3 аргона при 27 єС и 1,013·105 Па каждый. После изотермного смешения полученная газовая смесь нагрета до 327 єС при постоянном объеме. Вычислить общее возрастание энтропии, учитывая, что молярнаятеплоемкость обоих газов одинакова и равна 2. При 25 єС энтропии ромбической и моноклинной серы соответственно равны 31,88 и 32,55 Дж/(моль·К), а теплоты образования равны 0,00 и 0,30 кДж/моль. Рассчитать ДG и ДF для процесса Sромб → Sмон при 25 єС. Пренебречь приближенно различием плотностей обеих модификаций серы. Какая из двух модификаций серы является более устойчивой при 25 єС? Дайте приближенную оценку температуры перехода, при которой обе модификации серы находятся в равновесии, принимая для ДS и ДН значения при 25 єС. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 5. Термодинамика растворов: способы выражения концентрации растворов, парциальные мольные величины, закон Рауля и Генри Теоретические вопросы. 1. Способы выражения концентраций растворов. 2. Парциальные мольные величины. 3. Закон Рауля. 4. Закон Генри. Задачи. 1. Выразить концентрацию 20% (масс.) водного раствора Al2(SO4)3, плотностью 1,226 г/мл, через молярность, мольные доли и моляльность. 2. Рассчитать плотность раствора метанола, с содержанием метанола 20 масс. %, если парциальный мольный объем воды равен 18,0 мл, метанола - 37,8 мл. 3. Рассчитать теплоту растворения 1 моль HCl в 3 моль H2O, если изменения парциальных мольных энтальпий H2O 36,28 кДж/моль и HCl -5,77 кДж/моль. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 6. Идеальная растворимость твердых тел. Криоскопия. Осмотическое давление. Теоретические вопросы. 1. Растворимость твердых тел. 2. Законы предельно разбавленных растворов. Температура кипения предельно разбавленных растворов. Температура замерзания предельно разбавленных растворов. Осмотическое давление предельно разбавленных растворов. 3. Равновесие жидкость - пар. 4. Перегонка жидких бинарных смесей. Задачи. 1. Жидкий SO2 кипит при 10°С. Теплота испарения ее при этой температуре 25,52 кДж/моль. вычислить температуру кипения раствора, содержащего 1 моль SO3 на 20 моль SO2. 2. Водный раствор содержит 0,5% (масс.) мочевины (NH2)2CO и 1% (масс.) глюкозы C6H12O6. Какова его температура замерзания, если криоскопическая постоянная воды равна 1,86°. 3. При 60°С давление пара этанола равно 470 гПа, а давление пара метанола - 833 гПа. Смесь этих спиртов, которую можно считать идеальной, содержит 50% (масс.) каждого компонента. Каков состав пара над раствором при этой температуре. | ||||||||||||||||||||||||||||||||||||||
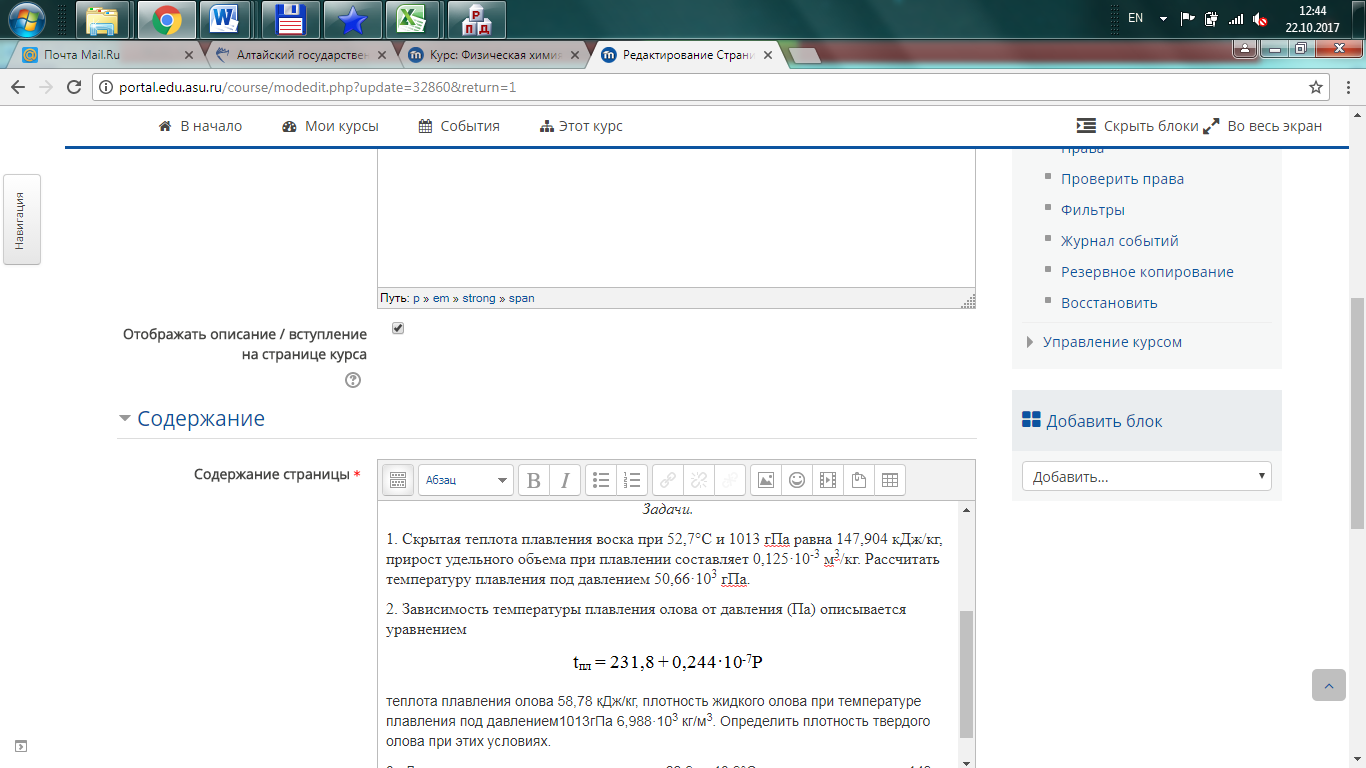
Практическое занятие № 7. Фазовые равновесия: уравнение Клапейрона - Клаузиуса Теоретические вопросы. 1. Уравнение Клапейрона-Клаузиуса.. 2. Применение уравнения Клапейрона-Клаузиуса к процессам плавления и фазового перехода. 3. Применение уравнения Клапейрона-Клаузиуса к процессам испарения и возгонки. Задачи. 1. Скрытая теплота плавления воска при 52,7°С и 1013 гПа равна 147,904 кДж/кг, прирост удельного объема при плавлении составляет 0,125·10-3 м3/кг. Рассчитать температуру плавления под давлением 50,66·103 гПа. 2. Зависимость температуры плавления олова от давления (Па) описывается уравнением
теплота плавления олова 58,78 кДж/кг, плотность жидкого олова при температуре плавления под давлением1013гПа 6,988·103 кг/м3. Определить плотность твердого олова при этих условиях. 3. Давление этиламина при температуре -22,9 и -13,9°С соответственно равно 148 и 244 гПа. Определить теплоту испарения в этом температурном интервале. | ||||||||||||||||||||||||||||||||||||||
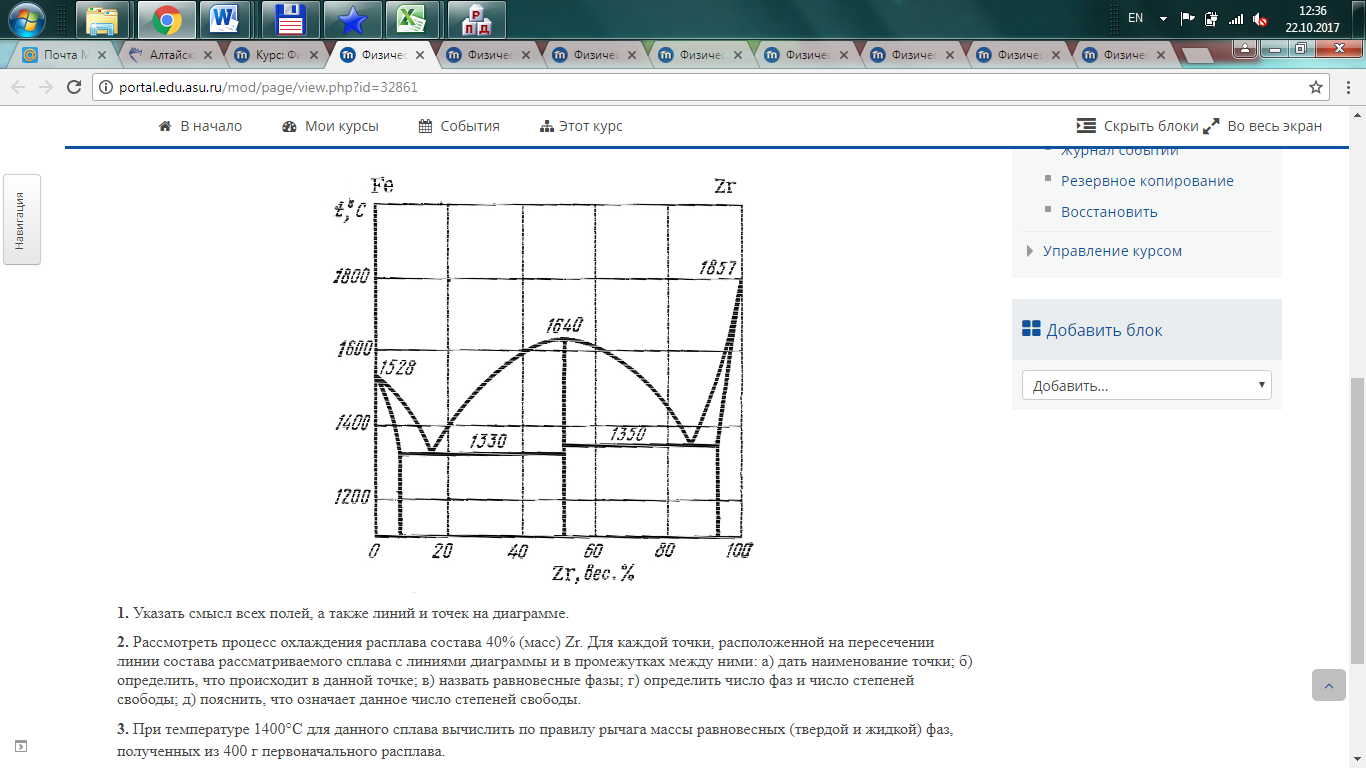
Практическое занятие № 8. Фазовые равновесия: правило фаз Теоретические вопросы. 1. Основные понятия теории фазовых равновесий: фаза, система, компонент, степень свободы. 2. Правило фаз Гиббса. 4. Правило фаз Гиббса для однокомпонентных систем. 5. Правило фаз Гиббса для двухкомпонентных систем 6. Правило фаз Гиббса для трехкомпонентных систем Задачи. 1. Используя рисунок, необходимо:
1. Указать смысл всех полей, а также линий и точек на диаграмме. 2. Рассмотреть процесс охлаждения расплава состава 40% (масс) Zr. Для каждой точки, расположенной на пересечении линии состава рассматриваемого сплава с линиями диаграммы и в промежутках между ними: а) дать наименование точки; б) определить, что происходит в данной точке; в) назвать равновесные фазы; г) определить число фаз и число степеней свободы; д) пояснить, что означает данное число степеней свободы. 3. При температуре 1400°C для данного сплава вычислить по правилу рычага массы равновесных (твердой и жидкой) фаз, полученных из 400 г первоначального расплава. 4. Вычислить состав химических соединений. | ||||||||||||||||||||||||||||||||||||||
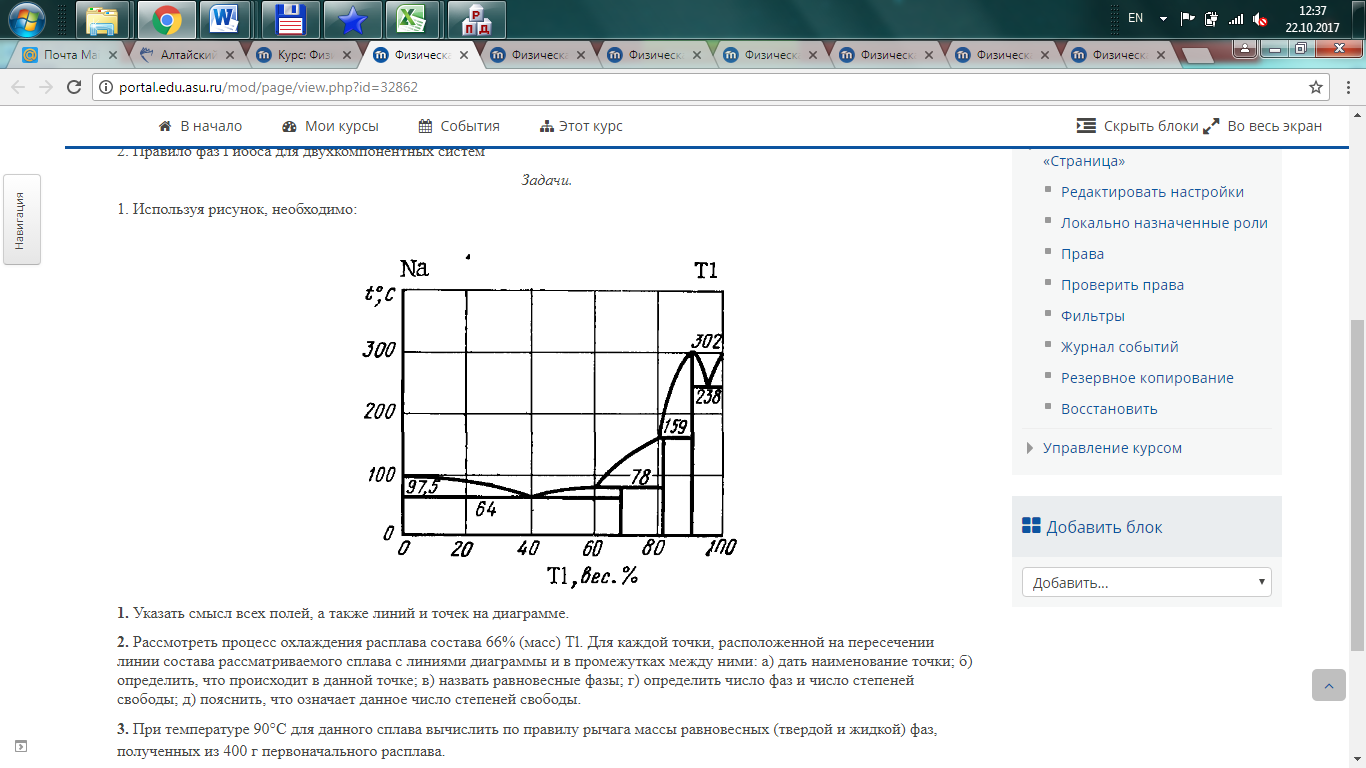
Практическое занятие № 9. Фазовые равновесия: диаграммы состояния Теоретические вопросы. 1. Фаза, линия солидуса, линия ликвидуса, эвтектика, перетектика. 2. Правило фаз Гиббса для двухкомпонентных систем Задачи. 1. Используя рисунок, необходимо:
1. Указать смысл всех полей, а также линий и точек на диаграмме. 2. Рассмотреть процесс охлаждения расплава состава 66% (масс) Tl. Для каждой точки, расположенной на пересечении линии состава рассматриваемого сплава с линиями диаграммы и в промежутках между ними: а) дать наименование точки; б) определить, что происходит в данной точке; в) назвать равновесные фазы; г) определить число фаз и число степеней свободы; д) пояснить, что означает данное число степеней свободы. 3. При температуре 90°C для данного сплава вычислить по правилу рычага массы равновесных (твердой и жидкой) фаз, полученных из 400 г первоначального расплава. 4. Вычислить состав химических соединений. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 10. Химическое равновесие. Вычисление константы равновесия реакции. Уравнение изотермы реакции Теоретические вопросы. 1. Вычисление степени диссоциации. 2. Константа равновесия химической реакции. 3. Уравнение изотермы. Задачи. 1. Пользуясь значением константы равновесия Kp = 50 реакции H2 + I2 = 2HI рассчитать, сколько молей водорода надо взять на каждый моль иода, чтобы I2 при 444єС превратился н а90 % в иодистый водород? 2. Из смеси, содержащей 1 моль азота и 3 моль водорода, в состоянии равновесия при давлении 10,13·105 Па образуется 0,5 моль аммиака. Вычислите Kp для реакции N2 + 3H2 = 2NH3. Чему равен выход аммиака (в объемных процентах)? 3. Для реакции CO2 = CO + 1/2 O2 при 1500 К и 1,013·105 Па, б = 4,8·10-4.Определить в каком направлении пойдет процесс при следующих значениях исходных парциальных давлений компонентов:
| ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 11. Химическое равновесие: уравнение изобары и изохоры химической реакции Теоретические вопросы. 1. Уравнение изобары и изохоры химической реакции. 2. Зависимость константы равновесия от температуры Задачи. 1. Давление диссоциации CaCO3 при температуре 1150 К равно 0,669·105 Па. Теплота диссоциации 167360 Дж/моль. Определить температуру, при которой давление диссоциации CaCO3 равно 1,013·105 Па. 2. Определить константу равновесия и тепловой эффект при 400К реакции C6H11CH3 + C6H6 = C6H5CH3 + C6H12 если для реакции C6H6 + 3H2 = C6H12 (1) C6H5CH3 + 3H2 = C6H11CH3 (2) известны значения констант равновесия как функции температуры: lg Kp,1 = 9590/T - 9,9194lgT + 0,002285T + 8,566 lg Kp,1 = 10970/T - 20,387. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 12. Понятие химической кинетики. Определение константы скорости и порядка реакции. Часть I. Теоретические вопросы. 1. Скорость химической реакции. Факторы, влияющие на скорость химической реакции. 2. Основной постулат химической кинетики. Задачи. 1. Концентрация атомов трития в воздухе приблизительно 5·10-15 моль/л. Период полураспада трития 12 лет. Через сколько лет распадется 90% трития, содержащегося в воздухе? Пополнение содержания трития в воздухе за счет реакций синтеза не учитывать. 2. Раствор (20%-ный) тростникового сахара, имевший правое вращение 34,50є, инвертируется в 0,5 н. молочной кислоте при 298 К. Вращение раствора по истечении 1435 мин достигает +31,10 є, после 11360 мин оно составляет +13,98є и, наконец, после полной инверсии равно -10,77є. Раствор тростникового сахара вращает плоскость поляризации вправо, а смесь продуктов инверсии влево. Угол вращения в обоих случаях пропорционален концентрации растворенных веществ. Реакция протекает по уравнению первого порядка, вычислите константу скорости инверсии и определите, сколько времени потребуется, чтобы инверсии подверглось 90% сахара. 3. Определите константу реакции А(г) → В(г) + С(г) + D(г) по изменению давления в ходе реакции. Вычислите среднее значение константы скорости реакции (V = const, 298K), если
| ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 13. Понятие химической кинетики. Определение константы скорости и порядка реакции. Часть II. Теоретические вопросы. 1. Порядок реакции. Молекулярность реакции. 2. Константа скорости для химических реакций первого, второго и третьего порядков. Задачи. 1. При определенной температуре 0,01 н. раствор уксусно-этилового эфира омыляется 0,002 н. раствором NaOH за 23 мин на 10 %. Через сколько минут он будет омылен до такой же степени 0,005 н. раствором NaOH, если реакция омыления эфира - реакция второго порядка, а щелочи диссоциированы полностью? 2. Окисление FeCl2 при помощи KClO3 в присутствии НСl - реакция третьего порядка. Если время выражать в минутах, а концентрации в - в моль/л, то константа скорости этой реакции равна приблизительно единице. Вычислите концентрацию FeCl2 через 1,5 часа после начала реакции, если начальные концентрации всех реагирующих веществ равны 0,2 моль/л. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 14. Кинетика сложных реакций Теоретические вопросы. 1. Сложные реакции: обратимые, параллельные, последовательные 2. Константа скорости для разного типа сложных реакций. Задачи. 1. Превращение роданида аммония NH4CNS в тиомочевину (NH2)2CS — обратимая мономолекулярная реакция. Рассчитайте константу скорости прямой и обратной реакций при 425 К, используя следующие данные:
При достижении состояния равновесия 21,2 % роданида аммония превращается в тиомочевину. 2. При смешении раствор содержал 73,2 % этилового спирта, 0,677 моль НСООН и 0,0261 % НСl (вода не учитывается). Для исследования кинетики реакции образования этилформиата при 298 К отбирали в различное время пробы объемом 5 мл и оттитровывали Ва(ОН) 2. Результаты титрования:
Вычислите константы образования k1 и разложения k-1 этилформиата в этом растворе и константу равновесия обратимой реакции К, если концентрации воды, этанола и НСl постоянны. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 15. Влияние температуры на скорость химических реакций Теоретические вопросы. 1. Правило Вант-Гоффа. 2. Уравнение Аррениуса. Определение энергии активации графически и аналитически. Задачи. 1. Две реакции одинакового порядка имеют равные предэкспоненциальные множители, но их энергии активации различаются на 41,9 кДж/моль, Рассчитайте соотношения констант скоростей этих реакций при 600 К. 2. Щелочное омыление этилового эфира уксусной кислоты характеризуется следующими константами скоростей при различных температурах:
Вычислите энергию активации и время протекания половины реакции при 298 К, если: 1) взаимодействуют 0,025 моль/л, 2) 0,0125 моль/л раствора эфира и щелочи. 3. В растворе содержится 0,1 моль этилацетата и 0,1 моль NaOH. При 283,2 К в течение 15 мин омыляется 10 % эфира, а при 298,2 К за тот же промежуток времени — 20 %. Вычислите количество эфира, которое омылится в течение 5 мин при 313,2 К. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 1. Теория активированного комплекса. Теоретические вопросы. 1. ППЭ. ППЭ для случая двух атомов, ППЭ для случая трех атомов. 2. Что такое активированный комплекс? 3. Чем активированный комплекс отличается от обычных молекул? 4. Основные положения теории активированного комплекса. 5. Основные формулы в ТАК для расчёта константы скорости химической реакции. Задачи. 1. Две реакции одинакового порядка имеют равные энергии активации, но их энтропии активации различаются на 42 Дж/(моль*K). Рассчитайте соотношения их констант скоростей при 300 K. 2. Вычислите константу скорости димеризации этилена 2С2Н4 →С4Н8 при 673 K, если для 1-бутена ДН = 147 466 Дж/моль; ДS≠ = - 147 Дж/(моль*K). 3. Для реакции пиридина с этилиодидом C6H5N + C2H5I →C8H10NI при 303 K k = 1,72*10-6 л/(моль*с), ДS≠ = - 118,5 Дж/(моль*K). Рассчитайте теплоту активации ДH≠ и энергию активации Е. 4. Константа скорости k для реакции 2NO + О2 → 2NO2 при 600 K равна 6,63*105, а при 645 K — 6,52*105 моль/л. Для обратной реакции k при этих же температурах равна соответственно 83,9 и 407. Вычислите: 1) константы равновесия для этих температур; 2) энергию активации Е прямой и обратной реакций; 3) теплоту активации ДH≠ прямой и обратной реакций. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 2. Теория активных столкновений. Теоретические вопросы. 1. Суть теории активных столкновений. 2. Основные формулы в ТАС для расчёта константы скорости химической реакции. Задачи. 1. Термическое разложение диоксида азота 2NO2 → 2NO + O2 является гомогенной бимолекулярной реакцией. При 627 K константа скорости реакции равна 1,81*103 см3моль-1*c-1. Стерический множитель равен 0,019. Вычислите энергию активации E, приняв диаметр молекулы NO2равным 3,55*10-8 см. Определите долю молекул, обладающих при 627 K энергией, большей E. 2. Константа скорости мономолекулярной реакции разложения азоизопропана C3H7N = NC3H7→ N2 + C6H14 выражается следующим уравнением: k1 = 5,71*1013е-40900/RT. Подсчитайте максимально возможное с точки зрения теории столкновений значение предэкспоненциального множителя, приняв у C3H7N = NC3H7 = 5*10-8 см, c C3H7N = NC3H7 = 1 моль на 22,4 л. Температура опыта 563 K. Сравните полученное значение с опытными. 3. Опытное значение константы скорости реакции между метилиодидом и этилатом натрия CH3I + C2H5ONa →CH3OC2H5 + NaI, протекающей в растворе этилового спирта при 291 K 4,96*10-4 л*моль-1с-1. Приняв радиусы молекул равными соответственно 2,64*10-8 и 2,74*10-8 см, вычислите с помощью уравнения теории столкновений энергию активации этой реакции (р = 0,8). | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 3. Влияние растворителя на величину константы скорости реакции. Теоретические вопросы. 1. Предельный закон Дебая-Хюккеля. 2. Первичный солевой эффект. 3. Вторичный солевой эффект. Задачи. 1. Определите константу скорости реакции СН3Вr + KI = СН3I + KВr в воде при 298 K, если предэкспоненциальный множитель 1,7*1013см3/(моль*с) и энергия активации 76,6 кДж/моль. 2. Определите константу скорости реакции СН3Вr + KI = СН3I + KВr в СН3ОН при 298 K, если предэкспоненциальный множитель 2,3*1013см3/(моль*с) и энергия активации 76,2 кДж/моль. Сопоставьте скорость реакции, протекающей в воде и в метаноле. 3. Определите, во сколько раз изменится константа скорости реакции С2Н5ВrCOO - + S2O32- = C2H4S2O3COO2- + Br - если ионную силу раствора изменить от 0,01 до 0,04. 4. При изучении кинетики некоторой реакции получено, что при ионной силе раствора 5,61 константа скорости этой реакции равна 5,164*10-4. Определите константу скорости этой реакции при ионной силе, равной нулю. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 4. Катализ Теоретические вопросы. 1. Основные закономерности катализа. 2. Гомогенный катализ. Гетерогенный катализ. 3. Ферментативный катализ. Вывод кинетического уравнения ферментативной реакции: а) состоящей из двух элементарных односторонних реакций б) состоящей из двух взаимно противоположных элементарных реакций и третьей элементарной односторонней реакции. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 5. Электропроводность растворов электролитов Теоретические вопросы. 1. Удельная электропроводность. 2. Эквивалентная электропроводность. 3. Закон Кольрауша. 4. Графики зависимости удельной электропроводности, эквивалентной электропроводности и степени диссоциации раствора электролита от концентрации. Задачи. 1. Молярная электрическая проводимость раствора с массовой долей 38 % H2SO4 равна 140 См*см2/моль при 293 К. Определите удельную электрическую проводимость указанного раствора, если его плотность 1,286 г/см3. 2. Электрическое сопротивление 0,02 М раствора KCl при 298 K равно 82 Ом, а сопротивление 0,0025 М раствора K2SO4 в этой же ячейке оказалось равным 326 Ом. Удельная электрическая проводимость раствора KCl равна 2,77*10-3 См/см. Определите молярную электрическую проводимость раствора K2SO4 и постоянную ячейки. 3. Электроды, имеющие поверхность 5 см2 и находящиеся на расстоянии 10 см, помещены в 0,01 М раствор уксусной кислоты при 295 K. При разности потенциалов в 70 В через раствор проходит ток силой 0,005 А. Определите удельную и молярную электрические проводимости раствора, пренебрегая особенностями конструкции ячейки. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 6. Растворы электролитов. Теоретические вопросы. Средний коэффициент активности электролита. Теория Дебая-Хюккеля. Основные положения. Предельный закон Дебая-Хюккеля. Задачи. Вычислить величину ионной силы для раствора, содержащего на 1 литр раствора а) 0,98 г H2SO4; б) 0,01 мольNaCl; в) 0,05 моль CuSO4; г) 0,01 моля CaCl2 и 0,1 моля Na2SO4. Определите константу А в уравнении Дебая-Хюккеля при 25°С для воды, метилового спирта и глицерина. Диэлектрические постоянные для этих сред соответственно равны 78,6; 31,2 и 56,2. Применяя предельный закон Дебая-Хюккеля вычислите значения коэффициента активности для 0,01М водного раствора KCl. Коэффициент А для воды в этих условиях равен 0,54. Вычислите величину коэффициента активности HCl при 25°С в ее 0,01 М водном растворе, предполагая справедливость закона Дебая-Хюккеля с учетом размера ионов. Коэффициенты А и В для данного случая соответственно равны 0,513 и 0,307·108. Средний эффективный диаметр иона HCl (а) равен 5,3·10-8 см. Молярные электрические проводимости 0,1М растворов LiNO3, NaNO3 и NaCl при 291К соответственно равны 79,2; 87,2; 92,0 См·см2/моль. Рассчитайте молярную электрическую проводимость 0,1 М раствора LiCl. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 7. Числа переноса Теоретические вопросы Подвижность ионов. Числа переноса ионов. Методы определения чисел переноса. Электрохимические цепи. Электролиз. Кулонометрия. Задачи. Водный раствор сульфата меди подвергался электролизу между медными электродами до тех пор, пока на катоде не выделилась медь массой 0,300 г. До электролиза раствор у анода содержал ионы меди массой 1,2140 г, после электролиза – 1,4300 г. Определите числа переноса Cu2+ и SO42-. Раствор с массовой долей гидроксида калия 0,1818% был подвергнут электролизу между платиновыми электродами. После электролиза 64,5 г катодного раствора содержали гидроксид кали массой 0,1256 г, в то время как концентрация средней части электролита не изменилась. В серебряном кулонометре во время электролиза отложилось количество серебра, эквивалентное 0,0310 г KOH. Определите числа переноса К+ и OH-. Раствор HCl подвергся электролизу с платиновыми электродами. Катодное отделение содержало до электролиза 0,177 г и после электролиза 0,163 г хлорид-ионов. В серебряном кулонометре, включенном последовательно, выделилось количество серебра, эквивалентное 0,0825 г хлорид-ионов. Определите t+ и t-. Раствор нитрата серебра, содержащий на 25 г воды нитрат серебра массой 0,1857 г, подвергся электролизу с серебряным анодом. После электролиза анодное пространство содержало 23,14 г воды и нитрат серебра массой 0,2361 г. В последовательно включенном серебряном кулонометре за это время выделилось серебра массой 0,078 г. Определите числа переноса ионов Ag+ и NO3-. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 8. Электродные потенциалы Теоретические вопросы. 1. Уравнение Нернста. ЭДС. 2. Электроды 1 рода. 3. Электроды второго рода. 4. Окислительно-восстановительные электроды. Задачи. 1. Вычислите активность лития в амальгаме, если потенциал электрода LiCl | Li (Hg) c = 1М при 298К по отношению к хлорид-серебренному электроду сравнения в том же растворе равен – 2,20 В. Стандартный потенциал амальгамы лития равен – 2,441 В. Средний коэффициент активности расвтора LiCl примите равным 0,774. Считайте, что литий находится в ртути в атомном состоянии. 2. Вычислите относительно стандартного водородного электрода потенциал медного электрода в растворе, содержащемCuSO4 массой 0,16 г в 200см3 воды. Средний коэффициент активности ионов данного раствора равен 0,573. Стандартный электродный потенциал Cu2+/Cu равен 0,337. | ||||||||||||||||||||||||||||||||||||||
Практическое занятие № 9. Электрохимические элементы. Теоретические вопросы. 1. Электрохимические цепи. 2. ЭДС электрохимических цепей. Задачи. 1. Вычислите ЭДС гальванического элемента Zn | ZnCl2(aq) | AgCl, Ag c=0,0102М если средний коэффициент активности ZnCl2 в указанном растворе равен 0,714, а стандартные потенциалы электродов Zn2+|Zn и Cl-| AgCl, Ag соответственно равны -0,758 и 0,226 В. 2. Вычислите ЭДС элемента:
Стандартный электродный потенциал серебряного электрода равен 0,799 В. Средний коэффициент активности AgNO3 в 3,0 М растворе равен 0,283 В. |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |