Конспект урока по теме:
«Сера. Её физические и химические свойства. Применение».
, филиал МБОУ Сосновская СОШ №2
в селе Третьи Левые Ламки, учитель химии и биологии.
Предмет (направленность): химия.
Возраст детей: 9 класс.
Место проведения: класс филиала МБОУ Сосновская СОШ №2 в селе Третьи Левые Ламки.
Цели урока:
Обучающие:
- охарактеризовать положение серы в Периодической системе сформировать представления об аллотропных модификациях серы, физических и химических свойствах серы знать области применения серы
Развивающие:
- продолжить формирование умений обучающихся характеризовать химические свойства простых веществ исходя из положения элемента в Периодической системе и строения его атома. закрепить знания, умения и навыки обучающихся по составлению ЛСМ и уравнений окислительно-восстановительных реакций.
Воспитывающие:
- развивать у обучающихся навыки логического мышления, умения делать выводы, обобщать и сравнивать,
- развивать навыки работы с различными источниками информации
Оборудование и реактивы: сера, железо, бертолетова соль, вода, пробирки, спиртовка, спички, кристаллизатор, ложка для сжигания веществ, модель молекулы серы S8, ступка, пестик, компьютер, проектор, экран.
Тип урока: изучение нового учебного материала.
Вид урока: комбинированный
Ход урока:
1. Организационный момент.
2. Формирование знаний, умений, навыков.
Продолжаем изучать неметаллы и следующий представитель - сера.
Сера - химический элемент 6А группы, или подгруппы кислорода.
Дадим характеристику положения серы в П. С. химических элементов, составляя ЛСМ.
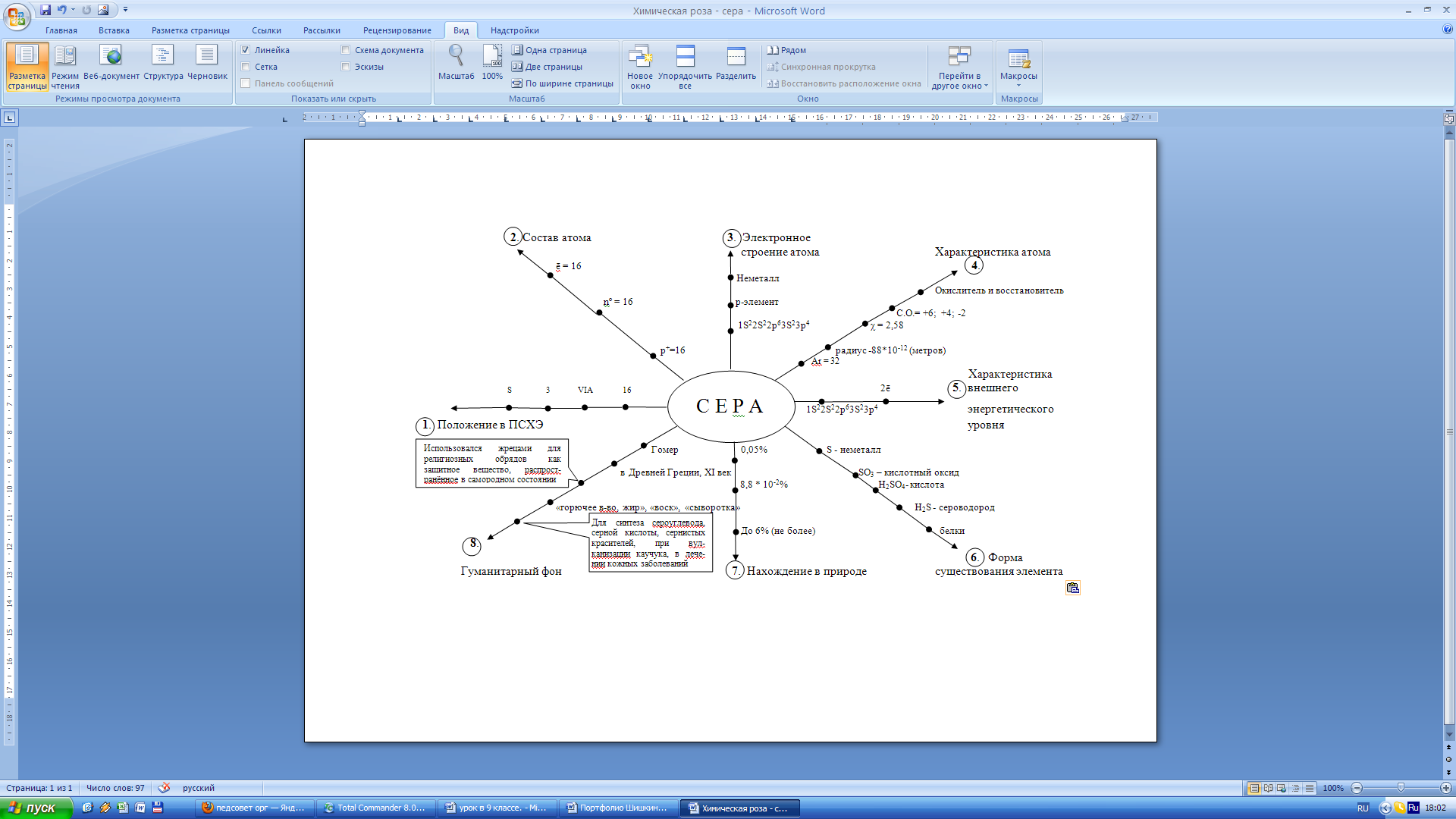
Акцентирую внимание обучающихся на окислительно-восстановительных свойствах серы.
Возможные степени окисления серы:
Sє+2з→S-2 (H2S) , Sє - окислитель
Sє-6з→S+6 (H2SO4, SO3 ), Sє - восстановитель
Sє-4з→S+4 (H2SO3 ,SO2 ), Sє - восстановитель
Физические свойства серы.
Сера - твердое кристаллическое вещество желтого цвета, не растворяется в воде, но хорошо растворяется в сероуглероде; плохо проводит тепло и электрический ток.
Аллотропные модификации серы( с демонстрацией превращения одной модификации в другие модификации и модели кристаллической решетки):
- ромбическая S8(t пл=112,8є С ), ее кристаллы имеют вид лимонно-желтых полупрозрачных октаэдров. В эту модификацию при комнатной температуре превращаются все другие модификации.
- моноклинная (t пл=119,3 єС ), игольчатые кристаллы.
- пластическая (t пл=160 єС ), легкоподвижная жидкость темно-коричневого цвета.
При t =800є С молекула серы состоит из 2 атомов – S2, а при t =1700єС молекула состоит из отдельных атомов.
Природные соединения серы.
Самородная Сульфидная(H2S, ZnS, FеS2) Сульфатная (CaSO4 .2H2O - гипс, Na2SO4.10H2o – глауберова соль В организме человека химический элемент сера содержится в белках, витаминах и гормонах.Химические свойства серы.
1.Взаимодействие с металлами с образованием сульфидов(демонстрация опыта):
2з

Fe0 +Sє→Fe+2S-2, S є– окислитель
2.Взаимодействие с водородом с образованием сероводорода:
2з

H20+Sє→H2+S-2 , Sє - окислитель
3.Взаимодействие с кислородом с образованием оксида серы(IV):
4з

Sє+O20→S+4O2-2, Sє - восстановитель
4.Взаимодействие с бертолетовой солью (демонстрация опыта):
12з
3Sє+2K+Cl+5O3-2→ 2K+Cl - + 3S+4O2-2 , Sє - восстановитель
Просмотр презентации «Применение серы»
3.Закрепление знаний
Осуществите превращения:
S→ZnS→SO→Na2SO3
4.Задание на дом: §22, упр. №1, с 134 учебника
Литература: , учебник «Химия-9» для общеобразовательных учреждений, М., «Дрофа»,2011, 267с.




