«Утверждаю»
Заведующий кафедрой общей
____________
Обобщающее занятие по темам 12-15
Вопросы к проверочной самостоятельной работе по темам 12-15
Тема: «Физическая химия поверхностных явлений».
Дайте определение процессам адсорбции и абсорбции. В чем отличия этих явлений? Поясните, почему адсорбция является самопроизвольным процессом. Сформулируйте правило Дюкло-Траубе? Приведите примеры, иллюстрирующие это правило, с использованием изотермы поверхностного натяжения. Что такое поверхностная активность, её изменение в гомологических рядах? Как поверхностная активность связана с поверхностным натяжением? Поверхностная энергия Гиббса и поверхностное натяжение. Дайте определение, покажите их взаимосвязь. Что такое ПАВ? Как зависит поверхностное натяжение от концентрации ПАВ в растворе и расположения их в поверхностном слое? Изобразите графически. Адсорбция газов на твердых телах. Уравнение Ленгмюра, его анализ. Изотерма Ленгмюра. Сформулируйте основные положения теории адсорбции Ленгмюра. Факторы влияющие на адсорбцию газов на твердом адсорбенте. Молекулярная адсорбция из растворов. Правило Ребиндера, и его практическое применение. Ионная адсорбция из растворов, факторы влияющие на неё. Сформулируйте правила Панета-Фаянса, и его практическое применение. Какие молекулы называются ПАВ, ПИВ, ПНВ. Поведение этих молекул в полярных и неполярных растворителях. Дайте определения понятию сорбции и её виды (адсорбция, абсорция, хемосорбция). Чем отличается физическая адсорбция от хемосорбции. Структура биомембран, сущность поверхностных явлений, протекающих в биомембранах. Роль процессов адсорбции в жизнедеятельности организма. Физико-химические основы процесса гемосорбции. Принцип метода хроматографии. Использование в медико-биологических исследованиях. Строение ПАВ. Виды ПАВ и применение их в медицине. ПАВ в организме. Природа ПИВ. Изотерма поверхностного натяжения ПИВ. Поведение ПИВ в воде. Формирование поверхностного слоя в гетерогенных системах жидкость-газ. СЭП и пути её изменения.Тема «Физическая химия дисперсных систем и растворов ВМС»
Ba(NO3)2 + K2SO3 → BaSO3↓ + 2KNO3. Изобразите схематически строение мицеллы и укажите знак и заряд гранулы, если стабилизатором будет K2SO3. Укажите составляющие компоненты.
Золь карбоната бария получается по уравнению:K2CO3 + Ba(NO3)2 → BaCO3↓ + 2KNO3. Изобразите схематически строение мицеллы и укажите знак и заряд гранулы, если стабилизатором будет Ba(NO3)2. Укажите составляющие компоненты.
Золь хлорида серебра получен реакцией ионного обмена в избытке хлорида натрия. Изобразите схематически строение мицеллы и укажите знак и величину заряда гранулы. Укажите составляющие компоненты. Золь гидроксида железа получен взаимодействием осадка гидроксида железа (III) c соляной кислотой. Представьте схематически строение мицеллы. Укажите составляющие компоненты. Золь иодида серебра получен в избытке нитрата серебра. Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты. Золь берлинской лазури Fe4[Fe(CN)6]3 получен в избытке хлорида железа (III). Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты. Золь сульфата бария получен реакцией двойного обмена в избытке сульфата калия. Изобразите схематически строение мицеллы, укажите потенциалопределяющие ионы. Укажите составляющие компоненты. Золь гидроксида железа (III) получен методом гидролиза соли FeCl3. Напишите мицеллу этого золя и укажите знак и величину заряда гранулы. Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты. Золь берлинской лазури Fe4[Fe(CN)6]3 получен в избытке К4[Fe(CN)6]. Представьте схематически строение мицеллы, и объясните, от чего зависит знак и величина заряда гранулы. Укажите составляющие компоненты. Перечислите и охарактеризуйте конденсационные методы получения золей. Перечислите и охарактеризуйте методы диспергирования при получении золей. Классификация дисперсных систем по размеру частиц и агрегатному состоянию. Классификация дисперсных систем по межфазному взаимодействию. Дайте определение электроосмосу. Чем электороосмос отличается от электрофореза? Что такое электрофорез? Как его используют в медицине. Обратные электрокинетические явления: потенциал течения, потенциал седиментации. Виды устойчивости дисперсных систем. Какими факторами обуславливаются эти виды устойчивости? Виды диализа. Применение диализа в биологии и медицине. Коагуляция и факторы ее вызывающие. Правило Шульце-Гарди (валентности-значности). Дайте пояснение на примере лабораторной работы – получение золя Fe(ОН)3. Какой закон объясняет оптические свойства коллоидных растворов(эффект Тиндаля)? Что такое опалесценция? Всегда ли при протекании химической реакции образуется мицелла? Назовите основные условия получения неорганического коллоидного раствора. Объясните на конкретном примере образование и строение любой мицеллы. На какие стадии делится процесс коагуляции? Опишите признаки каждой стадии. Молекулярно-кинетические и оптические свойства дисперсных систем. Сравните интенсивность этих свойств в коллоидных и истинных растворах. Дайте определение коагуляции, порога коагуляции и коагулирующей способности электролита. Значение процессов коагуляции для жизнедеятельности организма. Коллоидная защита, ее роль в жизнедеятельности. Пептизация, биологическая роль. 62.Коллоидные ПАВ; биологически важные коллоидные ПАВ (мыла, детергенты, желчные кислоты). Мицеллообразование в растворах ПАВ. Определение критической концентрации мицеллообразования. Липосомы. Высокомолекулярные вещества (ВМВ). Классификация. Структура. Формамакромолекул и типы связей между ними. Гибкость макромолекул.
Расчетные задачи
Задача 1.
Коагуляция 400 мл гидрозоля сульфида мышьяка наступила при добавлении к нему 3,75 мл раствора сульфата алюминия с концентрацией 0,005 моль/л. Вычислить порог коагуляции и коагулирующую способность катионов алюминия по отношению к этому золю?
Задача№2.
К 5 мл золя Fe(OH)3 для начала явной коагуляции необходимо добавить один из следующих растворов: 4 мл 3 М KCl; 0,5 мл 0,01 М K2SO4; 3,9 мл 0,0005 М K4[Fe(CN)6]. Вычислить пороги коагуляции и определить, какой из электролитов имеет максимальную коагулирующую способность.
Задача №3.
Золь хлорида серебра получен при добавлении 20 мл раствора хлорида натрия (С = 0.01 моль/л) к 10 мл раствора нитрата серебра (С = 0.09 моль/л). Составить формулу мицеллы золя и указать направление движения гранул при электрофорезе.
Задача№4
В результате взаимодействия избытка хлорида бария с серной кислотой был получен золь. Приведите строение мицеллы, укажите ее составные части.
Какими методами можно определить заряд коллоидной частицы (гранулы)?
Задача № 5
Золь гидроксида железа (III) получен при добавлении к 85 мл дистиллированной воды 15 мл 2%-го раствора FeCI3. К какому электроду будут перемещаться в электрическом поле частицы образовавшегося золя? При ответе необходимо учитывать, что в дисперсной среде присутствуют ионы FeO+ и СI-. Приведите строение мицеллы.
Задача 6
В четыре пробирки с 1М растворами СН3СООК, КCNS, К2SO4 и KCl поместили по 0,5 г полярного полимера. В каком из растворов электролита набухание полимера максимально, в каком – минимально и почему?
Задача 7.
Рассчитать относительную молекулярную массу белка миоглобина, если постоянные в уравнении Марка–Хаувинка для раствора данного белка в воде равны: К= 2,32⋅10-2 см3/г, α = 0,5; характеристическая вязкость [η] = 3,1 см3/г.
Задача 8.
Изоэлектрическая точка пепсина желудочного сока находится при рН 2,0. Каков будет знак заряда макромолекулы фермента при помещении его в буферный раствор с рН 8,5. Ответ пояснить.
Задача 9.
Желатина помещена в буферный раствор с рН 3. Определить знак заряда частиц желатины, если изоэлектрическая точка белка равна 4,7. Ответ пояснить.
Задача 10.
Изоэлектрическая точка белка альбумина равна 4,9. Белок помещен в буферную смесь с концентрацией водородных ионов 10–6 моль/л. Определить направление движения частиц белка при электрофорезе. Ответ пояснить.
Задача 11.
Концентрация кетоновых тел, накапливаемых в крови больных сахарным диабетом в течение суток, достигает 0,2 моль/л. Рассчитать, какое количество кетоновых тел адсорбируется из крови при проведении гемосорбции, если величина предельной адсорбции равна 3·10–3 моль/г, К = 610–2 моль/л?
Задача12
Полимер массой 3,5 г поместили в емкость с ацетоном. Через 1 ч масса полимера увеличилась на 1,5 г. Рассчитать степень набухания.
Задача 13.
Адсорбция уксусной кислоты на угле описывается уравнением Лэнгмюра. Величина предельной адсорбции составляет 5·10-3 моль/г, константа константа адсорбционного равновесия К равна 0,06 моль/л. Рассчитать адсорбцию уксусной кислоты при равновесной концентрации 0,05 моль/л и массу адсорбированной уксусной кислоты адсорбентом массой 2,5 г.
Задача 14.
Пороги коагуляции гидрозоля гидроксида железа (III) сульфатом натрия и хлоридом калия соответственно равны 0,32 и 20,50 ммоль/л. Определить знак заряда коллоидных частиц золя. Вычислить коагулирующую способность этих электролитов и сопоставить их соотношение с вычисленными по правилу Шульце – Гарди.
Задача 15
Пороговые концентрации электролитов для золя BaSO4 оказались равными: с(KCl) = 256 ммоль/л, c(KNO3) = 260,0 ммоль/л, c(Ba(NO3)2) = 6,0 ммоль/л, , c(Al(NO3)3) = 0,067 ммоль/л. Вычислить коагулирующую способность этих электролитов и сопоставить их соотношение с вычисленными по правилу Шульце – Гарди. Какой из реагентов Ba(NO3)2 или H2SO4 взят в избытке при получении золя?
Эталоны решения задач
Задача 1
Коагуляция 400 мл гидрозоля сульфида мышьяка наступила при добавлении к нему 3,75 мл раствора сульфата алюминия с концентрацией 0,005 моль/л. Вычислить порог коагуляции и коагулирующую способность катионов алюминия по отношению к этому золю.
Эталон решениия. Порог коагуляции раствора сульфата алюминия можно рассчитать по формуле:
1000 СэлVэл 1000· 0,005 моль/л · 3,75 мл
Спор = ----- = ------------ = 0,0464 ммоль/л
Vкр + Vэл (400 + 3,75) мл
Концентрация катионов алюминия в 2 раза больше, чем концентрация соли Al2(SO4)3, поэтому
Спор(Al3+) = 2Спор( Al2(SO4)3 ) = 2 0,0464 = 0,0928 ммоль/л
Коагулирующая способность катионов алюминия по отношению к золю сульфида мышьяка составляет:
КС = 1/Спор = 1 : 0,0928 = 10,78 л/моль
Задача 2
Рассчитать относительную молекулярную массу белка миоглобина, если постоянные в уравнении Марка–Хаувинка–Куна для раствора данного белка в воде равны: К= 2,32⋅10-2 см3/г, α = 0,5; характеристическая вязкость [η] = 3,1 см3/г.
Эталон решения:
Для расчетов используем уравнение ![]()
3,1 = 2,32⋅10-2 М0,5
М0,5 = ![]() = 1,336⋅102 = 133,6, т. е. М0,5 = 133,6.
= 1,336⋅102 = 133,6, т. е. М0,5 = 133,6.
Возводим обе части равенства в квадрат и получаем относительную молекулярную массу:
М = (133,6)2 = 17849.
Ответ: 17849
Задача 4
Изоэлектрическая точка пепсина желудочного сока находится при рН 2,0. Каков будет знак заряда макромолекулы фермента при помещении его в буферный раствор с рН 8,5?
Эталон решения:
При помещении пепсина в раствор с рН среды большей ИЭТ подавляется диссоциация аминогрупп и макромолекулы фермента приобретают отрицательный заряд.
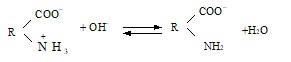
Задача 5
Желатина помещена в буферный раствор с рН 3. Определить знак заряда частиц желатины, если изоэлектрическая точка белка равна 4,7.
Эталон решения:
При помещении желатины в раствор с рН среды, меньшим ИЭТ, подавляется диссоциация карбоксильных групп и частицы желатины приобретают положительный заряд:
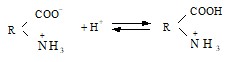
Задача 6
Изоэлектрическая точка белка альбумина равна 4,9. Белок помещен в буферную смесь с концентрацией водородных ионов 10–6 моль/л. Определить направление движения частиц белка при электрофорезе.
Эталон решения:Если концентрация ионов водорода 10–6 моль/л, то рН среды равен: рН= –lg[H+]=.10–6 = 6
Поскольку рН среды > рI (6 > 4,9), то согласно следующему уравнению белок приобретает отрицательный заряд и при электрофорезе перемещается к аноду
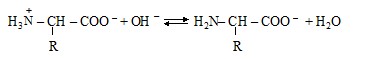
Ответ: заряд молекулы белка отрицательный, перемещение к аноду.
Задача 7
Полимер массой 3,5 г поместили в емкость с ацетоном. Через 1 ч масса полимера увеличилась на 1,5 г. Рассчитать степень набухания.
Эталон решения: Степень набухания полимера определяется по формуле:
![]()
, где m0 – масса полимера до набухания; m – масса полимера после набухания.
![]()
Ответ: б = 42,86%.
Задача 8
Адсорбция уксусной кислоты на угле описывается уравнением Лэнгмюра. Величина предельной адсорбции (емкость адсорбента) составляет 5·10-3 моль/г, константа адсорбционного равновесия К равна 0,06 моль/л. Рассчитать адсорбцию уксусной кислоты при равновесной концентрации 0,05 моль/л.
Эталон решения:
Уравнение Лэнгмюра для адсорбции на твердых адсорбентах имеет вид: C
Г = Г∞ ---
К + C
Определяем величину адсорбции:
5·10-3 моль/г · 0,05 моль/л
Г = ----------- = 2,27·10-3 моль/г
0,06 моль/л + 0,05 моль/л
Ответ: 2,27·10-3 моль/г
Задача 8
Пороги коагуляции гидрозоля гидроксида железа (III) сульфатом натрия и хлоридом калия соответственно равны 0,32 и 20,50 ммоль/л. Определите знак заряда коллоидных частиц золя. Вычислите коагулирующую способность этих электролитов и сопоставьте их соотношение с вычисленными по правилу Шульце – Гарди.
Эталон решения:
Порог коагуляции рассчитывают по формуле:
![]()
Величина, обратная порогу коагуляции, называется коагуляционной способностью (коагулирующим действием): ![]()
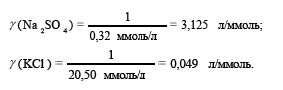
Коагулирующее действие электролитов на коллоидные растворы подчиняется правилу Шульце – Гарди: Коагуляцию золей вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. Коагулирующая способность ионов тем сильнее, чем выше заряд иона-коагулянта. г = z6 – коагулирующее действие иона коагулянта пропорционально его заряду в шестой степени.
г(СI-) : г(SO42-) = 0,049 : 3,125 = 1 : 63,8. Так как катионы во всех электролитах однозарядны, то ионами-коагулянтами являются анионы, следовательно, заряд коллоидной частицы – положительный.
Ответ: г = Na2SO4 обладает наибольшим коагулирующим действием. Гранула золя заряжена положительно, для анионов Cl–и SO42-правило Шульце – Гарди выполняется




