ЦЕНТРА РОССИИ
Второй отборочный этап
ХИМИЯ
Задание 1. В раствор серной кислоты с массовой долей 15% поместили алюминиевый шарик массой 10,8 г. Через некоторое время, когда диаметр шарика уменьшился вдвое, массовая доля кислоты стала 6%.
Рассчитайте: а) массу исходного раствора серной кислоты; б) объем выделившегося водорода; в) массовую долю сульфата алюминия в получившемся растворе.
Задание 2. При взаимодействии 1 г смеси меди, алюминия и магния, взятых в виде порошков, с разбавленным раствором HCl выделяются 900 мл (н. у.) водорода. Из такой же массы указанной смеси можно получить 0,125 г оксида меди (II) в индивидуальном состоянии.
1) Рассчитайте массовую долю (%) каждого компонента смеси.
2) Напишите уравнения реакций, с помощью которых можно из данной смеси выделить медь и получить оксид меди (II). Укажите условия получения оксида меди (II).
3) Почему при высокой температуре нельзя получить чистый CuO?
Задание 3. 13,6 г образца фосфора прореагировало с азотной кислотой. При этом произошло выделение одинаковых объемов сначала бурого, затем бесцветного газов. По окончании реакции к полученному водному раствору добавили избыток нитрата серебра и
получили 166,4 г осадка ярко-желтого цвета.
1) Какова массовая доля фосфора во взятом образце?
2) Запишите уравнения приведенных реакций.
Задание 4. Вещество массой 14,9 г, образованное двумя видами химических частиц с одинаковым электронным строением 1s22s22p63s23p6, полностью прореагировало с 20,0 г 98 %-ной серной кислоты.
1) Напишите уравнение реакции.
2) Определите массу образовавшейся соли.
3) Напишите уравнение реакции водного раствора образовавшейся соли с металлическим магнием.
Задание 5. Осуществите следующие превращения:
![]()
ЦЕНТРА РОССИИ
Второй отборочный этап
ХИМИЯ
Задание 1. Если к твердому нитрату натрия добавить концентрированную фосфорную кислоту, то при нагревании смеси из нее можно отогнать азотную кислоту.
1) Напишите уравнение реакции (фосфорная кислота в избытке).
2) Означает ли данный эксперимент, что фосфорная кислота сильнее азотной?
3) Можно ли получить азотную кислоту при реакции 30 %-ных растворов азотнокислого натрия и фосфорной кислоты?
4) Почему концентрированная азотная кислота на свету приобретает желтую окраску?
5) Все соли азотной кислоты – нитраты – хорошо растворимы в воде. Их растворы обладают незначительными окислительными свойствами. Цинк и алюминий в щелочном растворе восстанавливают нитраты и нитриты до аммиака. Приведите уравнения взаимодействия нитрата и нитрита калия с алюминием и цинком в щелочном растворе. Коэффициенты расставьте с помощью электронного баланса.
Задание 2. Качественный анализ минерала леонита показал присутствие в нем ионов калия, магния и сульфат-ионов. При прокаливании образца минерала массой 14,64 г его масса уменьшается на 2,88 г. Такая же навеска минерала при растворении в воде и последующем прибавлении избытка раствора хлорида бария образует 18,64 г осадка. Определите формулу леонита.
Задание 3. Смесь этена и пропена объемом 11,2 л имеет плотность по водороду 16,8. К смеси прибавили такой же объем водорода и пропустили ее над платиновым катализатором. Объем смеси на выходе из реактора составил 17,92 л. Определите состав начальной и конечной смеси газов (в % по объему) и степень превращения (в %), считая, что она одинакова для обоих алкенов. Все объемы измерены при н. у.
Задание 4. Атом углерода в органических соединениях называют первичным, вторичным, третичным или четвертичным, в зависимости от того, с каким числом соседних углеродных атомов он связан (с одним, двумя, тремя или четырьмя). В таблице представлены сведения о структуре некоторых углеводородов, не содержащих кратных связей.
Алкан | Число первичных атомов С | Число вторичных атомов С | Число третичных атомов С | Число четвертичных атомов С |
I | 4 | 1 | 0 | 1 |
II | 2 | 5 | 0 | 0 |
III | 4 | 1 | 2 | 0 |
IV | 1 | 2 | 1 | 0 |
V | 3 | 0 | 3 | 0 |
VI | 8 | 0 | 4 | 1 |
VII | 2 | 0 | 0 | 0 |
VIII | 0 | 0 | 0 | 0 |
IX | 2 | 5 | 2 | 0 |
X | 4 | 0 | 2 | 0 |
Изобразите структурные формулы углеводородов I – X.
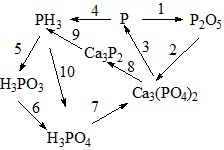
Задание 5. Осуществите цепочку превращений:
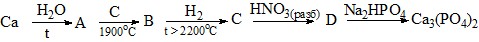
ЦЕНТРА РОССИИ
Второй отборочный этап
ХИМИЯ
Задание 1. Образец сплава цинка с алюминием массой 10,55 г растворили в избытке соляной кислоты. При этом выделилось 7,28 л газа (приведено к н. у.). Определите массовые доли металлов в сплаве. Какой объем газа выделится при растворении того же сплава в горячем растворе концентрированной щелочи?
Задание 2. Приведите по 1 примеру реакций между двумя кислотами при условии, что: а) обе кислоты – неорганические, б) одна кислота органическая, другая – неорганическая. Решите аналогичную задачу для двух оснований.
Задание 3. Ниже представлена схема синтеза вещества П – основного компонента многих жаропонижающих и болеутоляющих препаратов (Панадол, Тайленол, Эффералган и т. д.). Известно, что П содержит 63,6 % углерода, 5,94 % водорода, 21,2 % кислорода и 9,26 % азота, а на нейтрализацию водного раствора 1,51 г П расходуется 10,0 мл одномолярного раствора NaOH. Расшифруйте цепочку превращений и назовите вещество П по номенклатуре ИЮПАК.
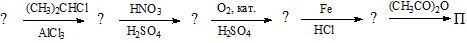
Задание 4. Осуществите следующие превращения:
Задание 5. Три изомерных вещества А, Б и В содержат 49,0% углерода, 2,7% водорода и элемент X. Продукты сгорания этих веществ в кислороде не содержат нелетучего остатка и полностью поглощаются раствором щелочи. Плотность паров этих веществ в пересчете на нормальные условия равна 6,56 г/л. Молекула соединения А имеет нулевой дипольный момент, дипольный момент молекулы Б больше, чем молекулы В. Установите структурные формулы этих трех изомеров.




