Лабораторная работа 48
Изучение спектра атома водорода.
ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ РИДБЕРГА.
Цель работы: Исследовать спектр атомарного водорода, вычислить постоянную Ридберга.
Теоретическое описание
Квантово-механический подход к изучению процессов поглощения атомов позволяет их исследовать и объяснять их строение. Состояние атома в квантовой механике описывается волновой функцией ?n, а его энергия Еn. В случае простейшего атома - атома водорода, состоящего из протона и электрона, квантовая механика позволяет получить точные решения волнового уравнения Шредингера (1):
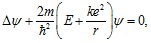 (1)
(1)
где m - масса электрона, е - его заряд, Е - полная энергия, 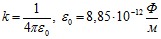 (для расчетов часто принимают k=9·109 м/Ф). Решение уравнения (1) для атома водорода дает набор дискретных уровней энергии для связанных состояний (En <0):
(для расчетов часто принимают k=9·109 м/Ф). Решение уравнения (1) для атома водорода дает набор дискретных уровней энергии для связанных состояний (En <0):
![]() (2)
(2)
где ![]() , n = 1,2,3,....- главное квантовое число. Обычно формулу (2) записывают в виде:
, n = 1,2,3,....- главное квантовое число. Обычно формулу (2) записывают в виде:
![]() (2а)
(2а)
где A=13,6 эВ.
С ростом n уровни энергии атома сближаются, в пределе (n>?) дискретный спектр приближается к непрерывному, а квантовая система к классической. Это и есть принцип соответствия Бора, который позволяет выразить постоянную Ридберга через фундаментальные постоянные.
Для простоты Бор принял, что в атоме водорода электроны вращаются вокруг ядра атома водорода (протона) по окружности радиусом r с циклической частотой ?. Согласно второму закону Ньютона, имеем:
![]() (3)
(3)
Согласно принципу квантования состояния электрона в атоме:
![]() (4)
(4)
Решение системы (3), (4) дает выражение для радиусов круговых орбит электронов в атоме водорода:
![]() (5)
(5)
Полная энергия 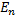
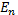 электрона в атоме есть сумма кинетической и потенциальной энергий:
электрона в атоме есть сумма кинетической и потенциальной энергий:
![]() (6)
(6)
Выражая из системы уравнений (3), (4) скорость электрона, имеем:
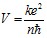 , (7)
, (7)
Подставляя (7) и (5) в (6), получаем формулу, выражающую полную энергию электрона в атоме водорода на n-ой стационарной орбите:
![]() (8)
(8)
Видно, что формула (8), полученная с помощью постулатов Бора, совпадает с формулой (2), полученной с помощью точного решения уравнения Шредингера для атома водорода.
Однако, к сожалению, теория Бора, достаточно правильно описывая закономерности в атоме водорода и водородоподобных ионах (содержащих один электрон), даёт не вполне правильные результаты уже для атома гелия, следующего за водородом и содержащем всего два электрона. Таким образом, теорию Бора можно рассматривать лишь как промежуточный этап на пути поиска верной теории - квантовой механики, точно описывающий закономерности микромира.
При переходе атома водорода из состояния n2 с энергией Е2 в состояние n1 с энергией Е1 излучается квант света с частотой 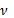
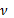 , равной:
, равной:
![]()
![]() (9)
(9)
Подставляя энергию электрона в состоянии n2 и в состоянии n1 из формулы (2) (или, что то же самое, из (8)), имеем:
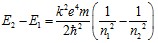 (10)
(10)
Далее можем записать:
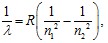 (11)
(11)
Формула (11) называется обобщенной формулой Бальмера. В данном случае: 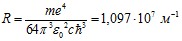 . (12)
. (12)
Следует отметить, что постоянную Ридберга иногда вводят не для волнового числа ![]() , а для частоты ?. В этом случае
, а для частоты ?. В этом случае ![]()
![]() . В формуле (11) с увеличением n2 разность между волновыми числами
. В формуле (11) с увеличением n2 разность между волновыми числами ![]() уменьшается, стремясь при n2>? к предельному значению (для n1 =2 ,
уменьшается, стремясь при n2>? к предельному значению (для n1 =2 , ![]() ). При этом линии сближаются, и уменьшается их интенсивность. Совокупность спектральных линий, закономерно меняющих свою интенсивность, называют спектральной серией. Предельное волновое число при n2>? называется границей серии.
). При этом линии сближаются, и уменьшается их интенсивность. Совокупность спектральных линий, закономерно меняющих свою интенсивность, называют спектральной серией. Предельное волновое число при n2>? называется границей серии.
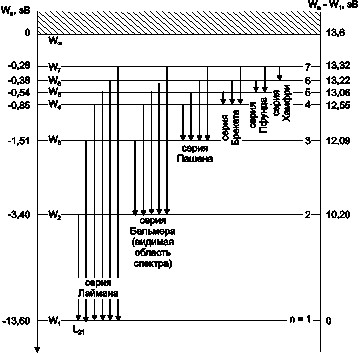
В области видимого человеческим глазом спектра излучения атома водорода можно наблюдать только серию Бальмера: n1=2, n2=3,4,5... (рис.1). Однако, существуют и другие серии, лежащие вне области видимого света. Это, например, серия Лаймана, все линии которой лежат в ультрафиолетовой области спектра. Для этой серии n1=1. Линии остальных серий (Пашена, Брэкета, Пфунда и др.) лежат в инфракрасной области спектра. Набор уровней энергии и возможные переходы в атоме принято показывать на энергетической диаграмме, приведённой на рисунке 1. Здесь принято Еn=Wn – полная энергия электрона в атоме на n - ом уровне.
Состояние атома, в котором электрон находится на низшем энергетическом уровне (для атома водорода это состояние с энергией Е1= -13,6 эВ), называется основным. Атом без внешних возмущений может находиться в этом состоянии неопределённо долго. Энергетический уровень Е1, соответственно, является бесконечно тонким. Этот вывод вытекает непосредственно
Рис. 1. Энергетический спектр атома водорода.
из соотношения неопределенностей: ![]() , где
, где ![]() - неопределенность значения энергии,
- неопределенность значения энергии, ![]() - неопределенность времени пребывания атома в этом состоянии. Так как
- неопределенность времени пребывания атома в этом состоянии. Так как ![]() , то
, то ![]() . Остальные энергетические уровни En являются возбужденными, так как возникают под действием внешних воздействий и могут существовать ограниченное время
. Остальные энергетические уровни En являются возбужденными, так как возникают под действием внешних воздействий и могут существовать ограниченное время![]() n, поэтому возбужденные уровни несколько размыты, по порядку величины:
n, поэтому возбужденные уровни несколько размыты, по порядку величины: ![]() .
.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Установка состоит из двух основных частей: источника линейчатого спектра и спектрометра. В лабораторной установке в качестве источников используются ртутная лампа (для калибровки) и объект исследования - облучатель ФПК09М, с находящимся внутри источником спектра водорода (водородная лампа). В качестве спектрометра используется универсальный монохроматор УМ-2.
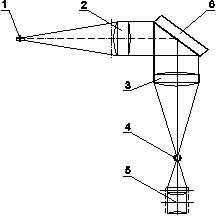
Рис. 3. Схематическое устройство спектрометра УМ-2: 1- входная щель;
2 – входной объектив; 3 - выходной объектив; 4 – выходная щель;
5- окуляр; 6 – монохроматор (дифракционная решетка)
Принцип действия спектрометра основан на разложении наблюдаемого излучения в линейчатый спектр и измерении длин волн наблюдаемых спектральных линий. Спектрометр состоит из коллиматора, диспергирующего элемента и зрительной трубы. В фокальной плоскости объектива коллиматора (2) установлена сменная входная щель (1) постоянной ширины. В качестве диспергирующего элемента в спектрометре применена дифракционная решетка (6). Сканирование спектра осуществляется поворотом решетки вокруг оси. Поворот осуществляется при помощи микрометрического винта. Показания шкалы микрометрического винта соответствуют определенному значению длины волны. Дифрагированное излучение направляется на зрительную трубу, которая состоит из объектива (3) и окуляра (5). В фокальной плоскости объектива зрительной трубы размещена выходная щель (4), предназначенная для определения длины волны.
ВЫПОЛНЕНИЕ РАБОТЫ
Приборы и принадлежности: 1. Универсальный монохроматор УМ-2.
2. Ртутная лампа и пусковое устройство для нее. 3. Облучатель ФПК09М, с находящимся внутри источником спектра водорода (водородная лампа).
Задание 1. Градуировка шкалы монохроматора.
Градуировка проводится по известному спектру паров ртути. Длины волн спектральных линий приведены в таблице 1.
Расположить выходное отверстие ртутной лампы против объектива монохроматора. Включить ртутную лампу. Наблюдая спектр и вращая барабан монохроматора, совместить визир (острие) с одной из линий спектра. Записать деление барабана в таблицу 1. По барабану монохроматора провести измерения положения всех линий спектра ртути. По окончании измерения выключить ртутную лампу. Пользуясь полученными данными, построить на миллиметровой бумаге градуировочный график. По оси абсцисс отложить число делений барабана монохроматора, по оси ординат – длины волн наблюдаемых спектральных линий ртути.Таблица 1
№ п/п | Положение и окраска линии | Относительная яркость | Длина волны, нм | Длина волны по монохроматору, дел |
1. | Красная | 4 | 708,2 | |
2. | Красная | 3 | 690,8 | |
3. | Красная яркая | 10 | 623,4 | |
4. | Оранжевая 1-я | 4 | 615,2 | |
5. | Оранжевая 2-я | 4 | 612,0 | |
6. | Желтая 1-я | 10 | 579,0 | |
7. | Желтая 2-я | 10 | 576,9 | |
8. | Зеленая яркая | 12 | 546,0 | |
9. | Зелено-голубая | 7 | 491,6 | |
10. | Синяя | 8 | 435,8 | |
11. | Фиолетовая 1-я | 6 | 407,8 | |
12. | Фиолетовая 2-я | 8 | 404,7 |
Задание 2. Определение спектра излучения атома водорода.
Поместить перед объективом монохроматора газоразрядную трубку атомарного водорода. Включить водородную лампу. Записать по показаниям шкалы барабана монохроматора положение видимых линий спектра атома водорода. Измеренные данные записать в таблицу 2. По окончании измерения выключить водородную лампу. По градуировочному графику определить длины волн измеренных линий атома водорода.Таблица 2
№ п/п | Положение и окраска линии | Длина волны по монохроматору, дел | Длина волны по градуировочному графику, нм |
|
| Постоянная Ридберга, м-1 |
1. | ||||||
2. | ||||||
и т. д. |
Задание 3. Исследование спектра атома водорода в видимой области.
По полученным значениям длин волн линий в спектре водорода вычислить энергию фотонов, соответствующую этим линиям: ![]()
![]() .
.
![]()
![]() .
.
КОНТРОЛЬНЫЕ ВОПРОСЫ
Каков механизм излучения света атомами? Что понимают под спектром излучения вещества? Какие постулаты выдвинул Бор в теории атома водорода? Объясните вывод из теории Бора обобщенной формулы Бальмера. Записать сериальные формулы для всех спектральных линий спектра водорода. Получить выражение кинетической, потенциальной и полной энергии электрона в атоме водорода. Почему полная энергия электрона в атоме водорода отрицательна? По схеме энергетических уровней атома водорода определить