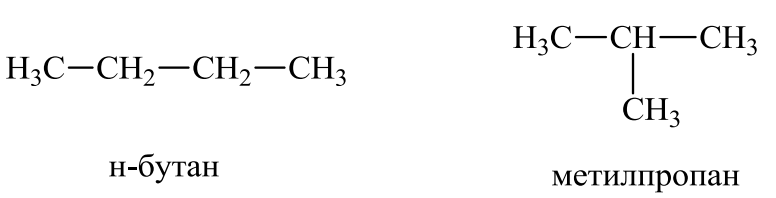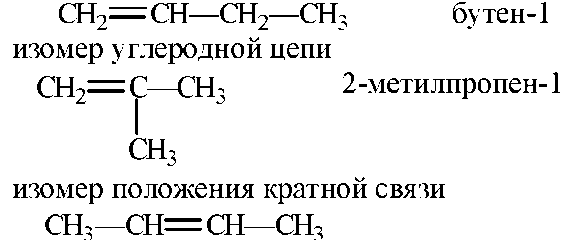Задача 1
Два элемента (А и Б), находящиеся в одном и том же периоде и в одной и той же группе периодической системы (в её коротком варианте), образуют друг с другом стабильное бинарное соединение В с массовой долей одного из элементов 25,6%. Количество протонов в ионах, составляющих это вещество, различается на 10 (у Б больше, чем у А), а количество электронов – на 13. Это соединение хорошо растворимо в воде, а при пропускании в его раствор газообразного аммиака (реакция 1) выпадает белый осадок, постепенно темнеющий (буреющий) на воздухе (реакция 2). Если продукт реакции 2 прокалить на воздухе (реакция 3), будет получен черный порошок Г, содержащий 36,78 мас.% кислорода. Если добавить этот порошок к бесцветному прозрачному раствору вещества Д, который можно купить в аптеке, то наблюдается бурная реакция с выделением газа (реакция 4), в котором вспыхивает тлеющая лучинка.
1) Определите элементы А и Б, а также формулу вещества В.
2) Напишите электронные конфигурации нейтральных атомов элементов А и Б, а также ионов, входящих в состав соединения (в виде 1s22s2…).
3) Определите вещества Г и Д. Напишите уравнения реакций 1-4.
4) Для реакции 1 напишите полное и сокращенное ионное уравнение.
5) Для реакции 4 напишите схему электронного баланса, укажите окислитель и восстановитель
Задача 2
На анализ в лабораторию принесли банку без этикетки, на которой стоял значок «взрывоопасно!». В банке находилось вещество А, представляющее из себя белый порошок, довольно плохо растворимый в холодной воде, содержащий 31,84 мас.% металла и действительно взрывающийся от удара или поджигания (при горении пламя окрашено в фиолетовый цвет). При нагревании 4,9 г вещества А (реакция 1) был получен молекулярный кислород, кроме того, осталось 2,98 г белого кристаллического вещества Б. При приливании к твердому веществу Б концентрированной серной кислоты (реакция 2) выделялся газ В (эта реакция – лабораторный способ получения газа В) с резким запахом, вызывающий покраснение смоченной водой лакмусовой бумажки. Раствор вещества Б давал белый творожистый осадок при реакции с нитратом серебра (реакция 3). Электролиз водного раствора Б (реакция 4) привел к выделению на аноде ядовитого желто-зеленого газа Г. Газ Г оказался в 2,45 раз тяжелее воздуха, при его пропускании через горячий раствор гидроксида калия (реакция 5) была получена смесь веществ А и Б.
1) Установите формулы всех неизвестных веществ, ответ подтвердите расчетами.
2) Напишите уравнения реакций 1-5.
3) Рассчитайте массовые доли веществ в растворе, полученном при пропускании 6,72 л газа Г через 178,7 г горячего водного раствора гидроксида калия с концентрацией 31,337%.
Задача 3.
В лаборатории устанавливали состав газообразного органического соединения Х, которое является одним из компонентов газообразного автомобильного топлива. Для анализа был взят образец объемом 448 мл (н. у.) и массой 1,16 г. Продукты сгорания этого образца (реакция 1) полностью поглотились при последовательном пропускании их через трубки с оксидом фосфора (V) и концентрированным раствором гидроксида калия (реакции 2 и 3). Масса трубок увеличилась соответственно на 1,8 г и 3,52 г.
1) Установите брутто-формулу Х. Выводы подтвердите соответствующими расчетами.
2) Напишите структурные формулы изомеров вещества Х.
3) Напишите уравнения химических реакций 1-3, упомянутых в задаче.
4) Вещество Х при нагревании в присутствии платины теряет 3,45% своего веса (реакция 4) и превращается в вещество Y. Установите брутто-формулу вещества Y и напишите уравнение реакции 4.
5) Приведите все изомеры вещества Y (включая геометрические), способные обесцветить раствор перманганата калия. Назовите все изомеры по номенклатуре ИЮПАК.
Задача 4.
Смесь паров этилена, пропина и этанола общей массой 5,0 г была пропущена через избыток горячего аммиачного раствора оксида серебра (гидроксид диамминсеребра), при этом выпало 5,88 г осадка (реакция 1). Если весь этанол в смеси предварительно дегидрировать до альдегида А пропусканием над оксидом меди (II) при нагревании (реакция 2), то такая смесь (этилен, пропин и альдегид А) при пропускании через избыток горячего аммиачного раствора оксида серебра дает 16,68 г осадка (реакция 1 и 3).
1) Напишите полные уравнения реакций 1-3, при написании уравнений используйте структурные формулы органических веществ.
Рассчитайте количества веществ (моль) и процентное содержание (мас. %) всех компонентов в исходной смеси. Рассчитайте, сколько максимально граммов бромной воды (0,5% раствор брома в воде) может обесцветить исходная смесь.4) Расшифруйте цепочку превращения, напишите полные уравнения всех реакций, используя структурные формулы органических веществ:
1) KMnO4, H2SO4 | Электролиз | Br2, hv | KOH, спирт, t° | |
А | Б | В | Г | Этилен |
2) KOH |
Задача 5.
Одним из самых распространенных сахаров и питательных веществ для человека является глюкоза. Она образуется вместе с кислородом в растениях в результате фотосинтеза. Известно, что для синтеза 1 моля глюкозы в результате этой реакции необходимо 2800 кДж энергии, такое же количество энергии выделяется при метаболизме 1 моль глюкозы в организме человека (аэробный гликолиз).
1) Напишите термохимическое уравнение реакции фотосинтеза с образованием глюкозы из СO2 и Н2O. Рассчитайте массу глюкозы в граммах, которую нужно съесть, чтобы восполнить суточную потребность человеческого организма в энергии (приблизительно 11200 кДж), считая глюкозу единственным источником энергии.
2) Представим, что вы выпили сладкий чай с конфетами, с общим содержанием 36 г глюкозы, и вся эта глюкоза моментально расщепилась в организме по аэробному пути с выделением соответствующего количества энергии. Выделенная энергия целиком пошла на разогрев тела, потерь энергии в окружающую среду не было. На сколько градусов повысилась бы температура тела? Теплоемкость тела принять равной 2,8 кДж/(кг•град), вес кг.
3) При нехватке кислорода в организме глюкоза превращается в молочную кислоту. Этот процесс в биохимии называют анаэробный гликолиз. Аналогичная реакция происходит при сквашивании молока и называется молочнокислое брожение. При этом процессе происходит образование 2 моль молочной кислоты из 1 моль глюкозы, а побочных продуктов нет. Также известно, что при превращении 72 г глюкозы в молочную кислоту выделяется 46,4 кДж теплоты
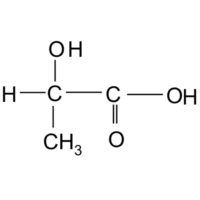
Установите брутто - и структурную формулу молочной кислоты (является альфа-гидроксикарбоновой кислотой) и напишите термохимическое уравнение молочнокислого брожения. Во сколько раз этот процесс дает меньше энергии по сравнению с окислением глюкозы до CO2 ?
РЕШЕНИЯ (КЛЮЧИ) И КРИТЕРИИ ОЦЕНИВАНИЯ
Задача 1 РЕШЕНИЕ
№ | Элемент ответа (допускаются иные формулировки и способы решения, удовлетворяющие условию задачи) | Баллы |
1. | Поскольку элементы находятся в одном и том же периоде и в одной и той же группе периодической системы, наиболее вероятно, что один из них находится в главной подгруппе, а другой – в побочной, т. е. является d-металлом. Степени окисления можно подобрать по разнице в 13 для количества электронов. Неметалл скорее всего – галоген (хорошая растворимость В), в степени окисления -1. Разница в электронах на 13 говорит о том металл имеет степень окисления +2. Судя по свойствам, это марганец (А=Mn), и вещество представляет собой бромид марганца (Б=Br). К такому же ответу можно было бы прийти, подбирая пары элементов по разности количества протонов (35-25=10). Итого имеем формулу вещества В = MnBr2, которую можно было также вывести по массовой доле. А в нашем рассуждении можно провести проверку: Действительно, массовая доля марганца в MnBr2 равна 55 / 215 ? 0,256 = 25,6%. | По 1 баллу за каждый элемент + 1 балл за формулу, Всего 3 балла |
2. | Электронные конфигурации: Mn0: 1s22s22p63s23p64s23d5 (всего 25 электронов) Mn+2: 1s22s22p63s23p64s23d3 (всего 23 электрона) Br0: 1s22s22p63s23p64s23d104p5 (всего 35 электронов) Br-1: 1s22s22p63s23p64s23d104p6 (всего 36 электронов) | По 0,5 балла за каждую конфигурацию, всего 2 балла |
3 | Уравнения реакций: Реакция 1: MnBr2 + 2NH3 + 2H2O = Mn(OH)2v+ 2NH4Br; Реакция 2: При окислении гидроксида марганца (II) на воздухе по данным разных авторов образуются гидроксиды марганца (III) или (IV) переменного состава. В качестве правильного ответа принимается схема реакции без коэффициентов и любая формула типа MnOOH, MnO(OH)2, Mn2O3*nH2O, MnO2*nH2O, Mn2O3, MnO2 Вариант схемы Mn(OH)2 + O2 = MnO2*nH2Ov + H2O Реакция 3: При прокаливании гидроксидов образуются оксиды, при этом в данном случае это могут быть Mn2O3, MnO2 и Mn3O4 Формулу оксида выводим (или подбираем) по массовой доле кислорода. Под данные задачи подходит оксид MnO2 (вещество Г = MnO2 ) Тогда уравнение будет иметь вид: MnO2*nH2O = MnO2 + nH2O (допускается схема получения из другого гидроксида) Реакция 4: По описанию Д – пероксид водорода (H2O2), который каталитически разлагается при контакте с оксидом марганца 2H2O2 = 2H2O + O2 (кат MnO2) | По 0,5 балла за формулы Г и Д и за каждое уравнение реакции, Всего 3 балла |
4 | Полное ионное уравнение: Mn2+ + 2Br - + 2NH3 + 2H2O = Mn(OH)2v+ 2NH4+ + 2Br -; Сокращенное ионное уравнение: Mn2+ + 2NH3 + 2H2O = Mn(OH)2v+ 2NH4+ | 1 балл |
5 | Схема электронного баланса O-1 +1e > O-2 – реакция восстановления 2O-1 -2e > O20 – реакция окисления Кислород в степени окисления -1 (O-1 или пероксид водорода) является и окислителем и восстановителем, то есть это реакция диспропорционирования | 1 балл |
Итого | 10 баллов |
Задача 2 РЕШЕНИЕ
№ | Элемент ответа (допускаются иные формулировки и способы решения, удовлетворяющие условию задачи) | Баллы |
1. | Можно сразу найти молярную массу газа Г M(Г) = М(возд) ? 2,45 = 29 ? 2,45 = 71, что может соответствовать только хлору (желто-зеленый газ), то есть газ Г – это хлор Сl2 Реакция хлора с раствором KOH приводит к получению веществ А и Б, то скорее всего, оба они содержат хлор. Одно из них является хлоридом, это вещество Б, это подтверждается качественной реакцией вещества Б с нитратом серебра то есть Б - хлорид калия KCl, В - хлороводород НСl Установим формулу А Скорее всего, вещество А содержит калий, хлор и кислород. Калий определяется по фиолетовому цвету пламени, а также по тому факту, что вещество А получается в реакции с гидроксидом калия. Наиболее вероятно присутствие в формуле одного атома калия, и молекулярная масса вещества М = 39/0,3184 = 122,5. За вычетом хлора и калия остается 122,5-39-35,5=48, что может соответствовать трем атомам кислорода (KClO3). Можно рассуждать по-другому: Из схемы термического разложения А: А > Б + О2 Также количества веществ А и Б должны относиться между собой как целые числа, скорее всего, n(A) = n(Б) По условию, n(Б) = m/M = 2,98/74,5 = 0,04 моль M (A) = m/n = 4,9/0,04 = 122,5, что соответствует формуле KClO3 А - KClO3 – хлорат калия Тривиальное название - бертолетова соль, используется в пиротехнике и при изготовлении спичек Участник мог предложить другие схемы расчета и определения веществ, засчитываются любые методы и предположения, подкрепленные проверкой (без проверки баллы уменьшаются в 2 раза). Итак, А - KClO3 Б – KCl В – НСl Г – Сl2 | За каждую формулу по 1 баллу Всего 1?4= 4 балла |
2. | Реакция 1: 2KClO3 = 2KCl + 3O2 (термическое разложение) Реакция 2: 2KCl + H2SO4(конц.) = K2SO4 + 2HCl (или KHSO4) Реакция 3: KCl + AgNO3 = AgClv + KNO3 Реакция 4: 2KCl + 2H2O = H2 + 2KOH + Cl2 (электролиз) Реакция 5: 3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O (при нагревании) | 1 б 0,5 б 0,5 б 1 б 1 б |
3 | В исходном растворе: m(KOH) = m(р-ра) ? ?(KOH) = 178,7 ? 0,31337 = 56 г n(KOH) = m/M = 56/56 = 1 моль n(Cl2) = V/Vm = 6,72/22,4 = 0,3 моль, n(Cl2) = m ? M = 0,3 ? 71 = 21,3 г Хлор полностью поглотится раствором, поэтому масса конечного раствора m(р-ра)конечн = 178,7 + 21,3 = 200 г Из уравнения 3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O Следует, что KOH взят в избытке, после окончания реакции его останется 1-0,6 = 0,4 моль, m(KOH)остат = 0,4?56 = 22,4 г n(KClO3) = 0,1 моль, m(KClO3) = 0,1?122,5 = 12,25 г n(KCl) = 0,5 моль, m(KCl) = 0,5?74,5 = 37,25 г ? (KOH) = 22,4/200 = 0,112 = 11,2 % ? (KClO3) = 12,25/200 = 0,06125 = 6,125 % ? (KCl) = 37,25/200 = 0,18625 = 18,625 % | 2 балла |
Итого | 10 баллов |
Задача 3 РЕШЕНИЕ
№ | Элемент ответа (допускаются иные формулировки и способы решения, удовлетворяющие условию задачи) | Баллы |
1. | На основании анализа результатов исследования можно предположить: Уравнение реакции горения искомого соединения в общем виде:
n(CxHy(Oz)) = 0,448 / 22,4 = 0,02 моль М(CxHy(Oz)) = 1,16 : 0,02 = 58 г/моль n(CO2) = 3,52 /44 = 0,08 моль n(H2O) = 1,8 / 18 = 0,10 моль
n(C) = n(CO2) = 0,08 моль; m(C) = 0,08 ? 12 = 0,96 г n(Н) = n(H2O) ? 2 = 0,2 моль; m(Н) = 0,2 ? 1 = 0,20 г m(C) + m(Н) = 0,96 г + 0,20 г = 1,16 г m(CxHy(Oz)) по условию задачи равна 1,16 г, следовательно, кислорода в исходном соединении нет. Его формулу можно представить так – CxHy
x : y = n(C) : n(Н) = 0,08 : 0,20 = 1 : 2,5 М(CH2,5) = 14,5 г/моль
Истинная формула искомого соединения C4H10 | 3 балла за вывод формулы |
2 | Бутан имеет два изомера.
| По 0,5 балла за каждый изомер, всего 1 балл |
3. |
В последнем случае принимается любое уравнение реакции | По 1 баллу за каждое уравнение, всего 3 балла |
4 | По условию молекулярная масса бутана должна уменьшится на 3,45%, тогда М(Y) = 58-58*0,0345 = 56 Это означает, что произошло дегидрирование с отщеплением 2 атомов водорода, с образованием бутена C4H8 (Y) Уравнение 4: C4H10 = C4H8 + H2 (кат Pt) | 1 балл |
5 | Таких изомеров 4
| 2 балла |
Итого | 10 баллов |
Задача 4 РЕШЕНИЕ
№ | Элемент ответа (допускаются иные формулировки и способы решения, удовлетворяющие условию задачи) | Баллы |
1. | Из исходной смеси с аммиачным раствором оксида серебра реагирует только пропин: Реакция 1: СН3-С?СН + [Ag(NH3)2]OH = СН3-С?СAgv +2NH3 + H2O При дегидрировании этанола над оксидом меди образуется ацетальдегид (А): Реакция 2: С2Н5ОН + СuO = CH3CHO + Cu + H2O Ацетальдегид также вступает в реакцию с аммиачным раствором оксида серебра, окисляясь до уксусной кислоты: Реакция 3: CH3CHO + 2[Ag(NH3)2]OH = CH3COONH4 + 2Agv + 3NH3 + H2O (допускается написание CH3COОH). *Если участник вместо [Ag(NH3)2]OH пишет Ag2O, баллы снижаются вдвое | 3 балла (1 балл за каждое уравнение) |
2 | По условию m(СН3-С?СAg) = 5,88 г, М(СН3-С?СAg) =147 г/моль, то n(СН3-С?СAg) = m/М = 0,04 моль Из уравнения 1 n(СН3-С?СН) = n(СН3-С?СAg) = 0,04 моль М(СН3-С?СН) = 40 г/моль, m(СН3-С?СН) = M*n = 1,6г Масса серебра в реакции 3 равна m(Ag) = 16,68-5,88=10,8г n(Ag) = m/М = 10,8/108 = 0,1 моль Из уравнения 3 n(CH3CHO) = n(Ag)/2 = 0,05 моль Из уравнения 2 n(C2Н5OН) = n(CH3CHO) = 0,05 моль Масса этанола в исходной смеси m(C2Н5OН) = M*n = 0,05*46 = 2,3г Масса этилена в смеси m(C2H4) = 5-1,6-2,3 = 1,1 г n(C2H4) = m/М = 1,1 / 28 = 0,0393 моль Массовые доли компонентов смеси: ?(C2H4) = 1,1/5 = 22% ?(СН3-С?СН) = 1,6/5 = 32% ?(C2Н5OН) = 2,3/5 = 46% | По 0,5 балла за каждое количество вещества (моль) По 0,5 балла за каждый % Всего 3 балла |
3. | С бромной водой реагируют этилен и пропин: C2H4 + Br2 = C2H4Br2 C3H4 + 2Br2 = C3H4Br4 Общее количество брома n(Br2) = n(C2H4) + 2n(C3H4) = 0,0393+2*0,04 = 0,1193 моль (примерно 0,12 моль) Масса брома m(Br2) = M*n = 0,1193*160=19,088 г (примерно 19,2 г) Масса бромной воды m(Br2 + вода) = m(Br2)/?(Br2) = 19,088/0,005=3817,6г (примерно 3840 г) | 2 балла |
4 | Уравнения проведенных реакций: 1) 5CH3CHO + 2KMnO4 + 3H2SO4 = 5CH3COOH + 2MnSO4 + K2SO4 + 3H2O CH3COOH + KOH = CH3COOK + H2O Б = ацетат калия CH3COOK 2) 2CH3COOK + 2H2O = C2H6 + 2CO2 + H2 + 2KOH В = этан C2H6 3) C2H6 + Br2 = C2H5Br + HBr (hv или t°) Г = C2H5Br бромэтан (этилбромид) 4) C2H5Br + KOH (спирт р-р) = C2H4 + KBr + H2O | За каждую верную стадию по 0,5 б, всего 2 балла |
Итого | 10 баллов |
Задача 5 РЕШЕНИЕ
№ | Элемент ответа (допускаются иные формулировки и способы решения, удовлетворяющие условию задачи) | Баллы |
1. | Реакция фотосинтеза: 6СО2 + 6H2O = C6H12O6 + 6O2 – 2800 кДж (эндотермическая реакция) В организме идет обратная реакция с выделением 2800 кДж C6H12O6 + 6O2 = 6СО2 + 6H2O + 2800 кДж Энергия 2800 кДж соответствует 1 молю (180 г) глюкозы, то 11200 кДж соответствуют х г глюкозы х = m(C6H12O6) = 11200?180/2800 = 720 г | 2 балла 3 балла |
2 | n(C6H12O6) = 36/180 = 0,2 моль При расщеплении такого количества глюкозы выделится энергии Q = 2800 ? 0,2 = 560 кДж Q = c ? m ? ?T, откуда ?T = Q / (c ? m) = 560 / (2,8 ? 50) = 4 градуса То есть если вся энергия пойдет на разогрев тела, его температура станет 36,6+4 =40,6°С | 3 балла |
3 | Уравнение анаэробного гликолиза: С6H12O6 = 2 C3H6O3 Молочная кислота = C3H6O3 Структурная формула молочной кислоты
Тепловой эффект в расчете на 1 моль глюкозы равен Q = 46,4*180/72 = 116 кДж/моль, что в 2800/116 = 24 раза меньше, чем при аэробном гликолизе Термохимическое уравнение С6H12O6 = 2 C3H6O3 + 116 кДж | 2 балла |
Итого | 10 баллов |
Итого за работу ? 50 баллов