Методы генной инженерии.
Секвенирование. Секвенирование позволяет довольно быстро определить полную нуклеотидную последовательность сегмента длиной 100 - 500 нуклеотидных пар, образующегося при расщеплении ДНК рестрикционными эндонуклеазами.
Ферментативный метод был изобретен британским ученым Фридериком Сенгером в 1975. В качестве матрицы при ДНК-секвенировании используется одноцепочечная ДНК. Для выяснения последовательности нуклеотидов в целевой части ДНК, проводят 4 полимеразные реакции. Необходимо:
Одноцепочечная молекула ДНК, которая изучается и используется в качестве матрицы Праймер – затравка, комплементарный небольшому участку анализируемой ДНК. Могут использоваться синтетические праймеры или природные субфрагменты, полученные при помощи рестриктаз. 3'-конец праймера должен заканчиваться перед участком ДНК, который будет секвенироваться. предшественники ДНК - дезоксирибонуклеозидтрифосфаты (dАTP dTTP, dGTP, dCTP) ДНК-полимераза I Терминаторы - дидезоксирибонуклеозидтрифосфаты (ddATP, ddTTP, ddGTP, ddCTP)dNTP и ddNTP метятся радиоактивным Р32 или S35
В каждую из четырех смесей реакции обязательно нужно добавить дезоксинуклеозидтрифосфаты (дЦТФ, дГТФ, дТТФ, дАТФ) и ДНК-полимеразу. Кроме этого, в каждую из пробирок добавляют один из дидезоксинуклеозидтрифосфатов (ддЦТФ, ддГТФ, ддТТФ и ддАТФ). ддНТФ в 3'-положении, вместо гидроксильной группы (ОН) содержит водород (Н). ddНТФ принимает участие в реакции полимеризации ДНК и сразу прекращает её. В каждой реакционной смеси соотношение между дЦТФ, дГТФ, дТТФ, дАТФ и одним из ддНТФ составляет 100:1. Из-за низкой концентрации ддНТФ реакция не заканчивается в начале секвенирования ДНК. В то же время реакционная смесь будет содержать большое количество фрагментов ДНК различной длины (из-за присоединения ддНТФ в различных точках растущей нити ДНК).
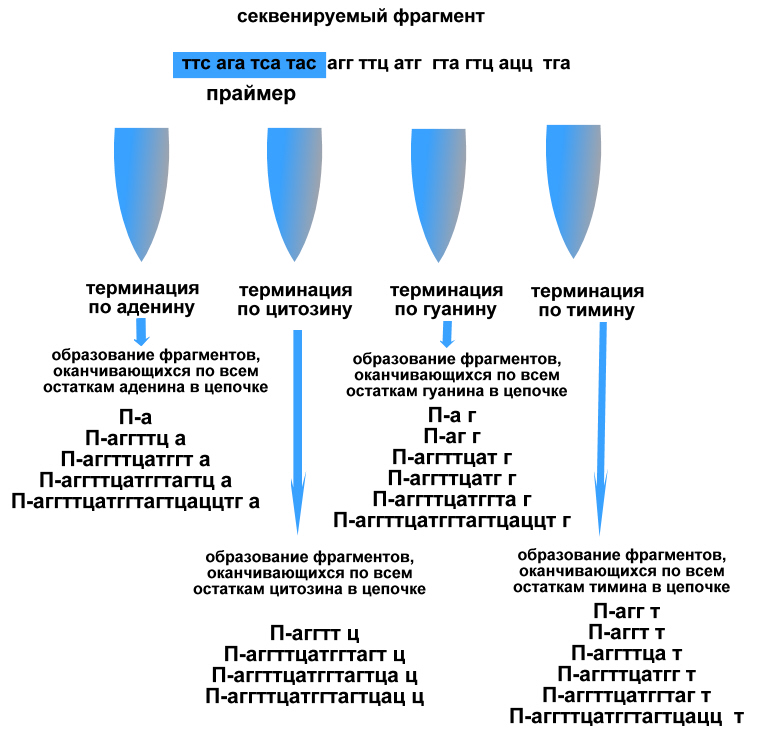
С помощью электрофореза продукты полимеризации ДНК разделяют и секвенируемую последовательность считывают с радиоавтографа и получают последовательность целевой ДНК. Длина выявленного радиоактивного фрагмента указывает на место расположения комплементарного нуклеотида в анализируемом фрагменте ДНК. Например, если в пробе в присутствии ддСТР, выявлены фрагменты длиной 3 и 4 нуклеотида, это значит, что в анализируемом фрагменте ДНК в 3 и 4 позиции находится гуанин.
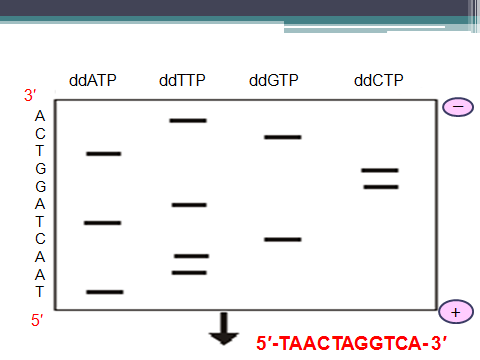
Химический метод (1976, У. Гилберт и А. Максам). Метод основан на специфической модификации нуклеотидов с последующим выщеплением их из полимерной цепи и анализом образовавшихся продуктов методом гель-электрофореза.
- Анализируемый фрагмент ДНК метят радиоактивным элементом с помощью фермента полинуклеотидкиназы. Препарат меченой ДНК делят на четыре порции и в каждой из них проводят: Модификацию нуклеотидов, и их выщепление специальными реагентами. Пуриновые основания модифицируются диметилсульфатом. Если такую модификацию обработать 0,1 М HCl при 0о С, то выщепляется метиладенин. Обработка поврежденных молекул пиперидином приводит к гидролизу ДНК по остаткам метилгуанина. Пиримидиновые основания модифицируются гидразином. В бессолевой среде модифицируется и цитозин, и тимин, в присутствии 2 М NaCl модифицируется только цитозин. Инкубация в щелочной среде (0,1 М NaOH) при температуре +90о С приводит к разрушению сахаро-фосфатной связи в местах выщепления оснований. В результате получается набор меченых фрагментов, длины которых определяются расстоянием от разрушенного основания до конца молекулы. Фрагменты подвергают электрофорезу, затем проводят радиоавтографию, и те фрагменты, которые содержат радиоактивную метку, оставляют «отпечатки» на рентгеновской пленке. По положению отпечатков можно определить, на каком расстоянии от меченого конца находилось разрушенное основание, а зная это основание - его положение. Так набор полос на рентгеновской пленке определяет нуклеотидную последовательность ДНК.
Клонирование – получение копий фрагмента ДНК. 2 способа:
1). С Помощью векторной ДНК.
2). ПЦР in vitro
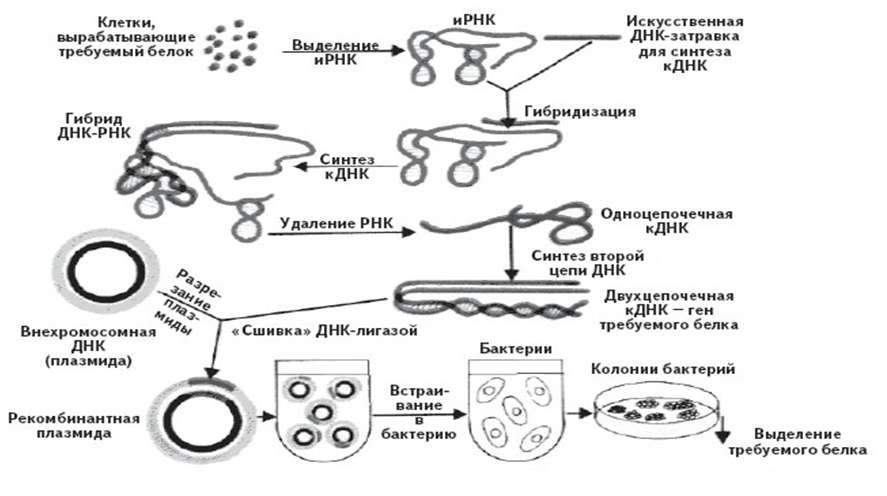
1) Если не удается выделить нужный ген путем рестрикции, процесс клонирования начинают с целенаправленного получения нужного гена. Для этого из клеток выделяют и-РНК, являющуюся транскрипционной копией этого гена, и с помощью фермента – обратной транскриптазы синтезируют комплементарную ей цепь ДНК. Затем и-РНК, служившая матрицей при синтезе ДНК, уничтожается специальным ферментом РНКазой H или путем щелочного гидролиза. Образовавшиеся молекулы оцДНК имеют тенденцию самопроизвольно формировать вторичную структуру, что приводит к образованию структуры типа «стебель-петля» на 3?-конце оцДНК. Этот конец в свою очередь используется в качестве затравки при синтезе второй цепи кДНК ДНК-полимеразой I. Получившаяся двойная спираль ДНК носит название к-ДНК (комплементарная ДНК). Она соответствует гену, с которого была считана и-РНК, запущенная в систему с обратной транскриптазой. Для клонирования к концам кДНК присоединяют с помощью ДНК-лигазы олигонуклеотидные адаптеры, содержащие сайты рестрикции, необходимые для соединения с вектором. К-ДНК встраивается в плазмиду, которой трансформируют бактерии и получают клоны, содержащие только выбранные гены человека. В качестве векторов используются плазмиды, бактериофаги (б\ф ?, они имеют большую емкость и позволяют вставлять более крупные куски генома.). В настоящее время удается получить искусственные векторы, обладающие более высокой емкостью, способные вместить от 100-до 200 тыс. п.н. Наиболее популярными в настоящее время являются векторные системы, основанные на искусственных хромосомах бактерий – BAC (bacterial artificial chromosome); Мини-хромосомы дрожжей YAC и сверхъемкие векторы PAC - умеренного бактериофага Р1:
Векторная ДНК должна обладать следующими свойствами:
- Автономно реплицироваться в бактерии-хозяине Иметь маркеры, (например, устойчивости к антибиотикам), которые позволяют легко обнаружить и идентифицировать трансформированные клетки Введение чужеродной ДНК не должно нарушать важных функций вектора.
2) Полимеразная цепная реакция является методом быстрого "клонирования" определенной части ДНК в пробирке в течение 30-40 циклов. ПЦР была изобретена американским биохимиком Кэри Мюллисом в 1983 году. Чувствительность метода такова, что амплифицировать в ПЦР и выявить целевую последовательность можно даже в том случае, если она встречается однажды в образце из 105 клеток. Точность метода: с ПЦР позволяет надежно выявлять однокопийные гены.
В основе ПЦР лежит естественный процесс клеточной репликации.
Каждый цикл состоит из трех этапов: денатурация, отжиг праймеров, синтез ДНК. Для каждого шага существует специальный температурный и временной интервал:
1) денатурация (94 °С, 0.5-1 мин);
2) отжиг праймеров (35-65 °С, 0.5-1 мин);
3) синтез (72 oС, 0.5-1 мин).
Аккуратное выделение ДНК, амплификация ДНК, и детекция продуктов амплификации (электрофорез) обеспечивают высокое качество полимеразной цепной реакции. Количество ампликонов фрагмента ДНК из одной клетки, образованных во время ПЦР, может быть найдено по следующей формуле: F = 2n, n-число циклов.
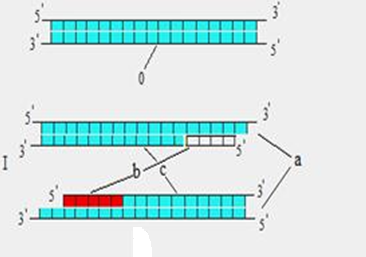
К анализируемому образцу ДНК добавляют в избытке 2 синтетических олигонуклеотида - праймера размером около 20 нуклеотидов. Каждый из них комплементарен одному из 3?-концов фрагмента ДНК. ДНК нагревают для разделения цепей двойной спирали, а при охлаждении происходит гибридизация праймеров с комплементарными участками фрагментов ДНК (отжиг). В результате в растворе будут находиться однонитевые ДНК с короткими двухцепочечными участками - затравками (праймерами). В систему вносят ДНК-полимеразу термофильной бактерии Thermus aquaticus (Taq-полимераза) для удлинения праймеров. Первоначально для ПЦР использовали фрагмент Кленова ДНК-полимеразы I E. coli. Однако недостатком данного подхода являлось то, что после каждого цикла реакции необходимо было вносить в реакционную смесь новую порцию фермента. Данная полимераза не инактивируется после длительной инкубации при 95 °С. Таким образом, в процессе рассматриваемой реакции эффективно амплифицируется только та последовательность ДНК, которая ограничена праймерами. Полученные фрагменты разделяют гель-электрофорезом, интересующий фрагмент выявляют с помощью специфичного генного зонда.1.2.
3. 
4.
Возможности генной инженерии:
- Изучение структуры и функции любого гена и продуктов его экспрессии. Изучение геномов различных организмов. Синтез генов. Получение генетически трансформированных видов микроорганизмов, растений, животных, способных стать продуцентами БАВ Получение различных препаратов


