ЦЕНТРА РОССИИ
Первый (отборочный) тур
ХИМИЯ
Задание1. ![]()
1) Напишите уравнения реакций, характеризующие данные превращения;
2) Элементы VI группы главной подгруппы Периодической системы называют «халькогены», что означает «рождающие руды». Приведите примеры (не менее 2-х) сульфидов (минералов), являющихся сырьем для черной и цветной металлургии, назовите эти минералы;
3) Попадание диоксида серы в атмосферу – одна из причин образования смога и кислотных дождей. Приведите уравнения химических реакций, описывающие образование кислотных осадков в атмосфере из SO2.
4) В диоксиде серы и сульфитах сера проявляет степень окисления +4, что говорит о ее способности к окислению и восстановлению. Приведите 2 примера реакций, в которых диоксид серы является окислителем, восстановителем. Укажите, в каком случае сера – окислитель, а в каком – восстановитель.
Задание 2. В 18,764 мл 5%-ного раствора (плотность 1,10 г/мл) сильной одноосновной кислоты НЭО3 содержится 9,632 • 1021 ионов.
1) Составьте формулу кислоты, назовите ее.
2) Приведите уравнения реакций, описывающие получение кислоты.
3) Изобразите структурную формулу кислоты. Является ли ее молекула плоской? Да или нет, почему?
4) Предположите окислительно-восстановительные свойства кислоты, подтвердите их уравнениями реакций (не менее 2-х).
Задание 3. Сопоставьте формулы веществ и их тривиальные названия
1. NH3, водный раствор А. Известковое молоко
2. Fe3O4 Б. Синильная кислота
3. Na2SO4 • 10H2O В. Нашатырь
4. Смесь СО и Н2 Г. Сода кристаллическая
5. K3[Fe(CN)6] Д. Купоросное масло
6. K4[Fe(CN)6] Е. Квасцы алюмокалиевые
7. KAl(SO4)2 • 12H2O Ж. Олеум
8. H2SO4 конц., техническая З. Желтая кровяная соль
9. Суспензия Са(ОН)2 в известковой воде И. Глауберова соль
10. NH4Cl К. Пирит, железный колчедан
11. Раствор SO3 в H2SO4 Л. Железная окалина
12. FeS2 М. Нашатырный спирт, аммиачная вода
13. CaOCl2 Н. Водяной газ
14. Na2CO3 О. Термит
15. Na2CO3 • 10H2O П. Известь хлорная (белильная)
16. NaHCO3 Р. Поташ
17. K2CO3 С. Известковая вода
18. Cмесь порошкообразных Al и Fe3O4 Т. Сода питьевая
19. Насыщенный водный раствор Са(ОН)2 У. Сода кальцинированная
20. Водный раствор HCN Ф. Красная кровяная соль
Задание 4. 31 г вещества Х при взаимодействии с магнием образует 67 г соединения Mg3X2, при обработке которого избытком соляной кислоты выделилось газообразное вещество. Сжиганием в избытке воздуха всего газообразного вещества получили твердое вещество – кислоту, которую полностью растворили в 100 г воды.
1) Определите исходное простое вещество.
2) Найдите концентрацию полученного раствора.
3) Объясните, почему высшая валентность, которую проявляет азот в своих соединениях, равна IV, а у фосфора высшая валентность равна V?
4) В чем сходство и в чем отличие свойств аммиака и фосфина? При ответе на вопрос рассмотрите: а) получение; б) отношение к воде; в) отношение к сильным кислотам.
Задание 5. При действии избытка хлороводородной кислоты на 20 г смеси меди, железа и цинка выделилось 4,48 л (н. у.) газа, а при обработке того же количества смеси избытком раствора едкого кали выделилось 2,24 л (н. у.) газа. Найдите массовые доли металлов в смеси.
ЦЕНТРА РОССИИ
Первый (отборочный) тур
ХИМИЯ
Задание 1.
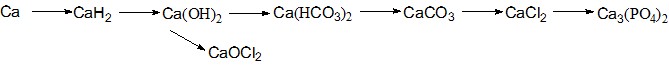
1) Напишите уравнения реакций, характеризующие данные превращения;
2) Известно, что кальций легко реагирует с кислотами, в том числе и с азотной. В зависимости от концентрации кислоты образуются различные продукты ее восстановления. При взаимодействии с разбавленной азотной кислотой среди продуктов значительную долю занимает аммиак, который растворяясь в кислоте, образует нитрат аммония. Напишите уравнение взаимодействия разбавленной азотной кислоты с кальцием, составьте электронный баланс, укажите окислитель и восстановитель, расставьте коэффициенты.
3) Все металлы II группы главной подгруппы образуют карбиды различного состава и строения. Например, известны Ве2С – производное метана, Mg2C3 – производное пропина, СаС2 – производное ацетилена и др. Все карбиды необратимо разлагаются водой. Напишите уравнения взаимодействия выше указанных карбидов бериллия, магния и кальция с водой. Расставьте коэффициенты.
Задание 2. Неорганическая соль железа (II) образует несколько кристаллогидратов, в том числе с массовой долей воды 45,32% и 10,59%.
1) Определите формулы кристаллогидратов.
2) Что такое купоросы? Какой из полученных кристаллогидратов является купоросом?
3) Что такое квасцы? Приведите пример квасцов, в состав которых входит железо.
Задание 3. 10 л смеси (н. у.) водорода и неизвестного газа имеют массу 7,82 г. Известно, что на получение всего водорода, входящего в состав смеси, было израсходовано 11,68 г металлического цинка в его реакции с серной кислотой.
1) Найдите молекулярную массу неизвестного газа.
2) Приведите 3 примера газообразных веществ, удовлетворяющих условию задачи.
3) Напишите реакции их взаимодействия с водородом, укажите условия протекания реакций.
4) Какой из указанных газов хорошо растворяется в воде? Как называется полученный раствор?
Задание 4. Запишите уравнения реакций, укажите условия их протекания и названия конечных продуктов; в случае необходимости расставьте коэффициенты:
![]()
![]()
![]()
![]()
![]()
![]()
Задание 5. Смешали 150 г раствора нитрата свинца (II) с массовой долей Рb(NO3)2 8% и 70 г раствора сульфида натрия с массовой долей Na2S 6%. Полученный осадок обработали избытком разбавленной азотной кислоты.
1) Составьте уравнения всех происходящих реакций. В окислительно-восстановительных реакциях расставьте коэффициенты, используя электронный баланс. Укажите окислитель и восстановитель.
2) Вычислите массы сульфата свинца (II) и серы, получившихся после обработки веществ разбавленной азотной кислотой.
3) Что произойдет, если образовавшуюся реакционную смесь отфильтровать, и фильтрат упарить и прокалить?
ЦЕНТРА РОССИИ
Первый (отборочный) тур
ХИМИЯ
Задание 1.
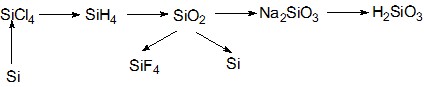
1) Напишите уравнения реакций, характеризующие данные превращения;
2) Кристаллическая решетка SiO2 и силикатов состоит из атомов кремния, окруженных четырьмя атомами кислорода – кремнекислородных тетраэдров [SiO4]. Взаимное расположение этих тетраэдров, связанных общими вершинами, может быть различным, что обуславливает существование огромного многообразия структур силикатов. Представив проекцию SiO4 на плоскость в виде
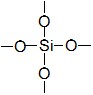
Изобразите строение линейного и циклического анионов, содержащих 6 атомов кремния.
Задание 2. Осуществите цепочку превращений:
![]()
![]()
Задание 3. При сгорании19,6 г некоторого органического вещества образовалось 26,88 л углекислого газа и 18 г воды. Относительная плотность данного вещества по гелию равна 24,5. Установите молекулярную формулу вещества, назовите его и определите возможное строение, если известно, что:
а) данное вещество взаимодействует с аммиачным раствором оксида серебра;
б) не имеет геометрических изомеров;
в) взаимодействует с водным раствором перманганата калия при 0 0С с выпадением бурого осадка;
г) при взаимодействии с перманганатом калия в кислой среде при нагревании углекислый газ не выделяется.
Напишите уравнения всех указанных реакций.
Задание 4. Определите формулу кристаллогидрата сульфата металла, если известно, что массовая доля соли в нем равна 51,351% и масса воды в 0,5 моль кристаллогидрата на 9 г меньше массы безводной соли.
Задание 5. Смесь метиламина и пропана объемом 7,84 л (н. у.) смешали с газообразным бромоводородом. Полученная газовая смесь имеет плотность 2,955 г/л и объем 5,6 л (н. у.). Определите объемные доли компонентов в исходной смеси.


