МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ имени ШАКАРИМА г. СЕМЕЙ
Инженерно-технологический факультет
Кафедра химия
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНЫМ ЗАНЯТИЯМ
ПО ДИСЦИПЛИНЕ
«ОСНОВЫ ТЕОРЕТИЧЕСКОЙ ЭЛЕКТРОХИМИИ»
для специальности
5В072000 – «Химическая технология неорганических веществ»

СЕМЕЙ
2014
1 РАЗРАБОТАНО
Составители ________ «___» _______ 20___г
старший преподаватель кафедры «Химия»
2. ОБСУЖДЕНО
2.1 На заседании кафедры «Химия»
наименование кафедры
Протокол от « ____» ______________20__г., №___
дата
Заведующий кафедрой ________
подпись
СОДЕРЖАНИЕ
стр. | ||
1 | «Равновесие в растворах электролитов. Электролитическая диссоциация». | 4 |
2 | «Электростатическая теория сильных электролитов» 1 | 4 |
3 | «Неравновесные явления в растворах электролитов. Законы Фарадея» | 5 |
4 | «Электропроводность растворов электролитов» | 6 |
5 | Определение ионной проводимости» (лабораторная работа1). | 8 |
6 | «Термодинамика электродного равновесия» | 10 |
7 | Работа с одним реактором в постоянном (непрерывном) режиме» (лабораторная работа2). | 11 |
8 | Работа только с одним реактором в постоянном (непрерывном) режиме с эффектом смешивания» (лабораторная работа3). | 13 |
9 | «Теории двойного электрического слоя» | 15 |
10 | Электрохимические свойства окислительно – восстановительных систем» (лабораторная работа4). | 16 |
11 | «Неравновесные электродные процессы» | 18 |
12 | «Окислительно-восстановительные реакции, протекающие в гальванических элементах» (лабораторная работа 5). | 18 |
№ 1. Тема: «Равновесие в растворах электролитов. Электролитическая диссоциация».
Цель занятия:
Рассмотрение классической теории электролитов, равновесных процессов в растворах электролитов.
Содержание занятия:
1. Теория электролитической диссоциации.
2. Степень диссоциации, константа диссоциации.
3. Активность, коэффициент активности. Ионная сила раствора.
4. Растворимость, произведение растворимости.
Упражнения. Задачи.
Задача 1.
Найти при 25°С константу равновесия реакции
Hg2Cl2 + 2FeCl2 = 2Hg + 2FeCl3 | (1.10) |
Задача 2.
Даны растворы KCl, NaNO3, NaCl и KNO3 с концентрацией по 0,01 моль/кг H2O. Средние ионные коэффициенты активности электролитов первых трех растворов равны соответственно 0,9022; 0,9047; 0,9059. Рассчитайте средний ионный коэффициент активности KNO3.
Задача 3.
Вычислите растворимость CuCl при 298 К в воде и в 0,025 М растворе MgSO4, если произведение растворимости (ПР) CuCl равно 3,2•10?7 (моль/л)2 и ![]() .
.
Задача 4.
Вычислите произведение растворимости Ca(OH)2 при 298 К. Растворимость гидроксида кальция составляет 0,155 г/100 г воды.
Задача 5.
Вычислите кажущуюся константу ионизации муравьиной кислоты, ионная сила которой 0,01 моль/л при 298 К, предположив, что коэффициент активности недиссоциированной формы кислоты равен 1 (gHA = 1). Термодинамическое значение константы ионизации равно 1,75•10?4 моль/л.
Задача 6.
Если константа диссоциации NH4OH равна 1,8•10-5, то при какой концентрации степень ее диссоциации равна 0,01?
№ 2. Тема: «Электростатическая теория сильных электролитов»
Цель занятия:
Ознакомление с теорией сильных электролитов.
Содержание занятия:
Основные положения теории Дебая-Хюккеля. Понятие об ионной атмосфере. Радиус ионной атмосферы и физический смысл этой величины. Зависимость радиуса ионной атмосферы от концентрации, температуры, заряда ионов и диэлектрической проницаемости. Уравнения теории Дебая-Хюккеля и границы их применимости. Ассоциация ионов. Константа ассоциации. Принципиальное отличие ионной пары от молекулы. Теория Бьеррума.
Контрольные вопросы:
Задача 1.
Рассчитайте средний коэффициент активности ?± 0,001 М раствора MgSO4, если константа А в предельном законе Дебая-Гюккеля для водных растворов при 25оС равна 0,509 (л/моль)1/2•K3/2.
Задача 2.
Определите ионную силу раствора Al2(SO4)3, моляльная концентрация которого равна 0,2 моль/кг H2O.
Задача 3.
Вычислите активность электролита aЭ и среднюю ионную активность a± ZnSO4, если его концентрация в растворе 0,1 моль/л, а средний ионный коэффициент активности равен 0,148.
Задача 4.
Ионная сила раствора KCl равна 0,2 моль/л. Какова его молярная концентрация? Какова должна быть молярная концентрация раствора BaCl2 той же ионной силы?
Задача.
Ионная сила pacтвоpa NаCl равна 0,2. Какова его моляльность? Какова должна быть моляльность раствора АlСl3 той же ионной силы?
№ 3. Тема: «Неравновесные явления в растворах электролитов. Законы Фарадея»
Цель занятия:
Ознакомление с процессами электролиза. Законы Фарадея.
Содержание занятия:
Классификация проводников и прохождение постоянного электрического тока через проводники I и II рода. Основные типы электрохимических систем и их составные части. Определения понятий катод и анод. Направление тока в электрохимической системе (ячейке, цепи). Различие между химическими и электрохимическими реакциями. Электролиз как окислительно-восстановительный процесс.Контрольные вопросы:
Задача 1.
Написать уравнения процессов, происходящих при электролизе водного раствора сульфата натрия с нерастворимым анодом. Укажите, какие вещества образуются в катодном и анодном пространствах.
Ом?1•см?1.
Задача 2.
Гальванический элемент составлен из алюминиевого и никелевого электродов. Определите, какой из электродов Al|Al3+ или Ni|Ni2+ будет являться положительным и отрицательным полюсом элемента. Запишите уравнения электродных реакций.
Задача 3.
Установить, в каком направлении возможно самопроизвольное протекание реакции
2NaCl + Fe2(SO4)3 = 2FeSO4 + Cl2 + Na2SO4
Задача 4.
Гальванический элемент составлен из 2-х электродов: иод-серебряного, помещенного в раствор 0,1М НJ, и водородного, опущенного в 0,01М раствор кислоты НХ. Разность равновесных потенциалов между этими электродами составила 0,117В. Рассчитайте константу диссоциации Ка кислоты НХ, если известны только значение Ео для серебряного электрода, равное 0,799, и величина ПРAgJ=1,1?10-16.
№ 4. Тема: «Электропроводность растворов электролитов»
Цель занятия:
Рассмотрение количественной характеристики электропроводности электролитов.
Содержание занятия:
1. Физический смысл удельной электропроводности и методы ее измерения.
2. Молярная и эквивалентная электропроводности и их связь с удельной электропроводностью.
3. Зависимость удельной и эквивалентной электропроводности от концентрации электролита.
4. Предельная эквивалентная электропроводность.
5. Скорость движения ионов, абсолютная скорость и подвижность ионов. Принцип независимого движения ионов Кольрауша.
6. Электропроводность смеси электролитов.
7. Аномальная подвижность ионов.
8. Числа переноса и их связь со скоростями движения ионов.
Контрольные вопросы:
Задача 1.
Сопротивление ячейки для измерения электропроводности в которой содержится 0,02 М раствор KCl равно 35,16 Ом при 291 К, а для 0,1 М раствора уксусной кислоты ? 179 Ом. Какова степень диссоциации уксусной кислоты? Для уксусной кислоты L0 = 350,0 Ом?1•см2•моль-экв?1. Удельная электропроводность 0,02 М раствора KCl при 291 К равна 0,002399 Ом?1•см?1.
Задача 2.
Раствор с концентрацией H2SO4 70 мас. % имеет плотность 1,615 г/см3 и удельную электропроводность 0,2157 Ом?1•см?1 при 291 К. Найдите значения эквивалентной и молярной электропроводности раствора.
Задача 3.
Эквивалентная электропроводность пропионовокислого натрия при бесконечном разведении равна 89,3 Ом?1•см2•моль-экв?1 (298 К). Подвижности ионов Na+ и H+ соответственно равны 50,5 и 350,0 Ом?1•см2•моль-экв?1. Какова эквивалентная электропроводность бесконечно разбавленного раствора пропионовой кислоты при 298 К?
Задача 4.
Предельные подвижности ионов H+ и CH3COO? соответственно равны 349,8 и 40,9 См•см2•моль-экв?1. Значение эквивалентной электропроводности равно 12,77 См•см2•моль-экв?1. Найдите константу диссоциации и рН раствора при с = 1,59•10-4 моль/л.
Задача 6.
Сопротивление водного 0,1 М раствора AgNO3 равно 42,4 Ом. Кондуктометрическая ячейка, в которой измерялось сопротивление имела электроды из двух плоских параллельных пластин площадью по 2 см2 каждая. Расстояние между пластинами 0,9 cм. Определите удельное сопротивление, эквивалентную и удельную электропроводности.
Задача 5.
В ячейку для измерения электропроводности помещены платиновые электроды в форме дисков диаметром 1,34 см, расстояние между электродами 1,72 см. Ячейка заполнен 0,05 н раствором NaNO3. При напряжении 0,5 В через данный раствор идет переменный ток силой 1,85 мА. Найдите величину удельной и эквивалентной электропроводности раствора NaNO3.
Задача 6.
Удельная электропроводность насыщенного раствора AgBr равна 1,576•10?6 Ом?1•см?1, а воды, взятой для растворения 1,519•10?6 Ом?1•см?1. Найдите растворимость AgBr (S) в воде и произведение растворимости (ПР), если известно, что эквивалентные электропроводности при бесконечном разведении для KBr, KNO3, AgNO3 имеют значения 137,4; 131,3; 121,0 Ом?1•см2•моль-экв?1, соответственно.
Задача 7.
Числа переноса анионов в водных растворах 0,1 н хлорида калия, 0,1 н хлорида натрия и 0,1 н нитрата калия при 18оС соответственно равны 0,505, 0,610, 0,497. Вычислите число переноса аниона в 0,1 н растворе нитрата натрия при той же температуре, не принимая в расчет взаимодействие между ионами.
Задача 8.
При температуре 298 К методом перемещения границы в 0,005 н растворе хлорида калия было определено значение числа переноса иона хлора 0,5069, а в 0,01 н растворе хлорида натрия при той же температуре ? 0,6082. Определите числа переноса ионов хлора, натрия и калия в 0,005 н растворе по отношению к хлориду калия и в 0,01 н растворе по отношению к хлориду натрия в предположении, что никакого взаимодействия между ионами нет.
№ 5. Тема: Определение ионной проводимости (лабораторная работа 1)
Цель работы
Цель данного упражнения заключается в определении ионной проводимости ???![]()
![]() и ?R необходимых для обработки экспериментальных данных в процессе выполнения следующих упражнений.
и ?R необходимых для обработки экспериментальных данных в процессе выполнения следующих упражнений.
Требуемые элементы
¦ 1 литр растворителя этила ацетата с концентрацией 0.05 M. ¦ программа SACED-QRIA QRC. ¦ 1 растворителя гидрата окиси соды с концентрацией 0.05 M.¦ Оборудование QRIA
Выполнение упражнения
Для реализации данного упражнения необходимо выполнение следующих процедур:
1. Введите раствор ацетата соды внутрь реактора 3. Накройте крышку и настройте смеситель, как объясняется в руководстве по установке.
2. Запустите программу SACED-QUSC.
3. Выберите опцию «Охват данных»( “Data capture”). Выберите «время охвата»( time of capture) (значок часов), выберите «имя файла»( the name of the file) для сохранения данных в файле (значок диска) и наконец нажмите «значок воспроизведение» (play icon)
4. Включите систему термостатизации и выберите 25?C.
5. Включите систему мешалки для облегчения быстрой термостатизации.
6. Возьмите образец в нижнем мундштуке реактора и определите проводимость раствора при данной температуре.
7. Повторите измерения при 35 и 45?C.
8. Запишите результаты в таблице 3.5.1.
9. Опустошите реактор с помощью нижнего клапана. 10. Промойте его водой несколько раз. 11. Повторите предыдущие шаги с раствором гидрата окиси соды. 12. Прочистите реактор еще раз. 13. Выключите систему.Результаты и таблицы
После заполнения данных, произведите следующие вычисления:

Заключения и комментарии
Принимая во внимание полученные данные, ответьте на следующие вопросы:
? Как температура влияет на проводимость каждой субстанции? ? Какие факторы приводят к такому поведению? ? Почему разные субстанции имеют разные поведения при одинаковых изменениях температуры?7.3.5.6 Дополнительные графики
Представьте в графической форме эволюцию проводимости в функции температуры обоих субстанций.
Графическое представление вариации проводимости ацетата соды и гидрата окиси соды
в функции температуры.
№ 6. Тема: «Термодинамика электродного равновесия».
Цель занятия:
Ознакомление с понятием электродный потенциал. Уравнение Нернста. Электродные системы.
Содержание занятия:
1. Понятие электродного потенциала. Уравнение Нернста для электродного потенциала.
2. Термодинамическая трактовка равновесных электродных потенциалов.
3. Химический потенциал и изобарно-изотермический потенциал системы. Соотношение между ними.
4. Классификация электродов.
5. Какие электродные системы пригодны для использования в качестве электродов сравнения?
6. Диффузионный потенциал и условия его возникновения.
Контрольные вопросы:
1. Как рассчитать ЭДС элемента по изменению термодинамических функций для данной реакции?
2. К каким типам электродов относятся водородный, хингидронный и оксидно-ртутный электроды?
3. Что такое поверхностный, внутренний и внешний потенциалы?
4. На каком принципе основано измерение рН раствора с помощью стеклянного электрода?
5. Что такое Гальвани - и Вольта-потенциалы?
№ 7. Тема: Работа с одним реактором в постоянном (непрерывном) режиме.
Цель работы
Целью данного упражнения является проведение базовой реакции гидролиза этилацетата при работе с одним реактором. Знание системы и реакции облегчит проведение изучение.
Требуемые элементы
¦ 10л раствора этилацетата 5М для проведения данного упражнения
¦ 10 л. раствора гидроксида соды 0.1 М
¦ оборудование QRSA
¦ программа SACED-QRSA
¦ Руководство по эксплуатации QRSA
Проработка упражнения
Для осуществления упражнения, следуйте шагам:
Введите растворы этилацетата и гидроксида соды в соответствующие баки реагентов. Запустите программу SACED-QRSA. Выберите опцию «Охват данных»( “Data capture”). Выберите «время охвата»( time of capture) (значок часов), выберите «имя файла»( the name of the file) для сохранения данных в файле (значок диска) и наконец нажмите «значок воспроизведение» (play icon) Включите систему термостатизации и выберите 25?C. Расположите клапана в позиции, показанных ниже, так чтобы реагенты вошли напрямую ТОЛЬКО в реактор 1 и продолжили движение в бак проходя сквозь кондукционную сетку.Позиционирование клапанов.
3-ходовые клапана имеют следующие индикаторы направления, которые указывают различные возможные направления потоков
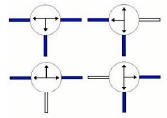 Рис. 3.6.1
Рис. 3.6.1
В следующей диаграмме мы отмечаем индикатор направления, в которой мы должны оперировать:
¦ Коллектор 1, клапан V-1 открыт, клапана V2 и V3 закрыты.
¦ Коллектор 2, клапан V-4 открыт, клапана V5 и V6 закрыты
В этом случае, оба реагента войдут только в Реагент 1.
¦ Клапан VT-1 должен быть в позиции, указанной на рисунке, с потоком продукта, идущим только в коллектор-3.
¦ Клапан V-7 должен быть закрыт.
Как только клапана установлены в вышеуказанных позициях, расположите 3-ходовые клапана базового модуля в позицию «рециркуляции». Настройте насосы реагентов в желаемую позицию, мануально, и включите клапана (уже подготовленных для использования). Проверьте, что клапана расходомеров открыты.9. Включите насосы с помощью программы оборудования.
10. Если мячик, измеряющий поток сильно свисает за пределы шкалы, скорректируйте поток с помощью потока расходомера.
11. Как только поток стабилизируется, поверните 3-ходовый клапан базового модуля в сторону реактора, и реагенты пойдут в направлении реактора 1.
12. Примите во внимание различные значения проводимости в таблице, полученные в момент, когда продукт достигает коллектора кондукционной клетки.
13. Выключите систему.
Результаты и Таблицы.
Когда вы приняли в учет полученные значения, сделайте требуемые вычисления для того, чтобы получить значения временной эволюции конверсии.
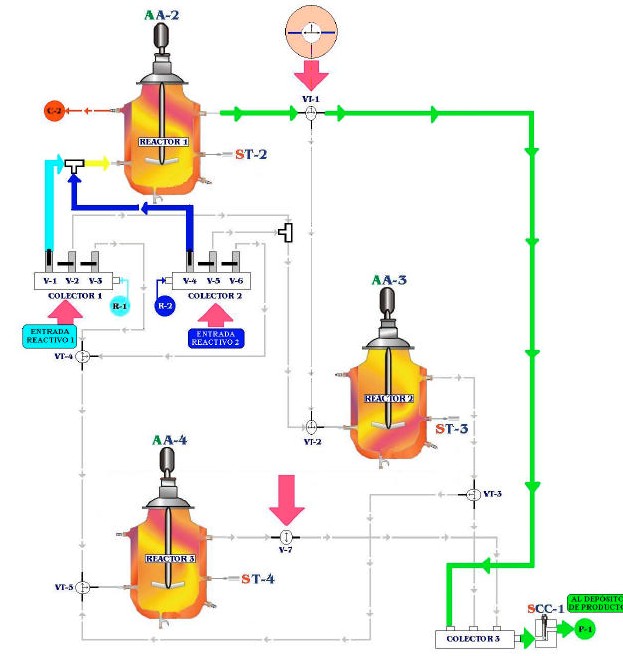
Рис. 3.6.2 Позиции клапанов для того, чтобы работать с реактором в постоянном режиме.
№ 8. Тема: Работа только с одним реактором в постоянном (непрерывном) режиме с эффектом смешивания.
Цель работы
Цель данного упражнения произвести базовую операцию гидролиза этилацетата с помощью одного реактора, чтобы ученики могли узнать систему и реактор с большей легкостью и мы увидим как ссылочная концентрация изменится при добавлении эффектов смешивания.
Требуемые элементы
Требуемые элементы для осуществления данной практики:
¦ 10 л. раствора этилацетата 5М
¦ 10 л. раствора гидроксида соды 0.1М
¦ оборудование QRSA
¦ программа SACED-QRSA
¦ Руководство по эксплуатации QRSA
Проработка упражнения.
Для осуществления упражнения, следуйте шагам:
Введите растворы этилацетата и гидроксида соды в соответствующие баки реагентов. Запустите программу SACED-QRSA. Выберите опцию «Охват данных»( “Data capture”). Выберите «время охвата»( time of capture) (значок часов), выберите «имя файла»( the name of the file) для сохранения данных в файле (значок диска) и наконец нажмите «значок воспроизведение» (play icon) Включите систему термостатизации и выберите 25?C. Включите мешальную лопасть Установите клапана в позициях Расположите клапана в позиции, показанных ниже, так чтобы реагенты вошли напрямую ТОЛЬКО в реактор 1 и продолжили движение в бак проходя сквозь кондукционную сетку.Позиционирование клапанов.
3-ходовые клапана имеют следующие индикаторы направления, которые указывают различные возможные направления потоков
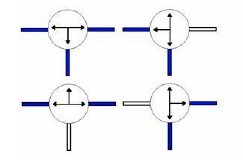
В следующей диаграмме мы отмечаем индикатор направления, в которой мы должны оперировать:
¦ Коллектор 1, клапан V-1 открыт, клапана V2 и V3 закрыты.
¦ Коллектор 2, клапан V-4 открыт, клапана V5 и V6 закрыты
В этом случае, оба реагента войдут только в Реактор-1.
¦ Клапан VT-1 должен быть в позиции, указанной на рисунке, с потоком продукта, идущим только в коллектор-3.
¦ Клапан V-7 должен быть закрыт.
8. Как только клапана установлены в вышеуказанных позициях, расположите 3-ходовые клапана базового модуля в позицию «рециркуляции».
9. Настройте насосы реагентов в желаемую позицию, мануально, и включите клапана (уже подготовленных для использования).
10. Проверьте, что клапана расходомеров открыты
11. Включите насосы с помощью программы оборудования.
12. Если мячик, измеряющий поток сильно свисает за пределы шкалы, скорректируйте поток с помощью потока расходомера.
13. Как только поток стабилизируется, поверните 3-ходовый клапан базового модуля в сторону реактора, и реагенты пойдут в направлении реактора 1.
14. Примите во внимание различные значения проводимости в таблице, полученные в момент, когда продукт достигает коллектора кондукционной клетки.
15. Выключите систему.
Результаты и Таблицы.
Когда вы приняли в учет полученные значения, сделайте требуемые вычисления для того, чтобы получить значения временной эволюции конверсии.
№ 9. Тема: «Теории двойного электрического слоя»
Цель занятия:
Ознакомление с моделями двойного электрического слоя.
Содержание занятия:
1.Мембранное равновесие и мембранный потенциал.
2.Диффузионный потенциал.
3. Теория строения двойного электрического слоя Гельмгольца.
4.Теория строения двойного электрического слоя Гуи-Чапмена.
5. Теория Штерна строения двойного электрического слоя.
6. Современные представления о строении двойного электрического слоя.
Контрольные вопросы:
1. Образование ДЭС.
2. Заряд и емкость двойного электрического слоя.
3. Связь между ёмкостью ДЭС и поверхностным натяжением.
4. Толщина диффузного слоя. Её зависимость от концентрации, распределение потенциала в диффузном слое.
№ 10. Тема: Электрохимические свойства окислительно – восстановительных систем
Цель работы
Провести наблюдения за электрохимическими свойствами окислительно-восстановительных систем
Реактивы и приборы: 0,0002М КMnO4; 10% растворы FeSO4 или ZnCl2; раствор KCNS; раствор KI; H2SO4 разбавл.; 10% раствор NaCl; раствор K2Cr2O7; раствор Na2S2O3; бромная или хлорная вода; стекляная вата раствор крахмала; раствор йода; HNO3 разбавл.; 6Н HCl; U-образная трубка; 2 медных электрода; гальванометр; 2 стекляных фильтра; штатив лабораторный; 2 резиновые пробки с отверстиями.
Проведение опыта А. Во внутрь U-oбразной трубки заталкивают тампон из стеклянной ваты так, чтобы она была разделена на две примерно одинаковые части. В одно колено наливают подкисленный серной кислотой раствор КМпО4 а в другое — 10 % - ный раствор FeS04 или SnCl2. В оба раствора погружают платиновые (или медные) электроды, подсоединяют их к клеммам гальванометра и измеряют ЭДС этой гальванической цепи. Затем замыкают клеммы гальванометра накоротко и оставляют их в таком положении на некоторое время, наблюдая за изменениями, происходящими в растворах. По окончании опыта в колено с раствором сульфата железа прибавляют несколько капель раствора роданида калия.
Результат опыта. При подключении платиновых электродов к гальванометру стрелка прибора заметно отклоняется, что указывает на прохождение через него электрического тока. По мере работы гальванического элемента наблюдается обесцвечивание раствора перманганата калия вблизи поверхности электрода. В другом колене трубки появляются ионы железа (III), которые обнаруживаются по появлению ярко-красной окраски после добавления к раствору роданида калия.
Проведение опыта Б. Берут такую же U-образную трубку, как и в предыдущем опыте, и наполняют одно колено раствором 10%-ного хлорида натрия, другое — раствором хлорида олова такой же концентрации. В оба колена погружают платиновые (или медные) электроды, подсоединяют их к гальванометру и измеряют ЭДС цепи. Затем в колено с раствором хлорида натрия добавляют небольшое количество хлорной или бромной воды и вновь повторяют измерение ЭДС.
Результат опыта. После добавления к раствору хлорной или бромной воды ЭДС гальванического элемента сильно возрастает.
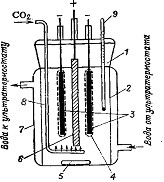
Проведение опыта В. U-образную трубку заполняют 6 н. раствором соляной кислоты. В оба колена плотно вставляют резиновые пробки, в отверстия которых вводят трубки двух стеклянных фильтров (рис.). Необходимо добиться того, чтобы все пространство трубок вплоть до пористых стеклянных пластинок обоих фильтров было заполнено 6 н. раствором НС1 — пузырьков воздуха не должно быть. В одну из воронок наливают раствор, содержащий окислитель, в другую — раствор, содержащий восстановитель. Затем в обе воронки погружают платиновые (или медные) электроды, которые подсоединяют к клеммам гальванометра. Ниже приведены комбинации растворов, которые можно использовать в этом опыте для составления окислительно-восстановительных гальванических элементов:
Раствор внутри трубки | Раствор в левом фильтре | Раствор в правом фильтре | |
№1 | 6Н HCl | 0,0002М КMnO4, подкисленный H2SO4 | SnCl2, 10% - ый раствор |
№2 | 6Н HCl | 1Н KI + крахмал | HNO3 разбавленный |
№3 | 6Н HCl | KI подкисленный | K2Cr2O7 подкисленный |
№4 | 6Н HCl | Раствор I2 | Раствор Na2S2O3 |
Результат опыта. Через некоторое время после начала работы окислительно-восстановительного гальванического элемента в зависимости от взятой пары растворов в левом стеклянном фильтре будут наблюдаться следующие изменения цвета растворов: комбинация растворов №1 — обесцвечивание, №2 — появление синей окраски, № 3 — появление коричневой окраски, № 4 — обесцвечивание.
Обьяснение. В основе работы гальванического элемента, демонстрируемого в опыте А, лежит следующая окислительно-восстановительная реакция:
4КМnO4 + 16H2S04 + 10SnCI2 > 4MnSO4 + 2K2SO4 + SnCI4 + 5Sn (SO4)2 + I6H2O
Как видим, в этой реакции олово (II), отдавая электроны, окисляется:
5Sn2+ > 5Sn4++ 10ё-
а марганец, приобретая электроны, восстанавливается:
2MnO4 + 16Н+ + 10ё - > 2Mn2+ + 8Н20
В случае применения вместо SnCl2 раствора FeSO4 реакции окисления и восстановления соответственно будут иметь вид
5Fe2+ > 5Fe3+ + 5ё- (окисление)
MnO4 + 8Н+ + 5ё - > Mn2+ + 4Н20 (восстановление)
Появляющиеся в результате этой реакции ионы железа (III) образуют при взаимодействии с роданидом соединение, окрашивающее раствор в ярко-красный цвет. Как известно, ионы железа (II) не образуют с роданидом окрашенного соединения.
В основе работы гальванического элемента, применяемого в опыте Б, лежат следующие реакции окисления и восстановления:
Sn2+ > Sn4+ + 2е - (окисление)
С12 + 2е - > 2С1- (восстановление)
В опыте В при применении комбинации растворов № 1 имеет место та же окислительно-восстановительная реакция, что и в опыте А. ,
В случае применения комбинации растворов № 2 в левом фильтре U-образной трубки будет происходить реакция окисления иодида:
2І - > І2 + 2е - (І2 с крахмалом дает интенсивное синее окрашивание и восстановленне азотной кислоты до азотистой:
NО3- + 2Н+ + 2е - > NO2 - + Н20
При использовании растворов в комбинации № 3 реакции окисления и восстановления будут протекать по уравнениям:
6І - > 3I + 6e - (окисление)
Сr2О72- + 14Н+ + 6е - > 2Сг3+ + 7Н20 (восстановление)
В комбинации растворов №4 имеет место окислительно-восстановительная реакция между иодом и тиосульфатом натрия:
2Na2S2О3 + І2 > 2NaІ+ Na2S4О6
или в ионной форме:
2 S2О3 > S4О6 2- + 2е- (окисление)
І2 + 2е - >2І - (восстановление)
№ 11. Тема: «Неравновесные электродные процессы»
Цель занятия:
Ознакомление с теориями перенапряжения.
Содержание занятия:
1. Перенапряжение. Виды перенапряжений.
2. Понятие о диффузионном перенапряжении.
3. Теории диффузионного перенапряжения.
4. Общая характеристика реакционного (химического перенапряжения).
5. Перенапряжение при выделении кислорода.
Контрольные вопросы:
1. Предельный диффузионный ток iд. Факторы, влияющие на величину iд.
2. Уравнение Тафеля. Константы «а» и «в», определение из поляризационных измерений.
3. При выделении хлора из раствора поваренной соли при 40оС были получены следующие данные:
I, А/см2 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,8 | 1,0 |
Е, В | 1,45 | 1,5 | 1,53 | 1,56 | 1,57 | 1,62 | 1,64 |
Проверить, подчиняется ли поляризация электрода при выделении хлора уравнению Тафеля; если подчиняется, найти коэффициенты в уравнении. Принять, что парциальная упругость хлора равна 1 атм, активность ионов С1- 1 г - ион/л.
4. Уравнение диффузионного перенапряжения при постоянном миграционном переносе. Влияние миграции тока в растворе бинарного электролита.
№ 12. Тема: Окислительно-восстановительные реакции, протекающие в гальванических элементах
Цель работы
Наблюдение за окислительно-восстановительными реакциями протекающими в гальванических элементах.
Реактивы и оборудования: серебряная проволока, медная пластинка, 1М Сu(NO3)2; 1М AgNO3; 0,1М HСl; 3 химических стакана на 200 мл; аппарат для получения H2S.
Проведение опыта А. В химический стакан наливают примерно 150 мл 1,0 М раствора нитрата серебра, погружают в него тщательно очищенную и обезжиренную медную пластинку и наблюдают за изменениями, протекающими в стакане.
Результат опыта А. Через некоторое время после погружения в стакан медной пластинки раствор окрашивается в голубой цвет, что указывает на появление на нем ионов меди (II). Кроме того, на медной пластинке появляется хорошо заметный налет металлического серебра.
Объяснение. В стакане происходят такие же химические реакции, какие бы протекали в гальваническом элементе, составленном из серебряного и медного электродов:
Ag | Ag+ | KN03 | Си2+ | Си
?Ag ?Cu
В этом элементе положительные ионы серебра принимают электроны от серебряной пластинки и превращаются в нейтральные атомы металлического серебра. В правом полуэлементе, наоборот, атомы меди отдают электроны медной пластинке, превращаются в ионы и переходят в раствор. Эти электроны двигаются через внешнюю цепь (соединительные прохода, вольтметр и т. д.) к серебряному электроду. Все эти процессы можно представить следующими уравнениями:
В правом полуэлементе Си (тв) > Си2+ (водн) + 2ё-
В левом полуэлементе 2Ag+ (водн) + 2е - > 2Ag (тв)
Суммарная реакция Си (тв) + 2Ag+ (водн) > Си2+ (водн) + 2Ag (тв)
Таким образом, в медном полуэлементе протекает реакция окисления, а в серебряном — восстановления.
В нашем опыте перенос электронов происходит непосредственно от атомов меди к ионам серебра, находящимся в растворе вблизи поверхности медной пластинки. По существу, этот местный перенос заменяет соединительные провода, через которые осуществляется переход электронов от атомов меди к ионам серебра в электрохимическом элементе.
Проведение опыта Б. В химический стакан наливают примерно на две трети его объема 1,0 М раствор соляной кислоты, погружают в него тщательно зачищенные и обезжиренные металлические пластинки из - меди, серебра и цинка и наблюдают за изменениями, протекающими на ітоверхности этих пластинок.
Результат опыта. Из всех металлов только цинк бурно реагирует с раствором соляной кислоты. С поверхности цинковой пластинки интенсивно выделяются многочисленные пузырьки газа. Поверхность пластинок из меди и серебра остается неизменной — пузырьков газа не образуется, что свидетельствует об отсутствии реакции взаимодействия этих металлов с кислотой.
Объяснение. Реакцию взаимодействия металлического. чинка с соляной кислотой можно представить в следующем виде
Zn(тв) + 2Н+ (водн) > Zn2+ (водн) + Н2 (г)
Как видим, в этой реакции атом цинка теряет два электрона, превращаясь в ион Zn2+, т. е. цинк окисляется. Каждый ион водорода приобретает по электрону, превращаясь в атом водорода, т. е. водород восстанавливается. После восстановления два атома водорода соединяются в молекулу Н2. Как и в предыдущем опыте, суммарную реакцию можно разделить на две реакции, чтобы показать приобретение электронов (ионами водорода Н+) и отдачу электронов (атомами цинка):
Zn (тв) > Zn2+ + 2е-
2Н+ + 2е - > Н2
Суммарная реакция Zn (тв) + 2H+ > Zn2+ + Н2
Из этого опыта следует, что не все металлы реагируют с разбавленными кислотами. Так, например, магний, алюминий, железо и никель выделяют водород подобно цинку. Другие же металлы, например медь, ртуть, серебро и золото, не выделяют водород вовсе не потому, что соответствующие реакции слишком медленны. Просто одни металлы (подобно цинку) отдают свои электроны ионам водорода, а другие нет.
Проведение опыта В. В химический стакан наливают примерно на две трети его объема 1,0 М раствор нитрата меди Сu(NO)2 погружают в нее цинковую пластинку и наблюдают за изменениями, протекающими на ее поверхности в растворе.
Результат опыта. Через небольшой промежуток времени после погружения в раствор цинковая пластинка покрывается красноватым налетом металлической меди, а голубая окраска раствора постепенно исчезает.
Дальнейшее проведение опыта В. После того как голубая окраска, обусловленная в растворе присутствием ионов меди Сu2+, исчезнет, через раствор пропускают ток сероводорода H2S.
Результат опыта. Через некоторое время после начала пропускания сероводорода в растворе образуется белый осадок сульфида цинка ZnS.
Объяснение. Реакцию между металлическим цинком и водным раствором нитрата меди можно записать следующим образом:
Zu (тв) + Сu2+ > Zn2+ + Сu (тв)
В ходе этой реакции цинк теряет эпектроны, образуя ионы Zn2+:
Zu (тв) Zn2+ + 2е-
Это означает, что происходит окисление цинка. Поскольку цинк окисляется, отдавая электроны. какое-то вещество должно восстанавливаться, принимая эти электроны. Восстанавливаются ноны меди:
Cu2+ + 2е - > Сu (тв)
Таким образом, на этрт раз медь получает электроны от цинка (напомним, что при реакции между металлической медью и раствором нитрата серебра медь будет отдавать электроны ионам серебра).
Замечание. Необходимо отметить, что реакция получения электронов ионами меди от атомов металла цинка сильно смещена вправе. В этом легко убедиться, если поместить пластинку из металлической меди в раствор сульфата цинка. При этом не произойдет никаких видимых изменений, и попытка обнаружить присутствие ионов меди, пропуская сероводород H2S, чтобы осадить из раствора черный сульфид меди, не будет иметь успеха.



