Уважаемые ученики, отправляйте, пожалуйста, ответы на *****@***ru
Химия 8 класс
Автор (ы): ,
Урок 41.
Современная формулировка периодического закона. Изотопы (стабильные и радиоактивные).
В результате экспериментальных исследований было установлено, что, например, в природном кислороде, кроме атомов кислорода с массой 16 есть также атомы кислорода с массой 17 и 18. Их соотношение таково:
![]()
Оказалось, что другие элементы также состоят из атомов с разной массой. Так, в природной воде, кроме атомов водорода с массой 1, также есть атомы водорода с массой 2; соотношение чисел этих атомов следующее:
![]()
В ядерных реакциях также получен водород с атомной массой 3 . Причем «тяжелая вода» вредна для живых организмов. Поэтому притчи о «живой» и «мертвой» воде имеют реальное научное объяснение.
Таблица «Изотопы некоторых элементов, обнаруженных в земной коре».
Название элемента | Число изотопов | Массовые числа |
Гидроген(Водород) | 3 | 1, 2, 3 |
Оксиген(Кислород) | 3 | 16, 17, 18 |
Хлор | 2 | 35, 36 |
Кальций | 6 | 40, 42, 43, 44, 46, 48 |
Феррум(Железо) | 4 | 54, 56, 57, 58 |
Уран | 3 | 234,235, 238 |
Разновидности атомов одного и того же химического элемента, имеющие одинаковое число протонов в ядре, но разную массу, называют изотопами.
«Изотоп» означает «занимающий то же место».
В природе существуют химические элементы изобары - атомы, имеющие одинаковое атомное число, но разные величины зарядов ядра, например:
![]()
Атомные массы элементов в периодической системе является средним значением массовых чисел природных смесей изотопов. Поэтому они не могут, как предлагал , служить главной характеристикой атома, а следовательно, и элемента. Такой характеристикой, как мы теперь знаем, является заряд ядра. Он определяет число электронов в нейтральном атоме, которые распределяются вполне определенно вокруг ядра. Характер же распределения электронов определяет химические свойства атомов. Указанные соображения позволили дать новое определение химического элемента: Химический элемент - это совокупность атомов с одинаковым зарядом ядра.
А также уточнить формулировку периодического закона:
Свойства элементов, а также свойства и формы их соединений находятся в периодической зависимости от заряда ядра атома элемента.
Почему же атомные массы большинства элементов дробные? Выяснилось, что следует разграничивать понятия «относительная атомная масса» и «относительная атомная масса элемента».
Элемент Хлор состоит из двух изотопов с относительными атомными массами, очень близкими к 35 и 37 изотопов![]()
![]() Cl в естественной смеси содержится 75%, а изотопа
Cl в естественной смеси содержится 75%, а изотопа ![]()
![]() Cl - 25%. Отсюда средняя относительная атомная масса элемента хлора равна
Cl - 25%. Отсюда средняя относительная атомная масса элемента хлора равна
Ar = 35 • 0,75 + 37 • 0,25 = 35,5
Итак, атомная масса элемента тем больше, чем больше тяжелых изотопов входит в состав элемента.
Можно объяснить аномалию в положении в периодической системе Калия и Аргона, рассчитав их относительную атомную массу с учетом природных изотопов:
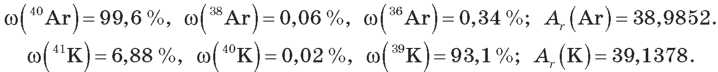
Изотопы делятся на стабильные и радиоактивные. Натрий, Алюминий, Флуор не имеют стабильных изотопов. У олова их десять.
Различают природные радиоактивные изотопы (Уран) и изотопы искусственного происхождения - радионуклиды. Опасные изотопы: Sr (замещает в костях Са), Cs, I. Радиоактивные изотопы в процессе радиоактивного излучения распадаются на атомы других элементов, вследствие чего происходит ядерная реакция, сопровождающаяся вредным излучением:
![]()
Скорость радиоактивного излучения характеризуется периодом полураспада и может длиться от доли секунды до миллиардов лет. В химических реакциях радиоактивные превращения атомов не происходят.
Домашнее задание:
Выучить§ учебника
Упражнение 1. Найдите среди элементов такой, относительная атомная масса которого - 23, а число протонов - 11:
![]()
Упражнение 2. Найдите среди элементов такой, относительная атомная масса которого - 40, а число протонов - 18. ![]()
Упражнение 3.
Составьте ядерные реакции:
3517Cl + 10n > 3516S +…
23892U + 10n > 14256Ba + 9136Kr + …



