Генная инженерия – группа молекулярных методов, позволяющих получить молекулу ДНК, объединяющую в себе материал из разных источноков.
Генная инженерия представляет собой набор методов, которые позволяют не только получать рекомбинантные ДНК, но и вводить такие рекомбинантные молекулы в клетку, создавая условия для экспрессии в ней чужеродных генов. При использовании методов генной инженерии можно получить организмы с новыми, в том числе и не встречающимися в природе свойствами.
В становлении генной инженерии ведущую роль сыграла генетика микроорганизмов.
Примерной датой рождения генной инженерии считается 1972 г, когда была создана первая рекомбинантная ДНК, объединяющая в своем составе генетический материал трех источноков: геном онкогенного вируса обезьян SV40, часть генома бактериофага ? и ген лактозного оперона кишечной палочки (П. Берг, США). Полученная молекула не была исследована на функциональную активность, так как авторы эксперимента предположили, что полученные результаты могут привести к созданию микроорганизмов, опасных для здоровья человека.

Пол Наим Берг (англ. Paul Naim Berg; род. 30 июня 1926 года, Бруклин, США) — американский биохимик, почётный профессор Стэнфордского университета, лауреат Нобелевской премии по химии. Будучи молодым исследователем он решил несколько ключевых проблем метаболической химии и продолжил исследовать механизмы, по которым ДНК и РНК управляют синтезом белков в живых системах. В 1972 Берг и его коллеги из Стэнфордского университета синтезировали первую рекомбинантную ДНК (р-ДНК), и впоследствии он помогал международному сообществу исследователей р-ДНК в их усилиях по решению потенциальных физических и этических проблем, вызыванных этой революционной теорией.
В 1980 году Берг получил Нобелевскую премию по химии вместе с Уолтером Гилбертом и Фредериком Сингером за фундаментальные исследования нуклеиновых кислот.
https://ru. wikipedia. org/wiki/%D0%91%D0%B5%D1%80%D0%B3,_%D0%9F%D0%BE%D0%BB
http://velchel. ru/index. php? cnt=9&nbio=511&nobsub=4&sub=0
Первая функционально активная молекула рекомбинантной ДНК была создана в 1973-1974 гг (С. Коэн, Д. Хелински, Г. Бойер). Были созданы плазмиды, состоящие из ДНК разных видов бактерий, а также других организмов. Например, были созданы плазмиды, содержащие участок ДНК из ооцитов шпорцевой лягушки, кодирующий синтез рРНК, фрагмент ДНК морского ежа, отвечающий за синтез гистоновых белков и другие.
В 1962 году в бактериях были обнаружены ферменты, способные отличать свою ДНК (бактериальную) и чужеродную (фаговую) (В. Арбер). Эти ферменты разрушают фаговую ДНК в бактериях. Эти ферменты были названы эндонуклеазами рестрикции или рестриктазами. Естественной функцией рестриктаз является защита бактерий от заражения вирусами.

Ве?рнер А?рбер (нем. Werner Arber; род. 3 июня 1929, Гренихен, Швейцария) — швейцарский микробиолог и генетик, лауреат Нобелевской премии в области медицины и физиологии 1978 года. Открыл рестрикционные ферменты.
В 1949—1953 годах учился в Швейцарской политехнической школе, где занимался изотопом Cl-34. После окончания политеха в 1953 году начал работать в биофизической лаборатории Университет Женевы в области электронной микроскопии. Занимался исследованиями мутантами бактериофага лямбда, которые легли в основу его докторской диссертации.
В 1958—1960 годах работал в Университете Южной Калифорнии, затем вновь вернулся в Женеву. В 1971 году перешёл в Университет Базеля.
https://ru. wikipedia. org/wiki/%D0%90%D1%80%D0%B1%D0%B5%D1%80,_%D0%92%D0%B5%D1%80%D0%BD%D0%B5%D1%80
http://velchel. ru/index. php? cnt=9&sub=0&nobsub=2&nbio=485
Рестриктазы (эндонуклеазы рестрикции) – ферменты, способные разрезать ДНК в строго определенном месте (сайте рестрикции). Для каждой рестриктазы существует свой сайт рестрикции (палиндром).
Первая рестриктаза была выделена Х. Смитом в 1970 г из штамма Haemophilus influenzae (Hind III).
Сайты узнавания для некоторых рестриктаз представлены на рисунке:
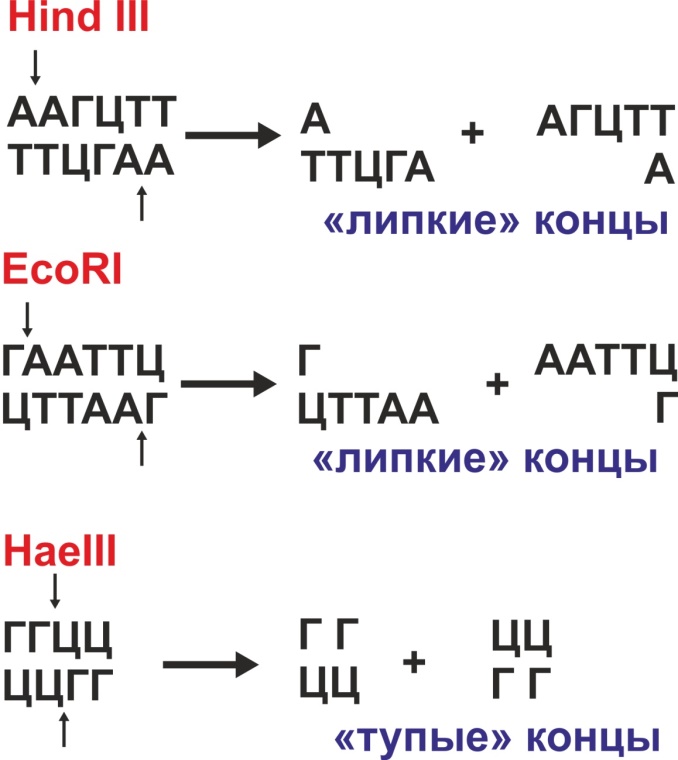
Известны 3 класса рестриктаз. Они отдичаются по характеру разрывов, вносимых в ДНК и условиям реакции. Для получения гибридных ДНК используются ферменты класса II. Рестриктазы класса II разрезают ДНК в зоне участка узнавания. Фермент узнает небольшую последовательность из 4 – 6 нп. Сайты узнавания представляют собой палиндромы.
Палиндром – последовательность ДНК, читающаяся одинаково в обеих цепях ДНК в направлении 5’- 3’.
Разрезание цепей ДНК при помощи рестриктаз происходит в середине последовательности или в стороне от оси симметрии. В первом случае образуются двухцепочечные «тупые» концы, во втором – выступающие одноцепочечные «липкие» концы. Для генно-инженерных работ чаще используются «липкие» концы, так как при обработке ДНК, полученной от разных видов организмов одной и той же рестриктазой, образуются одинаковые «липкие» концы, способные к объединению между собой.
Общая схема молекулярного клонирования состоит из следующих этапов:
- Выделение ДНК из организма – донора; Расщепление ДНК ферментами рестриктазами с образованием фрагментов ДНК с «липкими концами»; Расщепление векторной молекулы (плазмида, фаг, космида и др.) той же рестриктазой, что и исследуемый образец ДНК; Лигирование (сшивание) векторной молекулы и фрагмента исследуемой ДНК с образованием гибридной (рекомбинантной) молекулы; Введение рекомбинантной молекулы в клетку-хозяина (реципиента). Этот процесс называется трансформацией. Отбор клеток, несущих рекомбинантную ДНК (трансформированные клетки); Получение специфического белкового продукта, синтезируемого клетками-хозяевами
К настоящему времени создано несколько типов клонирующих векторов:
- Плазмиды – кольцевые двухцепочечные экстрахромосомные самореплицирующиеся молекулы ДНК бактерий. В плазмидах клонируют фрагменты ДНК до 10 т. п.н. Фаги. Первыми были разработаны выкторы на основе фага ? E. coli. ДНК фага ? составляет примерно 50 т. п.н. Значительная часть (20т. п.н.) несущественна для размножения фага и может быть заменена на чужеродную ДНК. В фаге можно клонировать фрагмент ДНК до 20т. п.н. Космиды – векторы, объединяющие в себе свойства плазмиды и фага. Созданы искусственно. Могут амплифицироваться в бактерии как плазмиды и упаковываться в фаговые головки. Могут включать вставку чужеродной ДНК до 40т. п.н. Искусственная дрожжевая хромосома (yeast artificial chromosome –YAC). Вектор разработан на основе ДНК дрожжей. Применяются для клонирования больших фрагментов ДНК (от 100 до 1000 т. п.н.) эукариот.
Клонирующий вектор должен соответствовать следующим требованиям:
Вектор должен содержать участок, куда чужеродная ДНК может быть встроена без нарушения важных функций; Вектор должен содержать регуляторные последовательности, обеспечивающие репликацию встроенной ДНК, не имеющей своих регуляторных последовательностей; Вектор должен иметь генетические маркеры, позволяющие легко обнаруживать трансформированные клетки. Желательно, чтобы маркер инактивировался при встраивании чужеродной ДНК; Вектор должен быть многокопийным.Гены для молекулярного клонирования можно полочать несколькими способами:
Непосредственное выделение из природных источников (библиотеки генов, ПЦР); Химический синтез; Синтез кДНК (синтез ДНК на матрице мРНК)Первым был клонирован ген соматотропного гормона человека в 1977 году (К. Итакура, Г. Бойер).
При помощи рестриктаз можно построить рестрикционную карту. Рестрикционная карта – карта ДНК с указанием точек разрыва различными рестриктазами.
Пример построения рестрикционной карты представлен на слайдах 6, 7 и 8.
Построение рестрикционной карты состоит из 3 этапов:
Этап 1. Обработка одного фрагмента ДНК двумя разными рестриктазами;
Этап 2. Обработка фрагментов ДНК, полученных при расщеплении одной рестриктазой А рестриктазой В (и наоборот);
Этап 3. Построение рестрикционной карты путем наложения фрагментов, полученных при разрезании фрагмента ДНК.
В настоящее время в ДНК-диагностике применяется много различных методов. Большинство методов основано на технологии ПЦР (полимеразной цепной реакции) с использованием рестрикционных эндонуклеаз. Широко распространен метод полиморфизма длины рестрикционных фрагментов. Метод основан на различиях в длине образующихся после рестрикции фрагментов ДНК. Достаточно часто в ДНК происходят нуклеотидные замены, приводящие к появлению в изучаемом фрагменте ДНК лишних сайтов для некоторых рестриктаз. В результате фрагмент ДНК с нуклеотидной заменой и без нее будут разрезаться на разное число фрагментов. Полученные фрагменты можно идентифицировать при помощи электрофоретического анализа.
Все большее значение в настоящее время приобретают молекулярные методы, основанные на гибридизации нуклеиновых кислот. Основой данной группы методов является создание зондов, комплементарных изучаемым фрагментам ДНК.
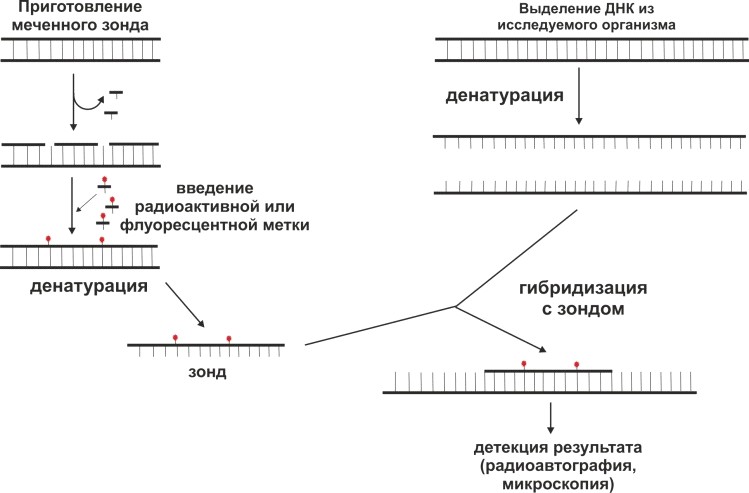
Зонд – одноцепочечная молекула ДНК, несущая радиоактивную или флуоресцентную метку и комплементарная последовательности-мишени изучаемой ДНК. Существует большое количество модификаций данного метода. Возможности метода очень широки – от определения локализации гена до расшифровок сложных перестроек между хромосомами.
Основные типы молекулярной гибридизации:
Блот-гибридизация (to blot – промакать фильтровальной бумагой). Применяется для определения наличия и местоположения определенной последовательности в геноме, а так же для обнаружения генных мутаций и диагностики генных болезней.
ДНК – проба расщепляется подходящими рестриктазами, разделяют полученные фрагменты с помощью гель-электрофореза, переносят разделенные фрагменты на специальный фильтр, гибридизуют с зондом и идентифицируют результаты.
Гибридизация in situ (на месте). Применяют для картирования генов в хромосомах и диагностики хромосомных болезней. Метафазные хромосомы фиксируют на предметном стекле, ДНК денатурируют и гибридизуют с радиоактивно меченым зондом. Результаты гибридизации выявляют при помощи радиоавтографии под световым микроскопом.
Общая схема гибридизационного анализа включает в себя следующие этапы:
Создание меченого зонда. При синтезе зонда в его последовательность включается радиоактивная или флуоресцентная метка; Выделение ДНК и денатурация с целью получения ДНК-матрицы; Гибридизация полученной ДНК-маприцы с радиоактивным зондом; Детекция полученных результатов.Широкое распространение получил метод выявления в геномной ДНК отдельных последовательностей, названный Саузерн-блоттингом. Первый этап идентификации гена, соответствующего специфическому зонду, состоит в дроблении геномной ДНК, чаще всего при помощи рестриктаз. После обработки ДНК рестриктазами образуется множество фрагментов разной длины. При электрофорезе в агарозном геле эти фрагменты образуют пятно, в котором неразличимы отдельные полосы. При помощи специфического зонда возможно выявить искомые последовательности. ДНК в геле денатурируют и накладывают на него нитроцеллюлозный фильтр. ДНК переносится на фильтр, где фиксируется при помощи высокой температуры или ультрафиолета. Эта процедура называется блоттингом (от англ. blotting – промокание). Фильтр помещают в раствор с гибридизационным зондом. Зонд связывается с комплементарным участком ДНК. Если зонд был радиоактивным, к фильтру прикладывают радиоактивную пленку и выявляют свечение в определенном месте.
Процедура блоттинга по Саузерну представляет собой перенос ДНК на нитроцеллюлозный фильтр. Для этого в ванночку с солевым буфером выкладывают гель, сверху накладывают фильтр и слой фильтровальной бумаги. Сверху накладывается груз. При промокании фильтровальной бумаги происходит перенос ДНК на фильтр. Существуют также ванночки для вакуумного переноса ДНК.
После проявления на пленке визды полосы меченной зондом ДНК.

Саузерн-блоттинг (от англ. Southern blot) — метод, применяемый в молекулярной биологии для выявления определенной последовательности ДНК в образце. Метод Саузерн-блоттинга сочетает электрофорез в агарозном геле для фракционирования ДНК с методами переноса разделённой по длине ДНК на мембранный фильтр для гибридизации. Метод называется по имени изобретателя, английского биолога Эдвина Саузерна.[1]
Другие технологии переноса (блота), например, вестерн-блоттинг, нозерн-блоттинг, саузвестерн-блоттинг используют сходные методы, но для определения РНК или белка в образце, и называются по образцу метода, придуманного Саузерном. Так как Саузерн-блот назван по имени ученого, термин пишут с заглавной буквы, в то время как вестерн-блот и нозерн-блот — со строчной буквы.
https://ru. wikipedia. org/wiki/%D0%A1%D0%B0%D1%83%D0%B7%D0%B5%D1%80%D0%BD-%D0%B1%D0%BB%D0%BE%D1%82
Одним из самых современных гибридизационных методов является метод флуоресцентной гибридизации in situ (FISH).
Изначально метод был разработан для локализации последовательностей нуклеотидов в цитологических препаратах. В последствии метод нашел применение в диагностических лабораториях, связанных с диагностикой хромосомных патологий. Зондами в данном случае являются одноцепочечные ДНК, помеченные таким образом, чтобы было возможным проведение детекции при микроскопии. Для детекции используются специальные красители флуорохромы, дающие сигналы разного цвета.
Методом FISH возможно полное кариотипирование хромосом человека. При таком методе окраски легко определяются хромосомы каждой пары.
Методом FISH возможно также многоцветное окрашивание хромосом и определение хромосомных аббераций.
Разработка и совершенствование методов молекулярной гибридизации привело к созданию технологии биочипов. Технология биочипов применяется для анализа генов и их экспресии. Метод позволяет анализировать одновременно большое количество последовастей.
Биочипы представляют собой пластинки очень небольшого размера, на которые наносятся образцы анализируемой ДНК. На одном биочипе может размещаться до 30 000 проб ДНК. К каждой пробе добавляется гибридизационный зонд. При наличии в пробе искомой ДНК, происходит присоединение зонда, помеченного флуоресцентными красителями. Анализ результатов производится при помощи специальных компьютерных программ.
При помощи технологии биочипов выявляют полиморфизмы сразу большого количества генов. Биочипы применяются для выявления предрасположенности к различным группам болезней, разработки индивидуальных подходов к лечению, картирования генов и т. д.



