| 2016-2017 9 -11 класс |
|
ПО ХИМИИ
ШКОЛЬНЫЙ ЭТАП
Раствор сульфита натрия длительно нагревали и колбе с обратным холодильником с 5 г серы. Осадок 1 отфильтровали и растворили в концентрированной серной кислоте. Через фильтрат пропустили избыток хлора, затем прибавили избыток раствора хлорида бария. Образовался осадок 2 массой 23.3 г. Напишите уравнения проходящих реакции. Предложите возможные структуры продукта присоединения серы. Вычислите, какой объем газа (н. у.) образовался при растворении осадка 1 в кислоте. (10 баллов) |
вместе со своим классом был на экскурсии в музее Казанской химической школы. Из рассказа Миша узнал, что в первой в Казани химической лаборатории, созданной в 1806 году, было только 6 химических веществ: хлорид кальция, нитрат ртути(I), нитрат серебра, гидроксид калия, и растворы серной и соляной кислот. Миша сразу же сказал, что из этих 6 соединений он мог бы, не используя никаких других реактивов, кроме воды, не используя электролиз, получить не менее 20 других химических соединений и простых веществ. Считаете ли Вы это заявление Миши Великанова хвастовством? Подтвердите свой ответ уравнениями реакций. (10 баллов) |
При обжиге черного порошка А в атмосфере кислорода выделяется бесцветный газ Б, при пропускании которого через раствор сероводорода, выпадает желтый осадок простого вещества В. Черный порошок Г, являющийся твердым продуктом обжига, был растворен к дымящем растворе хлороводородной кислоты. В результате этого образовался зеленый раствор соединения Д. При добавлении к полученному зеленому раствору иодида калия (водный раствор) выпадает осадок Е и образуется бурый раствор вещества Ж. Определите вещества А-Ж, запишите уравнения упомянутых в условии задачи реакций. (12 баллов) |
На чашках весов в равновесии находятся сосуды с соляной кислотой. В один из сосудов уронили железный гвоздик массой 1,12г. Какое количество мела (СaCO3) надо опустить во второй сосуд, чтобы весы снова уравновесились? Считать, что соляная кислота взята в избытке. (8 баллов) |
Имеются четыре водных раствора – хлорида меди (II), сульфида натрия, гидроксида калия и бромная вода (раствор брома). Напишите 4 уравнения реакций, которые могут проходить при попарном сливании этих растворов. Составьте сокращенные ионные уравнения реакций. Какие внешние признаки реакций при этом будут наблюдаться? (10 баллов) |
Напишите уравнения реакций, соответствующих следующей цепочке превращений: CH3CH2CH2Cl→ A → CH3CHClCH3→ (CH3)2CHCH(CH3)2→ B → (CH3)2C=C(CH3)2 → D → 2,3 - диметилбутадиен-1,3 → E → 1,4- дибром-2,3-диметилбутан →1,2-диметилциклобутан. Одна стрелка соответствует одной реакции. Какие вещества обозначены буквами? (10 баллов) |
Органическое вещество массой 4,08г при сгорании образует только 10,56г углекислого газа и 2,16г воды. Известно, что это ароматическое соединение, содержащее только один заместитель у бензольного кольца, плотность паров которого примерно в 2 раза выше плотности хлора в тех же условиях. Рассчитайте формулу этого соединения и приведите формулы и названия четырех изомеров, относящихся к разным классам органических веществ. (10 баллов) |
Имеется раствор, содержащий хлорид и сульфат меди (II). Этот раствор подвергли электролизу. При этом на катоде образовалась медь, а газов на катоде при электролизе не выделялось. На аноде выделилось 5,6 л (н. у.) смеси двух газов, объемная доля хлора в которой составляла 80%. Напишите уравнения процессов, протекавших при электролизе на катоде и аноде и найдите массу меди, выделившейся на катоде. (9 баллов) |
Некоторый металл образует два хлорида. Один из них образуется при реакции металла с хлором, а второй – при действии на металл соляной кислоты. Из раствора он выделяется в виде дигидрата, массовая доля металла в котором составляет 0,5244. Определите металл, какие хлориды он образует?Назовите еще два металла, которые образуют разные хлориды при реакции с хлором и с соляной кислотой. (8 баллов) |
На чашках весов в равновесии находятся сосуды с соляной кислотой. В один из сосудов уронили железный гвоздик массой 1,12г. Гвоздик полностью растворился. Какое количество перманганата калия надо опустить и в какой сосуд, чтобы весы снова уравновесились? Считать, что соляная кислота находится в избытке. (13 баллов) |
Неорганический блок | ||||||||||||||||
В кислородных масках часто используется свойство СО2 взаимодействовать с надпероксидом калия (КО2) и пероксидом калия (К2О2) с образованием О2. В каком мольном соотношении надо смешать надпероксид и пероксид, чтобы объем выделившегося кислорода в точности равнялся объему выдыхаемого СО2?(8 баллов) | ||||||||||||||||
К смеси аммиака и диоксида углерода с относительной плотностью по аргону 0,83 добавили 8 л бромоводорода, после чего относительная плотность по аргону стала равной 1,47. Определите объём исходной смеси и её состав в % мольн.(10 баллов) | ||||||||||||||||
Напишите полные уравнения реакций, соответствующих цепочке химических превращений:
| ||||||||||||||||
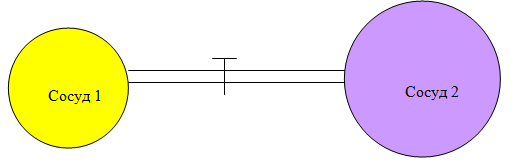
В двух сосудах объемом 2 л и 3 л при температуре 20 оС находятся указанные в таблице газы. Когда кран закрыт, давление газа в первом сосуде 2 атм, а во втором 3 атм. Каким будет конечное давление (P) когда кран будет открыт (воздух в сосудах считаем идеальным газом)? В указанных условиях ассоциацией и термической диссоциацией молекул можно пренебречь, система изотермическая(12 баллов) | ||||||||||||||||
|
| |||||||||||||||
Неизвестный металл массой 1,31 г растворили в избытке разбавленного раствора азотной кислоты, при этом выделения газа не наблюдалось. При добавлении к этому раствору избытка едкого натра при нагревании выделяется 122 мл газа (объём измерен при температуре 25 оС и давлении 101 кПа). Определите, какой металл был растворен в азотной кислоте? (10 баллов) |
Органический блок | |
1. | 2,32 г алкана пробромировали с получением смеси дибромпроизводных. Образовавшийся при этом бромоводород пропустили через избыток раствора нитрата серебра, осадок отфильтровали, высушили и прокалили до постоянной массы, равной 8,64 г. Определите, какой алкан был взят для бромирования.(8 баллов) |
2. | Продукты сжигания 696 мг дикетопиперазина, состоящего из остатков природной аминокислоты, пропустили последовательно через трубочку, наполненную перхлоратом магния, и трубочку с аскаритом (асбестом, пропитанном NaOH). Оказалось, что масса первой трубочки увеличилась на 360 мг, второй - на 1,056 г, и непоглощенными остались 97,8 мл газа (объем измерен при 25 оС и давлении 101 кПа). Установите эмпирическую (простейшую) и молекулярную формулы дикетопиперазина, предложите структурные формулы дикетопиперазина и аминокислоты.(10 баллов) |
3. | Напишите полные уравнения реакций, соответствующих цепочке химических превращений:
(10 баллов) |
4. | Сложный эфир массой 2,1 г (не содержащих элементов, кроме углерода, водорода и кислорода) был гидролизован в присутствии каталитических количеств серной кислоты. Полученная смесь органических продуктов имела плотность паров по воздуху Dвозд = 1,759. При добавлении к этой смеси избытка аммиачного раствора оксида серебра выпал осадок массой 9,475 г. Определите строение сложного эфира.(12 баллов) |
5. | При озонолизе (с последующим восстановительным гидролизом) образца некоторого природного полимера в качестве единственного продукта был получен 4‑оксопентаналь. Установите строение этого полимера. Где он используется? (10 баллов) |