
Предварительное рандомизированное исследование применения гормона роста при мышечной дистрофии Дюшенна и Беккера.
1 Введение
Мышечные дистрофии Дюшенна и Беккера ( МДД и МДБ ) являются наследственными, Х-хромосомыми, дегенеративными расстройствами, вызванными мутацией в гене дистрофина. Дистрофин играет ключевую роль в поддержании целостности сарколеммы и функционировании скелетных и сердечных мышц. Кардилмиопатия является видным клиническим признаком при обоих типах дистрофии. Клинически очевидная кардиомиопатия встречается у 73% пациентов старше 40 лет. Дилатационная кардиомиопатия представляет собой наиболее распространенный тип поражения сердца и главную причину смерти. При МДД, хотя сердечная недостаточность очень распространена и встречается практически у всех пациентов старше 18 лет, двигательная и дыхательная дисфункции прогрессируют быстрее, и представляют первую причину смерти. Роль гормона роста / инсулиноподобного фактора роста -1 ( ГР/ИФР-1 ) в модуляции структуры и функции сердца при нормальных условиях и при болезненных состояниях, недавно была обозначена в серии исследований у животных и человека. Однако использование ГР в качестве дополнительной терапии при сердечной недостаточности остается спорным. В самом деле, в то время как несколько неконтролируемых исследований зафиксировали значительное улучшение клинического статуса, функции миокарда у пациентов с дилатационной кардиомиопатией, недавние рандомизированные исследования не показали существенных изменений базовых показателей левого желудочка ( ЛЖ). В дополнение к сердечной мышце, скелетные мышцы являются типичной тканью-мишенью для анаболического и стимулирующего рост действие ГР, и его участие является известным фактом при всех мышечных дистрофиях. Кроме того, было документировано, что хорошо известные положительные эффекты кортикостероидов при МДД связаны с повышением циркулирующего уровня ИФР-1, что свидетельствует о связи между ГР/ИФР-1. Дальнейшее подтверждение использования ГР при мышечных дистрофиях описано в двух недавних исследованиях на животных. Такеши и соавт. показали, что 3-недельное лечение ГР предотвратило развитие сердечной недостаточности. Совсем недавно, Росс показал снижение конечного систолического стресса и улучшенную функцию систолических показателей у молодых хомячков после лечения ГР. Целью настоящего исследования было оценить влияние 3 - месячного лечения ГР на структуры и функции сердца у пациентов с Х-хромосомой мышечной дистрофией. Мы также измерили уровни циркулирующего мозгового натрийуретического пептида ( МНП ) и цитокинов, поскольку они коррелируют с тяжестью сердечной недостаточности и прогнозом. В связи с отсутствием данных о безопасности ГР в этой конкретной популяции пациентов, мы планируется пилотное исследование с двойным слепым плацебо контролируемым дизайном.
2 Методы
2.1 Протокол исследования.
Десять пациентов с КМП и шесть последовательных пациентов с МДД, с документированным поражением сердца были выбраны после письменного информированного согласия из большой когорты посещающих. Иммуногистохимический анализ дистрофина из скелетных мышц проводилась у всех больных для подтверждения диагноза в соответствии с ранее описанными методами. Протокол исследования был одобрен Комитетом по этике из Университета Федерико. Пациенты были рандомизированы для получения плацебо или рекомбинантного человеческого ГР. В частности, доза ГР была 0,23 и 0.07мг/кг/нед. у пациентов с Дюшенна и Беккера, соответственно, самостоятельно подкожно перед сном в течение 3 месяцев. Доза ГР была выбрана как обычная доза для замещения ГР у субъектов с его дефицитом, физиологического снижения секреции гормона роста с возрастом, нарушения секреции гормона роста после стимуляционных тестов у некоторых пациентов, и предыдущий опыт у больных хронической сердечной недостаточностью. Фон терапии остался неизменным у всех пациентов. При МДБ - это ингибитор ангиотензинпревращающего фермента ( фозиноприл, 20-30мг/сут ) , варфарин (чтобы соотношение между 1,5 и 3) , антиоксиданты ( витамин Е, 900мг/сут ; Витамин С, 1г/сут; глутатион 600 мг в течение 10 дней в месяц; убихинон 50мг/день ) , фуросемид ( 25-50мг/сут ) , дефлазакорт ( 15мг/сут). У одного пациента в группе плацебо и один в группе лечения принимали дигоксин 0.2мг/сут и амиодарон, 600мг/нед. Стандартная терапия для МДД включала : дефлазакорт 0.5мг/кг/сут ; фозиноприл 10мг/сут, и антиоксиданты (витамин Е, 600-900мг/сут ; глутатион 300-600мг/сут в течение 10 дней в месяц; убихинон, 50 мг / сутки).
2.2 Лабораторные исследования.
До начала исследования все испытуемые прошли следующие фармакологические тесты для оценки ГР : (1) ГР - высвобождающего гормона ( ГРВГ ) и (2) тест на толерантность к аргинину (ДТО ) , как ранее описано. Кроме того, анализы креатинкиназы, ИФР-1, гормона щитовидной железы, тестостерона, и инсулина в крови были измерены в исходном состоянии и после фазы лечения с использованием коммерческих тест систем. Нормальный ИФР-I варьируются в нашей лаборатории для возраста и пола соответствием и составило 215- 290мg / л у взрослых и 245- 365мg / л у детей препубертатного возраста. Тестостерон и инсулин анализировали РИА методом с использованием коммерческого набора (DSL, диагностической системы лаборатории, Inc) Оценка плазменного уровня ТТГ была выполнена сверхчувствительным иммунорадиометрическим анализом ( Bouty, Милан, Италия) с пределом обнаружения 0.05mU / л. Сывороточный T4 и T3 измерялся с использованием липофазных наборов ( Bouty, Милан, Италия). Плазменные уровни МНП были измерены имеющимся в продаже конкретными иммунорадиометрическими наборами для анализа для человеческого МНП. Плазменный интерлейкин-6 ( ИЛ-6) и фактора некроза опухоли - б (ФНО - б ) определяли энзимиммуным анализом с использованием коммерческих наборов ( MedgenixDiagnostics SA) , с детекцией в пределах 2 и 3 нг / л соответственно.
2.3 Кардиологическое обследование.
Было проведено ЭКГ больных кардиомиопатией, включая индекс (QT : PQ соотношении, нормальные значения 2.2 - 4.6s ), который был оценен как ранее описано. Суточный ЭКГ мониторинг проводится для выявления нарушений ритма. Сложность желудочковой экстрасистолии оценивалась по классификации Lown. Полная эхокардиография в M - режиме, двумерная (2D) , и доплеровский анализ проводили по стандартизации Американского общества эхокардиографии, как ранее описано. LV volumeswere рассчитывается в соответствии сбиплана области длин методом.
2.4 Оценка функции скелетных мышц.
Параметры оценки: (1 ) функциональное тестирование - тесты включали измерения времени, необходимого для вставания из положения лежа в положение стоя, подняться на четыре стандартных ступеньки лестниц, и хотьба на 10м так далеко, как возможно, и (2 ) динамические индексы, которые были оценены как ранее описано.
2.5 Легочная функция.
Оценка включала измерение скорости выдоха, максимальной произвольной вентиляции и максимального выдоха.
2.6 Статистический анализ.
Все значения представлены как среднее ± SE. Статистический анализ проводили с использованием пакета STATISTICA. Различия между группами сравнения эхокардиографическими индексами были выполнены с использованием двусторонней ANOVA с повторными измерениями одного фактора ( времени). Однофакторный дисперсионный анализ был использован для других сравнений. В случае необходимости, сравнения для определения значимости изменений в пределах одной группы с течением времени и между группами в каждый момент времени проводили тестом Неймана - Кеулса. Линейный регрессионный анализ был использован соответствующим образом. Из-за небольшого размера выборки группы Дюшенна ( трех пациентов в группе лечения и группе плацебо), у нас не выполняют анализ ANOVA. Использование соответствующих непараметрических тестов дали сходные уровни значимости.
3 Результаты
3.1 Лабораторные исследования
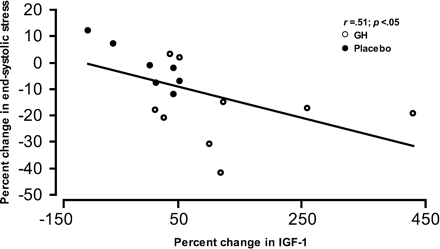
Базисные значения антропометрических и гормональных показателей были сопоставимы в группах плацебо и группе лечения. Там не было никаких существенных изменений оцениваемых параметров ( табл. 1). Семь из 16 пациентов показали низкий уровень циркулирующего ИФР-1 и отсутствие ответа на тесты с стимуляцией ГР (таблицы 1 и 2). Плазменные уровни ИФР-1 увеличились на 82% , по сравнению с исходным, в группе активного лечения, в то время как снизились на 9% в группе плацебо (табл. 2). Уровни гормонов щитовидной железы существенно не изменились в период лечения. Плазменные уровни МНП, которые были повышены по сравнению с нормальными значениями, сократились на 40 % в группе активного лечения, в то время никаких существенных изменений не было обнаружено в группе плацебо (табл. 2) . ИЛ-6 и ФНО - б были значительно увеличены по сравнению с контрольной группой, в то время никаких различий не наблюдалось в период лечения (табл. 2) . МНП и уровни цитокинов в плазме были сходны в популяции Дюшенна и Беккера в течение периода лечения (данные не показаны).
3,2 Кардиологическое обследование.
![]()
Никаких существенных изменений в кардиомиопатическом индексе не было (который был ненормальным у пяти пациентов с МДБ и трех С МДД) в обеих группах пациентов в течение всего периода исследования. Все пациенты, кроме одного, имели менее 100 предсердных экстрасистол за 24 часа; у одного пациента (из группы лечения) количество предсердных экстрасистол снизилось на 45% за 24 часа. У пациентов с МДБ класс Лауна составил от 0 до 5. В группе терапии наблюдалось снижение Лаун класса 4А - 1A у одного пациента, а у других пяти класс остается неизменным. В группе плацебо у одного пациента было уменьшение Лаун класса от 4В до 4А, в то время как у трех других он оставался неизменным. Все пациенты с Дюшенна имели Лаун класса 0 до 1, который остался в том же классе в течение всего периода лечения. Как и ожидалось, объем ЛЖ, как правило, выше и фракция выброса ниже у пациентов с МДБ, по сравнению с МДД, что отражает более обычное явление дилатационной кардиомиопатии. Беккер (см. таблицу 3). В группе пациентов МДБ, получавших лечение, масса левого желудочка увеличилась примерно на 42 г, в то время несколько снизилась в группе плацебо. Это гипертрофический ответ объясняется тенденцией к увеличению толщины задней и передней стенки левого желудочка в группе активного лечения. Был концентрическое ремоделирование полости ЛЖ, со значительным увеличением относительной толщины стенки в группе лечения на 12% , в то время никаких изменений не наблюдалось в группе плацебо. Концентрический рост, без сопутствующих изменений системного артериального давления, привел к значительному падению конечного систолического стресса на 13%. Конечный диастолический объем существенно не изменился после лечения ГР, в то время была тенденция к снижению конечного систолического объема в группе активного лечения (138 ± 15 против 113 ± 15 мл, ) с 6 %-ным увеличением фракции выброса ЛЖ. В группе плацебо фракция выброса не показала каких-либо изменений в течение периода лечения. Было небольшое увеличение ударного объема и сердечного выброса после терапии. Частота сердечных сокращений не показала существенных изменений. Все системное сопротивление снизилось на 18% в группе пациентов, получавших лечение, в связи с увеличением сердечного выброса и неизменным системным артериальным давлением. Результаты из группы пациентов с Дюшенна зеркально отражают тех из группы Беккера.
Характер диастолического наполнения не изменился среди четырех групп исследования в период лечения, несмотря на гипертрофический ответ после лечения больных.
Не все пациенты были в состоянии выполнить функциональные тесты. Никаких существенных различий не наблюдалось во временных функциональных тестов в течение всего периода наблюдения (табл. 3).
3.4 Тесты легочной функции.
Никаких изменений не наблюдалось среди четырех групп исследования в период лечения.
4 Обсуждение
Данное исследование обеспечивает первое доказательство, что ГР активирует миокардиальный рост при МДБ и МДД. Такой гипертрофический ответ был связан со значительным сокращением концентрического напряжения стенки, тенденцией к усиленной систолической функции, и никаких изменений в диастолическом наполнении и функции скелетных мышц. Системное сосудистое сопротивление несколько снизилося. Такие структурные и гемодинамические изменения были связаны со значительным сокращением уровня МНП плазмы. Эти сердечно-сосудистые эффекты очень напоминают наблюдаемые после лечения ГР у пациентов с кардиомиопатией. У пациентов, получавших ГР нет значительного улучшения дееспособности по оценке функциональных индексов. Так, в дополнение к сердечно-сосудистому состоянию, дыхательная мускулатура и функции скелетных мышц - также основные детерминанты физической нагрузки, могут отражать неспособность ГР действовать на эти ткани-мишени. Это может объясняться тем, что более продвинутые повреждения скелетных мышц по сравнению с сердечной мышцей обычно находятся на гистологическом уровне при мышечной дистрофии. С другой стороны, короткая продолжительность лечения,
![]()
возможно, исключает эффект гормона роста. Это последнее предположение опирается на предыдущие исследования у ГР - дефицитных пациентов, получавших терапию ГР, у которых 6 - месячный период, как правило, минимальное время - используемое в большинстве клинических испытаний, чтобы наблюдать изменения в функции сердечной и скелетных мышц. При недостаточности ГР сердечно-сосудистая система, как правило, восстанавливается раньше, чем функции скелетных мышц, клинические показатели, которые показывают начальную модификацию после 1 года терапии. В связи с этим, большинство наших пациентов отображали аномалии ГР/ИФР-1 оси аналогичные наблюдаемым при дефиците ГР. Может ли реактивация сердечного роста в условиях мышечной дистрофии улучшить выживаемость, остается вопросом для последующих более длительных исследований. С одной стороны, такой гипертрофический ответ можно рассматривать как компонент ремоделирования ЛЖ, так и гипертрофии ЛЖ связаной с увеличением кардиоваскулярной смертности. С другой стороны, экспериментальные данные подтверждают мнение, что, в противоречии с патологической гипертрофией, ГР - индуцированный сердечный рост показывает уникальные особенности, такие как сохранение плотности капилляров и диастолическую функцию, и систолическую производительность. Неизменное диастолическое наполнение у пациентов, получавших ГР, несмотря на увеличение массы левого желудочка, согласуется с этой концепцией. Значительное снижение уровня МНП плазмы ( -40 %) свидетельствует в пользу гипотезы, что ГР - индуцированных структурных и функциональных изменений в Х-хромосомой мышечные дистрофии может быть действительно полезным. МНП является желудочковым гормоном, циркулирующие уровни которого непосредственно связаны с конечным диастолическим давлением левого желудочка, степенью повреждения левого желудочка и его массой. Поэтому новые открытия, связанные с повышенным базовых циркулирующих уровней МНП стационарных больных с Х-связанной мышечной дистрофии, как здесь сообщается, поддерживают известное ухудшение структуры левого желудочка и механики этой популяции пациентов, и, возможно, его неблагоприятным прогнозом, несмотря на оптимальное лечение. С другой стороны, снижение МНП после терапии ГР может отражать улучшенный гемодинамический профиль и, возможно, лучший результат в группе активного лечения, и, как представляется особенно актуальна, поскольку это происходит в условиях повышенной массы левого желудочка индуцированного ГР. Пациенты с Х-хромосомой мышечной дистрофией продемонстрировали повышенные плазменные уровни цитокинов, которые существенно не изменились после 3 месяцев лечения ГР. Такая модель хронического воспаления обычно наблюдается при хронической сердечной недостаточности и, вероятно, причинно связаны с его патогенезом и прогрессированием, а также мышечной дисфункцией у пациентов с МДД. Кроме того, поскольку экспериментальной воспаление также ингибирует сигнализацию ГР, возможно, что высокие циркулирующие уровни ИЛ-6 и ФНО - б может вносить вклад в наблюдаемое ухудшение оси ГР/ИФР-1 ( см. ниже ) . В противоречие с МНП, отсутствие ИЛ-6 и ФНО - б измененные после 3 - месячного лечения ГР, либо предлагает терапию ГР для изменения цитокинов в этом клиническом исследовании или иной более длительный период лечения не потребуется. Эти данные сравнимы с предыдущим отчетом, показывающим, что изменения воспалительных цитокинов обычно происходят только после, по крайней мере, 6 месяцев терапии. Сорок четыре процента наших пациентов отображают аномалии оси ГР/ИФР-1, подобно тем, которые наблюдались при дефиците ГР, то есть низком уровне ИФР-1, и измененный ответ на тесты стимулирующим ГР. Возможные объяснения этого вывода включают в себя косвенные механизмы, такие как отсутствие физической активности или сопутствующее лечение кортикостероидами или, альтернативно, оно может отражать первичное неизвестное расстройство секреции ГР. Предыдущие исследования по изучению роли ГР/ИФР-1 оси у пациентов с мышечной дистрофией. Противоречивые результаты были получены. Наблюдение развивается медленнее, миодистрофия Дюшенна у пациентов с карликовостью приводит к гипотезе, что низкая активность ГР/ИФР-1 оси, может оказаться полезной при мышечной дистрофии. Две линии доказательств оспорили эту гипотезу. Во-первых, частое нахождение нарушений секреции гормона роста, особенно у пациентов с МДД, не было связано с более мягкой формой заболевания, в соответствии с нашими данными. Во-вторых, клинические испытания с ингибитором ГР мазинодололом, не смогли показать благоприятный эффект снижения секреции ГР от клинического статуса и естественной истории МДД. Очевидное ограничение текущего предварительного исследования имеет ограниченый размер выборки, что затрудняет определенные выводы, связанные с эффективностью ГР при МДД и МДБ. Тем не менее, более крупные и / или долгосрочные испытания, чтобы подтвердить и расширить наши выводы, может указывать на сильные биологические сердечно-сосудистые эффекты ГР. 3- месячная терапия при МДД и МДБ не вызывало клинически значимых побочных эффектов. Безопасность терапии ГР подтверждена также в отсутствии нарушений сердечного ритма при холтеровском мониторировании, и в стабильности всех гематологических показателей.
Ссылки.
↵ PerloffKJ. Neurological disorders and heart disease. Braunwald E. Heart disease. 5th ed. Philadelphia: WB
![]()
Saunders; 1997. p. 1865–1886.
↵ NigroG, Comi LI, Politano L. The incidence and evolution of cardiomyopathy in Duchenne muscular dystrophy. Int J Cardiol. 1990;26:271–277. CrossRef
Medline
Web of Science
↵ NigroG, Comi LI, Politano L et al. Evaluation of the cardiomyopathy in Becker muscular dystrophy. Muscle Nerve. 1995;18:283–291. CrossRef
Medline
Web of Science
↵ SaccаL, Cittadini A, Fazio S. Growth hormone and the heart. Endocr Rev. 1994;15:555–573. Abstract/FREE Full Text
↵ CittadiniA, Stroemer H, Katz SE et al. Differential cardiac effects of growth hormone and insulin-like growth factor-1 in the rat: a combined in vivo and in vitro evaluation. Circulation. 1996;93:800–809. Abstract/FREE Full Text
CittadiniA, Grossmann JD, Napoli R et al. Growth hormone attenuates early left ventricular remodeling and improves cardiac function in rats with large myocardial infarction. J Am Coll Cardiol. 1997;29:1109–1116. Abstract
SamarelAM. IGF-1 overexpression rescues the failing heart. Circ Res. 2002;90:631–633. FREE Full Text
↵ FazioS, Sabatini D, Capaldo B et al. A preliminary studyof growth hormone in the treatment of dilated cardiomyopathy. N Engl J Med. 1996;334:809–814. CrossRef
Medline
Web of Science
OsterzielKJ, Strohm O, Schuler J et al. Randomised, double-blind, placebo-controlled trial of human recombinant growth hormone in patients with chronic heart failure due to dilated cardiomyopathy. Lancet. 1998;351:1233–1237. CrossRef
Medline
Web of Science
IsgaardJ, Bergh CH, Caidahl K et al. A placebo-controlled study of growth hormone in patients with congestive heart failure. Eur Heart J. 1998;19:1704–1711. Abstract/FREE Full Text
↵ RifaiZ, Welle S, Moxley RT III et al. Effect of prednisone on protein metabolism in Duchenne dystrophy. Am J Physiol. 1995;268:E67–E74.
↵ TakeshiU, Ohkusa T, Yano M et al. Growth hormone preserves cardiac sarcoplasmic reticulum Ca2+release channels (ryanodine receptors) and enhances cardiac function in cardiomyopathic hamsters. Cardiovasc Res. 1998;40:64–73. Abstract/FREE Full Text
↵ RyokeT, Gu Y, Mao L et al. Progressive cardiac dysfunction and fibrosis in the cardiomyopathic hamster and effectsof growth hormone and angiotensin-converting enzyme inhibition. Circulation. 1999;100:1734–1743. Abstract/FREE Full Text
↵ MaedaK, Tsutamoto T, Wada A et al. High levels of plasma brain natriuretic peptide and interleukin-6 after optimized treatment for heart failure are independent risks factors for moribidity and mortality in patients with congestive heart failure. J Am Coll Cardiol. 2000;36:1587–1593. Abstract/FREE Full Text
![]()
↵ PolitanoL, Nigro V, Petretta VR et al. Development of cardiomyopathy in female carriers of Duchenne and Becker muscular dystrophies. JAMA. 1996;275:1335–1338. Abstract/FREE Full Text
↵ GhigoE, Bellone J, Aimaretti G et al. Reliability of provocative tests to assess growth hormone secretory status. Study in 472 normally growing children. J Clin Endocrinol Metab. 1996;81:3323–3327. Abstract
↵ MerolaB, Cittadini A, Colao A et al. Cardiac structuraland functional abnormalities in GH-deficient adults. J Clin Endocrinol Metab. 1993;77:1658–1661. Abstract
↵ LownB, Wolf M. Approaches to sudden death from coronary heart disease. Circulation. 1971;44:130–142. Abstract/FREE Full Text
↵ SahnDJ, DeMaria A, Kisslo J et al. The Committee on M-mode standardization of the American Society of Echocardiography: recommendations regarding quantitation in M-mode echocardiography: results of a survey of echocardiographic measurements. Circulation. 1978;58:1072–1083. Abstract/FREE Full Text
↵ JohannssonG, Grimby G, Sunnerhagen KS et al. Two years of growth hormone (GH) treatment increase isometric and isokinetic muscle strength in GH-deficient adults. J Clin Endocrinol Metab. 1997;82:2877–2884. Abstract/FREE Full Text
↵ MannDL. Mechanisms and models in heart failure. Acombinatorial approach. Circulation. 1999;100:999–1008. FREE Full Text
↵ SaitoK, Kobayashi D, Komatsu M et al. A sensitive assay of tumor necrosis factor б in sera from Duchenne muscular dystrophy patients. Clin Chem. 2000;46:1703–1704. FREE Full Text
↵ BergadPL, Schwarzenberg SJ, Humbert JT et al. Inhibition of growth hormone action in models of inflammation. Am J Physiol Cell Physiol. 2000;279:C1906–C1917. Abstract/FREE Full Text
↵ SesmiloG, Biller BM, Llevadot J et al. Effects of growth hormone administration on inflammatory and other cardiovascular risk markers in men with growth hormone deficiency. Ann Intern Med. 2001;133:111–122.
↵ ZatzM, Betti RT, Levy JA. Benign, Duchenne muscular dystrophy in a patient with growth hormone deficiency. Am J Med Genet. 1981;10:301–304. CrossRef
Medline
Web of Science
↵ MerliniL, Granata C, Ballestrazzi A et al. Growth hormone evaluation in Duchenne muscular dystrophy. Ital J Neurol Sci. 1988;9:471–475. CrossRef
Medline
Web of Science
↵ CollippPJ, Kelemen J, Chen SY et al. Growth hormone inhibition causes increased selenium levels in Duchenne muscular dystrophy: a possible new approach to therapy. J Med Genet. 1984;21:254–256.
Оригинальный текст статьи: http://eurheartj. oxfordjournals. org/content/24/7/664.long
Переведено проектом МОЙМИО: www.mymio.org
![]()



