Лабораторное занятие 10
Тема: «Работа гальванического элемента. Расчет ЭДС гальванического элемента. Формула Нернста»
Цель занятия: формирование понятий о электродном потенциале, гальваническом элементе.
Методические рекомендации по проведению работы и обработке экспериментальных данных:
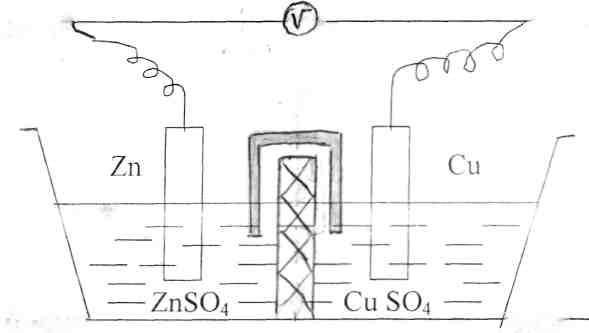
Устройство для непосредственного преобразования энергии химической реакции в электрическую энергию называется гальваническим элементом. Рассмотрим работу медно-цинкового гальванического элемента. Элемент составлен из цинковой пластины, погруженной в раствор сульфата цинка и медной пластины; погруженной в раствор сульфата меди. Оба раствора соприкасаются друг с другом.
Рис. I Схема медно-цинкового гальванического элемента
Они разделены перегородкой из пористого материала, пропускающего сульфат-ионы. При работе гальванического элемента протекает суммарная реакция: Zn + CuSO4 = ZnS04 + Сu
Здесь процессы окисления и восстановления разделены в пространстве, и чтобы осуществить процесс восстановления ионов меди, электроны от окислителя переходят по проводнику, т. е. создают ток по внешней цепи. Цинковый электрод источник электронов, поступающих во внешнюю цепь, принято называть отрицательным (анод), а медный электрод - положительным (катод). Уравнения электродных процессов, протекающих при работе гальванического элемента:
анодный процесс, окисление: Zn - 2ё = Zn
катодный процесс, восстановление: Сu+2 + 2ё = Сu°
Гальванический элемент можно записать в виде краткой электрохимической схемы:
А(-) Zn/ ZnS04// CuSO4, /Cu (+) К
А (-) Zn / Zn+2 // Сu+2 / Сu ° (+) К
где одна черта означает границу между электродами и раствором, две черты - границу между растворами, в скобках знаки электродов, причем анод записывается слева, катод - справа. Необходимое условие работы гальванического элемента - разность потенциалов его электродов. Электрод с меньшим потенциалом является анодом. Электродвижущая сила гальванического элемента (Э. Д.С.) - величина положительная и определяется как разность потенциалов катода и анода.
Э. Д.С = ЕК-Еа
1. ЗНАЧЕНИЕ ТЕМЫ. Действие гальванического элемента основано на протекании в нем окислительно - восстановительной реакции, в которой пространственно разделены процессы окисления и восстановления, а электроны от окислителя к восстановителю направлены по металлическому проводнику. Осуществление этого процессаnна практике позволяет промышленности получить самые различные виды электрических батареек, аккумуляторов и других источников постоянного электрического тока.
2. ЦЕЛЬ РАБОТЫ: Научиться работать с гальваническим элементом, писать
уравнения электродных процессов, иметь понятие об ЭДС элемента.
ХОД РАБОТЫ:
Опыт 1. Составление гальванических элементов.
Один из микростаканчиков заполнить IM раствором сульфата цинка, другой - IM раствором сульфата меди. Соединить стаканчики электролитным мостиком, заполненным насыщенным раствором хлорида калия в смеси с агар-агаром. Опустить в раствор сульфата цинка узкую цинковую пластинку, а в раствор сульфата меди - медную. Соединить электрическим проводом опущенные пластинки с гальванометром или другим регистрирующим прибором. Наблюдать отклонение стрелки гальванометра, указывающее на возникновение электрического тока.
Опыт 2. Составление концентрационного гальванического элемента. Наполнить микростаканчики раствором сульфата цинка разной концентрации: первый стаканчик - 1 M ZnS04, второй - 0,01 M ZnS04. Соединить стаканчики электролитным мостиком. Опустить в каждый стаканчик цинковые полоски и соединить их проводом с гальванометром. Отклоняется ли стрелка гальванометра? Написать уравнения химических реакций, протекающих на электродах гальванических элементов, и суммарное уравнение химической реакции в результате которой возникает электрический ток в данном элементе. В каком направлении перемещаются электроны во внешней цепи? Выписать из приложения к лабораторному практикуму числовые значения стандартных электродных потенциалов меди и цинка и вычислить ЭДС медно - цинкового элемента. Какие ионы и в каком направлении перемещаются в растворе? Вычислить стат. ЭДС серебр. концентрационного гальванического элемента. Представить преподавателю отчет письменный на утверждение о проделанной работе.
Вопросы для самопроверки:
1. Напишите молекулярные и ионные уравнения возможных реакций вытеснения металлов из их солей другими металлами и укажите стрелками переход электронов:
а) Zn(NO3)2 + Pb
б) AlCl3 + Mg
в) AgNO3 + Cu
2. Химически чистый цинк почти не реагирует с соляной кислотой. При добавлении к этим веществам соли никеля происходит энергичное выделение водорода. Объясните эти явления.
3. Вычислить э. д.с. медно-кадмиевого гальванического элемента, в котором концентрация ионов Сd2+ составляет 0,8 моль / л, а ионов Сu2+ - 0,01моль / л.
4. Гальванический элемент
( - ) 2 Сr / 2Crl3+ | Н2SО4 | (Pb) 3 Н2 / 6H+ (+)
образовавшийся при коррозии хрома, спаянного со свинцом, даёт ток силой 6 А. Какая масса хрома окислится и сколько литров водорода выделится за 55 с работы этого элемента?
Ответ: (0,04 л; 0,06 г)
5. Вычислите массу металла, окисляющегося при коррозии при нарушении целостности поверхностного слоя медного покрытия на алюминии, если за 45 с работы этой гальванопары нп катоде выделилось 0.09 л водорода (н. у.). Какую силу тока даёт эта гальванопара?
6. Составьте схему коррозионного гальванического элемента, образованного железом в контакте с медью: а) в кислой среде; б) во влажной среде. Напишите уравнение реакций, протекающих на анодном и катодном участках элемента.
Лабораторное занятие 11
Тема: «Электролиз»
Цель занятия: приобретение навыков практического осуществления процессов электролиза и составления схем различных их типов.
Методические рекомендации по проведению работы и обработке экспериментальных данных:
Опыт 1. Электролиз раствора йодида калия.
Электролизер заполните раствором йодида калия, опустите в раствор графитовые электроды и подключите их к источнику постоянного тока. Время проведения 3 минуты. При этом происходит выделение газообразного водорода на катоде и образование свободного йода на аноде, который опускается на дно электролизера тяжелыми струями бурого цвета.
Добавьте в раствор несколько капель фенолфталеина в область прикатодного пространства. По окончании опыта анод промойте раствором тиосульфата натрия Na2S2O3 для удаление йода, а затем дистиллированной водой.
В отчёте: составьте схему электролиза и опишите наблюдаемые явления;
объясните, почему окрасился раствор в области катодного пространства
при добавлении фенолфталеина.
Опыт 2. Электролиз раствора сульфата меди.
Налейте в электролизер раствор сульфата меди (II), опустите в него графитовые электроды и пропустите через раствор электрический ток. Через 5 – 10 минут прекратите электролиз и отметьте на катоде красный налет меди. Выключите ток и поменяйте местами электроды. Снова пропустите электрический ток. Что происходит с красным налетом меди?
В отчёте: объясните наблюдаемые изменения с красным налётом меди;
составьте уравнения реакций, происходящих на катоде и аноде, в первом и втором случае. Приведите значения стандартных потенциалов электродных реакций и вычислите теоретическое напряжение разложения электролита, подвергшегося электролизу.
Опыт 3. Электролиз раствора хлорида цинка.
Электролизер заполните раствором хлорида цинка, опустите в него графитовые электроды, подключите их к источнику постоянного тока и проведите электролиз в течение 3-5 минут.
По окончании опыта выньте катод и установите наличие цинкового покрытия на его поверхности. Присутствие хлора в анодной зоне определите по появлению синего окрашивания при добавлении 2-3 капель раствора йодида калия и одной капли раствора крахмала.
По окончании опыта выньте катод обработайте соляной кислотой (осторожно!) для снятия пленки цинка. Электроды и электролизер тщательно промойте водой, предварительно обработав анод раствором Na2S2O3.
В отчёте: составьте схему электролиза раствора хлорида цинка. Приведите значения стандартных потенциалов электродных реакций и вычислите теоретическое напряжение разложения электролита, подвергшегося электролизу.
Опыт 4. Электролиз раствора Na2SO4
В U – образный сосуд (или стеклянный сосуд) Залейте раствор сульфата натрия, прибавьте в оба колена сосуда по 3-4 капли раствора лакмуса. Опустите в оба колена графитовые электроды и пропустите через раствор на катодном и анодном участках?
В отчёте: укажите, какие газы выделяются на электродах; составьте схему электролиза раствора сульфата натрия.
Опыт 5. Электролиз раствора хлорида олова (II).
Электролизер заполните раствором хлорида олова (II), опустите в него графитовые электроды, подключите их к источнику постоянного тока и проводите электролиз в течение 3-5 минут. Наблюдайте на катоде появление блестящих кристалликов металлического олова. Окисление или восстановление олова происходит на катоде? Напишите уравнение катодного
процесса. Докажите образование свободного хлора на аноде, для чего выньте анод из электролиза, прибавьте в анодное пространство в анодное пространство по 3-4 капли растворов йодида калия и крахмала и наблюдайте появление синего окрашивания.
В отчёте: составьте схему электролиза раствора хлорида олова (II). Приведите значения стандартных потенциалов электродных реакций и вычислите теоретическое напряжение разложения электролита, подвергшегося электролизу.
Вопросы для самопроверки:
1. Что называется электролизом?
2. В чем сущность электролиза?
3. Какова последовательность электродных процессов на катоде электролизера?
4. Какова последовательность электродных процессов на аноде электролизера?
5. В чем суть электрического рафинирования металлов?
6. какие закономерности определяют процесс электролиза?
7. Какие продукты образуются при электролизе на инертных электродах водных растворов: а) AgNO3 б) KBr в) Na2SO4?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 |



