Лабораторная работа 7
Титриметрия. Титрование с одним индикатором. Определение массовой доли ![]() методом титрования НСl
методом титрования НСl
Цель: Определить массовую долю (%)![]() в техническом карбонате натрия.
в техническом карбонате натрия.
Реактивы:
- 0,1 н. НСl (из фиксанала)
IIocvдa:
- Бюретка (25мл) Конические плоскодонные колбы (100 мл) - 3 шт Градуированная пипетка (10 мл) Мерная колба (250 мл) Воронка стеклянная (45 мм) Чашка Петри Устройство для заполнения пипеток Фильтровальная бумага Штатив Шпатель
Выполнение работы:
1. Взять навеску 1-1,2 г технического карбоната натрия на аналитических весах.
2. При помощи воронки перенести навеску в мерную колбу на 250 мл, растворить в небольшом количестве дистиллированной воды, перемешать.
3. Довести до метки в колбе дистиллированной водой, перемешать.
4. В 3 конические колбы на 100 мл градуированной пипеткой внести аликвоты (10 мл) приготовленного раствора. В каждую колбу добавить по 3 капли индикатора - метилоранжа. Растворы должны иметь желтую окраску.
5. Закрепить вертикально бюретку, предварительно промыв ее 0,1 н. НСl.
б. Заполнить бюретку 0,1н. НСl.
7. Титровать раствор карбоната натрия 0,1 н. НСl (на белом фоне) до изменения окраски с желтой на розовую.
NB! Вблизи точки эквивалентности рабочий раствор добавлять медленно, по каплям, тщательно перемешивая.
Протокол работы:
Масса навески соды, г Объем 0,1н. НСl, пошедший на титрование, мл:1 колба -
2 колба -
3 колба -
Среднее значение VНСl =
Расчеты:
Массовая доля (%)![]() в образце (щ):
в образце (щ):
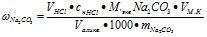 100
100
Мэкв![]() =(fэкв
=(fэкв ![]() )∙M
)∙M![]() = Ѕ ∙ 105,99 = 53 г/моль
= Ѕ ∙ 105,99 = 53 г/моль
Vм. к – объем мерной колбы, мл
Vаликв. – объем аликвоты раствора для анализа, мл
Сн HCl – молярная концентрация эквивалента НСl, моль/л
m![]() - масса аналитической пробы, г
- масса аналитической пробы, г
Домашние задания.
1.На титрование 0,3240 г технической соды с индикатором метиловым оранжевым пошло 32,54 см3 0,1н. НСl (К НСl = 0,9950). Определить массовую долю ![]() в образце.
в образце.
Ответ: 52,86%
2. Для приготовления 500 мл раствора было взято 20,00 мл хлороводородной кислоты (с = 1,19 г/см3). Вычислить молярную концентрацию полученного раствора.
Ответ: 0,5000 моль/л
3. Какая масса гидроксида натрия, содержащего 2% индифферентных примесей, необходима для приготовления 200 мл 0,1М раствора. Ответ: 0,8163 г
4. Вычислить молярную концентрацию раствора NaOH, Т(NaOH) и Т(NaOH / НСl), если на титрование 20,00 мл его израсходовали 19,20 мл 0,1000 М НСl, приготовленной из фиксанала.
Ответ: 0,09600 моль/л
5. Какой объем раствора карбоната натрия с массовой долей 15% (с = 1,16г/см3) потребуется для приготовления 120 мл 0,45М раствора ![]() . Ответ: 32,9 мл
. Ответ: 32,9 мл
6. В 500 мл раствора содержится 2,6578 г ![]() . Вычислить Т(
. Вычислить Т(![]() ), Т(
), Т(![]() /НСl) и молярную концентрацию эквивалента
/НСl) и молярную концентрацию эквивалента ![]() при нейтрализации этого раствора: 1) до СО2; 2) до NaHCO3.
при нейтрализации этого раствора: 1) до СО2; 2) до NaHCO3.
Ответ: Т(![]() ) = 0,0053164; 1) 0,1003 н., fэкв = Ѕ, Т(
) = 0,0053164; 1) 0,1003 н., fэкв = Ѕ, Т(![]() /НСl) = 0,003658; 2) 0,05016 моль/л; Т(
/НСl) = 0,003658; 2) 0,05016 моль/л; Т(![]() /НСl) = 0,001829
/НСl) = 0,001829



