УДК 547.836.3+547.551.1+544.362.2
Потенциометрическое определение рКа азотистых органических оснований в среде ацетонитрила
Быков1*+ Ярослав Валерьянович, Якимова1 Ирина Дмитриевна,
Яганова1 Надежда Николаевна
1 Кафедра общей химии. Пермский государственный аграрно-технологический университет
им.
ул. Петропавловская 23. г. Пермь. 614000. Пермский край. Россия.
Тел. (3422) 17-92-25. E-mail: *****@***ru
Ключевые слова: бензохинолины, 4-(7-циклогепта-1,3,5-триенил)анилин, пиридин, константы кислотности, потенциометрическое титрование, ацетонитрил.
Аннотация
Методом потенциометрического титрования с комбинированным стеклянным электродом впервые определены величины показателя константы кислотности бензохинолинов и 4-тропилированного анилина в среде безводного ацетонитрила. Построены ряды основности изучаемых соединений. Оценена возможность использования стандартной методики определения показателя кислотности азотистых органических соединений в неводных средах при замене внутреннего электролита стеклянного комбинированного электрода. Оценка точности метода измерений проводилась сравнением литературного и экспериментального значений показателя константы кислотности стандартного соединения - пиридина в одном и том же растворителе.
Введение
Величины рКа имеют важное значение при изучении таутомерии и структуры азотистых оснований, они рассматриваются в теории ароматичности ненасыщенных азотистых гетероциклов и в вопросах связи строения с терапевтической активностью [1]. Показатель кислотности рКа или родственный показатель рКR+ для ряда органических катионов может служить мерой химической устойчивости органических и неорганических соединений. Чем выше значение рКа (рКR+), тем термодинамически более устойчивым является соединение [2].
Для оснований при потенциометрическом титровании сильной кислотой в момент полунейтрализации по уравнению Гендерсона [1, 3]
рН = рКа + lg[органическое основание]/[соль],
рКа = рН.
Величина потенциала полунейтрализации электролита в неводном растворе зависит не только от факторов, определяющих величину константы диссоциации электролита, но и от факторов, которые определяют форму кривой титрования в буферной области. Поэтому, потенциал полунейтрализации по сравнению с константой диссоциации имеет ряд преимуществ при выборе условий потенциометрического титрования [4]. В работе [5] представлена схема нейтрализации слабого основания сильной кислотой в неводном растворителе и расчёт рК:
![]()
где, ![]()
![]() - потенциал полунейтрализации;
- потенциал полунейтрализации;
рКст – константа кислотности стандартного вещества.
При выборе растворителя для кислотно-основного титрования следует учитывать много факторов. Ацетонитрил CН3СN (AN) относят к апротонным диполярным растворителям. Такие вещества не содержат в своём составе лабильных атомов водорода, слабо проявляют склонность к образованию водородных связей, но вступают в побочные реакции гомо - и гетероконьюгации за счёт водородных связей коньюгирующих веществ [5]. Гомо - и гетеросопряжение в среде ацетонитрила менее свойственно основаниям, чем кислотам, поскольку ацетонитрил обладает большей сольватирующей способностью в отношении катионов, чем анионов. Эти процессы почти не сказываются при концентрации основания 10-3 М. [4].
Ацетонитрил обладает высокими дифференцирующими свойствами (диэлектрическая проницаемость ℰ= 38 при 25 ![]()
![]() [6]), и высоким значением константы автопротолиза рКs.
[6]), и высоким значением константы автопротолиза рКs.
Для определения констант автопротолиза применяют кондуктометрический, потенциометрический, спектрофотометрический методы. Наличие диффузионного потенциала при изменении э. д.с. в цепях с переносом является одной из причин различия рКs одного и того же растворителя у разных авторов (рКs для ацетонитрила 32,2 [5], 33,3 [4, 6, 7], 25,6 [8] 19,5 [9]).
Следует отметить, что численные значения констант автропротолиза зависят от температуры, например корректировку константы автопротолиза воды рКw (шкалы рН) с учётом влияния температуры проводят по уравнению Боуксвита (рКw = 14,17 при 20 ![]()
![]() [10]:
[10]:
рКw = ![]()
![]() ,
,
где Т – температура воды, К.
Из данных по рКа следует, что в ацетонитриле все протонированные амины более слабые кислоты, чем в воде, это объясняется низкой основностью ацетонитрила. Хотя в среднем, ∆рКа оснований в ацетонитриле и воде составляет 7,6 единиц [4] (7,9 [11], 8,13 [12] – сведения разноречивы), существует достаточно сложное количественное соотношение между рКа(СН3CN) и рКа(Н2О). [4].
При потенциометрическом титровании в неводных растворах в качестве индикаторного электрода обычно используют стеклянный электрод, в качестве электрода сравнения – каломельный или хлоридсеребряный. Имеются сведения о нестабильной работе стеклянного электрода в средах с низким содержанием воды [13, 14], поэтому при титровании в неводных средах рекомендуют производить замену водного раствора электролита в электродах [11]. Титрование в неводных средах имеет ряд ограничений, с этим связано много приближений и неточностей при определении величин рН. Целесообразно, при использовании этого инструментального метода, для потверждения достоверности результатов исследования иметь вещества-эталоны, рКа которых точно известны.
Для титрования соединений основного характера в неводных растворах в качестве титрантов широко применяются неводные растворы хлорной кислоты - одной из самых сильных кислот в среде неводных растворителей.
В связи с этим, целью данного исследования является изучение возможности определение рКа азаароматических гетероциклических оснований - бензохинолинов и азотистого основания 4-(7-циклогепта-1,3,5-триенил)анилина, в котором азотный основной компонент не входит в состав циклической системы, потенциометрическим методом с применением комбинированного стеклянного электрода в среде безводного ацетонитрила.
Результаты и их обсуждение
Измерение показателя pKa проводилось методом потенциометрического титрования 0.1н растворов органических оснований в безводном ацетонитриле 0.1н раствором хлорной кислоты в безводной уксусной кислоте [15].
Оценка точности метода измерений проводилась сравнением литературного и экспериментального значений pKa соединения в одном и том же растворителе. Для пиридина в ацетонитриле pKa = 12.33 [16], а экспериментальное значение pKa = 12.6778, что говорит о удовлетворительной точности применяемого метода.
Измеренные нами и неизвестные ранее величины показателя кислотности pKa для двух изомерных форм бензохинолинов и 4-(7-циклогепта-1,3,5-триенил)анилина составляют:
|
2 |
pKa1 = 12.6853 pKa2 = 7.7853 | pKa1 = 11.7403 pKa2 = 10.0653 |
| |
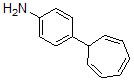
pKa = 10.7299 |
Значения pKa1 бензохинолинов, вероятнее всего, принадлежат нуклеофильному центру диметиламиногруппы и для сравнительной оценки устойчивости ароматического ядра малоинтересны. Показатели pKa2, являющиеся показателем основности гетероароматического ядра бензохинолинов, для двух форм отличаются довольно значительно. 2-Фенил-4-(4-N, N-диметиламинофенил)бензо[g]хинолин 1, обладающий более низким значением pKa2, является менее устойчивым (более реакционноспособным) соединением и представляется продуктом кинетического контроля реакции, тогда как 1-(4-N, N-диметиламинофенил)-3-фенилбензо[f]хинолин 2 с достаточно высоким значением показателя кислотности является более термодинамически стабильным соединением.
Кривая потенциометрического титрования, получаемая используемым методом на примере 2-(4-N, N-диметиламинофенил)-4-фенилбензо[g]хинолина 1, представлена на рисунке 1.
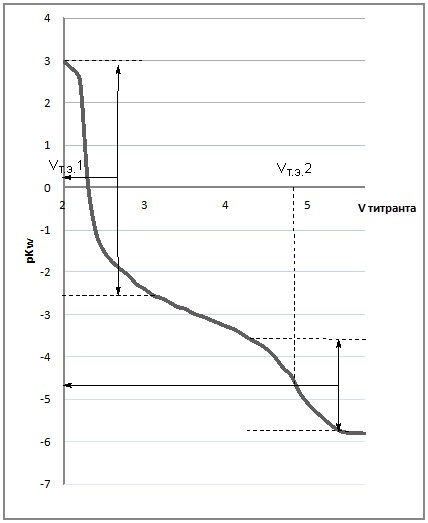
Рис 1. Кривая потенциометрического титрования 2-(4-N, N-диметиламинофенил)-4-фенилбензо[g]хинолина 1 в ацетонитриле по шкале pKw
Численное значение pKa принималось равным pKw (шкала рН) в точке полунейтрализации (pKw при Ѕ Vт. э.) с учетом поправки на шкалу используемого растворителя. Корректировка константы автопротолиза воды pKw (шкалы pH) с учетом влияния температуры производилась по уравнению Боуксвита. Экспериментальные и расчетные данные представлены в таблице 1.
Таблица 1.
Расчет pKa азотистых оснований
Соединение | Т, К | pKw | ЅVт. э. | pH (ЅVт. э.) |
| pKa = pH + ДpKs |
Пиридин (эталон) | 293.05 | 14.1646 | 2.5 | 3.66 | 9.0177 | 12.6778 |
2-(4-N, N-диметиламинофенил)-4-фенилбензо[g] хинолин (1) | 296.45 | 14.0494 | 1.150; 2.450 | 3.55; -1.29 | 9.0753 | 12.6853; 7.7853 |
1-(4-N, N-диметиламинофенил)-3-фенилбензо[f] хинолин (2) | 296.15 | 14.0594 | 1.300; 2.505 | 2.670; 0.995 | 9.0703 | 11.7403; 10.0653 |
4-(7-циклогепта-1,3,5-триенил) анилин (3) | 294.35 | 14.1201 | 0.830 | 1.690 | 9.04 | 10.7299 |
Основность органических соединений находится в прямой зависимости от показателя pKa [2]. На основании этого показателя (табл.1) можно построить два ряда, характеризующее основность гетероароматического ядра и характера аминогруппы.
Ряд основности гетероароматических ядер выглядит следующим образом:
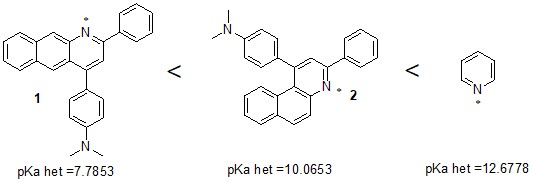
* - реакционный центр молекулы
Наиболее основным и термодинамически устойчивым соединением, ожидаемо, является пиридин. Изомерные формы бензохинолинов 1 и 2 заметно различаются по этому показателю. Так, линейная форма 1 является наименее устойчивой. Это, по-видимому, связано с меньшей симметричностью молекулы.
Основность аминогрупп образует следующий ряд:
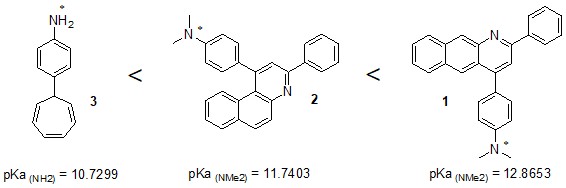
* - реакционный центр молекулы
В полученном ряду первичная аминогруппа соединения 3 является наименее устойчивой в сравнении с остальными соединениями ряда. Основность диметиламиногруппы зависит от структуры связанного с ней гетероароматического ядра. Менее термодинамически устойчивым (основным) соединением в ряду бензохинолинов является соединение 2. Основность третичной аминогруппы по-видимому повышается с уменьшением симметричности молекулы в целом. Таким образом, основность аминогрупп зависит не только от степени ее замещения, а в большей мере от пространственной структуры и характера заместителя.
Проведённое в данной работе изучение возможности применения стеклянного комбинированного электрода для потенциометрического титрования в неводных средах, показало, что при кислотно-основном титровании в среде безводного ацетонитрила наблюдаются выраженные скачки на кривых титрования, что позволяет с определённой точностью определять величины pKa исследуемых органических оснований. Неточности метода, связанные с использованием водных стандартов для настройки прибора, не сильно искажают результаты анализа. Так же, при замене водного раствора электролита в комбинированном электроде на насыщенный раствор хлорида калия в безводной уксусной кислоте, электрод сохраняет свою функцию.
Экспериментальная часть
Температуру плавления определяли на приборе ПТП. ИК спектры записывали на Фурье-спектрометре Bruker IFS 66ps в вазелиновом масле. Спектры ЯМР соединений записаны в CDCl3 на приборе Brucker при 400 MГц (1Н, внутренний стандарт - ТМС) и при 100 МГц (13С, внутренний стандарт – остаточные сигналы растворителя). Для колоночной хроматографии применяли Silicagel 60 (AlfaAesar, 0.063-0.2 мм). Кинетические исследования и контроль чистоты полученных соединений проводили методом хроматомасс-спектрометрии на приборе Agilent Technologies 6890N/5975B, колонка капиллярная НР-5ms, 30000х0.25 мм, температура испари°С, программирование температуры в пределах 20-40 град/мин, газ-носитель – гелий, 1 мл/мин; масс-спектры получены методом электронного удара (70эВ). Элементный анализ выполняли на приборе Leco CHNS 9321P (США).
Определения pKa проводили методом потенциометрического титрования на приборе Анион-4100 с комбинированным электродом ЭСК-10601/7 (внутренний электролит – насыщенный раствор хлорида калия в безводной уксусной кислоте). Потенциометрическое титрование 0.1н растворов органических оснований в безводном ацетонитриле 0.1н производилось раствором хлорной кислоты в безводной уксусной кислоте. Ацетонитрил квалификации ОСЧ, сорт 0, для хроматографии использовали без дополнительной очистки. Контроль чистоты осуществляли по границе пропускания в УФ-спектре (длина волны, при которой D=1, l =1 см) в спектре поглощения – 195 нм (195 нм [26]), показателю преломления 20 D
n =1.3441 (1.34411), плотности d20=0.7829 г/см3 (0.782 г/см3)
Численное значение pKa принималось равным pKw (шкала рН) в точке полунейтрализации (pKw при Ѕ Vт. э.) с учетом поправки на шкалу используемого растворителя. Корректировка константы автопротолиза воды pKw (шкалы pH) с учетом влияния температуры производилась по уравнению Боуксвита.
1,3-Диарилбензо[f]хинолин и 2,4-диарилбензо[g]хинолин [17]. Смесь 0,024 моль 4-(N, N-диметиламино)бензальацетофенона, 0,024 моль 2-нафтиламина 2 и 0,0024 моль гидрохлорида 2-нафтиламина растворяли в 12 мл абсолютированного метанола нагревали а ампуле при 100 0С в течение 8 часов. Полученную после окончания реакции смесь кристаллических продуктов реакции отфильтровывали и элюировали смесью петролейный эфир (40-70°С) – этилацетат с содержанием этилацетата от 0 до 10% (по объему).
4-(N, N-Диметиламинофенил)-2-фенилбензо[g]хинолин (1) Желтый порошок. Т. пл. 220-222°С. ИК спектр (н, см-1, тонкая пленка): 1609, 1579, 1530, 1364, 1196, 836, 802, 754. ЯМР 1Н спектр (300 МГц, СDCl3, д, м. д.): 3.02 с (6Н, NMe2), 6.86 д (2Н, Н3',5', 3J 8.7 Гц), 7.16 дд (1Н, Н8, 3J 7.5 Гц, 3J 7.5 Гц), 7.47-7.55 м (4Н, Н7, Н3'',4'',5''), 7.59-7.60 м (3Н, Н6, Н2',6'), 8.00 д (2Н, Н2'',6'', 3J 7.5 Гц), 8.09 д (1Н, Н9, 3J 8.7 Гц). ЯМР 13С спектр (100 МГц, СDCl3, д, м. д.): 39.77, 111.69, 120.40, 121.23, 124.89, 125.47, 127.22, 127.48, 127.78, 127.87, 127.94, 128.05, 128.62, 129.32, 130.84, 132.09, 142.71, 148.49, 148.78, 150.89, 154.77. Найдено, %: C 85.30; H 5.84; N 7.02. C27H22N2. Вычислено, %: C 86.60; H 5.92; N 7.48.
1-(4-N, N-Диметиламинофенил)-3-фенилбензо[f]хинолин (2). Желто-коричневые призмы из этанола. Т. пл. 171-174°С. ИК спектр (н, см-1, тонкая пленка): 1677, 1607, 1579 1545, 1514, 1480, 1451, 1361, 1115, 836, 755, 696. ЯМР 1Н спектр (300 МГц, СDCl3, д, м. д.): 2.99 с (6Н, NMe2), 6.88 д (2Н, Н3',5', J 8.4 Гц), 7.24 дд (1H, Н4'', J 7.5 Гц, J 7.5 Гц), 7.32 д (2Наром., J 8.4 Гц), 7.51-7.59 м (4Наром.), 7.90 д (1Наром., J 7.8 Гц), 7.91 с (1Н, Н2), 8.00 д (1Н, H7, 3J 7.2 Гц), 8.02 д (1Н, H5, 3J 9.0 Гц), 8.12 д (1Н, H6, 3J 9.0 Гц), 8.32 д (2Н, Н2'',6'', 3J 7.5 Гц). ЯМР 13С спектр (100 МГц, СDCl3, д, м. д.): 40.06, 111.73, 112.25, 121.55, 124.77, 125.68, 126.84, 127.59, 127.91, 128.21, 128.55, 128.74, 129.58, 130.14, 130.64, 132.25, 138.80, 149.12, 149.35, 149.82, 154.81. Масс-спектр, m/z (I, %): 377 (M+ + 1) (29), 376 (M+.) (100), 377 (M+ - 1) (24), 346 (15), 329 (46), 251 (12), 164 (16). Найдено, %: C 85.96; H 5.97; N 7.17. C27H22N2. Вычислено, %: C 86.60; H 5.92; N 7.48.
4-(7-циклогепта-1,3,5-триенил)анилин (3). 0,0015 моль анилина растворяли в 3 мл тетрагидрофурана, добавляли 0,001 моль перхлората тропилия. Смесь перемешивали при комнатной температуре в течение 2 ч. Реакционную массу разбавляли водой, выделившиеся кристаллы отфильтровывали и перекристаллизовывали из гексана [18].
Желтый порошок. Т. пл. 50-51°С. ИК спектр (н, см-1, тонкая пленка): 3472, 3349 (N-H). ЯМР 1Н спектр (300 МГц, СDCl3, д, м. д.): 32.59 (т, J1,2=5.4 Гц, J2,3=5.4 Гц, 1Н, С7Н в С7Н7), 3.60 (уш. с, 2Н, NH2), 5.35-5.40 (д. д, J1,2=5.4 Гц, J2,3=5.4 Гц, 2Н, С1,6Н в С7Н7), 6.19-6.24 (м, 2Н, С2,5Н в С7Н7), 6.68-6.73 (м, 4Н, орто-С6Н4-N и С3,4Н в С7Н7), 7.14 (д, J=8.1 Гц, 2Н, м-С6Н4-N) Масс-спектр, м/z (Iотн.%): 183(100) [М]+; 182(81); 106(5); 90(12); 77(7). Найдено, %: C 84.81; H 7.12; N 7.57. Вычислено, %: C 85.24; H 7.10; N 7.65.
Выводы
Изучена возможность применения стеклянного комбинированного электрода, содержащего в качестве внутреннего электролита насыщенный раствор хлорида калия в безводной уксусной кислоте для потенциометрического титрования в неводных средах. Показано, что при кислотно-основном титровании в среде безводного ацетонитрила наблюдаются выраженные скачки на кривых титрования, что позволяет определять величины pKa органических оснований. Исходя из полученных значений pKa 2-фенил-4-(4-N, N-диметиламинофенил)бензо[g]хинолина (pKa1 = 12.6853; pKa2 = 7.7853), 1-(4-N, N-диметиламинофенил)-3-фенилбензо[f]хинолина (pKa1 = 11.7403; pKa2 = 10.0653), 4-(7-циклогепта-1,3,5-триенил)анилина (pKa = 10.7299) и пиридина (pKa = 12.6778) установлено два ряда, характеризующие основность гетероароматического ядра и характер аминогруппы. Установлена зависимость между основностью гетероциклического фрагмента и симметричностью соединения. Наиболее основным и термодинамически устойчивым соединением является пиридин. Изомерные формы бензохинолинов заметно различаются по этому показателю: линейная форма, являясь наименее симметричной, наименее устойчива. Аналогичная зависимость получена для аминогрупп бензохинолинов в сравнении с 4-(7-циклогепта-1,3,5-триенил)анилином.Литература
овременные методы исследования в органической химии. М.: Изд-во иностранной литературы, 1959. 310с. , Тиопираны, соли тиопирилия и родственные соединения. Саратов: СГУ, 1987. 160с. , , Определение констант ионизации методом потенциометрического титрования со стеклянным электродом. Бийск: Алтайский ГТУ, 2013. 23с. , Кислотно-основное равновесие в среде амфипротнных растворителей и потенциометрическое титрование. Усп. хим. 1972. Т.41. Вып.11. С.2065. Основы аналитической химии. Физические и физико-химические (инструментальные) методы анализа. М.: Химия, 1977. Т. 3. 488с. Аналитическая химия неводных растворов. М.: Химия, 1982. 256 с. Kolthoff I. M., Chantooni M. K. The Stability Constant of the H2SO4∙HSO4- - Ion and Its Mobility In Acetonitrile. J. Phys. Chem. 1962. Vol.66. P.1675. Coetzee J. F., Padmanabhan G. R. Properties Of Bases In Acetonitrile As Solvent. II. The Autoprotolysis Constant Of Acetonitrile. J. Phys. Chem. 1962. Vol. 66. Р.1708. Romberg E., Cruse K. Dissoziationskonstanten in Acetonitril aus acidimetrischen Titrationen an der Glaselektrode. Z. Elektrochem. 1959. Bd. 63, № 3, S.404-418. Расчет температурной зависимости ионного произведения, удельной электропроводности воды и предельно разбавленных растворов электролитов. Вестник ИГЭУ. 2007. Вып. 2, C. 49. Электрохимия растворов. М.: Химия, 1976. 488с. Определение рН Соросовский образовательный журнал. 2001. Т.7. №4. Gagliardi L. G., Castells C. B., Rafols C., Roses M., Bosch E. Conversion Parameter Between pH Scales (pHw and pHss) In Acetonitrile/Water Mixtures At Various Compositions And Temperatures. Anal. Chem. 2007. Vol.79. №8. P.3180. Barbosa G., Sanz-Nebot V. Assignment Of Reference pH-values To Primary Standard Buffer Solutions For Standartization Of Potentiometric Sensors In Acetonitrile-Water Mixtures. Fresenius J. Anal. Chem. 1995. V. 353. P.148–155. Губен-Вейль. Методы органической химии. М.:Химия. 1967. 673 с. Kaljurand I., Kutt A., Soovali L., Rodima T., Maemets V., Leito I., Koppel I. Extension of the Self-Consistent Spectrophotometric Basicity Scale in Acetonitrile to a Full Span of 28 pKa Units: Unification of Different Basicity Scales. J. Org. Chem. 2005. Vol. 70. P. 1019. , , Синтез бензо[g]- и бензо[f]хинолинов региоселективной реакцией халконов с 2-нафтиламином. ЖОрХ. 2017. Т. 53. Вып. 4 . С. 557. Пат. 2479571 (2013), РФ// Б. И. 2013. №11.
Potentiometric determination of the pKa of nitrogenous organic bases in acetonitrile medium
Yaroslav Valer'yanovich Bykov1*+, Irina Dmitrievna Yakimova1,
Nadezhda Nikolaevna Yaganova1
Department of General Chemistry. Perm State Agro-Technological University n. a. Academician D. N. Pryanishnikov
Petropavlovskaya 23. Perm. 614,000. Perm region. Russia.
Tel. (3422) 17-92-25. E-mail: *****@***ru
Keywords: benzoquinolines, 4-(7-cyclohepta-1,3,5-trienyl)aniline, pyridine, acidity constants, potentiometric titration, acetonitrile.
Abstract
The potentiometer of the acidity constant of benzoquinolines and 4-tropylated aniline in anhydrous acetonitrile was determined for the first time by potentiometric titration with a combined glass electrode. Constructed basicity series of the compounds under study. The possibility of using the standard method for determining the acidity index of nitrogenous organic compounds in non-aqueous media when replacing the internal electrolyte of a glass combined electrode is evaluated. The evaluation of the accuracy of the measurement method was carried out by comparing the literature and experimental values of the indicator of the acidity constant of a standard compound - pyridine in the same solvent.


 1
1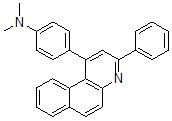
 3
3