Полученный порошок (измельченный до нужной степени) пересыпают в заранее подготовленную посуду или сразу же используют. При измельчении пылящих веществ работу следует проводить в вытяжном шкафу.
Фильтрование
Суть фильтрования состоит в том, что жидкость с находящимися в ней частицами твердого вещества пропускают через пористую перегородку (фильтр). Поры фильтра столь малы, что жидкость (фильтрат) через них проходит, а частицы твердого вещества задерживаются. Таким образом, осадок собирается на фильтре, а жидкость – в сосуде (рис. 21).
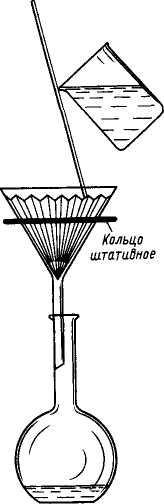
Рис. 21. Фильтрование
При фильтровании воронку с фильтром закрепляют в кольце штатива. Перед началом процесса фильтр смачивают чистым растворителем (водой). Край фильтра не должен доходить до края воронки примерно на 0,5 см. Фильтрование ускоряется, если в стебле воронки находится жидкость.
В зависимости от целей разделения жидкости и осадка применяют различные фильтры. Общее требование: материал фильтра не должен реагировать с жидкостью или осадком.
Фильтры могут быть бумажными (складываются из фильтровальной бумаги), стеклянными или фарфоровыми (пористая стеклянная или фарфоровая пластина), сыпучими (слой хорошо очищенного кварцевого песка), тканевыми или из стекловаты (или обычной ваты) и др.
Один из широко распространенных материалов для фильтров – фильтровальная бумага. Она отличается от обычной бумаги тем, что не проклеена, более чистая и волокнистая. Фильтровальную бумагу заранее можно нарезать кругами различного диаметра. Плотность (пористость) фильтровальной бумаги определяется по цвету бумажной ленты, которой оклеена пачка готовых фильтров.
Черная (розовая) лента – быстрофильтрующие с большими порами фильтры; белая лента – фильтры со средним размером пор; синяя лента – плотные фильтры, предназначенные для фильтрования мелкозернистых осадков.
Собираемая жидкость (фильтрат) может после фильтрования остаться мутной. В этом случае ее следует профильтровать повторно, используя фильтр с более мелкими порами.
Простой фильтр обычно употребляют в случаях, когда отделяют крупнокристаллический осадок. Для приготовления такого фильтра бумагу складывают вчетверо, как показано на рис. 22, затем обрезают и вкладывают в воронку.

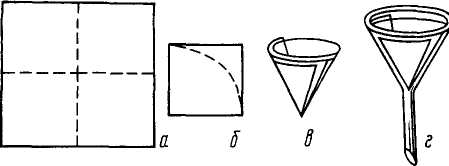
Рис. 22. Изготовление простого фильтра: Рис. 23. Складчатый (плоёный) фильтр
а-в – стадии изготовления; г – фильтр помешен в воронку
Складчатый (плоёный) фильтр (рис. 23) обладает большей площадью поверхности, поэтому фильтрование на нем идет быстрее.
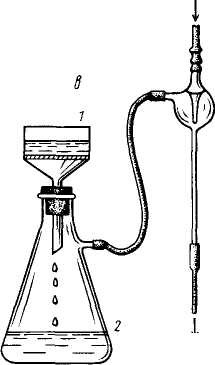
Если фильтрование следует провести быстро, в приемнике создают пониженное давление. В качестве приемника можно использовать колбу Бунзена (рис. 24). Установка для фильтрования при пониженном давлении, изображенная на рис. 24, состоит из фарфоровой воронки Бюхнера (1), колбы Бунзена (2), предохранительной склянки (на рисунке не показана) и вакуумного насоса (3).
В фарфоровую воронку Бюхнера помещают два круглых бумажных фильтра, смачивают их водой и проверяют, хорошо ли они прилегают к стенкам воронки. Если фильтры прилегают хорошо, то при включенном насосе звук ровный, если плохо, то звук неровный, свистящий. Края неплотно прилегающего фильтра прижимают пальцем. После этого, не выключая насоса, в воронку наливают до Ѕ ее высоты фильтрующуюся жидкость. В приемнике создается разреженное давление, и фильтрат проходит в приемник. Жидкость добавляют по мере ее расходования.
Осадок можно отмыть от жидкости, в которой он находился, непосредственно на фильтре. Для этого, не дожидаясь полного окончания фильтрования, на осадок наливают промывную жидкость, взмучивают его и жидкость отсасывают. При необходимости процедуру промывания повторяют.
Центрифугирование
Помимо фильтрования разделение жидкости и осадка возможно путем центрифугирования.
При быстром вращении ротора центрифуги (рис. 25) взвешенные в жидкости твердые частицы под действием центробежной силы отбрасываются от центра и таким путем отделяются от жидкости. После этого жидкость можно просто слить (декантировать) с осадка. Центрифугирование целесообразно применять для малых количеств осадков, а также, если они плохо отделяются от жидкости.
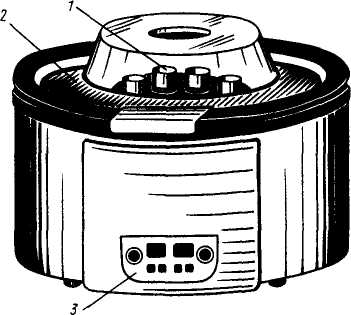
В гнезда центрифуги жидкость с осадком помещают в специальные конические пробирки. При этом пробирки устанавливают пбрами в диаметрально противоположные гнезда. Если необходимо отцентрифугировать смесь только в одной пробирке, напротив нее устанавливается пробирка с примерно равным объемом воды.
Лабораторная занятие 1
Тема «Классы неорганических соединений» (1 час)
Цель занятия: практическое закрепление знаний о классификации неорганических веществ, их получении, свойствах и генетической связи между ними.
Оборудование и реактивы: Пробирки, штатив, спиртовка, металлическая ложечка, стеклянная банка на 150-200 мл, щипцы. Сера, лакмус, фенолфталеин, основной карбонат меди, растворы сульфата меди, щелочи гидроксида натрия, соляной кислоты, 20% раствор серной кислоты, сульфата натрия, хлорида бария, цинк гранулированный.
Выполнение работы
Оксиды
ОПЫТ №1 Получение оксидов непосредственным окислением элементов.
Поместить на металлическую ложечку кусочек серы и нагреть в пламени спиртовки. Как только сера загорится внести ложечку в банку, не касаясь дна и стенок. Когда сера сгорит, ложечку вынуть, в банку налить немного дистиллированной воды и взболтать. Испытать раствор лакмусом. Написать уравнение реакции. Каков характер оксида? Сделайте вывод.
ОПЫТ №2 Получение оксидов разложением солей.
В сухую пробирку поместить немного основного карбоната меди ((СиОН)2СО3). Держа пробирку в наклонном положении, нагреть до полного разложения соли. Какого цвета вещество остается? Что выделяется на холодных стенках пробирки? Написать уравнение реакции. Сделайте вывод.
ОПЫТ №3 Получение оксидов разложением гидроксидов.
На раствор сульфата меди действуем избытком щелочи, получаем гидроксид меди. Полученный осадок нагреть. Объяснить почернение осадка и написать уравнение реакции. Сделайте вывод.
ГИДРОКСИДЫ
ОПЫТ №4 Взаимодействие с кислотами.
В пробирку налейте несколько капель раствора гидроксида натрия. Добавьте 1-2 капли фенолфталеина, затем по каплям приливайте раствор соляной кислоты. Что наблюдается? Напишите уравнение реакции. Сделайте вывод.
Кислоты
ОПЫТ №5 Взаимодействие кислот с металлами.
В пробирку с 3-4 мл серной кислоты (разб.) опустить кусочек цинка, пробирку нагреть до кипения. Что наблюдается? Написать уравнение реакции. Сделайте вывод.
Соли
ОПЫТ №6 Взаимодействие двух различных солей.
К 1 мл раствора сульфата натрия прилить 1 мл раствора хлорида бария. Что наблюдается? Написать уравнение реакции. Сделайте вывод.
Контрольные вопросы:
1. Какие классы неорганических веществ вы знаете?
2. Какие неорганические соединения относятся к классу оксидов?
3. Какие соединения называются основаниями? Приведите примеры.
4. Какие неорганические соединения относятся к классу кислот?
5. Приведите примеры различных солей. Как их классифицируют?
6. Возможен ли перевод всех средних солей в кислые и основные соли?
7. Возможен ли перевод всех кислых и основных солей в средние соли?
8. Сравните способы получения щелочей и нерастворимых оснований.
9. Сравните способы получения в лаборатории сернистой кислоты и кремниевой.
10. При каком условии растворы солей реагируют друг с другом?
11. Какие химические свойства имеют амфотерные гидроксиды? Приведите примеры.
Лабораторная занятие 2
Тема «Определение эквивалентной массы металла» (1 час)
Цель занятия: ознакомление с понятием эквивалент вещества и методикой расчета молярной массы эквивалентов по закону эквивалентов.
Оборудование и реактивы: прибор для измерения объема водорода, кислота соляная (W = 20%), кусочек металла, раствор сульфата меди.
ТЕОРЕТИЧЕСКОЕ ВВЕДЕНИЕ
Моль эквивалентов вещества (эквивалент) - это такое его количество, которое взаимодействует с одним молем атомов водорода или замещает то же количество атомов водорода в химических реакциях. Моль эквивалентов водорода равен одному 1 моль.
Чтобы определить эквивалент вещества надо исходить из конкретной реакции, в которой участвует данное вещество.
Ѕ Mg + Ѕ H2SO4 = Ѕ MgSO4 + Ѕ H2
Одному молю атомов водорода соответствует Ѕ моля магния, Ѕ моля MgSO4 и Ѕ H2SO4.
Отсюда
Э (Mg) = Ѕ моля, Э (MgSO4) = Ѕ моля, Э(H2SO4) = Ѕ моля.
NaOH + Ѕ H2SO4 = Ѕ Na2SO4 + H2O
Отсюда
Э (NaOH) = 1 моль, Э (Na2SO4) = Ѕ моля.
Ѕ Ca + ⅓ H3PO4 = Ca3(PO4)2 + Ѕ H2
Отсюда
Э (Ca) = Ѕ моля, Э (Ca3(PO4)2) = 1/6 моля, Э(H2) = Ѕ моля.
Ѕ H2 + ј O2 = Ѕ H2O
Отсюда
Э(О2) = ј моля, Э(Н2О) = Ѕ моля.
Массу 1 моля эквивалентов называют молярной массой эквивалентов (эквивалентная масса МЭ). Исходя из понятия моля эквивалентов и эквивалентной массы, для расчета молярной массы эквивалентов вещества можно использовать формулы:
для простого вещества
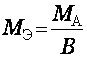
Для сложного вещества
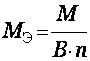 ,
,
где
МА - атомная масса элемента
М – молярная масса вещества
В - валентность элемента или функциональной группы

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




