| 9 класс 2018-2019 |
|
ПО ХИМИИ
ШКОЛЬНЫЙ ЭТАП - РЕШЕНИЯ
1 | К 265 г раствора нитрата свинца (II) с массовой долей соли 15% добавили цинковые опилки. Через некоторое время массовая доля нитрата свинца (II) в растворе стала равна 12,6 %. Вычислите массу выделившегося свинца. | |||||||||||||||||||||||||
v(Pb(NO3)2) в исх. р-ре=265•0,15/331=0,12 моль Пусть Х моль – v(Pb) образовалось в реакции Конечный р-р: 0,126=(0,12–х)•331/(265–141.8х)=(39,7–331х)/(265–141,8х) Х=0,02 моль m(Pb)=4,18 г Проверяем: щ2-? (12,6% неизвестно) В растворе после реакции: m((Pb(NO3)2) =(0,12 –0,02)•331=32,4 г m нового раствора =265–141,8•0,02=262–2,84 =259,2 щ=33,1/259,2 =0,127 | ||||||||||||||||||||||||||
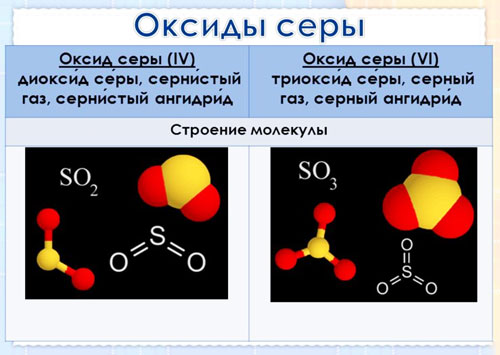
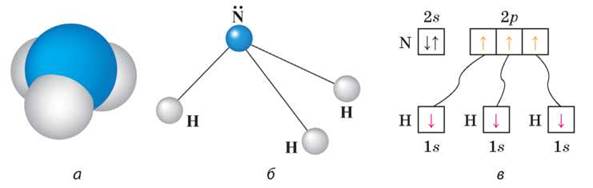
Какую пространственную конфигурацию имеют молекулы SO2, SO3, CO2, NH3? Какие из этих молекул полярны (диполи)? | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
3 | При некоторой температуре равновесие в системе СО2+Н2↔СО+Н2О (г) установилось при концентрациях 2,6,3 и 4моль/л соответственно. После этого водяной пар убрали из системы водопоглощающим средством. Рассчитайте новые равновесные концентрации. | |||||||||||||||||||||||||
| ||||||||||||||||||||||||||
4 | Вычислите процентное содержание KIO3 в растворе, если при взаимодействии 3,21 г этого раствора с избытком KI в разбавленном сернокислом растворе, образуется 0,635 г йода. | |||||||||||||||||||||||||
KIO3+ 5KI+3H2SO4= 3K2SO4+3I2+3H2O v(I2)= 0,635/254=0,0025 моль v(KIO3)= 0,0025/3=8,3•10-4 m(KIO3)= 8,3•10-4•214=0,178 (г) щ=0,178 /3,21 =0,0555 (5,55%) | ||||||||||||||||||||||||||
5 | Какую массу 10%-ного раствора гидрокарбоната натрия необходимо добавить к 150 г 8%-ного раствора соляной кислоты, чтобы уменьшить ее массовую долю в 2 раза? | |||||||||||||||||||||||||
| ||||||||||||||||||||||||||
6 | В каком объёме воды можно растворить 4,2 г карбоната магния (ПР=2,1•10 -5)? (2 балла) | |||||||||||||||||||||||||
S (MgCO3)= S (MgCO3)= 0,0046 моль/л•84г/моль= 0,385г/л V=4,2/0,385=10,9 (л) |