Домашнее задание 25.01.2017
2 смена среда
Ин. яз.6кл.1 гр. (6а, б,г, к), (6в), 2 гр.
8а кл.1гр. , 2гр.
8к кл.1гр. , 2гр.
6А | Д/з | 6Б | д/з | 6В | д/з | 6Г | д/з | 6К | д/з |
Русский | П.112,склонять чилительные, записанные ранее. | Биология | §15, в тетради ответить на вопросы 1-7 | Информат | §12 РТ: № 000, № 000 | Русский | П.62-63. | Русский | Стр. тр. 337 учить |
Информат | §12 РТ: № 000, № 000 | Ин. яз | 1гр. с 49 упр 8, РТ с 30 упр 3 2гр. стр.49 упр.8 | Русский | П.62-63. | Литерат | Учебник 2 часть стр.3-16. | Математ | № 000 |
Математ | № 000 | Математ | П.33 прочитать № 000 | Литерат | Учебник 2 часть стр3-16. | Ин. яз | 1гр. с 49 упр 8, РТ с 30 упр 3 2гр. стр.49 упр.8 | Физкульт | Прогулки на лыжах |
Ин. яз | 1гр. с 49 упр 8, РТ с 30 упр 3 2гр. стр.49 упр.8 | Русский | Упр.№ 000, № 000 | Математ | П.33 прочитать № 000 | Информат | §12 РТ: № 000, № 000 | Физкульт | Выполнить утреннюю гимнастику |
Физкульт | Прогулки на лыжах | Литерат | Стр.288 ответить на вопросы 1-5 | Ин. яз | 1гр. стр.49 упр.8 2гр. стр.48 упр.1,2,3 | Математ | П.33 прочитать № 000 | Информат | §12 РТ: № 000, № 000 |
Физкульт | Выполнить утреннюю гимнастику | Информат | §12 РТ: № 000, № 000 | Ин. яз | 1гр. с 49 упр 8, РТ с 30 упр 3 2гр. стр.49 упр.8 |
7Б | Д/з | 7В | Д/з | 7Г | Д/з | 7К | Д/з |
География | п. 24-27 подготовить презентации и подготовиться к тесту по теме Африка | Алгебра | Выучить свойства, таблицу основных степеней, №17.8-17.13,№17.16-17.22 | Русский | П. 53. Упр. 331и 332 | Русский | У. 299 |
Ин. яз | Нем. яз. Стр.112 упр.5, 6 заполнить пропуски, записать. пересказать Англ. яз. р. т. стр. 45-49 упр. 1,2,3,4 | Русский | П. 41 упр. 262 | Алгебра | №21.29 | Технолог | Инструмент для резьбы по дереву.(юноши) |
Музыка | Подготовить сообщение или презентацию о композиторе: | Литерат | Стр. 209-234 прочитать | Геометр | П.30-31, № 000-226 | Технолог | Повторить свойства тканей из химических волокон, определение лицевой стороны в ткани |
Технолог | Инструмент для резьбы по дереву.(юноши) | Ин. яз | Нем. яз. Стр.112 упр.5, 6 заполнить пропуски, записать. пересказать Англ. яз. р. т. стр. 45-49 упр. 1,2,3,4 | Музыка | Подготовить сообщение или презентацию о композиторе: | География | п. 24-27 подготовить презентации и подготовиться к тесту по теме Африка |
Технолог | Повторить свойства тканей из химических волокон, определение лицевой стороны в ткани | Географ | п. 24-27 подготовить презентации и подготовиться к тесту по теме Африка | Ин. яз | Нем. яз. Стр.112 упр.5, 6 заполнить пропуски, записать. пересказать Англ. яз. р. т. стр. 45-49 упр. 1,2,3,4 | Музыка | Подготовить сообщение или презентацию о композиторе: |
Русский | Параграф 46, упражнение 280 | Музыка | Подготовить сообщение или презентацию о композиторе: | География | п. 24-27 подготовить презентации и подготовиться к тесту по теме Африка | Ин. яз | Нем. яз. Стр.112 упр.5, 6 заполнить пропуски, записать. пересказать Англ. язстр.73 упр.55,56 |
8А | Д/з | 8Б | Д/з | 8В | Д/з | 8Г | Д/з | 8К | Д/з |
Ин. яз | 1гр. с 74 упр 45, 46 2гр. Упр 39 стр 73 (чтение и письменный перевод текста); упр. 41,42,43 стр73( работа по этом у же тексту) (или упр 40,42,43,44 стр 71) | Химия | Параграф 31,32 (повторить), выполнить задания, смотри файл ниже | Географ | П. п.24-25, пов. п.23, на к/к нанести крупные озёра и реки РФ, | Алгебра | №22.7(б)-22.12(б). | Ин. яз | 1 группа: Англ. яз. р. т. стр. 36-37 упр. 1,2,4 2 группа: р. т. стр.37 упр.1,2,3 |
Химия | Параграф 31,32 (повторить), выполнить задания, смотри файл ниже | Алгебра | №22.7(б)-22.12(б). | Русский | П.186-187, упр.251 | Биология | Стр.158-161, рисунок на стр.159 в тетр. | Физика | П.38 упр.15(1-3) |
Физика | П.38 упр.15(1-3) | Геометр | Повторять п.63-65. | Биология | Стр.158-161, рисунок на стр.159 в тетр. | Химия | Параграф 31,32 (повторить), выполнить задания, смотри файл ниже | Русский | Упр.№ 000 |
Алгебра | №22.7(б)-22.12(б). | Биология | Стр.158-161, рисунок на стр.159 в тетр. | Физика | П.38 упр.15(1-3) | Русский | П. 35 учить | Алгебра | П.22 №22.7 |
Биология | Стр.158-161, рисунок на стр.159 в тетр. | Русский | П. 35 учить | Алгебра | №22.7(б)-22.12(б). | Физика | П.38 упр.15(1-3) | Химия | Параграф 31,32 (повторить), выполнить задания, смотри файл ниже |
Литерат | "О любви" прочитать и ответить на вопросы | Физика | П.38 упр.15(1-3) | Химия | Параграф 31,32 (повторить), выполнить задания, смотри файл ниже | Геометр | Повторять п.63-65. | Технолог | Бытовые электроприборы. (юноши) Повторить конспект (деочки) |
25.01.17. ХИМИЯ 8 А, Б,В, Г,К.
Порядок выполнения домашнего задания по химии
Прочитайте (повторите) параграфы 31,32 школьного учебника «ХИМИЯ 8 КЛАСС» автор . Прочитайте и рассмотрите статью «Как узнать: что получится в процессе реакции обмена и правильно составить уравнение реакции обмена» Выполните тест№1 по теме «РЕАКЦИИ ЗАМЕЩЕНИЯ И ОБМЕНА» Выполните предложенное задание №1 по данной теме.Как узнать: что получится в процессе реакции обмена и правильно составить уравнение реакции обмена?
Действительно, как узнать: какие продукты реакции могут возникнут в ходе конкретной реакции обмена? К примеру, что образуется при взаимодействии нитрата бария и сульфата калия?
Ва(NО3) 2 + К2SO4 → ?
Может быть ВаК2(NО3) 2 + SO4 ?ИлиВа + NО3SO4 + К2? Или ещё что-то? Конечно же, в процессе этой реакции образуются соединения: ВаSO4 и КNО3 . А откуда это известно? И как правильно написать формулы веществ? Начнём с того, что чаще всего упускается из вида: с самого понятия «реакция обмена». Это значит, что при данных реакциях вещества меняются друг с другом составными частями. Поскольку реакции обмена в большинстве своём осуществляются межу основаниями, кислотами или солями, то частями, которыми они будут меняться, являются катионы металлов (Na+, Mg2+,Al3+,Ca2+,Cr3+), ионов Н+ или ОН-, анионов – остатков кислот,(Cl-, NO32-,SO32-, SO42-, CO32-, PO43-). В общем виде реакцию обмена можно привести в следующей записи:
Kt1An1 + Kt2An1 = Kt1An2 + Kt2An1
Где Kt1 и Kt2 – катионы металлов (1) и (2), а An1 и An2 – соответствующие им анионы (1) и (2). При этом обязательно надо учитывать, что в соединениях до реакции и после реакции на первом месте всегда устанавливаются катионы, а анионы – на втором. Следовательно, если в реакцию вступит хлорид калия и нитрат серебра, оба в растворённом состоянии
KCl + AgNO3→
то в процессе её образуются вещества KNO3 и AgCl и соответствующее уравнение примет вид:
KCl + AgNO3=KNO3 + AgCl
При реакциях нейтрализации протоны от кислот (Н+) будут соединяться с анионами гидроксила (ОН-) с образованием воды (Н2О):
НCl + КОН = КCl + Н2O
Степени окисления катионов металлов и заряды анионов кислотных остатков указаны в таблице растворимости веществ (кислот, солей и оснований в воде). По горизонтали приведены катионы металлов, а по вертикали – анионы кислотных остатков.
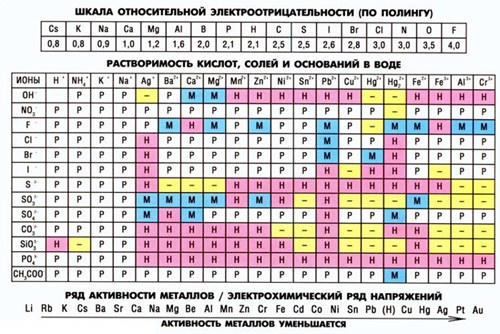
Исходя из этого, при составлении уравнения реакции обмена, необходимо вначале в левой его части установить степени окисления принимающих в этом химическом процессе частиц. Например, требуется написать уравнение взаимодействия между хлоридом кальция и карбонатом натрия. Составим исходную схему этой реакции:
СаCl + NаСО3 →
Над катионами и анионами проставим соответствующие заряды:
Са2+Cl - + Nа+СО32- →
Совершив уже известное действие «крест»-на-«крест», определим реальные формулы исходных веществ:
СаCl2 + Nа2СО3 →
Исходя из принципа обмена катионами и анионами, установим предварительные формулы образующихся в ходе реакции веществ:
СаCl2 + Nа2СО3 → СаСО3 + NаCl
Над их катионами и анионами проставим соответствующие заряды:
Са2+СО32- + Nа+Cl-
Формулы веществ записаны правильно, в соответствии с зарядами катионов и анионов. Составим полное уравнение, уравняв левую и правую его части по натрию и хлору:
СаCl2 + Nа2СО3 = СаСО3 + 2NаCl
В качестве другого примера приведём уравнение реакции нейтрализации между гидроксидом бария и ортофосфорной кислотой:
ВаОН + НРО4 →
Над катионами и анионами проставим соответствующие заряды:
Ва2+ ОН - + Н+РО43- →
Определим реальные формулы исходных веществ:
Ва(ОН)2 + Н3РО4 →
Исходя из принципа обмена катионами и анионами (25), установим предварительные формулы образующихся в ходе реакции веществ, учитывая, что при реакции обмена одним из веществ обязательно должна быть вода:
Ва(ОН)2 + Н3РО4 → Ва2+ РО43- + Н2O
Определим правильную запись формулы соли, образовавшейся в процессе реакции:
Ва(ОН)2 + Н3РО4 → Ва3(РО4)2 + Н2O
Уравняем левую часть уравнения по барию:
3Ва (ОН)2 + Н3РО4 → Ва3(РО4)2 + Н2O
Поскольку в правой части уравнения остаток ортофосфорной кислоты взят дважды, (РО4)2, то слева необходимо также удвоить её количество:
3Ва (ОН)2 + 2Н3РО4 → Ва3(РО4)2 + Н2O
Осталось привести в соответствие количество атомов водорода и кислорода в правой части у воды. Так как слева общее количество атомов водорода равно 12, то справа оно так же должно соответствовать двенадцати, поэтому перед формулой воды необходимо поставить коэффициент «6» (поскольку в молекуле воды уже имеется 2 атома водорода). По кислороду так же соблюдено равенство: слева 14 и справа 14. Итак, уравнение имеет правильную форму записи: 3Ва (ОН)2 + 2Н3РО4 → Ва3(РО4)2 + 6Н2O
Тест№1 «Реакции замещения и обмена»
1.В химическом уравнении Са+2H2 О=Са(ОH)2 +Н2 коэффициентами являются соответственно
А) 2,2,2,1 Б) 1,2,1,1 В)0,2,0,0 Г) 1,2,2,2
2. Одним из продуктов взаимодействия алюминия с соляной кислотой является
А) кислота
Б) кислород
В) водород
Г) оксид алюминия
3. К схеме реакции замещения относится
А) Na+H2O=NaOH+H2
Б) Ca +H2=CaH2
B) CaCO3=CaO+CO2
Г)NaOH+HCl=NaCl+H2O
4. К схеме реакции обмена относится
А) Na+H2O=NaOH+H2
Б) Ca +H2=CaH2
B) CaCO3=CaO+CO2
Г) NaOH + HCl=NaCl+H2O
5. Отметьте неверное высказывание
А) реакция получения гидроксида натрия при взаимодействии натрия с водой – реакция замещения;
Б) если в раствор сульфата меди (II) опустить железную пластинку, то она покроется налетом меди;
В) при взаимодействии соляной кислоты и гидроксида калия получается сульфат калия и вода;
Г) реакция нейтрализации – взаимодействие кислоты и основания с образованием соли и воды.
6. В схеме химической реакции К+ H2O =Х +Н2 вещество Х – это…
А) H2О
Б) КOH
В) O2
Г) HNO3
7. В схеме химического уравнения Н2SO4+ X =Na2SO4 +Yвещества Х и Y– это соответственно
А) H2O2 и NaCl
Б) NaOH и H2O
В) O2 и Na2O
Г) N2O5 и H2O
8. Расставьте коэффициенты в схеме уравнения
Ва(ОН)2+ НNO3= Ва(NO3)2+ Н2Oсумма коэффициентов равна
А) 9 Б) 6 В) 4 Г) 5
Задание №1 «Реакции замещения и обмена»
Превратите схемы реакций в химические уравнения, поставив коэффициенты и дописав пропущенные вещества
1) ? + H2O = NaOH + H2
2) CaCl2 + Na2CO3=CaCO3+ ?
3) CaCO3+HCl= CaCl2+CO2+ ?
4) Zn + HCl= ZnCl2+ ?
5) H2SO4 + KOH = ? + H2O
6) Fe + Cu SO4= ?+ Fe SO4
7) ZnO+ ? = Zn+ H2O
8) Cu(OH)2 + H2SO4 = Cu SO4 + ?



